JAK/STAT信号通路在高糖诱导人脐静脉内皮细胞损伤中的作用*
廖静秋, 林佳琼, 张伟杰, 许 翎, 智喜梅, 林 凯, 吴 文△
(1南方医科大学,广东 广州 510515; 2广东省人民医院,广东省医学科学院,广东省老年医学研究所东病区内分泌科,广东 广州 510080)
JAK/STAT信号通路在高糖诱导人脐静脉内皮细胞损伤中的作用*
廖静秋1, 2,林佳琼1, 2,张伟杰2,许翎2,智喜梅2,林凯2,吴文2△
(1南方医科大学,广东 广州 510515;2广东省人民医院,广东省医学科学院,广东省老年医学研究所东病区内分泌科,广东 广州 510080)
[摘要]目的: 探讨Janus激酶/信号转导子及转录激活子(JAK/STAT)信号通路是否介导高糖诱导的人脐静脉内皮细胞(HUVECs)损伤。方法: CCK-8检测细胞存活率;Western blot法检测内皮细胞JAK2、STAT3、caspase-9 和内皮型一氧化氮合酶(eNOS)的表达水平;DCFH-DA染色荧光显微镜照相法检测内皮细胞内活性氧簇(ROS)水平;罗丹明123染色荧光显微镜照相法测定线粒体膜电位(MMP)。结果: 高糖(40 mmol/L葡萄糖)处理HUVECs 6~12 h能上调JAK2的磷酸化,于9 h达最高峰;高糖处理HUVECs 6~12 h能上调p-STAT3水平,其中12 h表达最多;JAK/STAT通路抑制剂AG490预处理1 h可显著抑制由高糖引起的内皮细胞损伤,表现为细胞存活率升高、凋亡相关蛋白caspase-9表达和胞内ROS生成减少、MMP及eNOS表达升高。结论: JAK/STAT信号通路参与了高糖诱导的人脐静脉内皮细胞损伤过程。
[关键词]JAK/STAT信号通路; 高糖; 人脐静脉内皮细胞; AG490
糖尿病血管病变(diabetic angiopathy)是糖尿病患者最常见的慢性并发症,也是糖尿病患者失明、截肢以及死亡的主要原因之一,严重影响患者预后和生活质量。高血糖通过直接或间接的影响引起血管内皮功能异常,启动或加重糖尿病血管病变[1]。
研究表明高糖可通过核因子κB(nuclear factor-κB,NF-κB)通路[2]、p38丝裂原活化蛋白激酶(p38 mitogen-activated protein kinase,p38 MAPK)通路[3]等细胞信号通路诱导内皮细胞损伤。Janus 激酶/信号转导子及转录激活子(Janus kinase/signal transducer and activator of transcription,JAK/STAT)通路是细胞信号转导的重要通路之一。新近研究发现,JAK/STAT通路参与了糖尿病并发症的发生发展。Marrero等[4]发现,高糖在肾小球滤过膜细胞通过激活JAK/STAT通路导致肾小球滤过膜细胞的增殖,从而引起糖尿病肾病。此外,另有研究表明在牛视网膜毛细血管内皮细胞,高糖可通过激活JAK/STAT通路上调血管内皮生长因子(vascular endothelial growth factor,VEGF)表达[5]。而对于JAK/STAT通路是否参与高糖诱导血管内皮细胞的多种损伤,目前鲜有报道。
为此,本研究旨在探讨高糖在诱导人脐静脉内皮细胞(human umbilical vein endothelial cells, HUVECs)损伤过程中,JAK/STAT通路是否被激活;JAK/STAT通路抑制剂AG490能否抑制高糖诱导HUVECs的多种损伤,从而探讨JAK/STAT通路在高糖损伤血管内皮细胞中的作用,为深入阐明JAK/STAT通路在高糖损伤血管内皮细胞的作用及机制提供新颖的实验依据。
材料和方法
1材料
DCFH-DA和罗丹明123(rhodamine 123, Rh123)购自Sigma; CCK-8试剂盒购自Dojindo;DMEM(低糖)培养基购自HyClone;胎牛血清(fetal bovine serum,FBS)购自Gibco;JAK2抗体、p-JAK2抗体、p-STAT3抗体和eNOS抗体购自CST;STAT3抗体、caspase-9抗体和GAPDH抗体购自Proteintech;HUVECs购自广州吉妮欧公司。
2方法
2.1人脐静脉内皮细胞的体外培养
细胞培养在含10% FBS的低糖DMEM培养基中,同时加入1×105U/L青霉素和100 mg/L链霉素,置于5% CO2、37 ℃的温箱中培养。待细胞融合达80%后,用0.25%胰蛋白酶-EDTA消化,适度消化后加完全培养基终止胰蛋白酶的消化作用。用灭菌枪头将瓶壁细胞吹落形成细胞悬液。1 200 r/min离心5 min, 弃上清, 按1∶3传代。实验前换用无血清的DMEM培养液培养12 h,然后进行分组实验。
2.2实验分组
实验分为4组:正常对照(control)组;高糖(high glucose,HG)损伤组:应用40 mmol/L葡萄糖处理HUVECs 24 h;AG490+HG组:10 μmol/L AG490作用于HUVECs 1 h,撤去,用PBS洗2次,接着用40 mmol/L葡萄糖作用24 h;AG490组:10 μmol/L AG490作用于HUVECs 1 h。
2.3CCK-8实验测定细胞存活率
将HUVECs接种于96孔培养板中,细胞在培养孔内生长至大约80%时,按照实验要求给予不同处理,于每孔中加入10 μL CCK-8溶液,37 ℃孵育2 h,使用酶标仪检测各孔吸光度(A),波长设定为450 nm。按公式:细胞存活率(%)=处理组A/对照组A×100%,求出处理组细胞存活率,重复3次。
2.4Western blot法检测JAK2、STAT3、caspase-9和eNOS的表达
将HUVECs接种于60 mm培养皿中,贴壁生长至80%时给予不同处理因素,弃培养液,用预冷的PBS洗2次,各皿加入80 μL裂解液后置4 ℃裂解30 min,12 000 r/min离心15 min,取上清,蛋白浓度采用BCA法进行测定。总蛋白经SDS-PAGE分离后,转移到PVDF膜上。用5%脱脂奶粉封闭90 min,分别加入各种I抗[p-JAK2和JAK2(1∶2 000),p-STAT3、STAT3和 caspase-9(1∶5 000),eNOS(1∶1 000)],4 ℃过夜,然后用TBST洗3次(每次10 min),加入 II 抗(1∶10 000),室温孵育60 min,然后再用TBST洗3次(每次10 min)。ECL发光液将PVDF膜显色,暗室曝光,凝胶成像系统扫描分析结果。
2.5细胞内活性氧簇(reactive oxygen species,ROS)含量的检测
DCFH-DA是一种自身不能发荧光的化合物,可自由穿过细胞膜,被胞内ROS氧化为有荧光的DCF。通过检测DCF的荧光强度即可反映细胞内ROS水平。将HUVECs接种于6孔培养板中,当细胞生长贴壁生长至80%时,给予各实验组不同的处理因素后,弃培养液,PBS 冲洗3次,将HUVECs与10 μmol/L DCFH-DA于37 ℃孵育30 min,再用PBS冲洗3次。在荧光显微镜下随机地选取5个不重复区摄片,采用ImageJ 1.41软件分析各视野平均绿色荧光强度,进而对每组的各个样本进行统计分析。
2.6细胞线粒体膜电位(mitochondrial membrane potential,MMP)含量的测定
Rh123是一种可被线粒体吸收的绿色荧光染料,其吸收值随细胞MMP 的改变而变化,因此可根据其荧光强度来间接反映MMP的高低。将HUVECs接种于6孔培养板中,贴壁生长至大约80%时,给予各实验组不同的处理因素,弃培养液,用PBS冲洗3次,将HUVECs与10 μg/L Rh123于37 ℃避光孵育45 min, 再用PBS冲洗3次。在荧光显微镜下随机地选取5个不重复区摄片。用ImageJ 1.41软件分析各视野平均荧光强度,进而对每组的各个样本进行统计分析。
3统计学处理
实验数据以均数±标准差(mean±SD)表示,用SPSS 20.0统计学软件进行统计分析,采用SNK-q检验(实验组组间比较)及Dunnett-t检验(实验组与对照组比较),以P<0.05为差异有统计学意义。
结果
1高糖上调人脐静脉内皮细胞的p-JAK2和p-STAT3蛋白表达
使用高糖(40 mmol/L)处理HUVECs 6~12 h可显著上调JAK2蛋白磷酸化水平(P<0.05),其中在9 h时p-JAK2表达达到最高峰;应用高糖处理HUVECs 6~12 h可显著上调p-STAT3表达(P<0.01),并且在12 h时STAT3蛋白磷酸化水平最高,见图1。

Figure 1.High glucose (40 mmol/L) up-regulated the protein levels of p-JAK2 and p-STAT3 in HUVECs. Mean±SD.n=3.*P<0.05,**P<0.01vscontrol group.
图1高糖促进人脐静脉内皮细胞p-JAK2和p-STAT3的蛋白水平
2JAK/STAT通路介导高糖引起的人脐静脉内皮细胞的细胞毒性
高糖(40 mmol/L)处理HUVECs 24 h可产生细胞毒性,使细胞存活率降低至(68.6±2.4)%。在高糖处理细胞前,分别应用5、10、20、40和80 μmol/L AG490(为JAK/STAT通路的抑制剂)预处理HUVECs 1 h,其中10、20、40和80 μmol/L AG490均能显著抑制HG引起的细胞毒性,使细胞存活率明显升高,但各组之间无明显差异;而单独应用80 μmol/L AG490处理细胞1 h则对细胞存活率无明显影响,见图2。据此,本实验应用10 μmol/L AG490作为后续实验的有效保护浓度。
3JAK/STAT通路介导高糖引起的人脐静脉内皮细胞凋亡
分别用不同葡萄糖糖浓度(10~40 mmol/L)处理HUVECs 24 h,随着葡萄糖浓度升高,caspase-9的表达水平也逐渐升高,与对照组相比,各组均有统计学意义(P<0.05),其中浓度为40 mmol/L时,caspase-9表达增加最多。同时,用40 mmol/L葡萄糖处理HUVECs 6~24 h均能明显增加的caspase-9的表达水平(P<0.01),其中12 h的水平达最高峰。但是,在HG作用前,用10 μmol/L AG490预处理HUVECs 1 h能明显抑制HG对caspase-9的上调作用,与HG处理组比较,差异有统计学显著性(P<0.05)。10 μmol/L AG490本身对caspase-9的基础表达水平无明显影响,见图3。

Figure 2.The inhibitor of JAK/STAT signaling pathway antagonized high glucose (HG, 40 mmol/L glucose)-induced cytotoxicity in HUVECs. Mean±SD.n=3.*P<0.05,**P<0.01vscontrol group;#P<0.05vsHG group.
图2JAK/STAT通路抑制剂减轻高糖引起的人脐静脉内皮细胞的细胞毒性

Figure 3.The inhibitor of JAK/STAT signaling pathway attenuated high glucose (HG, 40 mmol/L glucose)-induced apoptosis of HUVECs. Mean±SD.n=3.*P<0.05,**P<0.01vscontrol group;#P<0.05vsHG group.
图3JAK/STAT通路抑制剂减轻高糖引起的人脐静脉内皮细胞的凋亡
4JAK/STAT通路介导高糖引起的人脐静脉内皮细胞的氧化应激
图4显示,HG作用于HUVECs 24 h可使胞内DCFH的平均荧光强度(mean fluorescence intensity,MFI;反映ROS水平的一个指标)明显增强,与正常对照组相比,两组差异有统计学显著性(P<0.05)。但经AG490预处理1 h可使胞内ROS堆积明显减少,MFI从 (9.8±2.7)%减少至 (4.2±2.0)%,与高糖组相比,差异有统计学显著性(P<0.05)。而单独AG490预处理则对胞内ROS生成无明显作用,见图4。
5JAK/STAT通路介导高糖引起的人脐静脉内皮细胞的线粒体损伤
HG作用HUVEC 24 h使胞内Rh123的MFI(反映MMP大小的指标)从(9.4±1.2)%降低至 (3.5±0.7)%,差异有统计学显著性(P<0.05)。然而,AG490预处理1 h可使MFI升高至(6.1±1.1)%,与HG处理组比较,差异有统计学显著性(P<0.05)。单独AG490预处理本身对HUVECs的MMP大小无显著作用,见图5。
6JAK/STAT通路介导高糖对人脐静脉内皮细胞eNOS表达水平的下调作用
采用不同葡萄糖浓度(10~40 mmol/L)分别处理HUVECs 24 h后发现,葡萄糖浓度为40 mmol/L时对eNOS的表达具有明显的抑制作用。与对照组相比,差异有统计学显著性(P<0.01)。同时,用40 mmol/L葡萄糖处理HUVECs 3~24 h,其中12 h与24 h均可明显下调eNOS的表达水平(P<0.01),而且在24 h时表达量最低。采用AG490预处理HUVECs 1 h能减轻高糖引起的eNOS表达水平的降低,与HG处理组比较,差异有统计学显著性(P<0.05)。AG490本身对eNOS的基础水平无明显影响,见图6。
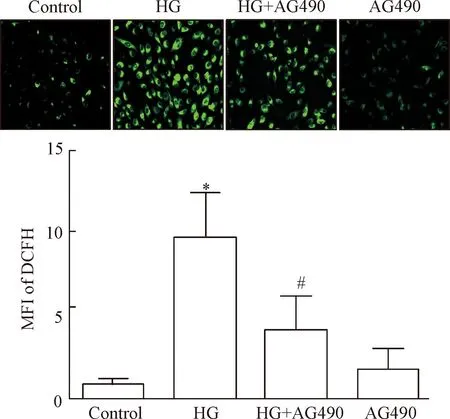
Figure 4.The inhibitor of JAK/STAT signaling pathway reduced high glucose(HG)-induced accumulation of reactive oxygen species (ROS) in HUVECs. Mean±SD.n=5.*P<0.05vscontrol group;#P<0.05vsHG group.
图4JAK/STAT通路抑制剂减少高糖引起的人脐静脉内皮细胞内活性氧堆积
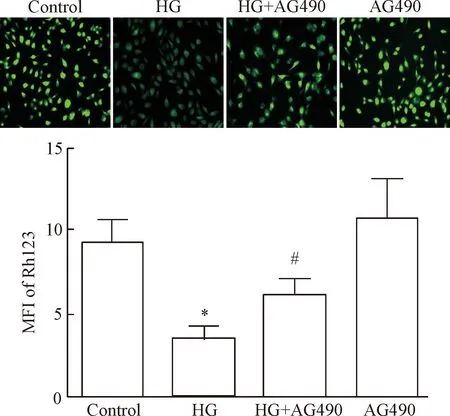
Figure 5.The inhibitor of JAK/STAT signaling pathway attenuated high glucose (HG)-induced reduction of MMP in HUVECs. Mean±SD.n=5.*P<0.05vscontrol group;#P<0.05vsHG group.
图5JAK/STAT通路抑制剂减轻高糖引起的人脐静脉内皮细胞线粒体膜电位降低

Figure 6.The inhibitor of JAK/STAT signaling pathway antagonized high glucose (HG, 40 mmol/L glucose)-induced decline of the expression of eNOS in HUVECs. Mean±SD.n=3.*P<0.05,**P<0.01vscontrol group;#P<0.05vsHG group.
图6JAK/STAT通路抑制剂减弱高糖对人脐静脉内皮细胞eNOS表达的下调作用
讨论
高血糖作为各型糖尿病的共同特征,除可引起代谢障碍外,更重要的一点是可引起内皮细胞的损伤,进而启动或加重糖尿病血管病变。本研究在高糖损伤人脐静脉内皮细胞模型再次证实,高糖对内皮细胞有明显的损伤作用,表现在使细胞存活率下降,凋亡相关蛋白caspase-9表达增多,ROS生成增加,线粒体膜电位丢失,eNOS生成减少,上述结果均与既往研究相一致[1, 6-7]。
目前研究已证实,外界刺激因子与调节各种细胞行为及细胞内各种信号转导通路的活化紧密相关,其中JAK/STAT信号传导通路在细胞信号转导这一过程中发挥着重要作用。JAK是一类胞质内非受体型可溶性酪氨酸蛋白激酶,包括4个家族:JAK1、JAK2、JAK3和TYK2。STAT是一类能与靶基因调控区DNA结合的胞质蛋白,是JAK的下游底物,其家族包括7个成员:STAT1、STAT2、STAT3、STAT4、STAT5a、STAT5b和STAT6。JAK家族酪氨酸磷酸化后募集胞质中的STATs,使其磷酸化后形成二聚体进入细胞核内,在核内它们与目的基因启动子结合,进而激活基因表达,实现对细胞的生理及病理反应进行相应的调控,在细胞的生长、活化、分化、凋亡等过程中发挥着重要作用[8]。
JAK/STAT通路在血管系统的病理生理中发挥着非常重要的作用。Manea等[9]发现,在人脐静脉内皮细胞株EAhy926,阻断JAK/STAT通路可抑制高糖引起的内皮素-1(endothelin-1,ET-1)的升高,而后者在维持血管内皮细胞稳态中发挥着重要作用;Amiri等[10]研究表明高糖可通过JAK2/STAT通路促进血管平滑肌的增殖; Tawfik等[11]应用HG和H2O2干预主动脉内皮细胞发现,JAK2在氧化应激诱导的主动脉内皮细胞凋亡中发挥了重要作用。由此可见,JAK/STAT通路与血管病变及内皮细胞功能紊乱密切相关。根据这一系列研究报道,我们推测JAK/STAT通路可能参与高糖诱导的血管内皮细胞的多种损伤,而在本研究中我们也证实了这一点。高糖在引起HUVECs细胞存活率下降、caspase-9表达上调、ROS生成增加、线粒体膜电位丢失及eNOS表达减少的同时,还伴有JAK2蛋白及STAT3蛋白的激活:HG诱导HUVECs 6 h时p-JAK2蛋白水平明显增加,9 h时升至顶峰,随后逐渐下降;HG处理HUVECs 6 h时p-STAT3显著增加,12 h时达顶峰。
在上述实验基础上,为进一步探讨JAK/STAT通路是否参与高糖诱导内皮细胞损伤过程,本研究观察了该通路抑制剂AG490对高糖损伤内皮细胞作用的影响。AG490是一种选择性拮抗JAK2酪氨酸磷酸化的抑制剂,可有效阻断其下游信号转导及STAT3的活化[12],进而抑制相应的生理、病理效应。在研究中我们发现,AG490可有效抑制高糖损伤内皮细胞这一过程,显著提高内皮细胞的存活率,减少凋亡蛋白caspase-9的表达及ROS的生成,保护线粒体膜电位以及抑制eNOS的生成减少,这为深入阐明JAK/STAT通路在高糖诱导内皮细胞损伤的作用及其机制提供了新颖的实验证据。
JAK/STAT通路是最早被确认的由脂肪组织细胞分泌的信号分子——瘦素的下游信号通路。研究表明,瘦素能引起血管内皮细胞功能失调和氧化应激[13-15]。但是瘦素-JAK/STAT通路是否介导高血糖引起的血管内皮细胞损伤迄今尚未明了,值得今后进一步研究探讨。
[参考文献]
[1]Sena CM, Pereira AM, Seiça R. Endothelial dysfunction:a major mediator of diabetic vascular disease[J]. Biochim Biophys Acta, 2013, 1832(12):2216-2231.
[2]Brownlee M. Biochemistry and molecular cell biology of diabetic complications[J].Nature, 2001, 414(6865):813-820.
[3]罗春英,刘小鹏,文格波,等. p38丝裂素活化蛋白激酶在高糖损伤人脐静脉内皮细胞中的作用[J]. 中国动脉硬化杂志, 2006, 14(10):853-856.
[4]Marrero MB,Banes-Berceli AK,Stern DM, et al. Role of the JAK/STAT signaling pathway in diabetic nephropathy[J]. Am J Physiol Renal Physiol, 2005, 290(4):F762-F768.
[5]Zheng Z, Chen H, Zhao H,et al. Inhibition of JAK2/STAT3-mediated VEGF upregulation under high glucose conditions by PEDF through a mitochondrial ROS pathwayinvitro[J]. Invest Opthalmol Vis Sci, 2010, 51(1):64-71.
[6]van den Oever IA, Raterman HG, Nurmohamed MT, et al. Endothelial dysfunction, inflammation, and apoptosis in diabetes mellitus[J]. Mediators Inflamm, 2010, 2010: 792393.
[7]Schalkwijk CG, Stehouwer CD. Vascular complications in diabetes mellitus: the role of endothelial dysfunction[J]. Clin Sci (Lond), 2005, 109(2):143-159.
[8]Aittomäki S, Pesu M. Therapeutic targeting of the Jak/STAT pathway[J]. Basic Clin Pharmacol Toxicol, 2014, 114(1):18-23.
[9]Manea SA, Manea A, Heltianu C. Inhibition of JAK/STAT signaling pathway prevents high-glucose-induced increase in endothelin-1 synthesis in human endothelial cells[J]. Cell Tissue Res, 2010, 340(1):71-79.
[10]Amiri F, Venema VJ, Wang X,et al. Hyperglycemia enhances angiotensin II-induced Janus-activated kinase/STAT signaling in vascular smooth muscle cells[J]. J Biol Chem, 1999, 274(45):32382-32386.
[11]Tawfik A, Jin L, Banes-Berceli AK,et al. Hyperglycemia and reactive oxygen species mediate apoptosis in aortic endothelial cells through Janus kinase 2[J]. Vasc Pharmacol, 2005, 43(5):320-326.
[12]Sriuranpong V, Park JI, Amornphimoltham P, et al. Epidermal growth factor receptor-independent constitutive activation of STAT3 in head and neck squamous cell carcinoma is mediated by the autocrine/paracrine stimulation of the interleukin 6/gp130 cytokine system[J]. Cancer Res, 2003, 63(11):2948-2956.
[13]Singh P, Hoffmann M, Wolk R,et al. Leptin induces C-reactive protein expression in vascular endothelial cells[J].Arteriosclerosis Thromb Vasc Biol, 2007, 27(9):e302-307.
[14]Korda M, Kubant R, Patton S,et al. Leptin-induced endothelial dysfunction in obesity[J]. Am J Physiol Heart Circ Physiol, 2008, 295(4): H1514-H1521.
[15]Yamagishi SI,Edelstein D,Du XL,et al. Leptin induces mitochondrial superoxide production and monocyte chemoattractant protein-1 expression in aortic endothelial cells by increasing fatty acid oxidation via protein kinase A[J]. J Biol Chem, 2001, 276(27):25096-25100.
(责任编辑: 陈妙玲, 罗森)
Role of JAK/STAT signaling pathway in high glucose-induced damage in human umbilical vein endothelial cells
LIAO Jing-qiu1, 2, LIN Jia-qiong1, 2, ZHANG Wei-jie2, XU Lin2, ZHI Xi-mei2,LIN Kai2, WU Wen2
(1SouthernMedicalUniversity,Guangzhou510515,China;2DepartmentofEndocrinology,EastWard,GuangdongGeriatricInstitute,GuangdongAcademyofMedicalSciences,GuangdongGeneralHospital,Guangzhou510080,China.E-mail:wuwen1964@163.com)
[ABSTRACT]AIM: To investigate whether Janus kinase/signal transducer and activator of transcription (JAK/STAT) signaling pathway mediates high glucose-induced damage in human umbilical vein endothelial cells (HUVECs). METHODS: The cell viability was examined by CCK-8 assay. The expression levels of JAK2, STAT3, caspase-9 and endothelial nitric oxide synthase (eNOS) were detected by Western blot. The intracellular levels of reactive oxygen species (ROS) were tested by DCFH-DA staining followed by photofluorography. Mitochondrial membrane potential (MMP) was measured by rhodamine 123 staining followed by photofluorography. RESULTS: Treatment of HUVECs with high glucose (40 mmol/L glucose) for 6~12 h enhanced the protein level of phosphorylated JAK2, peaking at 9 h. Treatment of the cells with high glucose for 6~12 h also increased the protein level of p-STAT3 with the peak value at 12 h. Pretreatment with the inhibitor of JAK/STAT pathway AG490 for 1 h before exposure of the HUVECs to high glucose significantly inhibited the high glucose -induced injury, as evidenced by an increase in the cell viability, decreases in the expression of caspase-9 and the intracellular ROS production, and increases in MMP and the expression of eNOS. CONCLUSION: JAK/STAT signaling pathway is involved in the high glucose-induced damage in HUVECs.
[KEY WORDS]JAK/STAT signaling pathway; High glucose; Human umbilical vein endothelial cells; AG490
doi:10.3969/j.issn.1000- 4718.2016.03.002
[中图分类号]R363.2; R587.2
[文献标志码]A
通讯作者△Tel: 020-83827812; E-mail: wuwen1964@163.com
*[基金项目]国家自然科学基金资助项目(No. 81450062);广东省自然科学基金资助项目(No. 2015A030313872)
[收稿日期]2015- 10- 30[修回日期] 2015- 12- 14
[文章编号]1000- 4718(2016)03- 0392- 06
杂志网址: http://www.cjpp.net

