云南黄连市售品质量评价*
张德伟,封海霞,谢汉林,丁 博,牟腊梅
(1.重庆市万州食品药品检验所,重庆 404000; 2.重庆市食品药品检验检测研究院,重庆 401121;3.重庆三峡学院,重庆 404000; 4.重庆文理学院,重庆 402160)
云南黄连市售品质量评价*
张德伟1,封海霞2,谢汉林3,丁 博3,牟腊梅4
(1.重庆市万州食品药品检验所,重庆 404000; 2.重庆市食品药品检验检测研究院,重庆 401121;3.重庆三峡学院,重庆 404000; 4.重庆文理学院,重庆 402160)
目的 建立测定云南黄连中黄连碱、盐酸巴马汀、盐酸小檗碱等单体生物碱和总生物碱含量的高效液相色谱(RP-HPLC)法和紫外分光光度(UV)法,比较不同商品来源云南黄连质量的差异。方法 HPLC法采用色谱柱Venusil MP C18柱(250 mm×4.6 mm,5 μm),流动相为乙腈-0.2%冰醋酸(三乙胺调pH=5.05)梯度洗脱,检测波长345 nm;UV法于349 nm波长处测定总生物碱吸光度。联合上述方法对10批云南黄连药材进行测定,并对测定结果进行聚类分析。结果 黄连碱、盐酸巴马汀、盐酸小檗碱进样量分别在0.200 0~2.000 0,0.092 4~0.924 0,1.278 0~12.780 0 μg范围内与峰面积呈良好的线性关系(r≥0.999 5),平均加样回收率依次为98.61%,97.35%,99.03%,RSD分别为1.28%,1.52%,1.19%(n=6)。UV法测总生物碱质量浓度在5.112~25.560 μg/mL范围内与吸光度呈良好的线性关系。采用聚类分析能将不同产地的10批云连药材分为3类。不同地区商品云南黄连生物碱含量存在显著性差异。结论 该法准确、可靠、重复性好,对市场上云南黄连的质量状况起到良好的评价作用,可为进一步系统研究云南黄连奠定基础。
云南黄连;黄连碱;盐酸巴马汀;盐酸小檗碱;总生物碱;高效液相色谱法;紫外分光光度法
云南黄连(Coptis teeta Wall.)又称云连,为毛茛科黄连属(Coptis)草本植物,产于云南西北部及藏东南地区,为我国传统中药黄连的源植物之一[1-2]。由于云连生长环境要求极高,市场上售卖的药材多以野生为主,由于长期过度采挖和生境的破坏,云连资源越来越匮乏,已于2002年被列为国家二级重点保护中药材[3]。云连味苦、性寒,具有清热燥湿、泻火解毒等功效。研究表明,黄连药材的主要成分为黄连碱、盐酸巴马汀、盐酸小檗碱等生物碱,尤其以小檗碱含量最高[4]。目前关于黄连中有效成分含量测定已有报道,但对市售不同区域产云南黄连的质量评价未作考察。因此,笔者收集了不同地区的市售云连,采用高效液相色谱(HPLC)法测定了3种单体生物碱的含量,以及用紫外分光光度(UV)法测定总生物碱的含量,为云连质量评价提供参考,为更加系统全面地研究云南黄连奠定基础。
1 仪器与试药
Agilent 1260型高效液相色谱仪(美国安捷伦科技有限公司),包括 G1311C四元泵,G1329B进样器,G1314F紫外检测器;Mettler XP204型电子天平(瑞士);TG18M型离心机(长沙平凡仪器仪表厂);圣德利超纯水机;DFY-200型万能粉碎机;KQ-800DE型数控超声波清洗器;UV-2501PC型紫外可见分光光度仪(岛津)。黄连碱对照品(成都曼思特生物科技有限公司,含量为 98%);盐酸巴马汀对照品(批号为 110732-201309)、盐酸小檗碱对照品(批号为 110713-201212),均供含量测定用,由中国食品药品检定研究院提供;乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。样品(购自云南、四川、重庆药材批发市场,共10批)经重庆三峡学院生命科学与工程学院周浓副教授鉴定为毛茛科植物云南黄连 Coptis teeta Wall.的干燥根茎,药材粉碎后过40目筛,备用。
2 方法与结果
2.1 单体生物碱含量测定[5]
2.1.1 色谱条件及系统适用性试验
色谱柱:VenusilMPC18(2)柱(250mm×4.6mm,5μm);流动相:A为乙腈,B为0.2%冰醋酸(三乙胺调pH=5.05),梯度洗脱(0→15 min→25 min→35 min→55 min,20%A→50%A→35%A→80%A);检测波长:345 nm;流速:1.0 mL/min;进样量:20 μL;柱温:30℃。在此条件下,色谱图见图1。
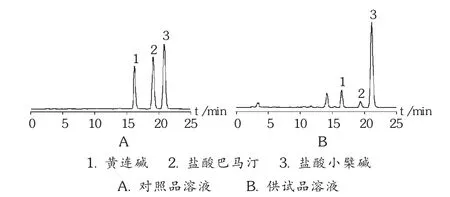
图1 高效液相色谱图
2.1.2 溶液制备
精密称取黄连碱、盐酸巴马汀、盐酸小檗碱对照品适量,加甲醇,分别制成质量浓度0.1000,0.046 2,0.639 0 g/L的溶液,即得对照品溶液。称取样品粉末约0.1 g,精密称定,置具塞锥形瓶中,加1%盐酸甲醇溶液50 mL,称定质量,60℃温浴30 min,超声提取60 min,放冷,补足失重,摇匀,用前以4 000 r/min离心10 min,即得供试品溶液。
2.1.3 方法学考察
线性关系考察:精密吸取2.1.2项下对照品溶液2,5,10,15,20 μL,注入液相色谱仪,以进样量(X)对峰面积(Y)进行线性回归,绘制标准曲线。结果见表1。
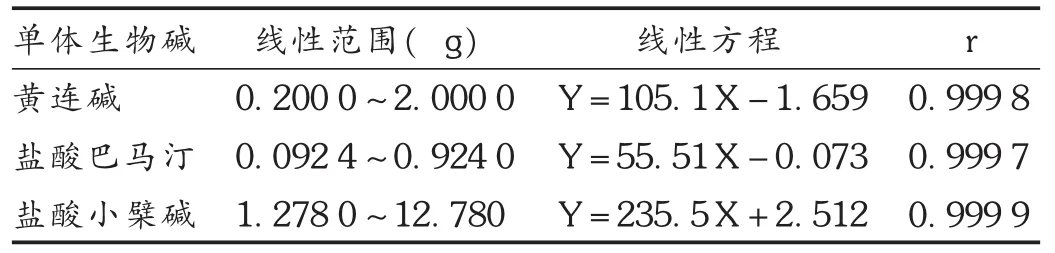
表1 3个单体生物碱的线性回归方程
精密度试验:精密吸取同一对照品溶液10 μL,按拟订色谱条件连续进样6次,记录峰面积。结果黄连碱、盐酸巴马汀、盐酸小檗碱的 RSD分别为1.2%,1.7%,0.8%(n=6),表明仪器精密度良好。
稳定性试验:取用云南黄连(批号为S4,购自成都市荷花池中药材市场)制备的同一供试品溶液,于0,2,4,8,12 h时进样10 μL。结果黄连碱、盐酸巴马汀、盐酸小檗碱的 RSD分别为0.8%,1.1%,0.6%(n=5),表明供试品溶液在12 h内稳定。
重复性试验:取用云南黄连(批号为S4,购自成都市荷花池中药材市场)0.1 g,依法平行制备6份供试品溶液,按拟订色谱条件进样测定。结果黄连碱、盐酸巴马汀、盐酸小檗碱含量的 RSD分别为 1.4%,1.8%,0.9%(n=6),表明方法重复性好。
加样回收试验:精密称取已知含量的云南黄连(批号为S4,购自成都市荷花池中药材市场)0.05 g,共6份,每份样品加入适量黄连碱对照品10 mL、盐酸巴马汀对照品10 mL、盐酸小檗碱对照品10 mL,挥干。按供试品溶液制备方法制备溶液,依法测定峰面积并计算含量。结果黄连碱、盐酸巴马汀、盐酸小檗碱平均回收率为98.61%,97.35%,99.03%,RSD分别为1.28%,1.52%,1.19%(n=6)。
2.1.4 样品含量测定
取10批云连,按2.1.2项下方法各制备3份供试品溶液,用0.22 μm微孔滤膜过滤后,进样量10 μL,依法测定峰面积,以外标两点法计算云南黄连中黄连碱、盐酸巴马汀、盐酸小檗碱的含量。结果见表2。
2.2 总生物碱含量测定[6]
2.2.1 溶液制备
称取盐酸小檗碱对照品适量,精密称定,加甲醇制成0.639 g/L的溶液,即得对照品贮备溶液;精密量取2 mL,置25 mL容量瓶,用甲醇稀释至刻度,即得对照品溶液。称取本品粉末约0.1 g,精密称定,置具塞锥形瓶中,加1%盐酸甲醇溶液50 mL,称定质量,超声提取60 min,放冷,补足失重,过滤,取滤液1.0 mL,置25 mL容量瓶中,加甲醇定容至刻度,摇匀,4 000 r/min离心10 min,即得供试品溶液。以相应的试剂为空白溶液。
2.2.2 标准曲线制备
精密吸取2.2.1项下对照品溶液1,2,3,4,5 mL,置10 mL容量瓶中,用甲醇定容至刻度,以相应的试剂为空白,照 2010年版《中国药典(一部)》附录ⅤA紫外-可见光光度法,于349 nm波长处测定吸光度(A),以 A为纵坐标、盐酸小檗碱质量浓度(C)为横坐标绘制标准曲线,得回归方程 A=0.068C-0.019 3,r=0.999 2 (n=5)。结果表明,盐酸小檗碱质量浓度在 5.112~25.560 μg/mL范围内与吸光度呈良好的线性关系。
2.2.3 样品含量测定
取2.2.1项下供试品溶液,照2010年版《中国药典(一部)》附录ⅤA紫外-可见光光度法,依法测定计算。结果见表2。
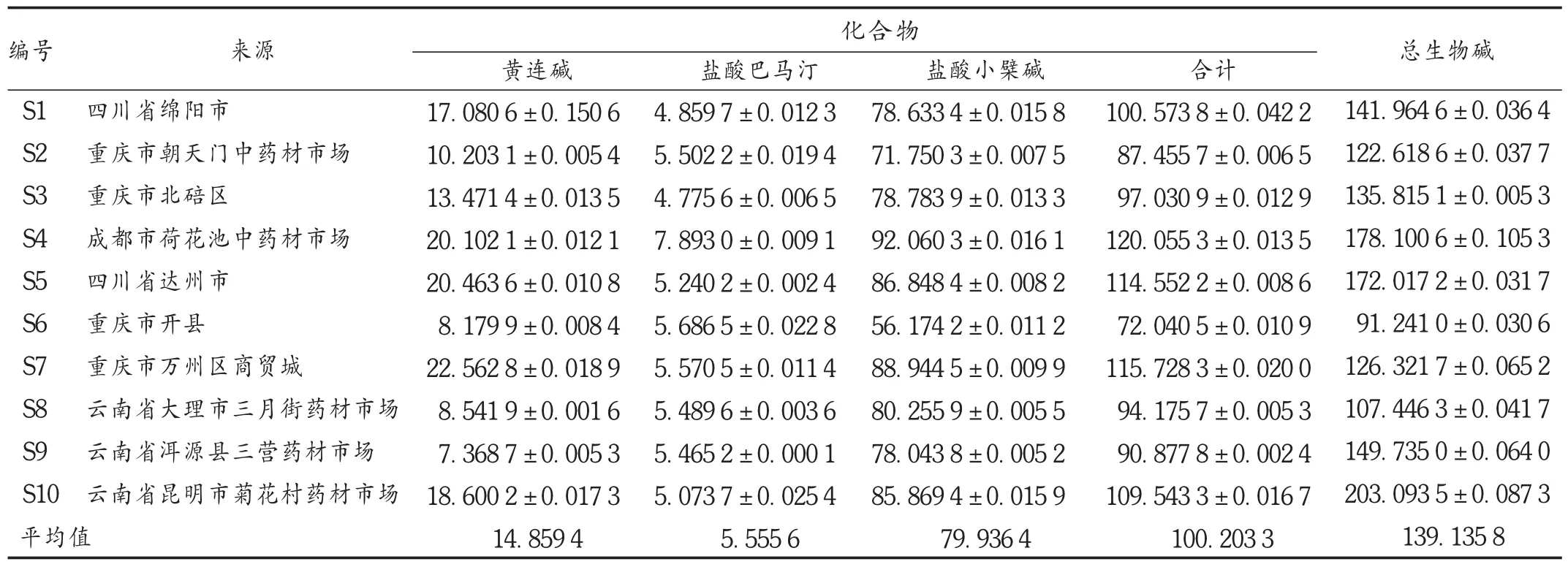
表2 不同商品来源云南黄连中生物碱含量(mg/g,n=3)
2.3 聚类分析
分别采用不同商品来源云连中生物碱含量测定结果进行聚类分析。采用SPSS统计软件的Ward法,选取平方Euclidean距离作为样品度量标准,对10批样品进行系统聚类分析,绘出树状图。结果见图2。
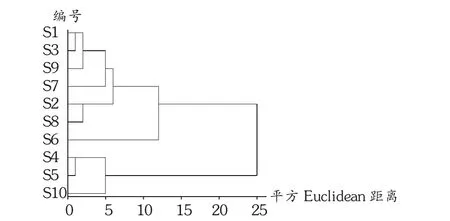
图2 高效液相色谱法测定不同商品来源云南黄连中生物碱含量的聚状分析树状图
根据聚类分析结果,将10批样品分为3类:第1类有6批药材,即S1~S3及S7~S9,此类药材中黄连碱、盐酸巴马汀、盐酸小檗碱及总生物碱(UV法测定)含量均低于均值,第2类有1批药材,即S6,此类药材中黄连碱和总生物碱(UV法测定)低于均值,其中总生物碱远低于均值,盐酸巴马汀和盐酸小檗碱略高于均值;第 3类有 3批药材,即 S4,S5,S10,此类药材中黄连碱、盐酸巴马汀、盐酸小檗碱及总生物碱(UV法测定)含量均高于均值。结果见表3。

表3 不同商品来源云连中生物碱含量聚类分析的不同组别各组分的平均含量(mg/g,n=3)
3 讨论
目前,市场上的黄连药材中,以雅连、味连为主,云连栽培规模小、产量低,以野生为主[7]。本试验中收集不同地区商品药材,测量其总生物碱含量,同时测定盐酸小檗碱、黄连碱、盐酸巴马汀在各批次样品中的含量。结果表明,不同地区经销的云连生物碱含量存在显著性差异,特别是黄连碱含量差异较大。
黄连类药材的有效成分主要为生物碱,化学成分复杂。在试验过程中,通过优化提取溶剂、提取时间,调整流动相、流速,更换色谱柱、变化柱温等条件,确定了本研究中样品的提取条件和色谱方法。结果表明,本方法简单易行、准确灵敏,重复性好,可用于评价不同商品来源云连及相关产品的品质。
本试验结果表明,市售云连来源复杂,质量参差不齐。造成市售云连质量差异的因素可能与来源、产地和生长年限等有关[8-9]。人工种植云连作为市售云连药材的主要来源,其种植来源问题亟需解决,种植药材质量也需要进一步提升,才能从基源上确保云连的临床用药安全和疗效。中药材市场作为商品云连流通的一个关键节点,对云连质量的影响不可忽视。建议相关部门应该更严格管理药材市场,控制好云连的市场准入关口,尽量消除商品云连的掺伪现象,从而保证云连品质。
[1]中国科学院昆明植物研究所.云南植物志:11卷[M].北京:科学出版社,2000:180-183.
[2]国家药典委员会.中华人民共和国药典(第二增补本)[M].北京:中国医药科技出版社,2013:97-98.
[3]傅国立.中国植物红皮书-稀有濒危物[M].北京:科学出版社,1992:522.
[4]王永占,沈 勇,史晓倩.HPLC法同时测定云黄连中四种生物碱的含量[J].中国药师,2013,16(7):947-949.
[5]彭 福,瞿显友,钟国跃,等.HPLC法测定黄连不同部位中6个生物碱[J].中草药,2012,43(3):509-512.
[6]赵梓辰,杨 丽,李雪莲,等.正交设计法优选黄连总生物碱提取测定方法[J].中药与临床,2015,6(2):28-29.
[7]杨艳娟,谢世清,杨生超,等.云南黄连的研究进展[J].安徽农业科学,2011,39(23):14 037-14 038.
[8]黄 骥,裴盛基,张明宇,等.云南黄连的生物学、生态学特性与地理分布研究[J].云南植物研究,2004,26(3):255-266.
[9]黄 骥,龙春林.云南黄连的传统种植及其在生物多样性保护中的价值[J].生物多样性,2006,14(1):79-86.
Quality Assessment of Coptis Teeta Wall.from Different Markets
Zhang Dewei1,Feng Haixia2,Xie Hanlin3,Ding Bo3,Mu Lamei4
(1.Wanzhou Institute for Drug and Food Control,Chongqing,China 404000; 2.Chongqing Institute for Drug and Food Control,Chongqing,China 401121; 3.Chongqing Three Gorges University,Chongqing,China 404000; 4.Chongqing University of Arts and Sciences,Chongqing,China 402160)
Objective To establish a quantitative method for Coptisine,Palmatine hydrochloride,Berberine hydrochloride,Total alkaloid in Coptis teeta by HPLC and UV,and to compare the quality of products from different commercial sources.Methods The HPLC method used venusil MP C18chromatographic column(250 mm×4.6 mm,5 μm),mobile phase of acetonitrile to 0.2% glacial acetic acid (triethylamine pH=5.05),gradient elution,detection wavelength of 345 nm;349 nm wavelength UV method in the determination of total alkaloids of absorbance.There were 10 samples detective and cluster analysis.Results The linear range of coptisine,palmatine hydrochloride,berberine hydrochloride were 0.200 0-2.000,0.092 4-0.924 0,1.278 0-12.780 0 μg(r≥0.999 5).The average recovery rates were 98.61%,97.35%,99.03%,RSD=1.28%,1.52%,1.19%(n=6).The UV method measured the mass concentration of total alkaloids showed a good linear relationship with absorbance in the range of 5.112-25.560 μg/mL.10 batches of different origin teeta herbs could be divided into 3 categories by cluster analysis.There were significant differences between different areas of goods teeta alkaloid content.Conclusion The method is accurate,reliable,repeated,which could be used in judge the quality of commercial Coptis teeta.
Coptis teeta;coptisine;palmatine hydrochloride;berberine hydrochloride;total alkaloid;RP-HPLC;UV
R284.1;R282.71
A
1006-4931(2016)03-0004-04
张德伟(1979-),男,汉族,大学本科,主管中药师,主要从事中药材品质研究及成分分析工作,(电话)023-58152381。
2015-10-14)
*重庆三峡学院2014年度大学生创新性实验计划项目,项目编号:2014020。

