铜暴露对草鱼幼鱼代谢行为的影响
袁 喜,黄应平,靖锦杰,蒋 清,胥 焘,涂志英,李为民(1.三峡库区生态环境教育部工程研究中心(三峡大学),湖北宜昌443002;2.三峡地区地质灾害与生态环境湖北省协同创新中心(三峡大学),湖北宜昌443002;3.中国科学院水生生物研究所,武汉430072)
铜暴露对草鱼幼鱼代谢行为的影响
袁喜1,2,3,黄应平1,2*,靖锦杰1,2,蒋清1,2,胥焘1,2,涂志英1,2,李为民1,2
(1.三峡库区生态环境教育部工程研究中心(三峡大学),湖北宜昌443002;2.三峡地区地质灾害与生态环境湖北省协同创新中心(三峡大学),湖北宜昌443002;3.中国科学院水生生物研究所,武汉430072)
摘要:为了探讨水体中铜污染对鱼的生态毒理效应和游泳能力的影响,在实验室条件下,测定了铜暴露草鱼(Ctenopharyngodon idella)幼鱼半致死浓度、不同浓度铜暴露(0、0.025、0.050、0.075、0.10 mg·L-1)96 h后组织(肝、鳃、肌肉)铜累积量、相对临界游泳速度(Ucrit)以及耗氧率(MO2)。结果表明:与对照组比较,铜暴露对组织(肝、鳃、肌肉)铜累积量无显著影响(P>0.05),铜对草鱼幼鱼的安全浓度为0.008 mg·L-1。铜暴露草鱼幼鱼相对临界游泳速度受抑制显著(P<0.05),不同浓度暴露后Ucrit分别较对照组下降了18.4%、21.8%、33.8%和38.1%。随着游泳速度的增加,其速度-代谢率关系为MO2=a+b×Uc,随着暴露浓度增加,速度参数c值增加,不同浓度铜暴露后c分别比对照组增加了37.78%、33.33%、56.67%和61.11%,表明游泳能量利用率下降。铜暴露导致草鱼幼鱼有氧代谢范围增加,0.1 mg Cu·L-1时有氧代谢范围比对照组增加了37.48%。铜暴露对草鱼幼鱼的游泳能力以及氧代谢行为产生影响,尤其是导致游泳效率降低、抑制游泳能力。
关键词:草鱼;铜;游泳能力;耗氧率
袁喜,黄应平,靖锦杰,等.铜暴露对草鱼幼鱼代谢行为的影响[J].农业环境科学学报, 2016, 35(2):261-265.
铜类杀菌药物及肥料的使用造成养殖水体重金属铜污染,并通过生物富集和生物放大效应对水生态系统产生重要影响,特别是对鱼类等水生生物有较强的毒性[1-2]。作为水生生物食物链的顶层类群,鱼体内污染物水平和鱼对污染物产生的生物效应可客观反映水环境的状况。研究表明长江沉积物中重金属铜的富集系数较高[3],关于重金属铜在草鱼(Ctenopharyngodon idella)组织中的积累与分布和毒性效应的研究文献报道较多,铜对草鱼存活率和生长[4]、体内酶活性、抗氧化功能、遗传物质[5]等方面的影响已有相关研究。但目前关于铜暴露导致草鱼幼鱼代谢及行为变化的研究尚鲜见报道。
鱼类生理生态行为对环境因子变化的适应性最先表现为行为上的改变[6],临界游泳速度(Ucrit)在某种程度上反映了动物的有氧运动能力,代谢率范围(Metabolicraterange)用于评价鱼类的有氧代谢能力[7-8]。本文通过研究不同浓度水体铜暴露对草鱼幼鱼游泳能力与代谢范围以及组织(鳃、肝、肌肉)铜累积量的影响,考察其幼鱼因水体铜浓度变化而引发的运动和代谢方面的改变,从而评估铜污染对草鱼幼鱼潜在的生态毒性,为水生态毒理学基础研究提供参考,对水体重金属污染、水产品养殖及环境治理决策具有实际意义。
1 材料与方法
1.1实验材料
实验用草鱼幼鱼于2015年1月购于宜昌养殖场。实验前将鱼在实验室鱼缸(420 L)中驯化2周。每2 d投喂饲料1次,饲料成分:蛋白质>38%,脂肪>5%,纤维素<5%,灰分<12%,湿度<11%。驯养用水为曝气后的自来水,驯养期间充气使水体溶氧水平接近饱和,日换水量约为水体的1/3,自然水温(15±1)℃,自然光照。在实验前48 h停止喂饵料。
驯养结束后,选取健康幼鱼60尾,随机平均分配至各浓度梯度组,实验鱼体长、体重参数如表1。根据急性毒性试验结果,本研究共设5个铜(Cu2+)浓度梯度,分别为0、0.025、0.050、0.075、0.10 mg·L-1,暴露时间为96 h。暴露期间不投饵,每日定时换水并补充相应浓度的硫酸铜溶液以保持水体铜浓度基本恒定,实验条件与驯养期间保持一致。

表1 草鱼幼鱼的体长、体重参数(平均值±标准差)Table 1 Body length and weight parameters of juvenile grass carp(mean±SD)
1.2实验方法
采用鱼类游泳能力测定装置[9]测定草鱼Ucrit。将每个处理实验鱼在暴露96 h后转入游泳能力测定装置中驯化2 h(流速为0.1 m·s-1)。适应结束后,采用逐步递增法,直至实验鱼运动疲劳,其判定标准为:实验鱼被水流冲到游泳区后面筛网上贴网不能游泳,则视为疲劳[9]。Ucrit计算公式:

式中:Ucrit为临界游泳速度,BL·s-1;U1为实验鱼所能完成的最大游泳速度(实验鱼疲劳前的速度),BL·s-1;U2为速度增量,BL·s-1;T1为在最大游泳速度下未能完成设定历时的实际持续时间,min;T2为设定时间步长,min。
实验中时间步长T2=30min,流速增量U2=1 BL·s-1。
实验过程中每间隔5 min测定一次水中溶解氧含量,利用充氧泵进行内外水槽水的交换,使密封水槽溶解氧量不低于饱和溶解氧浓度的75%。游泳运动代谢率的计算公式:

式中:MO2为标准体重的运动代谢率,mg O2·h-1· kg-1;Sf为实验鱼游泳时溶氧值随时间变化斜率的绝对值(表观耗氧量);S0是无实验鱼存在的溶氧值随时间变化斜率的绝对值(细菌耗氧量);60为时间常数,min·h-1;V是实验水体系统总体积,L;m为鱼体重,kg。
代谢范围为最大耗氧代谢率与最小耗氧率的差值。
鱼体组织Cu2+含量测定:将草鱼幼鱼用丁香酚溶液麻醉后,解剖分离出鳃、肝脏、肌肉组织并于-40℃保存。将各组织样本(以相同处理下12尾鱼组织为一个样本,分3组,对照组6尾鱼)称取2 g(湿重)并置于50 mL聚四氟乙烯消解罐中,加入4 mL HNO3(65%)过夜,然后加入2 mL HClO4(70%),电热板上150℃加热,蒸发至近干,冷却后加适量0.1% HNO3,转移到50 mL容量瓶,0.1%HNO3定容。采用SPEC TRA-240FS-石墨炉火焰型原子吸收分光光度计(Varian,美国)测定组织铜含量。利用标准物质法校准(DORM-2 National Research Council,Canada),回收率97.9%~108.3%。组织中重金属含量用mg·kg-1(湿重,平均值±标准误)表示。
1.3数据处理
实验数据利用SPSS 20.0进行单因素方差分析(One-way ANOVA,Duncan post hoc test)并检验差异显著性。统计数据表示为平均值±标准误(Mean±S.E),显著性水平为P<0.05。
2 结果与分析
2.1草鱼幼鱼鳃、肝脏、肌肉组织铜累积量特征
采用静水急性毒性试验法测定铜对草鱼幼鱼的毒性,统计铜污染暴露24、48、72、96 h后草鱼幼鱼死亡率,直线内插法计算获得LC50分别为0.12、0.094、0.093、0.078 mg·L-1,根据96 h LC50×0.1计算安全浓度为0.008 mg·L-1。急性铜暴露下草鱼幼鱼鳃(F=2.04;P=0.16)、肝脏(F=1.99;P=0.17)和肌肉(F=1.99;P= 0.17)组织中铜累积量各处理间差异不显著。铜暴露后幼鱼组织中Cu2+的累积量如图1所示。

图1 铜暴露后草鱼幼鱼鳃、肝脏、肌肉组织铜累积量Figure 1 Gill,liver and muscle copper contents in juvenile grasscarp after exposed to different copper concentrations
2.2铜暴露对草鱼幼鱼临界游泳速度的影响
铜暴露对草鱼幼鱼临界游泳速度的影响显著(F=36.21,P<0.001),如图2所示。随着铜浓度增加,草鱼幼鱼相对临界游泳速度逐渐下降,当铜浓度为0.075~0.10 mg·L-1时,草鱼幼鱼相对临界游泳速度显著降低(P<0.05)。对照组相对临界游泳速度为(6.83± 0.24)BL·s-1,0.025、0.050、0.075、0.10 mg·L-1暴露组分别为(5.58±0.19)、(5.34±0.18)、(4.53±0.11)、(4.23± 0.05)BL·s-1,为对照组的81.61%、78.19%、66.24%和61.90%。
2.3铜暴露对草鱼幼鱼耗氧率及活动代谢的影响

图2 铜暴露对草鱼幼鱼相对临界游泳速度的影响Figure 2 Effect of copper exposure on Ucritin juvenile grass carp
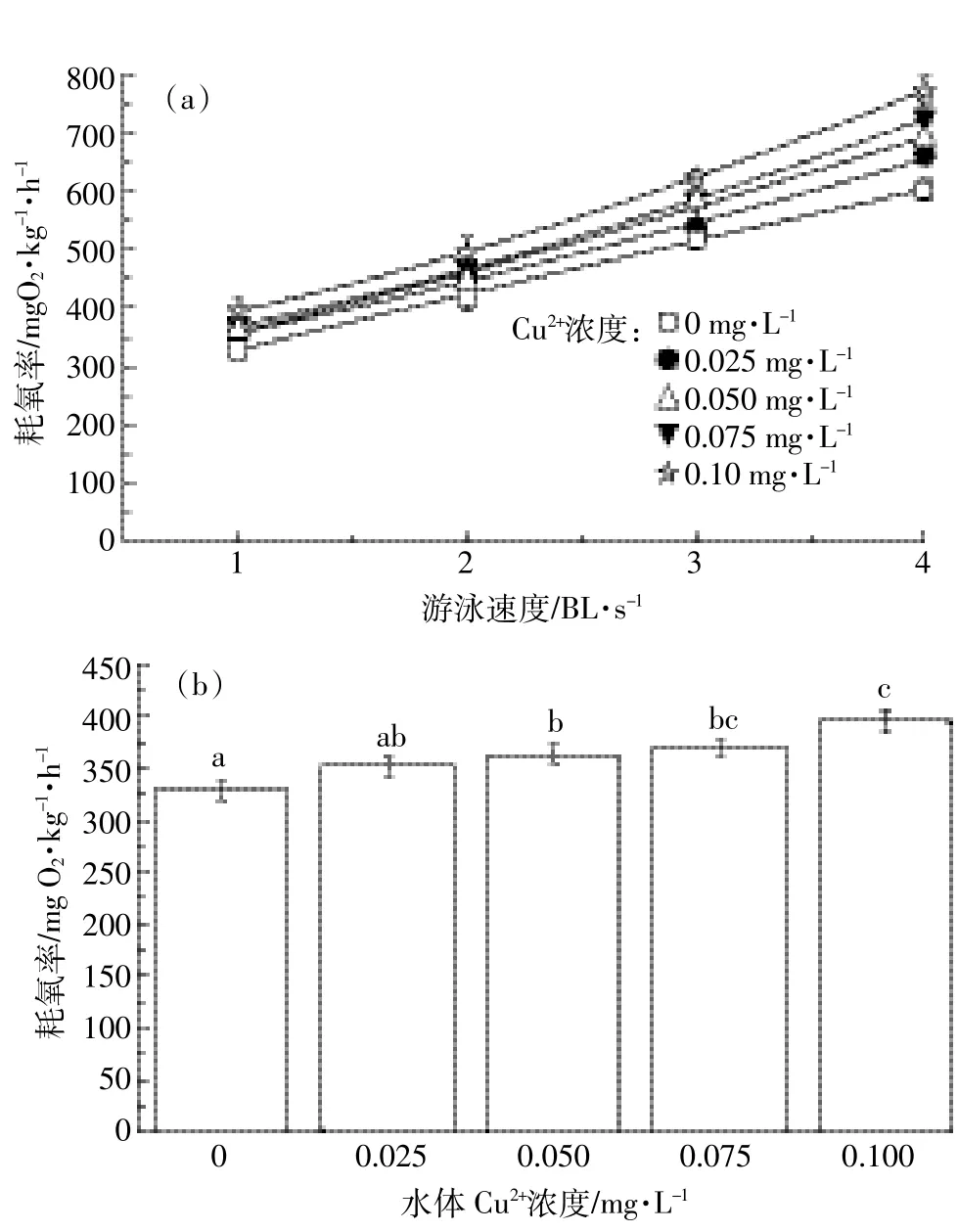
图3 铜暴露对草鱼幼鱼代谢率(a)及活动代谢(b)范围的影响Figure 3 Effect of copper exposure on metabolic rate(a)and metabolic rate range(b)of juvenile grass carp
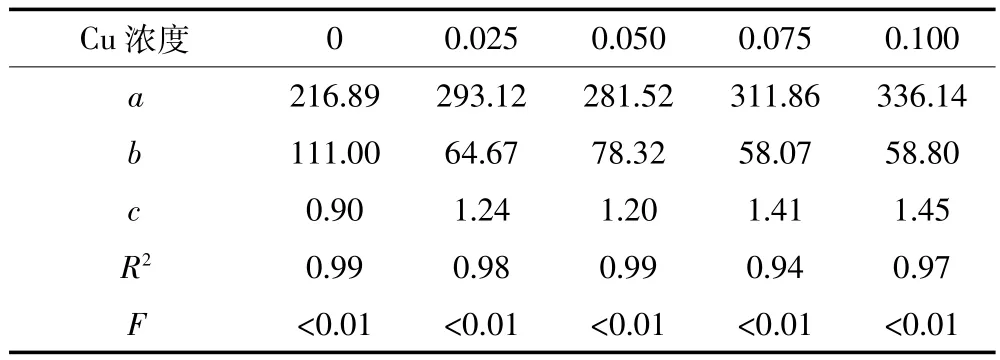
表2 不同铜暴露处理下草鱼幼鱼游泳速度与代谢率关系Table 2 Relationship between swimming speed and oxygen metabolic rate under different concentrations of copper exposed
图3a显示,随着游泳速度的增大(1~4 BL·s-1),草鱼耗氧代谢率呈增加趋势。游泳速度与草鱼幼鱼代谢率可以用指数关系MO2=a+b×Uc表示(a、b、c为相关参数),其结果见表2。随着暴露浓度增加,速度参数c值增加,不同浓度铜暴露使c分别比对照组增加了37.78%、33.33%、56.67%和61.11%。图3b显示,铜暴露对草鱼幼鱼有氧代谢范围影响显著(F=7.19,P= 0.005),随着暴露浓度增加,有氧代谢范围增大,浓度为0.10 mg·L-1时有氧代谢范围比对照组增加了37.48%。
3 讨论
在评价重金属污染安全时,污染物毒性以及污染物对鱼类行为影响的量化很重要,但是由于不同区系生物受生活环境等因素的影响,如不同物种对铜的耐受性和敏感度存在很大的差异[10]。如铜对广东鲂幼鱼(Megalobramaterminalis)安全浓度为0.01 mg·L-1[11],而对中华鲟(Acipenser sinensis Gray)幼鱼的安全浓度为0.002 mg·L-1[12],远低于中国渔业水质标准(铜的最高容许质量浓度为0.01 mg·L-1)。本研究中Cu2+对草鱼幼鱼安全浓度为0.008 mg·L-1,根据有毒物质对鱼类的毒性标准[13],可判断Cu2+对草鱼幼鱼具有高毒性。鳃是鱼类呼吸滤食的主要器官,直接暴露在重金属环境中,因而对重金属的积累较大;肝脏是金属硫蛋白合成的主要场所,肝脏等组织中重金属积累明显;相对其他组织器官而言,肌肉代谢较慢,而且没有直接暴露于重金属。因此,鱼类对重金属的累积量为肝脏>鳃>肌肉[14-15]。铜暴露导致鳃和肝脏组织铜硫蛋白络合物(Cu-MT)的含量明显增加,加速了Cu2+在鱼体内的代谢进程,多余的Cu2+结合蛋白进入血液循环,并排泄到体外[16]。因此急性铜暴露后,鱼体肝脏、鳃和肌肉组织重金属累积量无显著差异。
鱼类呼吸系统的变化能迅速反映出机体自身机能的变化,它们对外环境变化敏感,是反映机体机能状态的重要指标。代谢率和代谢范围的测定能在一定程度上反映鱼类有氧运动的能力,对鱼类行为测定具有重要的意义[17-18]。随着暴露浓度增加,草鱼幼鱼呼吸代谢作用增强,有氧代谢范围显著增加(F=7.19,P<0.01)。Cu2+等重金属产生毒性效应的途径之一是诱导活性氧的产生[19]。在正常生理状态下,鱼类抗氧化系统能够清除机体代谢所产生的活性氧;在其暴露于一定浓度污染物时,会诱导活性氧产生,导致相关抗氧化酶活性发生变化,对机体产生损伤[20]。低浓度Cu2+能够诱导鳃组织补偿(细胞增生、黏液分泌)反应[21],阻碍Cu2+的进入,降低鳃损害程度[22],而且铜暴露会刺激鳃膜以及口腔上皮,导致鱼大量更频繁地移动,使耗氧率增加[23]。本研究与其相似,低浓度铜暴露诱导产生补偿性反应,草鱼幼鱼呼吸代谢作用增强。耗氧率和游泳速度呈幂函数关系MO2=a+b×Uc,其中反映游泳效率的速度常数c值越大游泳效率越低[9]。实验中c值变化趋势随着暴露浓度的增加而上升,即铜暴露导致游泳效率下降。
研究表明,外源化学物质诱导所产生的解毒作用引起鱼类代谢水平升高,能量大量消耗导致活动能力降低[24-25]。重金属铜暴露使草鱼幼鱼能量的过量消耗,导致游泳能力的降低,不同浓度Cu2+暴露后Ucrit分别较对照组下降了18.4%、21.8%、33.8%和38.1%。另外,研究表明重金属暴露可能导致神经细胞内钙超负荷[26],甚至造成中枢神经系统结构损伤[27],影响神经细胞功能活动,阻碍了神经-肌肉突出的神经传导[28],影响肌肉收缩。因此,Cu2+暴露导致草鱼幼鱼临界游泳速度降低,也可能是神经系统损伤引起的。环境胁迫产生的应激行为反应机理十分复杂,涉及神经系统、内分泌系统及免疫系统的一系列活动,而且环境因素和重金属之间的相互作用对不同年龄鱼类运动和代谢行为影响的研究,在实际应用中具有更重要的生产实践意义,有待进一步的研究。
4 结论
(1)Cu2+对草鱼幼鱼具有较高毒性,安全浓度为0.008 mg·L-1,草鱼幼鱼对Cu2+反应灵敏。急性铜暴露草鱼肝脏、鳃和肌肉组织铜累积量无显著差异。
(2)低浓度Cu2+暴露诱导刺激鳃膜以及口腔上皮产生应激性反应,导致草鱼幼鱼大量更频繁地运动,呼吸代谢作用增强,能量过量消耗,游泳效率下降,游泳能力降低。
参考文献:
[1] Hu M Y, Ye Y F, Xue L Y, et al. Tissue-specific metabolic responses of cyprinus flammans to copper[J]. Archives of Environmental Contamination & Toxicology, 2015, 69(1):112-122.
[2] Eyckmans M, Celis N, Horemans N, et al. Exposure to waterborne copper reveals differences in oxidative stress response in three freshwater fish species[J]. Aquatic Toxicology, 2011, 103(1/2):112-120.
[3]单丽丽,袁旭音,茅昌平,等.长江下游不同源沉积物中重金属特征及生态风险[J].环境科学, 2008, 29(9):2399-2404. SHAN Li-li, YUAN Xu-yin, MAO Chang-ping, et al. Characteristics of heavy metals in sediments from different sources and their ecological risks in the lower reaches of the Yangtze River[J]. Environment Science, 2008, 29(9):2399-2404.
[4] Hamed N, Shima H, Esmail G, et al. Effect of sublethal doses of copper on growth performance and survival rate of grass carp(Ctenopharyngodon idella)[J]. American-Eurasian Journal of Toxicological Sciences, 2015, 4(3):138-142.
[5] Zhu Q L, Zhi L, Zhuo M Q, et al. In vitro exposure to copper influences lipid metabolism in hepatocytes from grass carp(Ctenopharyngodon idellus)[J]. Fish Physiology & Biochemistry, 2014, 40(2):595-605.
[6] Hansen J A, Woodward D F, Little E E, et al. Behavioral avoidance:Possible mechanism for explaining abundance and distribution of trout species in a metal-impacted river[J]. Environmental Toxicology & Chemistry, 1999, 18(2):313-317.
[7] Lee C G, Farrell A P, Lotto A, et al. Excess post-exercise oxygen consumption in adult sockeye(Oncorhynchus nerka)and coho(O. kisutch)salmon following critical speed swimming[J]. Journal of Experimental Biology, 2003, 206(18):3253-3260.
[8] Holt R E. Climate change in fish:Effects of respiratory constraints on optimal life history and behaviour[J]. Biology Letters, 2015,11(2). doi:10. 1098/rsbl. 2014. 1032.
[9] Tu Z, Li L, Yuan X, et al. Aerobic swimming performance of juvenile Largemouth bronze gudgeon(Coreius guichenoti)in the Yangtze River [J]. Journal of Experimental Zoology Part A:Ecological Genetics and Physiology, 2012, 317(5):294-302.
[10]王振,金小伟,王子健.铜对水生生物的毒性:类群特异性敏感度分析[J].生态毒理学报, 2014, 9(4):640-646. WANG Zhen, JIN Xiao-wei, WANG Zi-jian. Taxon-specific sensitivity differences of copper to aquatic organisms[J]. Asian Journal of Ecotoxicology, 2014, 9(4):640-646.
[11]曾艳艺,赖子尼,杨婉玲,等.铜和镉对珠江天然仔鱼和幼鱼的毒性效应及其潜在生态风险[J].生态毒理学报, 2014, 9(1):1673-5897. ZENG Yan-yi, LAI Zi-ni, YANG Wan-ling, et al. The toxicities and potential ecological effects of copper and cadmium to natural fish larvae and juveniles from the Pearl River[J]. Asian Journal of Ecotoxicology, 2014, 9(1):1673-5897.
[12]姚志峰,章龙珍,庄平,等.铜对中华鲟幼鱼的急性毒性及对肝脏抗氧化酶活性的影响[J].中国水产科学, 2010, 17(4):731-738. YAO Zhi-feng, ZHANG Long-zhen, ZHUANG Ping, et al. Effects of antioxidant enzyme in liver and acute toxicity of Cu2+on juvenile Chinese sturgeon[J]. Journal of Fishery Sciences of China, 2010, 17(4):731-738.
[13]张志杰,张维平.环境污染生物监测与评价[M].北京:中国环境科学出版社, 1991. ZHANG Zhi-jie, ZHANG Wei-ping. Pollution of the environment monitoring and evaluation[M]. Beijing:China Environmental Science Press, 1991.
[14]周新文,朱国念, Jilisa Mwalilino,等.重金属离子Cu、Zn、Cd的相互作用对Pb在鲫鱼组织中积累的影响[J].农业环境科学学报, 2002, 21(1):23-25. ZHOU Xin-wen, ZHU Guo-nian, Jilisa Mwalilino, et al. Effect of the interaction of copper, zinc and cadmium on the accumulation of lead in the tissues of the Carassius auratus[J]. Journal of Agro-Environment Science, 2002, 21(1):23-25.
[15]周彦锋,陈家长,杨光,等.重金属镉胁迫下鲫鱼不同组织中金属硫蛋白的动态变化[J].安全与环境学报, 2008, 8(3):18-21. ZHOU Yan-feng, CHEN Jia-zhang, YANG Guang, et al. On the dynamic variations of metallothionein in the different tissues of Carassius auratus due to the exposure of different concentrations of cadmium[J]. Journal of Safety and Environment, 2008, 8(3):18-21.
[16] Ghedira J, Jebali J, Bouraoui Z, et al. Metallothionein and metal levels in liver, gills and kidney of Sparus aurata exposed to sublethal doses of cadmium and copper[J]. Fish Physiology & Biochemistry, 2010, 36 (1):101-107.
[17] Palstra A P, Mes D, Kusters K, et al. Forced sustained swimming exercise at optimal speed enhances growth of juvenile yellowtail kingfish (Seriolalalandi)[J]. Frontiers in Physiology, 2014, 5:506-506.
[18] Yan G J, He X K, Cao Z D, et al. Effects of fasting and feeding on the fast-start swimming performance of southern catfish Silurus meridionalis[J]. Journal of Fish Biology, 2015, 86(2):605-614.
[19] Regoli F, Nigro M, Bertoli E, et al. Defenses against oxidative stress in the Antarctic scallop Adamussium colbecki and effects of acute exposure to metals[J]. Hydrobiologia, 1997, 355(1-3):139-144.
[20]孙翰昌,丁诗华,代梅,等. Cu2+对中华倒刺鲃超氧化物歧化酶活性的影响[J].西南大学学报(自然科学版), 2005, 27(5): 709-712. SUN Han-chang, DING Shi-hua, DAI-Mei, et al. Effect of copper on the activity of SOD(superoxide dismutase)in Barbodes(Spinibarbus sinensis)[J]. Journal of Southwest Agriculture University(Natural Science), 2005, 27(5):709-712.
[21] Arellano J M, Storch V, Sarasquete C. Histological changes and copper accumulation in liver and gills of the Senegal sole, Solea senegalensis [J]. Ecotoxicol Environ Safety, 1999, 44(1):62-72.
[22] Ortiz J B, Gonzalez de Canales M L, Sarasquete C. Quantification and histopathological alterations produced by sublethal concentrations of copper in Fundulus heteroclitus[J]. Ciencias Marinas, 1999, 25(1):119-143.
[23] Ohara J. Alterations in oxygen consumption by bluegills exposed to sublethal treatment with copper[J].Water Research,1971, 5(6):321-327.
[24] Hagenaars A, Vergauwen L, Benoot D, et al. Mechanistic toxicity study of perfluorooctanoic acid in zebrafish suggests mitochondrial dysfunction to play a key role in PFOA toxicity[J]. Chemosphere, 2013, 91(6):844-856.
[25] Xia J G, Nie L J, Mi X M, et al. Behavior, metabolism and swimming physiology in juvenile Spinibarbus sinensis exposed to PFOS under different temperatures[J]. Fish Physiology & Biochemistry, 2015, 41(5):1293-1304.
[26]马军,斯颀,叶广俊.镉对神经细胞内游离钙浓度的影响[J].中国公共卫生学报, 1996, 4(1):21-23. MA Jun, SI Qi, YE Guang-jun. Effect of cadmium on intracellular free Ca2+concentration of nerve cell[J]. Chinese Journal of Public Health, 1996, 4(1):21-23.
[27] Lasley S M, Gilbert M E. Impairment of synaptic function by exposure to lead[M]//Evelyn T C. Methods in Pharmacology & Toxicology. Totowa N J: Humana Press, 2004:217-241.
[28] López E, Figueroa S, Oset-Gasque M J, et al. Apoptosis and necrosis:Two distinct events induced by cadmium in cortical neurons in culture [J]. British Journal of Pharmacology, 2003, 138(5):901-911.
YUAN Xi, HUANG Ying-ping, JING Jin-jie, et al. Effect of copper exposure on metabolism behavior of juvenile grass carp(Ctenopharyngodon idella)[J]. Journal of Agro-Environment Science, 2016, 35(2):261-265.
Effect of copper exposure on metabolism behavior of juvenile grass carp(Ctenopharyngodon idella)
YUAN Xi1,2,3, HUANG Ying-ping1,2*, JING Jin-jie1,2, JIANG Qing1,2, XU Tao1,2, TU Zhi-ying1,2, LI Wei-min1,2
(1. Innovation Center for Geo-Hazards and Eco-Environment in Three Gorges Area, China Three Gorges University, Yichang 443002, China;2.Engineering Research Center of Eco-Environment in Three Gorges Reservoir Region, Ministry of Education, China Three Gorges University, Yichang 443002, China;3.Institute of Hydrobiology, Chinese Academy of Sciences, Wuhan 430072, China)
Abstract:In this investigation, the eco-toxicological effects of copper on the swimming capability of juvenile grass carp(Ctenopharyngodon idella)were measured. Copper concentrations were measured in the gill, liver and muscle tissues of juvenile grass carp after a 96 h exposure to a range of copper concentrations; 0, 0.025, 0.050, 0.075 mg·L-1and 0.10 mg·L-1. Relative critical swimming speed(Ucrit)and metabolic rate(MO2)range were also measured after exposure. While the exposure did not significantly affect tissue concentrations(P>0.05), it did significantly affect Ucritand MO2range(P<0.05). The safe concentration for juvenile grass carp was 0.008 mg Cu·L-1. Compared to the control group, Ucritdecreased by 18.4%, 21.8%, 33.8% and 38.1% after 96 h exposure to 0.025, 0.05, 0.075 mg Cu·L-1and 0.10 mg Cu·L-1, respectively. The oxygen consumption rate increased exponentially with swimming speed; MO2=a+b×Uc. The speed parameter, c, increased with copper concentration by 37.78%, 33.33%, 56.67% and 61.11%, indicating a decrease in swimming efficiency. MO2range increased by 37.48% after exposure to 0.10 mg Cu·L-1copper. Exposure to copper polluted environment significantly affects the metabolism and swimming performance of juvenile grass carp, especially resulted in the decrease of swimming efficiency, inhibited swimming ability.
Keywords:Ctenopharyngodon idella; copper; swimming performance; oxygen consumption rate
*通信作者:黄应平E-mail:chem_ctgu@126.com
作者简介:袁喜(1987—),男,湖北仙桃人,博士研究生,主要从事水污染控制及水生态研究。E-mail: chem_ctgu@126.com
基金项目:国家自然科学基金(51309140);国家水专项(2012ZX07104-003-04);湖北省创新群体项目(2015CFA021)
收稿日期:2015-09-26
中图分类号:X503.225
文献标志码:A
文章编号:1672-2043(2016)02-0261-05
doi:10.11654/jaes.2016.02.008

