突破高频考点
——pH
云南 李海春
突破高频考点
——pH
云南 李海春
《2 0 1 6年普通高等学校招生全国统一考试大纲》化学学科关于pH部分是两点要求:1.了解溶液pH的定义。2.了解测定溶液pH的方法,能进行pH的简单计算。笔者分析多年的高考化学试题发现:溶液pH这一知识点每年都考并且常考常新,重现率1 0 0%。这类题目能有效地考查考生的判断、推理运算等思维能力,充分体现体现了高考命题由知识向能力型的转变的趋势。现从高考真题的重现及规律方法予以探讨。
一、考点整合
1.理清溶液中H+或OH-的来源
①常温下,中性溶液:c(O H-)=c(H+)=1 0-7m o l·L-1
②溶质为酸的溶液:OH-全部来自水的电离,水电离产生的c(H+)=c(OH-)<1 0-7m o l·L-1。
③溶质为碱的溶液:H+全部来自水的电离,水电离产生的c(OH-)=c(H+)<1 0-7m o l·L-1。
④水解呈酸性或碱性的盐溶液:促进水的电离,水电离产生的c(OH-)=c(H+)>1 0-7m o l·L-1
溶液呈现酸、碱性的实质是c(H+)与c(OH-)的相对大小,不能只看pH,一定温度下pH=6的溶液也可能显中性,也可能显酸性,应注意温度。
2.pH的计算
①单一溶液的pH计算
强酸溶液:如HnA,设浓度为cm o l·L-1,c(H+)=n cm o l·L-1,pH=-l gc(H+)=-l g(n c)。

②混合溶液pH的计算类型
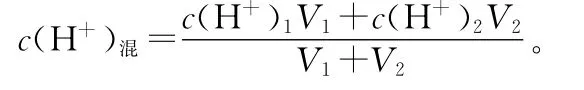

③强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最后求pH。

二、pH在高考试题中的再现
1.在选择题中的实例
例1 (2 0 1 4新课标Ⅱ,1 1)一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的H2S溶液中,c(H+)=c(H S-)=1× 1 0-5m o l·L-1
B.pH=a的氨水溶液,稀释1 0倍后,其pH=b,则a=b+1
C.pH=2 H2C2O4溶液与pH=1 2的N a OH溶液任意比例混合:c(N a+)+c(H+)=c(OH-)+c(HC2O-4)
D.pH相同的①CH3C O ON a ②N a HC O3③N a C l O三种溶液的c(N a+):①>②>③
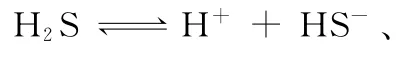
【答案】D
例2 (2 0 1 5浙江,1 2)4 0℃时,在氨-水体系中不断通入C O2,各种离子的变化趋势如下图所示。下列说法不正确的是( )

【答案】C
例3 (2 0 1 5四川,6)常温下,将等体积,等物质的量浓度的NH4HC O3与N a C l溶液混合,析出部分N a HC O3晶体,过滤,所得滤液pH<7,下列关于滤液中的离子浓度关系不正确的是( )
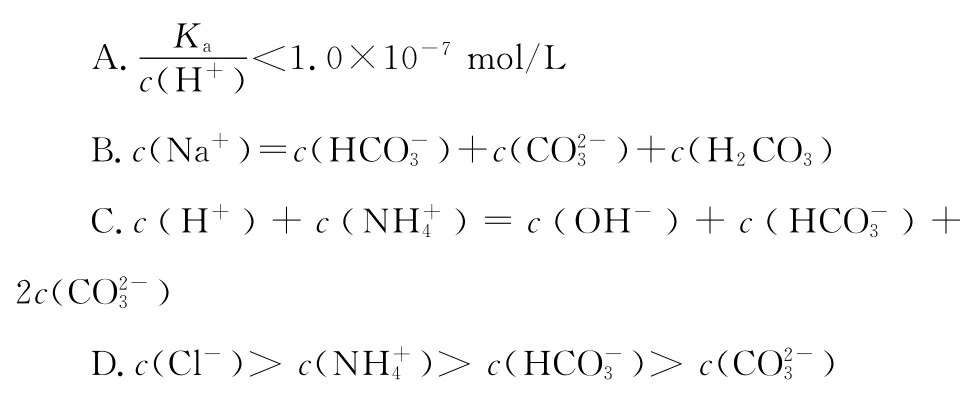

【答案】C
2.在客观题中的实例
例4 (2 0 1 5新课标Ⅱ,2 6节选)酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生M n O OH,回收处理该废电池可以得到多种化工原料,有关数据下表所示:

___化合物Z n(OH)2Fe(OH)2Fe(OH)3____Ksp近似值_ ____1 0-171 0-171 0-39
用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入新硫酸和双氧水,溶解,铁变为________加碱调节pH为________时,铁刚好完全沉淀(离子浓度小于1×1 0-5m o l/L时,即可认为该离子沉淀完全)。继续加碱调节pH为_________时,锌开始沉淀(假定Z n2+浓度为0.1m o l/L)。若上述过程不加双氧水的后果是________,原因是______________________________________________。
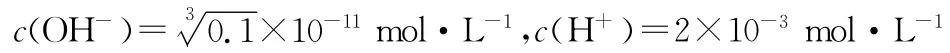
【答案】Fe3+2.7 6 Z n2+和Fe2+分离不开Fe(OH)2和Z n(OH)2的Ksp相近
例5 (2 0 1 5江苏,1 6节选)以磷石膏(主要成分C a S O4,杂质S i O2、A l2O3等)为原料可制备轻质C a C O3。
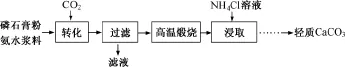
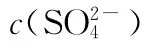

A.搅拌浆料 B.加热浆料至1 0 0℃
C.增大氨水浓度 D.减小C O2通入速率
(2)当清液pH接近6.5时,过滤并洗涤固体。滤液中物质的量浓度最大的两种阴离子为________和________(填化学式);检验洗涤是否完全的方法是_______________。
【解析】(1)注意题目中的原料是磷石膏粉和氨水浆料。由图所示当pH>1 1时,溶液中的c(S O24-)增大,说明有更多的S O24-,反应物为C a S O4、氨水、C O2,生成S O24-,还有C a C O3,相当于氨水和C O2反应生成(NH4)2C O3,(NH4)2C O3和C a S O4生成(NH4)2S O4和C a C O3。A项,搅拌浆料,增大反应物的接触面积,加快反应速率,正确;B项,加热到1 0 0℃,氨水挥发、C O2溶解度减小,则生成的(NH4)2C O3的量减少,无法实现C a S O4转化为C a C O3,错误;C项,增大氨水浓度可以提高反应速率,正确;D项,减小C O2通入速率,则转化速率降低,错误。(2)当pH接近6.5时,由图可知c(S O2-4)接近0.1m o l·L-1,溶液呈酸性,通入的C O2主要以NH4HC O3存在,故滤液中物质的量浓度最大的两种阴离子为S O2-4和HC O-3。可通过检验洗涤液中是否含有S O2-4来判断沉淀是否洗涤完全。
(作者单位:云南省富源县第一中学)

