碘化浸金原理及研究进展
李绍英,赵留成,赵礼兵,高志明,白丽梅,王 玲
(华北理工大学 矿业工程学院,河北 唐山 063009)
碘化浸金原理及研究进展
李绍英,赵留成,赵礼兵,高志明,白丽梅,王 玲
(华北理工大学 矿业工程学院,河北 唐山 063009)
系统总结了国内外碘化浸金工艺取得的研究进展。从热力学、动力学、溶液化学等方面讨论了碘化浸金的反应机理,阐明不同工艺参数对碘化浸金浸出效果的影响规律;列举碘化浸金在浮选金精矿、含铜难处理金矿、含碳金矿、含金废料等不同类型物料浸金应用的研究结果,并对碘化浸出贵液回收的工艺进行总结,最后展望了碘化浸金工艺的发展趋势。
冶金技术;碘化浸金;热力学;动力学;溶液化学;研究进展
碘化浸金指以含有一定比例的I2与I-的混合溶液作为浸出剂进行金矿的浸出,属于非氰浸金的一种,其氧化剂为I3-,络合剂为I-。碘化浸金具有浸出速率快、浸出矿浆pH值范围广(小于9.5即可)、适应性好(尤其针对含铜、砷等杂质元素的难处理金矿石)、浸出过程中不添加其他有毒化合物、环境友好等优点。为促进碘化浸金工艺的研发与应用,本文从碘化浸金热力学、动力学、溶液化学、应用研究、贵液回收等方面总结了国内外碘化浸金的相关研究成果。
1 机理研究
1.1 热力学研究
莫斯科国立贵金属勘探研究院对不同金的阴离子络合物AX2(X为阴离子)的稳定性顺序进行了研究,研究结果表明,其稳定性顺序为CN–>>I–>Br–>Cl–>SCN–>OCN–,金碘络合物离子强度比金氰络合物离子强度差,但优于溴、氯、硫氰酸盐、类氰酸盐的络合物离子强度[1-3]。
金在碘-碘化物溶液中发生的反应主要包括:

阳极反应为:

阴极反应为:

由式(3)~(5)可以得到:

如果碘-碘化物体系中碘离子过量,则可能会发生如下的反应:

综上可知,在一定条件下,金在碘-碘化物体系中的反应以式(6)为主,其能斯特方程为:
φ=-0.043+lg{[α(I3-)×α(I-)]/α2(AuI-2)}·0.0591/2 (10)
由式(10)可以看出标准状态下碘化浸金反应无法自发进行,但通过调整体系中各种离子浓度则反应可以自发进行。
针对碘化浸出过程 φ-pH图的研究最早由Marun[4]开始。Marun认为AuI4-和AuI2-,2种络合物离子在pH值0~14范围内稳定。其中,AuI4-是最稳定的,且碘浓度的变化影响不大,而当碘浓度降低,pH值较高时出现金的氧化物,金-碘络合区域变小。
李桂春等[5]重新绘制了 Au-I-I--H2O系的 φ-pH图,较为全面的考察了碘化浸金过程中的平衡条件,并且重点考察了双氧水对碘化浸金过程的影响,认为双氧水的存在有利于金碘络合离子的生成。
李绍英等[6]采用基于同时平衡原理的热力学计算方法,重新绘制了Au-I--H2O体系φ-pH图,并得到了不同碘离子浓度下的含金组分分布图及φ-log[I-]T图,同时对碘化浸出过程中AuI存在的条件及范围进行了研究。
1.2 动力学研究
Qi等[7]利用旋转圆盘技术研究了影响碘-碘化物体系溶金速率的因素,认为碘化浸金动力学反应为一级反应,一级反应速率与圆盘转速的平方根成正比。I3-浓度反应级数为1,I-反应级数为0.5,通过试验确定了反应活化能为34.4 kJ/mol,在c(I2)为5×10-3mol/L和c(NaI)为10-2mol/L时,金的溶解速率为2.1×10-9mol/(cm2·s)。
Davis等[8]的电化学研究表明,碘的溶金速度比氰化物快十几倍,金在碘-碘化物体系中的溶解依赖于碘、碘化物浓度及溶液pH值。在碘化钾浓度为0.1 mol/L,碘/碘化物摩尔比为0.35~0.4,pH值从2.7变化到11.5时,最大溶金速度为17 mg/(cm2·h);如果加入少量的次氯酸盐(<25 mmol/L),金的溶解速度将比用碘做氧化剂时快,但是,金在次氯酸盐-碘化物体系中的溶解速度强烈地依赖于溶液pH值,当pH值为2.7,KI浓度为0.02~0.1 mol/L,次氯酸盐-碘化物摩尔比为0.25时,金的溶解速度最快。
李绍英等[9]利用浮选金精矿进行了碘化浸金动力学研究,发现碘化浸金过程符合核收缩模型,浸出过程受界面反应化学控制,其表观活化能为31.674 kJ/mol,浸出反应速率方程为:
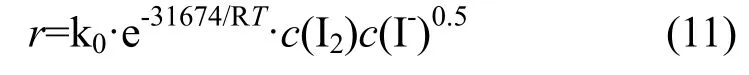
1.3 溶液化学研究
Davis等[10]还对碘化浸金相关体系的溶液化学进行了研究,详细讨论了不同条件下pH值对溶液中离子赋存状态的影响,研究结果对碘化浸金具有明显的指导意义。
I--I2-H2O系溶液化学研究结果表明,当I-为0.1 mol/L,总碘浓度为0.05 mol/L时,I--I2-H2O体系中稳定存在的主要物质是I3-和IO3-,在pH<9.5时,I3-是主要组分,当pH>9.5时,IO3-是主要组分。
Au-I--I2-H2O系溶液化学研究结果表明,当初始条件为固体金0.1 mol/L,I-的浓度为0.1 mol/L,I2的浓度为0.01 mol/L时,溶液中主要的平衡组分为I3-、AuI2-、I2和IO3-。在pH<9.5时,AuI2-的浓度主要受I3-的影响,当pH>9.5时,IO3-成为溶液中的主要组分,AuI2-在pH>9.5时则失去稳定性。
当I2的浓度为0.05 mol/L时,主要的平衡组分为I3-、AuI2-、I2、IO3-和固相AuI。在pH<8时,AuI的生成使金表面钝化,阻碍了AuI2-的生成,即使I3-的浓度升高、自由I-浓度降低(因而溶液的电位升高)也是如此。在pH>9.5时IO3-成为溶液中的主要组分,而AuI2-则在pH>10时失去稳定性。
2 应用研究
国外相关专利证明碘化法可以用于废料及堆浸工艺浸出金。1976年Homick等[11]提出利用碘化法从废料中回收金的专利。1985年Mcgrew等[12]提出利用碘化法在堆浸工艺过程中回收金的专利。2009年,Union[13]提出利用碘化钾-碘溶液回收金的专利。
Marun等人进行了2种试样的碘化浸金试验研究[14]。试验条件为:初始碘/碘化物摩尔比低于0.3,pH值3~5,浸出时间4 h。文献没有给出金的浸出率数据,只是在和氰化浸出作对比时得出了氰化浸出的金浸出率高,浸出时间长的结论。同时对浸出贵液进行了金的电解沉积试验,金的沉积率达到90%以上,电流效率为 0.12%~0.13%,并与碘和碘化物初始浓度基本无关。
Ceдeльникoвa等人用碘-碘化物溶液对乌拉尔一个矿山的含金氧化矿石进行浸出试验[15]。用n[I2]: n[I-]为0.1的碘溶液浸金,pH值在5.5~7.5之间,固液比1:5最佳(实际处理时用1:3)。反应平衡时金的回收率达95%,浸出速度比溴溶液浸金慢;电解沉积时,金浓度越高,电解速度越快,金的最大沉积率可达95%。
Angelidis[16]研究了用碘-碘化物溶液作为浸出剂从含毒砂、黄铁矿的金精矿中选择性溶金。试验证明碘化法能够快速溶金,且浸出剂用量相对较低。他们还研究了矿石中其他成分对浸出造成的影响,结果表明铁、锌矿物的存在对浸出无太大影响,而银、铅和铜矿物会发生副反应,消耗碘化物从而影响浸出率。
Baghalha[17]在室温条件下用碘-碘化物溶液对2种类型的金矿进行了浸出试验,研究了矿石类型、碘-碘化物浓度和溶液中氧气的存在对金浸出的影响,结果表明:用8 g/L的碘和20 g/L的碘化物溶液浸出碳质金矿(含有机碳1.6%)时,金的浸出率仅有20%,这是因为有机质吸附了大量金碘络合物,从而使得金的浸出率下降;相比之下,用4 g/L的碘和20 g/L的碘化物溶液浸出氧化金矿,在24 h之内浸出率即可达89%。
Wang等[18]针对双旗山浮选金精矿进行了碘化浸出试验研究。结果表明:在磨矿细度为-325目占80.49%,碘初始浓度1.2%,碘与碘化钾摩尔比1:10,浸出液pH值7,液固比4:1,搅拌强度200 r/min,25℃浸出4 h,金浸出率可达90.44%,实现了金的高效无氰浸出。
李桂春等[19]用碘化法对戈塘含碳原生金矿进行了试验。样品含金8.86 g/t,炭2.23%,铜0.005%,硫2.52%,经过试验确定了焙烧浸出的最佳条件:焙烧温度650℃,碘浓度1%,I2:I-为1:10,双氧水用量2%,浸出4 h,在弱酸性、中性矿浆中浸出,金的浸出率接近95%。
李桂春等[20]针对废旧线路板的解离及粉末中的金的碘化浸出做了研究。结果表明:线路板粉末中的金在初始碘质量浓度为1.1%,pH值为自然值,碘与碘离子摩尔比 1:10,固液比 1:9,双氧水用量1%时,室温下浸出3 h,金的浸出率可达95.53%。
徐渠等[21-22]探讨了用碘化法从废弃印刷线路板中浸取金,通过单因素条件实验和正交实验确定了最佳工艺条件,在此条件下金浸出率可达95%。
庞朝霞[23]针对废旧镀金元件上的金做了溶解和回收的研究。采用 I2-KI-H2O2浸金体系、I2-HNO3-H2O2浸金体系、I2-H2SO4-H2O2浸金体系对金进行溶解,结果表明从废旧电路板上直接溶解金,这3种方法比现有的报道都要好。
为了探索降低碘用量的途径,李桂春等[24]研究了使用助氧化剂(双氧水)、适当延长浸出时间、原矿焙烧后浸出等方法。对辽宁五龙金矿四道沟分矿的金矿石,研究了影响I--ClO-浸金的主要因素,得出I--ClO-体系浸金的最佳条件:次氯酸钠用量占矿浆体积的7%~ 9%,碘化钾浓度不小于0.25 mol/L,矿浆为偏酸性至中性,浸出4 h,金浸出率可达85%以上。但该法还有待进一步完善以提高浸出率。
李绍英等[25-28]通过碘化物对某浮选金精矿浸出效果的影响研究发现,3种碘化物中,碘化钾的浸出效果优于氢碘酸及碘化铵。采用碘化法分别对某含铜难浸金矿和浮选金精矿进行了浸出试验,考察了不同工艺参数对浸出效果的影响,试验结果表明2种物料均有较高的浸出率。
彭志成[29]采用焙烧-碘化浸出联合流程处理某含金硫精矿,最终金的浸出率达到78.78%。
3 贵液回收
李桂春等[30]研究了锌粉置换法、活性炭吸附法及电解沉积法,并探讨了用电解法回收碘。试验结果表明:1) 锌粉置换法可以置换贵液中的金,但由于浸出液显酸性或中性,会使得锌的消耗量增加,且循环浸出时锌会影响金的浸出;2) 活性炭吸附法适用于低 I-浓度的浸出液,因为高浓度 I-会和金形成竞争吸附;3) 当浸出液中金的含量较低时,先用活性炭吸附法,解析后的高浓度的解吸液用电解法沉积金;4) 电解法只能回收一部分碘,但可考虑用此法净化溶液,配制新的浸出剂进行循环使用。
庞朝霞[23]比较了锌粉置换回收金、亚硫酸钠还原回收金、电沉积法回收金3种方式。结果表明,与锌粉置换回收金的方法相比,利用亚硫酸钠还原法回收金,具有反应速率较快,得到的金比较纯,回收率较高等优点。电沉积法从碘化浸出液中回收金的合适工艺条件为:电解在双室电解槽中进行,阴极为石墨电极,阳极为钛板,采用阴离子交换膜把阴极和阳极分开,阴极液为金的碘化浸出液,其中金的浓度最好不要低于50 mg/L,槽电压为25 V左右,阳极液中碘与碘化钾的质量比为 1:4,碘化钾的质量分数为0.8%。室温条件下电解时间为2.5 h左右,金的沉积率可达到93%以上。
徐渠等[31]研究得出电解碘化浸金贵液的最佳工艺条件为:使用隔膜式电解槽,中间用阴离子交换膜隔开,碳棒作阴极,钛棒作阳极,阴极金浓度15~50 mg/L,阳极使用碘-碘化物溶液作为电解质,碘单质浓度0.1%~0.8%,碘与碘化物摩尔比1:10,电解时间1~4 h,槽电压10~14 V,此时金的电解沉积率大于95%。
Zhang等[32]研究了用强碱性离子交换树脂从碘-碘化物溶液中吸附金。结果表明,树脂吸附碘化物的能力远小于金碘络合物及三碘化物,但强于氯化物。树脂对三碘化物的强吸附能力影响了金和碘化物的吸附,吸附的三碘化物分解后通过物理吸附沉积在树脂上面,并释放碘化物离子到溶液中;如果树脂中的三碘化物的浓度远低于饱和度,则吸附金的效果较好。因此,为了促进金的吸附应该预先从溶液中除去大部分的三碘化物;利用还原法可以从树脂中提取碘,2 mol/L NaCl和0.3 mol/L Na2SO3对于金和碘的回收都很有效,提取出的金在含有亚硫酸盐的溶液中很稳定。
姜涛[33]对金碘化物溶液在活性炭上的吸附动力学及影响因素做了详细的总结。结果表明,金的吸附速率与活性炭的特性、溶液特性及吸附操作条件有关。金的吸附率不受其初始浓度(1.1~43.2 mg/L)的影响,活性炭自碘化物中的吸附不可能是化学反应控制的。铜、锌、镍离子对金的吸附均有不利影响但铜的影响最大。在pH值为2~10的范围,pH值对金的吸附影响均不明显。
4 结语与展望
目前,碘化浸金在浸金原理、应用研究等方面已经有了较为深入的研究,碘化浸金过程中不同工艺参数对浸出效果的影响规律已较为明确。碘化浸金具有浸出速率快、浸出效果好、对不同种类的金矿资源适应性强、浸出过程无毒环境友好等优点。但由于碘及碘化物价格较高,导致碘化浸金成本远高于传统的氰化法,可考虑通过贫液循环利用来降低成本。如果能解决这些问题,碘化浸金有可能成为一项实用的非氰浸金工艺。
[1] LI G C, LU S C. Iodide leaching gold from carbonaceous refractory gold ores[C]// 24th International mineral processing congress. Beijing: Science Press, 2008.
[2] 李桂春, 卢寿慈. 含炭难处理金矿石碘法浸出[J]. 北京科技大学学报, 2003, 25(6): 501-503. LI G C, LU S C. Iodine leaching of gold from lean gold ore with charcoal[J]. Journal of University of Science and Technology Beijing, 2003, 25(6): 501-503.
[3] SEDELNIKOVA G V, KRYLOV G S. Iodinated and brominated solvent of gold[J]. Schnigri, 2001(3): 43-52.
[4] MARUN J N, MEISSL R J, LARA R F, et al. Gold bearing ore processing with iodine-iodide solutions[C]// Proceeding of the 20th international mineral processing congress, Aachen Germany: GMDB (Gesellschaft fur Bergball, Metallurgie), 1997: 381-391.
[5] 李桂春, 吕进云. 碘化浸金过程的基本理论[J]. 黑龙江科技学院学报, 2009, 19(5): 345-347. LI G C, LV J Y. Basic theory of iodide leaching of gold process[J]. Journal of Heilongjiang Institute of Science and Technology, 2009,19(5): 345-347.
[6] 李绍英, 赵留成, 孙春宝, 等. 基于同时平衡原理的Au-I--H2O系热力学分析[J]. 中国有色金属学报, 2015, 27(7): 1987-1992. LI S Y, ZHAO L C, SUN C B, et al. Thermodynamic analysis for Au-I--H2O system based on principle of simultaneous equilibrium[J]. The Chinese journal of nonferrous metals, 2015, 27(7): 1987-1992.
[7] QI P H, HISKEY J B. Dissolution kinetics of gold in iodide solutions[J]. Hydrometallurgy, 1991, 27(1): 47-62.
[8] DAVIS A, TRAN T. Gold dissolution in iodide electrolytes[J]. Hydrometallurgy, 1991, 26(2): 163-177.
[9] 李绍英, 王海霞, 袁喜振, 等. 金精矿碘化浸出过程动力学[J]. 中国有色金属学报, 2014, 24(3): 814-819. LI S Y, WANG H X, YUAN X Z, et al. Leaching dynamics of gold concentrates by iodine-iodide solution[J]. The Chinese journal of nonferrous metals, 2014, 24(3): 814-819.
[10] DAVIS A, TRAN T, YOUNG D R. Solution chemistry of iodide leaching of gold[J]. Hydrometallurgy, 1993, 32(2): 143-159.
[11] HOMICK R P, SLOAN H. Gold reclamation process: US 3957505[P]. 1976-05-18.
[12] MCGREW K J, MURPHY J W. Iodine leach for the dissolution of gold: US4557759[P]. 1985-12-10.
[13] UNION R E. Recovery of gold from potassium iodideiodine etching solution: US7582136[P]. 2009-09-01.
[14] 李桂春, 卢寿慈. 非氰化提金技术的发展[J]. 中国矿业, 2003(3): 1-5. LI G C, LU S C. The development of non-cyanidationgold lixiviating technology[J]. China mining magazine, 2003(3): 1-5.
[15] 李桂春. 碘盐提金[M]. 北京: 煤炭工业出版社, 2005.
[16] ANGELIDIS T N K. Selective gold dissolution from a roasted auriferous pyrite-arsenopyrite concentrate[J]. Hydrometallurgy, 1995, 37(1): 75-88.
[17] BAGHALHA M. The leaching kinetics of an oxide gold ore with iodide/iodine solutions[J]. Hydrometallurgy, 2012(113/114): 42-50.
[18] WANG H X, SUN C B, LI S Y, et al. Study on gold concentrate leaching by iodine-iodide[J]. Int J Min Met Mater, 2013, 20(4): 323-328.
[19] 李桂春, 卢寿慈. 碘化浸金试验研究[J]. 中国矿业, 2004(7): 68. LI G C, LU S C. Experimental investigation for iodide leaching of gold[J]. China mining magazine, 2004(7): 68.
[20] 李桂春, 苑仁财, 康华, 等. 废旧电路板中金的碘化法回收工艺[J]. 黑龙江科技学院学报, 2012, 22(3): 233. LI G C, YUAN R C, KANG H, et al. Gold recovery process with iodine method from waste printed circuit board [J]. Journal of Heilongjiang Institute of Science and Technology, 2012, 22(3): 233.
[21] 徐渠, 陈东辉, 陈亮, 等. 碘化法从废弃印刷线路板中浸取金[J]. 有色金属, 2010, 62(3): 88-90. XU Q, CHEN D H, CHEN L, et al. Gold leaching from waste printed circuit board by iodine process[J]. Nonferrous metals, 2010, 62(3): 88-90.
[22] 徐渠. 碘化法从废弃印刷线路板中提取金的研究[D].上海: 东华大学, 2009.
[23] 庞朝霞. 碘化法浸取金的研究[D]. 上海: 华东理工大学, 2012.
[24] 李桂春, 吕进云. 降低碘化浸金碘用量的途径[J]. 黑龙江科技学院学报, 2009(6): 417-419. LI G C, LÜ J Y. Methods of reduce iodine dosage in iodide leaching of gold[J]. Journal of Heilongjiang Institute of Science and Technology, 2009(6): 417-419.
[25] 李绍英, 王海霞, 孙春宝, 等. 碘化物对金精矿碘化浸出的影响[J]. 中国有色金属学报, 2013, 23(5): 1434. LI S Y, WANG H X, SUN C B, et al. Effects of different iodides on gold concentrates leaching process in iodineiodide solution[J]. The Chinese journal of nonferrous metals, 2013, 23(5): 1434.
[26] 袁喜振, 李绍英, 孙春宝, 等. 浮选金精矿和含铜难浸金矿的碘化浸金研究[J]. 中国有色金属学报, 2014, 24(12): 3123-3128. YUAN X Z, LI S Y, SUN C B, et al. Gold extraction from gold concentrate and copper-bearing refractory gold ore by iodine-iodide solution[J]. The Chinese journal of nonferrous metals, 2014, 24(12): 3123-3128.
[27] 袁喜振, 孙春宝, 李绍英, 等. 某含铜难处理金矿提金试验[J]. 有色金属: 冶炼部分, 2014(11): 43. YUAN X Z, SUN C B, LI S Y , et al. Experiment of gold recovery from copper-bearing refractory gold ores[J]. Nonferrous metals: extractive metallurgy, 2014(11): 43.
[28] 袁喜振, 李绍英, 赵留成等. 含铜难处理金矿选择性浸出试验研究[J]. 中国科技论文, 2014, 9(3): 351-354. YUAN X Z, LI S Y, ZHAO L C, et al. Experimental study on selective leaching of refractory gold ores[J]. China sciencepaper, 2014, 9(3): 351-354.
[29] 彭志成, 丁德馨, 胡南, 等. 从难处理含金硫精矿中提取金的试验研究[J]. 矿业研究与开发, 2015, 35(2): 47. PENG Z C, DING D X, HU N, et al. Experiment study on gold leaching from refractory gold-bearing sulfur concentrate[J]. Mining research and development, 2015, 35(2): 47.
[30] 李桂春, 纪守峰, 王会平. 碘化浸金时从浸出液中提金及碘再生方法研究[J]. 矿冶工程, 2006, 26(3): 42-44. LI G C, JI S F, WANG H P. Research of cementing gold out from iodide leaching liquor and recovering of iodide liquor[J]. Mining and metallurgical engineering, 2006, 26(3): 42-44.
[31] 徐渠, 陈东辉, 陈亮, 等. 电解法从废弃印刷线路板的碘化浸金液中沉积金[J]. 中国有色金属学报, 2009, 19(6): 1130-1135. XU Q, CHEN D H, CHEN L, et al. Electrodepositing gold of iodine leaching solution from waste printed circuit board[J]. The Chinese journal of nonferrous metals, 2009, 19(6): 1130-1135.
[32] ZHANG H, JEFFERY C A, JEFFREY M I. Ion exchange recovery of gold from iodine-iodide solutions[J]. Hydrometallurgy, 2012, 125/126: 69-75.
[33] 姜涛. 提金化学[M]. 长沙: 湖南科学技术出版社, 1998.
Principle and Research Progress of Gold Extraction with Iodine-iodide Solution
LI Shaoying, ZHAO Liucheng, ZHAO Libing, GAO Zhiming, BAI Limei, WANG Ling
(College of Mining Engineering, North China University of Science and Technology, Tangshan 063009, Hebei, China)
The latest development of gold extraction with iodine-iodide solution is systematically reviewed. Firstly, the reaction mechanism is discussed from thermodynamics, dynamics, solution chemistry, and so on. Secondly, the effect of different technological parameters on gold leaching is illustrated. Thirdly, the test results on different gold ore, such as flotation gold concentrate, refractory gold-copper ore, carbon-bearing gold ore, gold-bearing waste, are given. Recycle technology of pregnant solution is also introduced. Finally, development tendency is prospected.
metallurgy; gold extraction with iodine-iodide solution; thermodynamics; dynamics; solution chemistry; research progress
TF111
:A
:1004-0676(2016)02-0077-05
2015-08-18
河北省自然科学基金(E2016209345)、河北省高等学校青年人才拔尖计划(BJ2016042)。
李绍英,男,博士,讲师,研究方向:贵金属选冶及难处理矿产综合回收。E-mail:muzi1201@126.com

