高效液相色谱法测定乙酰丙酮钌纯度的方法研究
姜 婧,常桥稳,晏彩先,李 杰,邱红莲
(昆明贵金属研究所,贵研铂业股份有限公司 稀贵金属综合利用新技术国家重点实验室,昆明 650106)
高效液相色谱法测定乙酰丙酮钌纯度的方法研究
姜 婧,常桥稳,晏彩先,李 杰,邱红莲*
(昆明贵金属研究所,贵研铂业股份有限公司 稀贵金属综合利用新技术国家重点实验室,昆明 650106)
建立了用高效液相色谱(HPLC)分析乙酰丙酮钌纯度的方法。以C18色谱柱为固定相,以乙腈/水53/47 (V/V)溶液为流动相,检测波长为270 nm,可以获得满足乙酰丙酮钌纯度测定要求的色谱图。在乙酰丙酮钌浓度为0.224~0.318 mg/mL时,线性相关系数(r)为0.9993,测定相对标准偏差(RSD)为0.85%,样品加标回收率为99.13%~101.37%。
分析化学;高效液相色谱法;乙酰丙酮钌;纯度
乙酰丙酮钌为钌(III)的有机配合物,在制备钌薄膜材料、电极材料、催化材料、纳米材料及复合材料等领域[1]有着重要的应用前景和潜在的市场前景。钌含量的测定方法有重量法、原子吸收法、分光光度法、荧光法、示波极谱法[2-6]等,但这些分析方法大多只适用于样品中的钌含量,不能分析化合物的纯度。为配合制备乙酰丙酮钌的技术攻关项目,本文提出用高效液相色谱法(HPLC)定量分析乙酰丙酮钌配合物纯度的方法,并应用于实际工作中。
1 实验部分
1.1 仪器与试剂
测定使用的高效液相色谱仪为美国Waters公司Empower 2色谱工作站,配有1525泵、717自动进样器,检测器为2998二极管阵列检测器,C18色谱柱(150×4.6 mm,5 µm)、C8色谱柱(150×4.6 mm,5 µm);紫外-可见分光光度计为美国Varian公司Cary 50型;分析天平为北京赛多利斯公司TB-215,感量0.01 mg。
乙酰丙酮钌对照样品,纯度99.79%,购自美国Alfa公司;三氯化钌(RuCl3·xH2O,昆明贵金属研究所自制);乙酰丙酮(Hacac,纯度﹥99.0%,天津);供试样品乙酰丙酮钌为昆明贵金属研究所自制;乙腈(色谱纯,默克公司);其余试剂均为分析纯,自制超纯水(Millipore Elix 5)。
1.2 实验方法
将对照品用流动相溶液超声溶解,以紫外-可见分光光度计扫描溶液选取检测波长。移取10 µL溶液注入液相色谱仪,记录色谱图。以色谱峰面积计算浓度和样品中乙酰丙酮钌含量。
2 结果与讨论
2.1 检测条件选择
2.1.1 检测波长的选择
取0.013 mg/mL的乙酰丙酮钌对照品溶液,用乙腈溶解(超声5 min以促进溶解)。以乙腈为参比,进行紫外-可见光谱扫描,所得谱图如图1所示。

图1 乙酰丙酮钌的紫外光谱扫描图Fig.1 UV-Vis spectra of ruthenium acetylacetonate
由图1可见,乙酰丙酮钌在波长270、330 nm处有最大吸收峰。从检测的灵敏度和所用溶剂的紫外截止波长考虑,将选择乙酰丙酮钌的检测波长设定为λ=270 nm。
2.1.2 固定相及流动相的选择
用乙酰丙酮钌的对照品配好溶液后,分别以C8柱、C18柱为固定相进行实验。对比发现,乙酰丙酮钌在C8柱上的保留时间较短,难以有效分离;而在C18柱上的保留时间较长,分离行为较好。最终选用C18柱作为固定相。
根据样品的溶解性,选用甲醇、乙腈、四氢呋喃等与超纯水组合进行试验,筛选流动相。结果表明,用甲醇-水作流动相时,样品主峰的拖尾因子较大;用四氢呋喃-水作流动相时,样品出峰时间太早;用乙腈-水作流动相时,样品主峰有明显的改善。
最终选用C18柱,以乙腈:水=53:47 (V/V)为流动相,其余测定条件为:进样量为 10 µL,流速 1 mL/min,柱温40℃,检测波长270 nm。所得对照品色谱图如图2所示。

图2 乙酰丙酮钌HPLC-PDA图Fig.2 HPLC-PDA chromatogram of ruthenium acetylactonate sample
图2 中出现多个色谱峰,乙酰丙酮钌的色谱峰强度最大,该峰出现在保留时间(tR)=8.029 min处。计算可得,分离度(Rs)=5;拖尾因子为 1.08;理论塔板数为1.61×104,具有较好的分离效果。此色谱条件被作为最终分析条件。
2.1.3 色谱峰纯度的检验
本实验所用检测器为二极管阵列检测器(diodearray detector,DAD)[7-8]是20世纪80年代发展起来的一种紫外检测器,其可以在全部紫外光波长获得色谱信号,故可对色谱峰进行定量检测和组分的定性检测。判断色谱峰纯度的方法是:于色谱峰的峰前沿、峰顶和峰后沿3个部位各选1点,将3个点的光谱图经归一化处理后进行比较,当他们基本相同时证明峰是单一组分。图3为乙酰丙酮钌色谱峰3个部位吸收峰的归一化光谱图,表明色谱峰为单一组分。

图3 乙酰丙酮钌纯度峰Fig.3 The peak purity of acetylacetone ruthenium peak
2.2 影响因素分析
2.2.1 干扰试验
针对实际试样中可能存在的共存物,检验其是否对测定有干扰,并了解共存物的最大允许浓度。
合成乙酰丙酮钌的原料为乙酰丙酮(Hacac)和水合三氯化钌,此2种原料可能存在于供试样品中而影响分析结果,需对其可能的影响情况进行分析。分别用流动相将2种原料溶解,配成0.331 mg/mL的溶液。在选定色谱条件下进样测定,结果发现水合三氯化钌在20 min内不出峰,而乙酰丙酮在1.8 min时出峰,与乙酰丙酮钌的保留时间不一致,RS>2,图2的色谱峰中亦未出现此2峰,故可判定合成原料不干扰测定。
2.2.2 溶液中乙酰丙酮钌的稳定性
为了使分析结果重现、可靠,分析方法中采用的样品及对照品在一定时间内必须稳定。因此,分析乙酰丙酮铱在溶液中的稳定性是必须的[9]。
称取14.55 mg乙酰丙酮钌对照品于50 mL的容量瓶中,流动相定容,配制浓度为0.291 mg/mL对照品溶液,按照选定的色谱条件,在24 h内进行间断测定,考察其稳定性。不同时刻的色谱峰面积测定结果如表1所示。由表1可见,24 h内测定,乙酰丙酮钌吸收峰面积的无明显变化,RSD=2.0%。说明对照品溶液具有较好的稳定性。
2.3 测定结果评估
2.3.1 线性关系
称取7份不同质量的乙酰丙酮钌对照品,分别置100 mL容量瓶中,用流动相溶解并稀释至刻度,摇匀过滤后按选定色谱条件进样测定。结果如表 2所列。根据表2数据,以乙酰丙酮钌色谱峰面积A对其质量浓度ρ进行线性拟合,得到的线性方程为:


表1 室温下不同放置时间测定的乙酰丙酮钌峰面积Tab.1 The peak areas of ruthenium acetylacetonate measured at different standing time at room temperature

表2 乙酰丙酮钌浓度与色谱峰面积的关系Tab.2 Relationship between the concentration of acetylacetone ruthenium and chromatographic peak area
式(1)线性的相关系数 r=0.9993,线性范围为0.224~0.336 mg/mL。
2.3.2 方法精密度
精密度(通常用相对标准偏差RSD表示)指在规定的测试条件下同一个均质样品,经过多次进样测定所得结果之间的接近程度,反应了正常测定条件下分析方法的再现程度。取不同浓度的乙酰丙酮钌对照样品溶液,按选定色谱条件,每个样品溶液重复进样3次,测定其峰面积并计算其相对标准偏差,结果如表3所示。
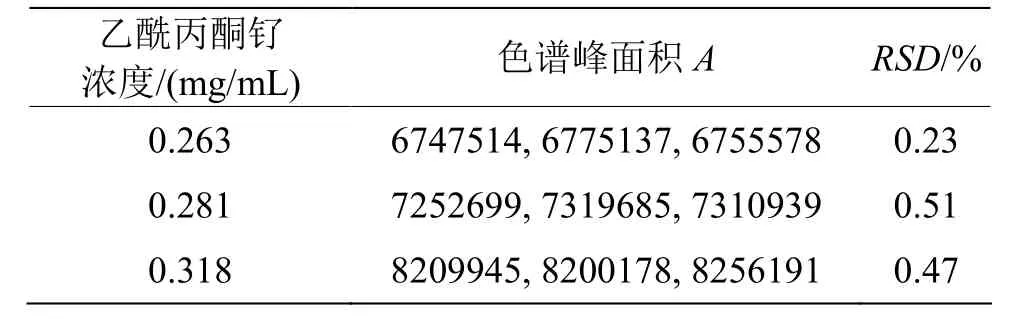
表3 测定乙酰丙酮钌方法的相对偏差Tab.3 RSD of the established analytical method for acetylacetone ruthenium
表3中,3个不同浓度对照品溶液的RSD分别为0.23%、0.52%、0.47%,表明方法的精密度良好。
2.3.3 方法准确度
本实验采用加标回收法判断方法准确度。准备同一批次的乙酰丙酮钌,在线性范围内配置好溶液后进样,得到其相对含量为99.17%;准确称取上述批次的乙酰丙酮钌样品3份,分别加入一定量的乙酰丙酮钌对照品,溶于50 mL容量瓶中用流动相配制成溶液,进样后根据工作曲线得到相对应的浓度,从而测得加标回收率。结果如表4所示。

表4 样品加标回收率Tab.4 Recovery of the standard addition (n=3)
由表4结果可见,样品加标回收率为99.13%~101.37%,平均回收率为100.10%,表明方法具有较高的准确度,可用于生产质量控制。
3 结论
本研究采用高效液相色谱法进行了乙酰丙酮钌的纯度分析。研究表明:
1) 以 C18色谱柱为固定相,乙腈:水=53:47 (V/V)为流动相,检测波长为270 nm,在选定色谱条件下,可以获得满足乙酰丙酮钌纯度分析使用的色谱图。
2) 对于可能存在的共存物乙酰丙酮及水合三氯化钌在最佳色谱条件下不影响乙酰丙酮钌的检测。
3) 在此色谱条件下测得乙酰丙酮钌在乙腈/水溶剂中24 h内稳定,相关系数为r=0.9993,线性范围为0.224~0.336 mg/mL。方法精密度良好、加标回收率为99.13%~101.37%。表明此法适用于检测乙酰丙酮钌的相对纯度。
本法操作简便快速、结果可靠,已用于产品质量控制并拟建立标准分析方法。
[1] BOGADO A L, BARBOSA M I F, SOUZA G D D, et al.On the ROMP of 2-norbornene with an in situ ruthenium carbene complex: ESI-MS, NMR and DFT analyses[J]. Journal of organometallic chemistry, 2010, 695(s12/13): 1708-1714.
[2] 乔亚华, 吴继宗. Ru3+和[RuNO]3+的速差动力学分析方法[J]. 核化学与放射化学, 2007, 29(1):15-22. QIAO Y H, WU J Z. Rate differential kinetic analytical method of Ru3+and [RuNO]3+[J]. Journal of nuclear and radiochemistry, 2007, 29(1): 15-22.
[3] 郭俊梅, 韩守礼, 谭文进, 等. 氢还原重量法测定三氯化钌产品中钌的含量[J]. 中国无机分析化学, 2014, 4(3): 44-51. GUO J M, HAN S L, TAN W J, et al. Determination of ruthenium in ruthenium trichloride by hydrogen reduction gravimetric method[J]. Chinese journal of inorganic analytical chemistry, 2014, 4(3): 44-51.
[4] 朱武勋. 原子吸收光谱法测定三氯化钉中Ru含量[C]//全国轻金属分析学术会议论文选编. 北京: 中国有色金属学会, 2004.
[5] 杨红艳, 李青, 马媛, 等. ICP-AES测定复杂二次资源物料中钌含量干扰情况研究[J]. 贵金属, 2013, 34(2): 56-60. YANG H Y, LI Q, MA Y, et al. Study on the interference in determination of Ru in secondary resource materials by ICP-AES[J]. Precious metals, 2013, 34(2): 56-60.
[6] 魏立山, 李欣, 寇宗燕. Ru-KIO4-偶氮氯磷-pC体系催化分光光度法测定微量钌[J]. 冶金分析, 2002, 22(6): 9. WEI L S, LI X, KOU Z Y. Kinetic spectrophotometric determination of trace ruthenium with RuIII-KIO4-chlorophosphonazo-pC system[J]. Metallurgical analysis, 2002, 22(6): 9.
[7] 王骏, 胡梅, 张卉, 等. 二极管阵列检测器在食品分析中的应用[J]. 食品与发酵工业, 2008, 39(34): 154-157. WANG J, HU M, ZHANG H, et al. The application of photodiode array detector in food analysis[J]. Food and fermentation industries, 2008, 39(34): 154-157.
[8] 胡育筑, 康继宏, 郁建, 等. 二极管阵列检测器在色谱峰纯度鉴定中的应用研究[J]. 中国药科大学学报, 1993, 24(5): 290-294. HU Y Z, KANG J H, YU J, et al. Application studies on chromatographic peak purity with photodiode-array detection [J]. Journal of China Pharmaceutical University. 1993, 24(5): 290-294.
[9] 汪正范. 色谱定性与定量[M]. 北京: 化学工业出版社, 2007: 9-13.
An Analytical Method for Determination of Ruthenium Acetylacetonate with High Performance Liquid Chromatography
JIANG Jing, CHANG Qiaowen, YAN Caixian, LI Jie, QIU Honglian*
(Kunming Institute of Precious Metals, State Key Laboratory of Advanced Technologies for Comprehensive Utilization of Platinum Metals, Sino-Platinum Metals Co. Ltd., Kunming 650106, China)
A method has been developed to measure the ruthenium acetylacetonate by a high pressure liquid chromatography. The operating conditions were as follows: a C18chromatographic column, a mixture of acetonitrile and water (V/V=53/47) as the mobile phase and 40℃ of the column temperature. The detection wavelength was fixed at 270 nm and the injection volume was 10 µL. Under these given operating conditions, the linear range of ruthenium acetylactonate is 0.224~0.318 mg/mL (r=0.9993) with a 0.85% of RSD, and the recovery for standard addition ranges from 99.13%~101.37%.
analytical chemistry; high performance liquid chromatography (HPLC); ruthenium acetylactonate; purity
O657.7
:A
:1004-0676(2016)02-0061-04
2016-04-21
云南省科技厅省院省校项目(2015IB019)、昆明市科技计划项目(2016KJJH059)。
姜 婧,女,工程师,研究方向:贵金属化学分析。E-mail:dianaair@126.com
*通讯作者:邱红莲,女,高级工程师,研究方向:贵金属化学分析。E-mail:qiuhonglian@ipm.com.cn
——庆祝中国共产党成立一百周年贵金属纪念币展

