α-硫辛酸对半胱氨酸诱导的血管内皮细胞凋亡的保护作用
荣季冬 姜顺涛 邓玉洁 刘会 张曙影 石蓓
α-硫辛酸对半胱氨酸诱导的血管内皮细胞凋亡的保护作用
荣季冬1姜顺涛1邓玉洁1刘会2张曙影3石蓓1
目的探讨以同型半胱氨酸(Hcy)预处理血管内皮细胞的损伤作用及不同剂量α-硫辛酸(ALA)对其保护作用。方法将HUVEC-12细胞株进行人工传代培养,并随机分为三组,空白对照组、Hcy组(0.2 mmol/L)、ALA组(0.2 mmol/L Hcy+0.5 mmol/L ALA)。干预24 h后应用MTT法观察其对内皮细胞存活的影响、激光显微镜直接观察其对对内皮细胞内活性氧的影响。结果细胞经Hcy处理后,细胞明显受抑制,且Hcy能诱导内皮细胞产生氧自由基(ROS),而ALA可拮抗Hcy的氧化应激作用,差异具统计学意义(P<0.01)。结论Hcy可通过增加细胞胞内ROS生成引起内皮细胞氧化损伤,而α-硫辛酸可通过抑制氧化应激保护受损内皮细胞。
血管内皮细胞;高半胱氨酸;α-硫辛酸
血管内皮细胞是一种多功能细胞,它不仅是血管壁组织和血液之间的第一道通透性屏障,而且还是人体最大的自分泌﹑旁分泌及内分泌器官,能够合成和分泌多种生物活性物质。炎症及氧化应激均可引起血管内皮细胞损伤,导致动脉粥样硬化(AS)和血栓形成。半胱氨酸(Hcy)是动脉粥样硬化性心血管疾病的独立危险因素,可参与损伤血管内皮细胞并导致形成[1]。α-硫辛酸是一种抗氧化剂,由于其低廉的价格以及良好的抗氧化作用已被广泛应用于临床。临床实验表明α-硫辛酸在改善人体体质﹑抗氧化﹑促进糖代谢﹑减轻糖尿病并发症﹑缺血再灌注引起的脑神经损害等方面都有很好的预防及缓解作用[2]。然而,α-硫辛酸是否可通过调节LOX表达参与保护内皮细胞,目前国内外尚无文献报道。本实验设计通过半胱氨酸建立血管内皮细胞损伤模型,并以α-硫辛酸进行干预,观察α-硫辛酸是否对半胱氨酸诱导的血管内皮细胞凋亡有保护作用。
1 材料与方法
1.1 一般材料
脐静脉内皮细胞株(HUVEC-12)购于中南大学湘雅医院中心实验室;同型半胱氨酸﹑DMSO﹑MTT试剂盒购于Sigma公司;0.25%胰酶-0.03 EDTA细胞消化液购于Gibco公司;1640培养基购于Hyclone公司。将HUVEC-12细胞株进行人工传代培养,并随机分为三组,空白对照组﹑Hcy组(0.2 mmol/L)﹑ALA组(0.2 mmol/L Hcy+0.5 mmol/L ALA)。
1.2 实验方法
(1)内皮细胞系的培养:脐静脉内皮细胞株(HUVEC-12)购于中南大学湘雅医院中心实验室,以1 640培养基作为细胞培养液,且培基中含10%FCS﹑100 U/ml青霉素及0.1 g/L链霉素。后以1×105/ml密度接种于75 ml培养瓶中,加培养液10 ml,于37℃,5%CO2饱和湿度条件下静置培养。以含0.25%胰蛋白酶-0.03%EDTA的消化液进行消化传代。
(2)α-硫辛酸对内皮细胞存活的影响:将生长状态良好的第2~5代HUVEC-12传代24 h后消化,加入含0.2 mmol/L的Hcy,再加入浓度为0.5 mmol/L ALA,孵育20 h后再加入MTT溶液,继续孵育4 h后用酶标仪在490 nm波长下测定各孔的吸光度。
(3)α-硫辛酸对内皮细胞膜上活性氧的影响:将生长状态良好的第2~5代HUVEC-12传代24 h后消化,6 h后观察细胞贴壁情况,加入浓度为0.2 mmol/L的Hcy预处理细胞2 h,再加入浓度为0.5 mmol/L的ALA共同孵育22 h。37℃细胞培养箱内孵育20 min后用激光共聚焦显微镜直接观察。
1.3 统计学方法
2 结果
2.1 细胞培养
所培养的HUVEC呈典型卵石形或多角形,见图1。
图1 HUVEC-12细胞
2.2 α-硫辛酸对半胱氨酸刺激后细胞存活的影响
Hcy组数值低于空白对照组(P<0.01),ALA组光吸收值与Hcy组比较明显升高,差异具有统计学意义(P<0.01),见表1。
表1 ALA对Hcy刺激HUVEC-12后细胞存活的影响(OD值,±s,n=3)
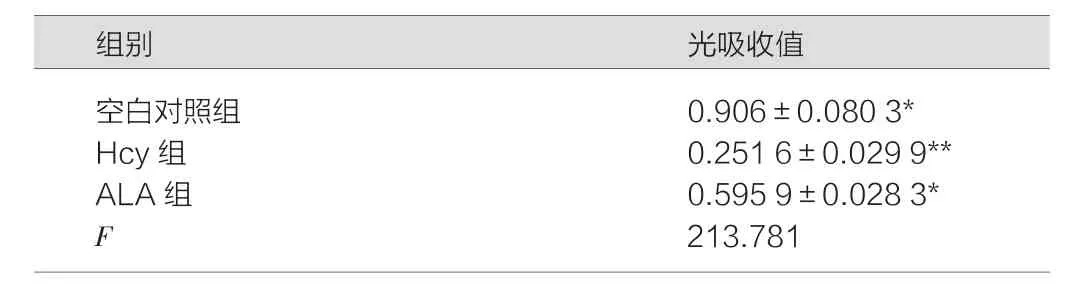
表1 ALA对Hcy刺激HUVEC-12后细胞存活的影响(OD值,±s,n=3)
注:*P<0.01 vs. Hcy组;**P<0.01 vs. 空白对照组
组别 光吸收值空白对照组 0.906±0.080 3*Hcy组 0.251 6±0.029 9**ALA组 0.595 9±0.028 3*F 213.781
2.3 α-硫辛酸对内皮细胞产生活性氧的影响
与空白对照组相比,Hcy(0.2 mmol/L)组致内皮细胞产生ROS则更为显著(P<0.01)。ALA组虽较空白对照组ROS产生无减少(P<0.05),但与Hcy组相比ROS产生减少(P<0.05),说明ALA能明显抑制Hcy所致的内皮细胞ROS生成,见图2,图3。

图2 ALA对Hcy(0.2 mmol/L)诱导内皮损伤后产生氧自由基的影响
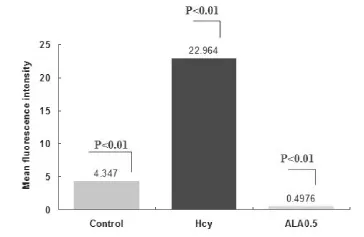
图3 不同药物对内皮细胞产生氧自由基的影响
3 讨论
血管内皮细胞不仅是血液和血管床之间的屏障,起到促进水及小分子的交换作用。同时也是一个内分泌器官,通过产生分泌一系列血管活性物质,对血管舒缩功能的调节﹑凝血及抗凝血,炎症反应的诱导等方面都具有重要的作用[3]。
高Hcy血症是血管内皮细胞损伤的危险因素,实验研究显示[4],血Hcy升高可损伤内皮细胞并导致脂质过氧化,产生的氧自由基可能参与AS过程。有研究表明[5],氧化应激在冠心病中明显加强,而且游离MDA在不稳定型和稳定型心绞痛患者间有明显差别。ALA作为一种“万能抗氧化剂”,不仅可参与保护内皮细胞,使其免受自由基和过氧化物的损伤[6]。新近有研究指出,ALA可改善早期糖尿病肾病患者氧化应激和血管内皮功能[7]。在孟馨等[8]的报道中,ALA还可参与抑制血管内皮细胞凋亡。我们推断通过应用ALA也可达到改善内皮功能障碍的作用,且其机制除了抑制活性氧产物增加外有关。
本次实验表明,Hcy对内皮细胞的存活具有抑制作用,在应用中等浓度Hcy损伤内皮细胞后,ALA组光吸收值较Hcy组升高(P <0.01)。结果表明在ALA作用下,内皮细胞的活性均可增加,且还可拮抗Hcy对内皮细胞的损害而发挥保护作用。
由于ALA可提高抗氧化应激的能力,清除过氧化脂质。本研究表明,Hcy能够使细胞膜上ROS释放增加,在其浓度为0.05~0.4 mmol/L呈剂量依赖。应用ALA后内皮细胞活性氧释放明显较Hcy组减少(P<0.05)。可见ALA可增强细胞的抗氧化能力,以此对抗Hcy对内皮细胞的损伤作用。
[1]邓宇鲲,闫冰,陈涛,等. 血浆同型半胱氨酸水平与颈动脉斑块相关性的研究[J]. 中国循环杂志,2014,29(5):363-366.
[2]王莹,王恩,王凤,等,α-硫辛酸对兔动脉粥样硬化斑块形成的影响[J]. 心脑血管病防治,2016,16(3):178-180.
[3]王全伟,凡文博,王智昊,等,氧化应激与心血管疾病关系的研究进展[J]. 中国老年学杂志,2014,34(1):192-194.
[4]Hemanth KB,Arun RR,Mahesh KJ,et al. Effects of fisetin on hyperhomocysteinemia-induced experimental endothelial dysfunction and vascular dementia[J]. Can J Physiol Pharmacol,2016,8(11):1-11.
[5]陈燕铭,吴琳,刘勇,等. 通心络对同型半胱氨酸损伤的内皮细胞的基因表达谱的影响[J].中国病理生理杂志,2011,27(1):42-47.
[6]崔珏,肖瀛,王斌,等. 硫辛酸改善高脂小鼠氧化应激和慢性炎症的研究[J].中国免疫学杂志,2010,26(7):583-586.
[7]姚伟峰,黄雌友,吴卫国,等. α-硫辛酸对早期糖尿病肾病患者氧化应激和血管内皮功能的影响[J].中国老年学杂志,2014,34(2):359-360.
[8]孟馨,王涤非,伊桐凝,等. α-硫辛酸对糖基化终产物诱导血管内皮细胞凋亡的影响[J].中国老年学杂志,2010,30(21):3104-3105.
The Protective Role of α-Lipoic Acid in the Homocysteine Induced Apoptosis of Vascular Endothelial Cells
RONG Jidong1JIANG Shuntao1DENG Yujie1LIU Hui2ZHANG Shuying3SHI Bei11 Department of Cardiology, The Affiliated Hospital of Zunyi Medical University, Zunyi Guizhou 563000, China, 2 Department of Cardiology, Guizhou Provincial People's Hospital, Guiyang Guizhou 550000, China, 3 Department of Cardiology, The Affiliated Zhongshan Hospital of Dalian University, Dalian Liaoning 116000, China
ObjectiveTo investigate the protective effect of different doses of alpha lipoic acid (ALA) on vascular endothelial cells pretreated with homocysteine (Hcy).MethodsHUVEC-12 cell lines were cultured in vitro, and randomly divided into three groups: blank control group, Hcy group (0.2 mmol/L), ALA group (0.2 mmol/L Hcy+0.5 mmol/L). after 24 hours, observe the effect of MTT on the survival of endothelial cells, and laser irradiation on the activity of reactive oxygen species in endothelial cells.ResultsAfter treated with Hcy, the cells were significantly inhibited, and Hcy could induce the production of oxygen free radicals (ROS) in endothelial cells, while ALA could antagonize the oxidative stress of Hcy, and the difference was statistically significant (P<0.01).ConclusionHcy can protect endothelial cells from oxidative damage by increasing intracellular ROS production, while alpha lipoic acid can protect endothelial cells from oxidative stress.
Endothelial dysfunction, Hyperhomocysteinaemia, α-lipoic acid
R913
A
1674-9308(2016)34-0139-02
10.3969/j.issn.1674-9308.2016.34.077
贵州省科学技术基金资助(编号:黔科合J字LKZ[2012]24号)
1遵义医学院附属医院心内科,贵州 遵义563000;2贵州省人民医院心内科,贵州 贵阳 550000;3大连大学附属中山医院心内科,辽宁 大连 116000
张曙影,E-mail:rongjidong@163.com

