铁碳微电解处理废水中的镉/锌/铅
吕星浩
(湘西土家族苗族自治州环境保护科学研究所,湖南 吉首 416000)
铁碳微电解处理废水中的镉/锌/铅

吕星浩
(湘西土家族苗族自治州环境保护科学研究所,湖南 吉首 416000)
摘要:以电解锌厂生产废水为研究对象,用铸铁屑和活性炭的混合材料组成铁碳微电解反应器,考察了处理时间、pH值、溶解氧浓度、铁碳加入量对废水中镉、锌、铅3种重金属离子去除率的影响.结果表明,在进水pH值3~5、废水停留时间30 min、溶解氧5 mg/L、铁碳添加量为50 g/L条件下,废水中镉、锌、铅3种重金属离子的去除率分别为96.5%,91.1%,72.6%.
关键词:铁碳微电解;重金属;废水
重金属废水是指矿冶、机械制造、化工、电子、仪表等工业生产过程中排出的含重金属离子的废水.电解锌废水中含有大量的镉、锌、铅、镍、汞等重金属离子,对环境造成重大影响[1].目前,电解锌废水的处理主要有化学转化法、介质提取法、物理化学浓缩法等[2-5].在这些处理方法中,化学沉淀法处理成本高,处理效果不稳定;吸附法中吸附剂使用寿命短,再生困难,操作费用高;微生物法中活体絮凝剂保存困难,难以实现工业化等[6]:因此,开发廉价、高效的重金属废水处理技术意义重大.微电解法是用铁碳材料和活性炭或者焦炭组成铁碳微电解反应器,使重金属离子通过电化学氧化还原反应和絮凝沉淀反应达到去除重金属离子污染的目的,具有适用范围广、寿命长、成本低廉和操作维护方便等优点,广泛应用于染料、印染、重金属、电解电镀废水的处理[7-8].笔者对铁碳微电解处理电解锌废水的工艺条件进行研究,考察了停留时间、进水pH值、铁碳用量对废水中Cd2+,Pb2+,Zn2+的去除效果,研究结果能为锌产品开发和电解锌废水污染治理提供依据.
1材料和方法
1.1材料和仪器
1.1.1 实验材料与试剂铁碳材料使用以铸铁屑和活性炭为主要材料按照一定比例组合制作的直径为10~20 mm的颗粒物.
实验用水样取自某公司工业废水,pH值为3.2,废水中Cd2+质量浓度为182.1 mg/L,Pb2+质量浓度为132.3 mg/L,Zn2+质量浓度为35 mg/L.NaOH:分析纯,天津市永大化学试剂有限公司.H2SO4:分析纯,衡阳市凯信化工试剂有限公司.
1.1.2 实验仪器AA-6300C 石墨炉原子吸收分光光度计(P/N 206-52430),岛津仪器(苏州)有限公司;小型增氧机(SL2800),长沙市鱼乐渔具商行.
1.2 实验装置与方法
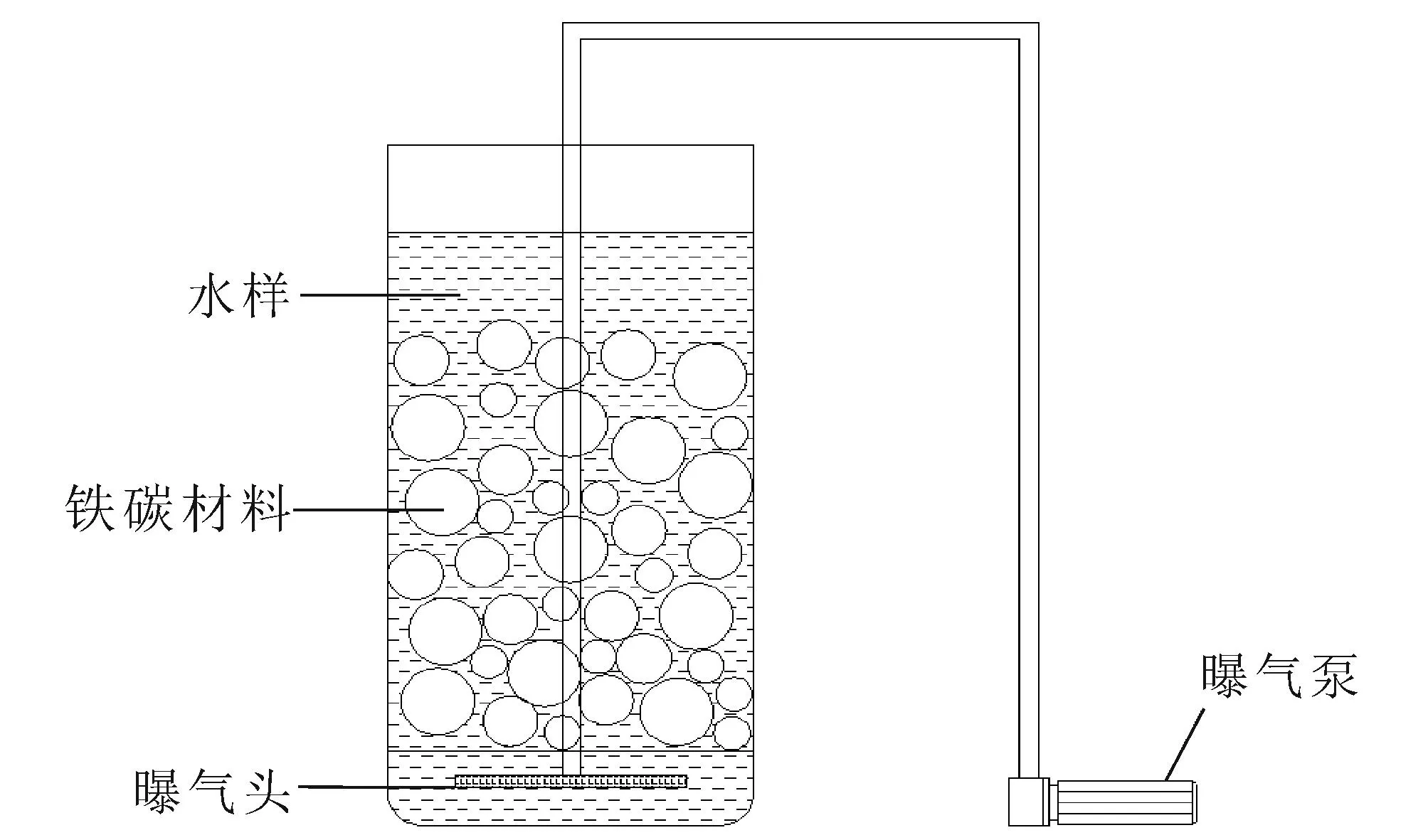
图1 铁碳微电解实验装置
1.2.1 实验装置的制作实验选用直径80 mm、长200 mm的柱状玻璃容器作为微电解反应器,底部设置有曝气头,铁碳材料放置在反应器内,装置如图1所示.
1.2.2 实验方法取水样500 mL,根据实验需求调节pH值,将所需的铁碳材料投加到反应器内,曝气.在规定的时间内取样,静置30 min,用石墨炉原子吸收分光光度计测定反应后的重金属离子含量,按下式计算去除率:
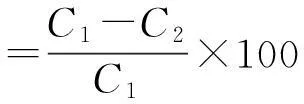
其中:C1是废水中金属离子的初始质量浓度,mg/L;C2是废水处理后金属离子的质量浓度,mg/L.
2结果与讨论
2.1 停留时间对重金属去除效果的影响
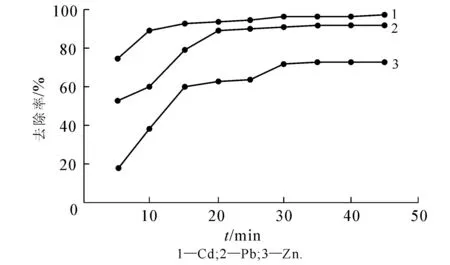
图2 停留时间对去除效果的影响
取水样500mL,按1.2.2节方法添加铁碳材料30g,不调节原始水样pH值的条件下进行反应.在不同时间段取样检测水样中Cd2+,Pb2+,Zn2+的剩余量,从而计算去除率,所得结果如图2所示.
从图2可以看出,随着反应时间的增加,3种重金属的去除率逐渐升高.Cd2+在反应10 min后去除率能达到96.5%,Pb2+和Zn2+在反应20,30 min后去除率也基本保持不变.3种重金属离子在超过30 min后,去除率均无明显增加,说明30 min内微电解反应已基本完成.因为原电池反应速度较快,随之产生的絮凝沉淀作用也可在短时间内完成,所以取适宜的停留时间为30 min.
2.2 进水pH值对重金属去除效果的影响
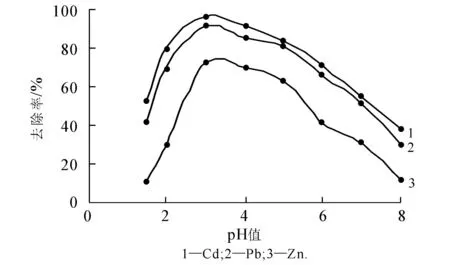
图3 进水pH值对去除效果的影响
取水样500 mL,按1.2.2节方法添加铁碳材料30 g,在反应30 min条件下,通过加酸和碱调节原始水样的pH值,考察原水pH值对废水中Cd2+,Pb2+,Zn2+去除率的影响,结果如图3所示.
从图3可以看出,pH值的变化对重金属离子的去除有很大的影响.当原始水样pH值为3时,Cd2+,Pb2+,Zn2+的去除率分别能达到96.5%,91.1%,72.5%.pH值过低或过高,重金属离子去除效率都会有所减小.这是因为微电解系统在酸性充氧条件下发生电化学反应,其反应过程为[9]:
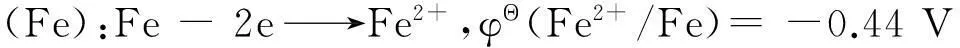

当废水中存在金属离子时,阴极还会发生如下反应:
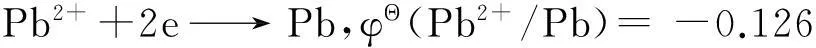
在强酸环境中,Fe2+不易被氧化为Fe3+,使得Fe(OH)3絮凝剂的生成遇到阻碍.而pH值过高时,铁失去电子能力会降低,不利于氧化还原反应,使得去除率下降.根据图3可知,pH值为3~5时,重金属离子去除效果能够达到排放标准.
2.3 溶解氧浓度对重金属去除效果的影响

图4 溶解氧对去除效果的影响
在5个盛有500 mL水样的烧杯中分别进行曝气10,30,60,120 min,测量其溶解氧浓度,然后马上将废水加入微电解反应器,在控制停留时间为30 min的条件下考察不同溶解氧浓度对重金属离子去除率的影响,结果如图4所示.
从图4可以看出,随着溶解氧浓度的增加,Cd2+,Pb2+,Zn2+的去除率也逐渐增加;当溶解氧大于5.3 mg/L时,Cd2+,Pb2+,Zn2+的去除率也趋于平稳.因为微电解反应器发生原电池反应,所以在有氧条件下,阴极将发生下列原电池反应[10-11]:
O2+ 4H++4e→2H2O,φΘ(O2)=1.23 V;
O2+ 2H2O+ 4e→4OH-,φΘ(O2/OH-)=0.40 V.
反应产生OH-,导致废水呈碱性,强化了金属离子的化学沉淀作用,因此随着溶解氧的升高,导致金属离子的去除率升高.考虑实际应用过程中的经济性,溶解氧控制在5 mg/L较适宜.
2.4 铁碳总量对重金属去除效果的影响
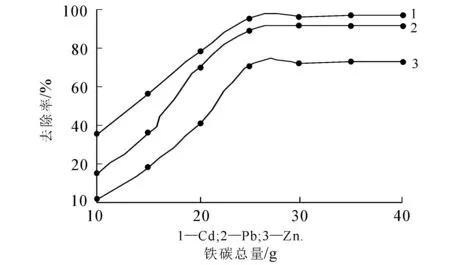
图5 铁碳总量对去除效果的影响
取水样500 mL,分别添加铁碳材料10,15,20,25,30,35 g,在控制停留时间为30 min的条件下考察铁碳总量对重金属离子去除率的影响,结果如图5所示.
从图5可以看出,随着铁碳总量的增加,Cd2+,Pb2+,Zn2+的去除率也逐渐增加.当添加量大于15 g时,Cd2+的去除率基本保持不变,而当添加量大于25 g时,Pb2+和Zn2+的去除率也趋于平稳.考虑实际应用过程中的经济性,选择添加量25 g最为适宜,也就是50 g/L.
随着铁碳总量的增加,反应器中原电池活性位不断增加,导致反应更加剧烈,金属离子去除率提高[12].但活性位增加到一定量后,已满足了原电池反应中金属离子含量所需的化学平衡,去除率不再明显提高.
2.5 最佳条件下的去除效果
为了考察单因素组合实验的实验效果,按1.2.2节方法,在进水pH值3~5,废水停留时间30 min,溶解氧5 mg/L,铁碳添加量50 g/L条件下做组合实验,平行实验5次,取平均值,结果见表1.从表1可以看出,用铁碳微电解法处理电解锌废水,Cd2+和Pb2+的去除率分别可达96.5%和91.1%,Zn2+的去除率为72.6%.这是因为铅、镉、锌的标准电极电位分别为φΘ(Pb2+/Pb)=-0.126 V,φΘ(Cd2+/ Cd)=-0.403 V,φΘ(Zn2+/Zn)=-0.762 V,锌的电极电位差最低,Zn2+被还原能力最差,所以去除率最低.

表1 最佳工艺条件组合实验的去除效果
3结论
(1)铁碳微电解法在适宜的pH值范围和适当反应时间条件下,可以处理多种重金属离子,出水可以直接达标排放.实验结果表明,在进水pH值3~5,停留时间30 min,铁碳添加量50 g/L,溶解氧5 mg/L的条件下,Cd2+,Pb2+,Zn2+的去除率分别为96.5%,91.1%,72.6%.
(2)铁碳微电解工艺不用投加化学药剂,具有适用范围广、寿命长、成本低廉及操作维护方便的优点,微电解装置简单,易于定型,可实现自动化操作.
参考文献:
[1] 郭燕妮,方增坤,胡杰华,等.化学沉淀法处理含重金属废水的研究进展[J].工业水处理,2011(12):9-13.
[2] 张默贺,叶正芳,赵泉林,等.铁碳微电解预处理TNT红水[J].环境工程学报,2012(9):3 115-3 120.
[3] KAMINARI N M S,SCHULTZ D R,PONTE M J J S,et al.Heavy Metals Recovery from Industrial Wastewater Using Taguchi Method[J].Chemical Engineering Journal,2007,126(2):139-146.
[4] ABDELAZIZ SMARA,RACHID DELIMI,ERIC CHAINET,et al.Removal of Heavy Metals from Diluted Mixtures by a Hybrid Ion ̄Exchange/Electrodialysis Process[J].Separation and Purification Technology,2007,57(1):103-110.
[6] 渠荣遴,李德森,杜荣骞,等.低浓度含重金属废水的植物修复作用研究[J].现代仪器,2003(3):32-34.
[7] 李福德.微生物治理电镀废水方法[J].电镀与精饰,2002(2):35-37.
[8] 程树培,催益斌,杨柳燕.高絮凝性微生物育种生物技术研究与应用进展[J].环境科学进展,1995,3(1):65-69.
[9] ALLAN C,VIEIRA DOS SANTOS,JORGE C.Evaluating the Removal of Cd(II),Pb(II) and Cu(II) from a Wastewater Sample of a Coating Industry by Adsorption onto Vermiculite[J].Applied Clay Science,2006,371:67-71.
[10] 刘维.铁碳微电解处理难降解有机废水的应用研究[D].长沙:中南大学,2011.
[11] 邱珉.铁碳微电解催化还原法处理铜冶炼废水中重金属离子的研究[D].昆明:昆明理工大学,2009.
[12] 赖波,秦红科,周岳溪,等.铁碳微电解预处理ABS凝聚干燥工段废水[J].环境科学,2011,32(4):1 055-1 059.
(责任编辑向阳洁)
Iron ̄Carbon Micro ̄Electrolysis Process to Remove Cd/Zn/Pb in Wastewater
LÜ Xinghao
(Xiangxi Tujia and Miao Autonomous Prefecture Environmental Protection Science
Research Institute,Jishou 416000,Hunan China)
Abstract:The wastewater from electrolysis ̄Zn factory was studied,and was treated by iron ̄carbon micro ̄electrolysis reactor.The effects of time,pH value,DO and the dosage of iron ̄carbon were investigated on the removing rate of Cd,Pb and Zn in the wastewater.The results show that the iron ̄carbon micro ̄electrolysis process can be effectively used for the treatment of heavy metal wastewater on the suitable conditions:pH value 3~5,staying reaction time 30 min,DO 5 mg/L and the dosage of iron ̄carbon 50 g/L.On the best condition,the removal rates of Cd,Pb and Zn reached 96.5%,91.1%,72.6% respectively.
Key words:iron ̄carbon micro ̄electrolysis;heavy metal;wastewater
作者简介:吕星浩(1981—),男,吉林伊通人,湘西自治州环境保护科学研究所工程师,主要从事环境污染治理工程技术研究.
收稿日期:2014-10-13
中图分类号:X703.1
文献标志码:B
DOI:10.3969/j.cnki.jdxb.2015.03.016
文章编号:1007-2985(2015)03-0073-04

