不同pH对NH4V3O8形貌及电化学性能的影响
黄剑锋, 乔晓宁, 许占位, 欧阳海波, 李嘉胤, 曹杉杉
(陕西科技大学 材料科学与工程学院, 陕西 西安 710021)
不同pH对NH4V3O8形貌及电化学性能的影响
黄剑锋, 乔晓宁, 许占位, 欧阳海波, 李嘉胤, 曹杉杉
(陕西科技大学 材料科学与工程学院, 陕西 西安710021)
摘要:以偏钒酸铵(NH4VO3)为原料,采用水浴辅助化学沉淀法,制备出了形貌可控的钒酸铵(NH4V3O8),并利用X射线衍射仪(XRD)、傅立叶变换红外光谱仪(FT-IR)、扫描电子显微镜(SEM)等对产物的物相、形貌及电化学性能进行了表征分析.结果表明:当体系的pH为1.5、2.0、3.0、4.0和5.0时,分别得到了花球状、束状、棒状、片状的NH4V3O8.其中,棒状结构的NH4V3O8电化学性能最好,在15 mA·g-1电流密度下,放电比容量高达260 mAh·g-1,20圈循环后容量保持率达96%.
关键词:化学沉淀法; NH4V3O8; 锂离子电池
0引言
随着石油、天然气等天然资源的不断消耗和生态环境的日益恶化,人类对可再生能源的需求日益强烈.因此,清洁、方便、高能量密度以及大功率的能源供应系统备受亲睐.其中,锂离子电池因其能量密度高、安全性能好、循环寿命长、环境友好等优点,已经在便携式电工工具、移动设备及笔记本电脑等领域得到了广泛应用[1-3].然而,电池的能量密度主要取决于正极材料,目前主流正极材料的实际放电比容量均比较低,如磷酸铁锂为170 mAh·g-1、钴酸锂为140 mA·g-1[4,5].因此,开发出高比容量、低成本的正极材料十分必要.
钒氧化物及钒酸盐材料由于其比容量较高(300 mAh·g-1)和生产成本相对较低的特点成为了近年来研究的热点[6].同时,我国钒资源较为丰富,但对其综合开发利用程度较低,严重制约了我国钒资源的开发.因此,开发出具有高比容量的钒酸盐嵌锂材料,不仅有助于提高我国钒资源的利用效率,而且能够促进经济的可持续发展[7].
近年来,NH4V3O8作为一种新型的钒酸盐嵌锂材料,凭借其比容量高、循环性能好的优点而受到了广泛关注[8-10].目前,制备NH4V3O8的方法主要为水热法.通常需要在高温下(>140 ℃)反应24 h以上,不利于实现大规模生产[9-15].同时,由于电极材料的结构、形貌对其电化学性能具有较大的影响,因此,探索出新型的、合成形貌可控的NH4V3O8材料的制备方法,对NH4V3O8电极材料的发展十分重要.
沉淀法是一种简便的制备无机纳米材料的方法[16,17].近年来,其已得到了广泛应用,但有关NH4V3O8材料的沉淀法合成还鲜有报道.本文尝试采用水浴辅助化学沉淀法,以NH4VO3为原料,通过水浴加热处理,制备出了具有多种形貌的NH4V3O8材料,并研究了溶液pH值对NH4V3O8的形貌以及电化学性能的影响.
1实验部分
1.1 钒酸铵(NH4V3O8)的制备
称取1.17 g 99.99%的NH4VO3溶于100 mL去离子水中,通过磁力搅拌器搅拌至完全溶解得到0.1 mol·L-1的浅黄色透明溶液;然后用2 mol·L-1的稀盐酸调节溶液pH值至1.5、2.0、3.0、4.0及5.0,并将盛有上述溶液的烧杯封口后,置于电热恒温水浴锅中90 ℃反应2 h;反应结束后,将所得固体物质离心、洗涤、干燥后即获得最终产物NH4V3O8.
1.2 电极片的制备
将所得产物NH4V3O8、导电剂乙炔黑和粘结剂聚偏氟乙烯PVDF以质量比8∶1∶1的比例充分混合,加入适量的N-甲基吡咯烷酮(NMP),研磨得到均匀浆液;将其涂在集流体铝箔得到厚度约为15μm的平整均匀极片,并在120 ℃条件下真空干燥10 h,切片成直径为15.8 mm的正极片.
实验采用CR2032纽扣电池,按照负极壳-弹簧片-垫片-锂片-滴加电解液-隔膜-滴加电解液-正极片-正极壳的顺序组装,并在充满氩气的手套箱中完成扣式电池的组装.其中,电解液采用商用锂离子电池电解液(LiPF6/EC+EMC+DMC (1∶1∶1)),隔膜采用Cergard2400聚丙烯微孔膜.
1.3 测试与表征
产物的物相采用日本理学产D/max 2200PC型X射线衍射仪(X-ray Diffraction,XRD)进行分析,测试条件为:铜靶Kα射线,X射线波长λ=0.154 18 nm,2θ=5 °~70 °.
采用天津布兰顿科技有限公司产ERTE70型红外光谱分析仪,通过特定位置的吸收峰对样品中的化学键进行鉴定.
产物的显微结构采用日本Jeol公司产JSM-6390A型扫描电子显微镜(Scanning Electron Microscope,SEM)进行观察.
电化学循环性能采用深圳新威产5 V/1 mA型高精度电池性能测试系统在1.5~4.0 V的电压范围内进行恒流充放电测试.
伏安循环曲线测试采用上海辰华产CHI-660E型电化学工作站,测试条件为:电压范围为1.5~4.0 V、扫描速率为0.1 mV/s;阻抗谱测试采用CHI-660E电化学工作站,测试频率为0.01~1 00 00 Hz.
2结果与讨论
2.1 产物的XRD分析
图1呈现了pH为1.5~5.0时所制备产物的XRD图.由图1可知,在pH为1.5~5.0条件下均可以得到NH4V3O8.当pH值较小(为1.5)时,所获得产物的衍射峰较弱,产物中存在部分NH4V4O10相(JCPDS No.31-0075)[18];当溶液pH为2.0~5.0时,各样品的衍射图谱与NH4V3O8的标准衍射图谱JCPDS No.88-1473完全一致,无其它杂质峰存在,说明产物为纯相的NH4V3O8.
由此得出:当pH值由1.5增大到5.0时,产物的结晶性存在明显差异,NH4V3O8的(001)晶面衍射峰不断增强.
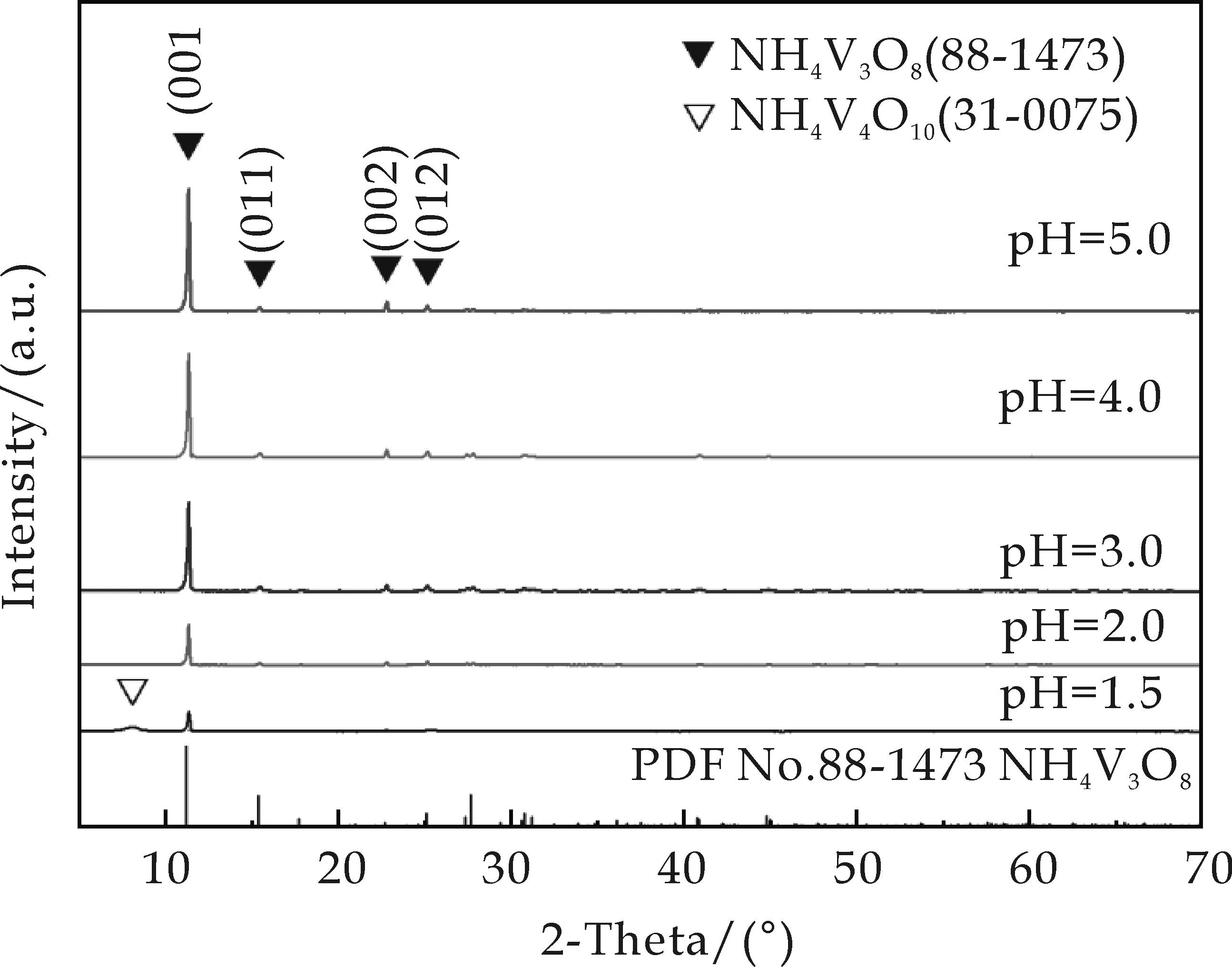
图1 不同pH条件下所得产物的XRD图
2.2 产物的FT-IR分析
图2为不同pH条件下制备的NH4V3O8的FT-IR图.由图2可知,当pH为1.5时,所得产物的FT-IR图与其它四个样品略有不同,其在1 000 cm-1和765 cm-1出现了NH4V4O10的特征吸收峰,分别由V=O键伸缩振动和V-O-V键不对称地伸缩振动引起[19];当pH为2.0~5.0时,所制备NH4V3O8的FT-IR图极为相似,在3 213 cm-1、1 402 cm-1、1 004 cm-1、968 cm-1、736 cm-1和528 cm-1处出现了六个NH4V3O8的特征红外吸收峰,与文献[13]报道相一致.这进一步证明当pH为2.0~5.0时,所得NH4V3O8样品具有类似结构,不同于pH为1.5时所制备产物.另外,这五个样品在3 410 cm-1和1 632 cm-1处均出现了红外吸收峰,表明样品中存在少量的结晶水[20].
由此可得:当pH为1.5时,所得产物的结构不同于其它四个样品,与XRD结果(当pH为1.5时,得到NH4V3O8与NH4V4O8混合相;当pH为2.0~5.0时,得到纯相NH4V3O8)相符.
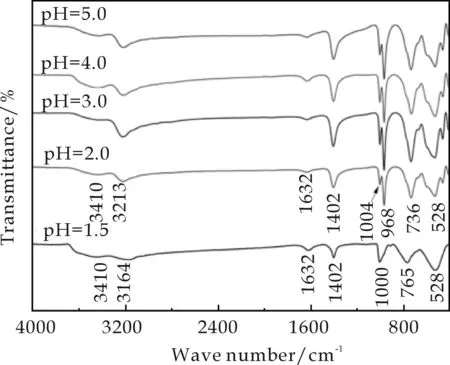
图2 不同pH条件下所得产物的FT-IR图
2.3 产物的微观形貌分析
图3为不同pH条件下所制备NH4V3O8的SEM图.从图3可知,当pH为1.5时,所得产物为规则的球状形貌,其直径可达5μm左右;当pH为2.0时,所制备NH4V3O8由大量一维纳米结构团聚而成集束状形貌,从其右上角的放大图可看出:所制备NH4V3O8呈现出纳米棒形貌,其直径在40~50 nm,长度达500~600 nm,然而分散性非常差,纳米棒直径团聚十分严重;当pH为3.0时,所得NH4V3O8仍为纳米棒形貌,可是分散性变好,直径增大为50~60 nm,同时出现了少量的片状结构;当pH增大到4.0以上时,产物NH4V3O8均呈现出形状不规则的片状,且随着pH由4.0增大至5.0,产物片状结构的尺寸由10μm增大到20~30μm.
由此可得:当pH从1.5增大到5.0时,NH4V3O8尺寸和形貌发生了明显变化.具体来说,pH较小时所制备NH4V3O8趋向于生长成一维纳米带和纳米棒;当pH增大到4.0后,NH4V3O8呈现出二维片状形貌.究其原因为:pH较小时,由于溶液H+数量多、浓度大,瞬间产生的晶核较多,使得产物NH4V3O8尺寸小,同时过多的H+会吸附在产物表面而抑制其某些晶面的生长,产物趋向于长成一维结构;当pH值较大时,溶液中H+数量少,因而产生的晶核较少,其不断长大表现出二维片状形貌.因此,不同NH4VO3溶液pH值所制备的NH4V3O8的结构不同,可能会导致各样品性能有所差异.

(a)pH=1.5 (b)pH=2.0

(c)pH=3.0 (d)pH=4.0

(e)pH=5.0图3 不同pH条件下所得产物的SEM图
2.4 产物的电化学性能分析
图4(a)为不同pH值条件下所制备NH4V3O8在15 mA·g-1的循环性能曲线.当pH为1.5时,所制备球状产物初次容量高达298 mAh·g-1,但由于NH4V4O10杂相存在,其容量衰减严重,20次循环后降低至229 mAh·g-1(占最高容量的76.8%);当pH为2.0、3.0、4.0及5.0时,所得产物NH4V3O8的首次放电容量分别是237 mAh·g-1、245 mAh·g-1、213 mAh·g-1和196 mAh·g-1.当pH为2.0~5.0时,所得NH4V3O8循环稳定性较好,经20次循环后其容量仍然保持在最大值的95%、96%、96%和97%;当pH为3.0时,所得NH4V3O8纳米棒具有高的容量和好的循环稳定性,这与该产物较低的结晶性及分散良好的纳米棒结构有关.
图4(b)呈现了不同pH值条件下所制备NH4V3O8在15 mA·g-1的首次充放电曲线.不同pH值所得样品的曲线形状有所不同.当pH为1.5时,所得产物在2.35 V、2.70 V处有两个充电平台,对应的放电平台位于2.5 V和2.8 V;当pH为2.0~5.0时,所制备纯相NH4V3O8均表现出三对充放电平台,但曲线形状略不相同.对比这几条曲线发现:pH为3.0时所得NH4V3O8纳米棒的充放电平台最为明显;pH为1.5时所得花球状产物的平台最不显著(可能由于其含有部分NH4V4O10杂相).
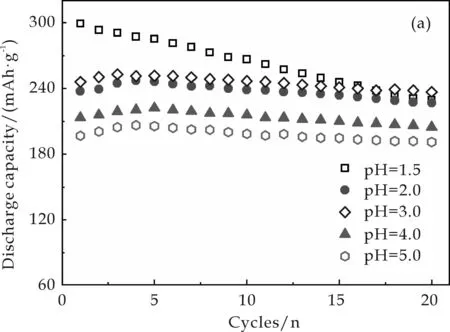
(a)循环性能图

(b)首次充放电曲线图4 不同pH条件下所得产物在15 mA·g-1电流密度下的电化学性能图
图5为不同pH条件下所制备NH4V3O8的倍率性能.从图5可知,当pH为1.5时,所制备NH4V3O8与NH4V4O8混合相性能最差,随循环次数增多、电流增大,其容量不断降低;当pH为3.0时,所得NH4V3O8纳米棒性能最好.在电流密度为15 mA·g-1、60 mA·g-1、120 mA·g-1、240 mA·g-1、300 mA·g-1条件下,其最大放电容量分别为260 mA·g-1、234 mA·g-1、179 mA·g-1、156 mA·g-1、129 mAh·g-1,且该样品在各电流(15~300 mA·g-1)下均有良好的循环稳定性.究其原因为:pH为3.0时所制备的纯相NH4V3O8纳米棒分散性好、尺寸小,不仅便于NH4V3O8电极材料和电解液充分接触,而且缩短了Li+和e-传输距离,有利于Li+快速脱嵌.
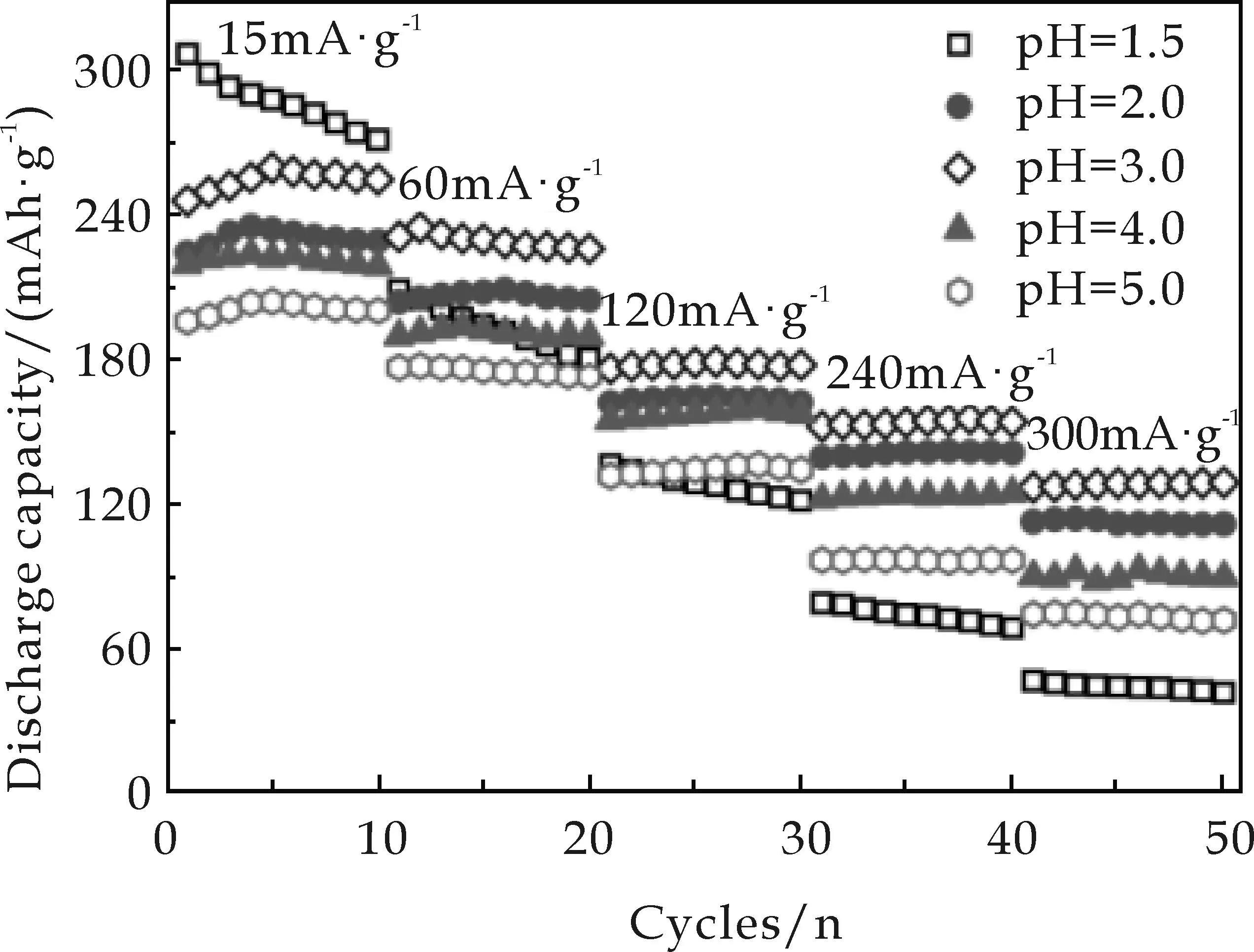
图5 不同pH条件下所得产物的倍率性能图
图6(a)为不同pH值条件下所制备NH4V3O8的CV曲线.当pH为1.5时,所得产物表现出了两对氧化还原峰(可能由于其含有部分NH4V4O10杂相),与图4(b)中该样品呈现出的充放电平台相对应;当pH为2.0~5.0时,所得的纯相NH4V3O8均有三对氧化还原峰,只是所处峰的位置及峰电流大小有所不同.经比较可知:pH为3.0时所得NH4V3O8纳米棒的氧化还原峰对称性较好,峰电流也较大,显示了其充放电过程中较好的可逆性,此推论可进一步解释为何该产物电化学性能较好.
图6(b)显示了不同pH条件下所制备NH4V3O8的交流阻抗谱.不同pH值所得产物的图谱形状类似,均由半圆及随后的斜线两部分构成.图中半圆与横轴截距大小反映了电极材料的电荷转移电阻Rct[21].从图6(b)得知,当pH为1.5、2.0、3.0、4.0和5.0时,所得NH4V3O8电极的Rct分别为48 Ω、89 Ω、120 Ω、188 Ω和266 Ω.不同pH值下制备产物的Rct大小不同,这与各样品的形貌及尺寸差异有关.尺寸较小的纳米的NH4V3O8材料的Li+和e-传输路径短,离子转移比较容易,因而Rct较小.这也从另一方面解释了为何pH为1.5~3.0时所得NH4V3O8性能相对较好.
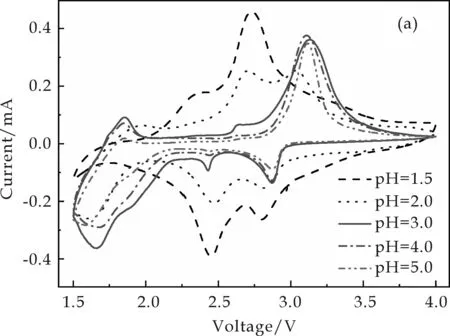
(a)CV曲线

(b)电化学阻抗(EIS)谱图6 不同pH条件下所得产物的CV和EIS曲线
3结论
以NH4VO3为原料,采用水浴辅助化学沉淀法(水浴温度为90 ℃,反应2 h)制备出了形貌可控的NH4V3O8电极材料.通过改变溶液pH值,产物的物相、形貌及性能均发生了明显变化.当pH为1.5时,所得花球状产物中有部分NH4V4O10相,性能较差;当pH为2.0~5.0时,均可得到纯相的NH4V3O8,产物的结晶性随pH值的增大而增强,产物形貌由纳米棒状变为片状;当pH为3.0时的纳米棒状NH4V3O8具有最佳的性能,在电流密度为15 mA·g-1、60 mA·g-1、120 mA·g-1、240 mA·g-1及300 mA·g-1时,其最大放电容量分别为260 mAh·g-1、234 mAh·g-1、179 mAh·g-1、156 mAh·g-1和129 mAh·g-1.
参考文献
[1] 庄全超,武山,刘文元,等.锂离子电池材料研究进展[J].电池,2003,33(2):116-118.
[2] 贾恒义.锂离子电池材料的研究与应用[J].电源技术,2011(7):869-871.
[3] Scrosati B.Recent advances in lithium ion battery materials[J].Electrochimica Acta,2000,45(15-16):2 461-2 466.
[4] 黄学杰.锂离子电池正极材料磷酸铁锂研究进展[J].稀有金属材料与工程,2004,9(4):176-180.
[5] 何志奇,于利红,郑曦,等.球形钴酸锂的乳液法合成及其结构、性能研究[J].化学学报,2005,63(24):2 185-2 188.
[6] 王海燕,唐有根,周东慧,等.锂离子电池用新型MV3O8(M=Li+,Na+,NH4+)嵌锂材料[J].化学进展,2013,25(6):927-939.
[7] D Wang,L Cao,J Huang,et al.Synthesis and electrochemical properties of LiV3O8via an improved sol-gel process[J].Ceramics International,2012,38(4):2 647-2 652.
[8] H K Park,G Kim.Ammonium hexavanadate nanorods prepared by homogeneous precipitation using urea as cathodes for lithium batteries[J].Solid State Ionics,2010,181(5):311-314.
[9] H Y Wang,K L Huang,S Q Liu,et al.Electrochemical property of NH4V3O8·0.2H2O flakes prepared by surfactant assisted hydrothermal method[J].Journal of Power Sources,2011,196(2):788-792.
[10] H Y Wang,Y Ren,W J Wang,et al.NH4V3O8nanorod as a high performance cathode material for rechargeable Li-ion batteries[J].Journal of Power Sources,2012,199(1):315-321.
[11] 韩园园,朱伟琼,李容.NH4V3O8纳米线的水热合成及超级电容器性能[J].应用化工,2013,42(1):12-14.
[12] S G.Leonardi,P Primerano,N Donato,et al.Behavior of sheet-like crystalline ammonium trivanadate hemihydrate (NH4V3O8·0.5H2O) as a novel ammonia sensing material[J].Journal of Solid State Chemistry,2013,202:105-110.
[13] L Q Mai,C S Lao,B Hu,et al.Synthesis and electrical transport of single-crystal NH4V3O8nanobelts[J].The Journal of Physical Chemisrty Letters B,2006,110(37):18 138-18 141.
[14] S D Huang.NH4V3O8:A novel sinusoidal layered compound formed by the cation templating effect[J].Chemical Communications,1998,10(10):1 069-1 070.
[15] 姚奇志.NH4V3O8一维纳米线的溶液相生长和表征[J].化学世界,2007(10):585-593.
[16] C Y Hu,J Guo,J Wen,et al.Preparation and electrochemical performance of LiNi0.5Mn0.5O2-xFx (0≤x≤0.04) cathode material synthesized with hydroxide co-precipitation for lithium ion batteries[J].Cheminform,2013,44(51):121-127.
[17] G J Xing,Y M Li,Y L Li,et al.Morphology-controllable synthesis of SrMoO4hierarchical crystallites via a simple precipitation method[J].Materials Chemistry and Physics,2011,127(3):465-470.
[18] H A Abbood,H Peng,X H Gao,et al.Fabrication of cross-like NH4V4O10nanobelt array controlled by CMC as soft template and photocatalytic activity of its calcinated product[J].Chemical Engineering Journal,2012,209(20):245-254.
[19] S Sarkar,P S Veluri,S Mitra.Morphology controlled synthesis of layered NH4V4O10and the impact of binder on stable high rate electrochemical performance[J].Electrochimica Acta,2014,132(3):448-456.
[20] L Q Mai,X Xu,C H Han,et al.Rational synthesis of silver vanadium oxides/polyaniline triaxial nanowires with enhanced electrochemical property[J].Nano Letters,2011,11(11):4 992-4 996.
[21] H Y Wang,K L Huang,Y Ren,et al.NH4V3O8/carbon nanotubes composite cathode material with high capacity and good rate capability[J].Journal of Power Sources,2011,196(22):9 786-9 791.
【责任编辑:晏如松】
Influences of pH on the morphology and electrochemical
performance of NH4V3O8
HUANG Jian-feng, QIAO Xiao-ning, XU Zhan-wei,
OUYANG Hai-bo, LI Jia-yin, CAO Shan-shan
(School of Materials Science and Engineering, Shaanxi University of Science &Technology, Xi′an 710021, China)
Abstract:NH4V3O8with controllable morphologies were successfully prepared via chemical precipitation process assisted by water bath method by using NH4VO3as raw material.The influences of different pH on phase, morphology of NH4V3O8were researched by X-Ray Diffraction (XRD), Fourier Transform Infrared Spectroscopy (FT-IR) and Scanning Electron Microscope (SEM).Results indicate that NH4V3O8with various morphologies of flower-like,bunch-like,nanorod and sheet can be obtained by water bath method with various pH of 1.5,2.0,3.0,4.0 and 5.0,respectively.Among them,the NH4V3O8nanorod displays the best electrochemical performance.At a current density of 15 mA·g-1,it showed discharge capacity of 260 mAh·g-1with capacity retention of 96% after 20 cycles,suggesting its promising application as lithium ion battery cathodes.
Key words:chemical precipitation; NH4V3O8; lithium ion battery
中图分类号:TB383
文献标志码:A
文章编号:1000-5811(2016)01-0057-05
作者简介:黄剑锋(1970-),男,重庆人,教授,博士生导师,研究方向:碳/碳复合材料抗氧化涂层、功能薄膜材料和纳米粉体
基金项目:国家科技支撑计划项目(2013BAF09B02);国家973计划前期研究专项项目(2014CB260411); 国家自然科学基金项目(51472152); 陕西省科技厅科研创新团队计划项目(2013KCT-06); 陕西科技大学学术团队计划项目(XSD1445); 陕西科技大学博士科研启动基金项目(BJ15-01); 陕西科技大学研究生创新基金项目
收稿日期:*2015-11-24

