先进技术在医用纺织材料中的应用
先进技术在医用纺织材料中的应用*
秦益民1李可昌2邓云龙2申胜标2郝玉娜2邵建华2
(1. 嘉兴学院材料与纺织工程学院,嘉兴,314001;
2. 青岛明月海藻集团有限公司,青岛, 266400)
摘要:阐述了高分子、纤维和纺织材料等功能化改性的研究进展,介绍了制备医用纺织材料的工艺技术及其产品的性能和应用。通过对高分子、纤维、纺织材料、复合材料等的化学、物理、生物等功能化改性,可以有效提高纺织材料的使用性能,开发具有高吸湿、抗菌、抗紫外、药物缓释和防护等功能的医用纺织新材料,在生物医用材料及功能性医用纺织品领域有重要的应用价值。
关键词:医用纺织材料,生物医用材料,功能化,改性技术,研究进展
中图分类号:TS106.6+7文献标志码:A
收稿日期:2014-11-02
作者简介:秦益民,男,1965年生,教授。主要从事功能性纤维的研究与开发。
医用纺织材料是一类基于纤维,用于医疗的具有生物相容性、无毒副作用的功能纺织材料,其制品广泛应用于病区防护、个人卫生、外科修复、人造器官等与人类健康密切相关的领域,涉及医生工作服、病人服、床单、手术巾、纱布、卫生巾、手术缝合线、人造血管、组织工程支架等种类繁多的医疗卫生产品[1],其制备过程包括化学纤维、纺纱、机织、针织、编织、非织造布和特殊织物等领域的传统和先进加工技术[2-4]。人口老龄化和人类对健康与长寿的追求为医用纺织材料的发展提供了不断增长的市场,社会的进步与生活水平的提高也对医疗卫生用品的性能、质量、可操作性等指标提出了更为严格的要求。结合医疗、材料、纺织、生物、机械、电子等相关领域的技术进步,纺织材料特有的强度、延伸性、柔性、透气和透湿性等性能为医疗卫生和保健领域的产品开发提供了技术保障,在与先进的材料加工技术结合后,医用纺织材料可以为医疗领域提供性能优越、质量可靠、使用便捷的新产品,其多功能及智能特性在与高表面积、高吸收性等传统性能结合后具有很高的应用价值[5]。
*山东省泰山学者蓝色产业计划项目(20130009)
本文综述了医用纺织材料领域的技术进展,并介绍了高分子材料改性、纤维加工、纺织成型及复合材料等领域的新技术及其在医用纺织材料中的应用。
1高分子材料的功能化改性技术
图1显示了以高分子为原料制备医用纺织材料的基本流程,其中高分子材料的理化特性对医用纺织材料的生物相容性、生物可降解性、吸湿性、抗菌性和其他功能特性起决定作用[6]。甲壳素、海藻酸等天然高分子及其改性产物具有良好的生物相容性、亲水性、生物可降解性等特性,适用于制备高吸湿、亲肤、护肤类医用纤维,而聚乙烯、聚丙烯、聚酯、聚酰胺、聚氨酯等合成高分子材料具有优良的力学性能,在防护、过滤、隔离等应用领域具有更好的应用价值。
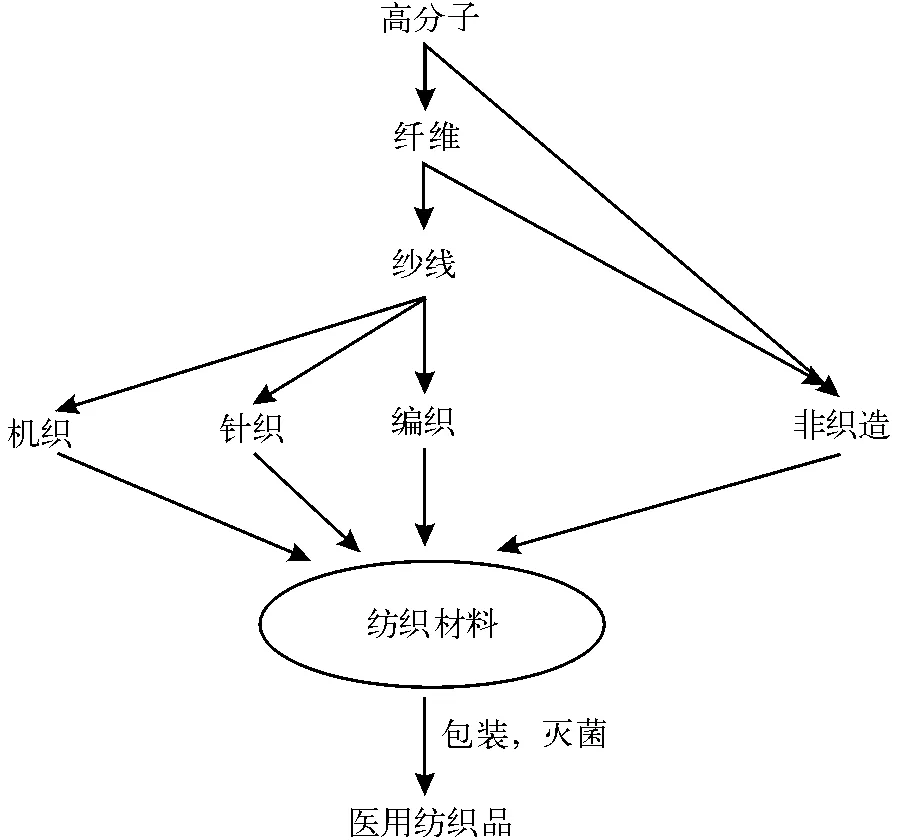
图1 医用纺织材料的结构框架示意
通过化学改性可以有效提高天然和合成类高分子材料的使用性能,在强化其特性的同时拓宽其应用范围。甲壳胺是一种具有特殊聚阳离子特性的天然高分子,其抑菌、促愈等性能在功能性医用敷料中有很高的应用价值。用氯乙酸、环氧乙烷、环氧丙烷等对甲壳胺进行化学改性后制备的羧甲基、羟乙基、羟丙基甲壳胺等改性产物是甲壳胺的水溶性衍生物,在与海藻酸钠共混后能制备具有很高吸湿性能的共混纤维材料,可应用于医用敷料的生产。
合成高分子的结构和性能可以通过聚合过程中单体组成的控制加以调节,共聚改性已成为医用高分子材料改性的一个重要途径。对羟基乙酸、乳酸等聚合过程中单体比例的调节可以有效控制共聚产物的亲水或疏水性,以及熔融温度、生物降解速度等综合性能,可以根据临床使用需要开发适合皮肤移植、手术缝合线等用途的共聚物。
在单体、支链、主链侧基的功能化改性过程中加入具有抗菌性能的化学基团后可以赋予高分子材料本质抗菌性能。把聚对苯二甲酸乙二醇酯用氧等离子体辉光放电处理后可以在其表面产生活性基团,在与季铵化甲壳胺耦合后得到接枝了具有抗菌作用的甲壳胺的聚对苯二甲酸乙二醇酯[7]。
2纤维材料的功能化制备技术
通过湿法、熔融、静电纺丝等化学纤维制备技术可以把各种类型的高分子材料加工成具有一定强度和延伸性的纤维材料,并通过纺织工艺加工成织物后应用于医疗卫生领域。在此过程中,通过对加工条件的控制可以制备具有特殊结构、理化性能和力学特性的纤维材料,使其具有应用过程中所需要的粗细度、形态结构、纯度、无菌性、吸湿性、蓬松性、舒适性等特性,起到止血、缓解疼痛、保暖、透气、低黏、无过敏、无刺激等医用纺织材料所需要的功效[8]。以下是几种适用于医用纺织材料的纤维成形和改性技术。
2.1超细纤维技术
超细纤维的直径小于5 μm或线密度低于0.33 dtex,由其制备的纺织品刚性低、手感柔软、比表面积高,并通过毛细效应使织物具有良好的吸湿和散湿性。用超细纤维加工制备的医用纺织材料具有舒适、美观、保暖、透气等性能,疏水和防污特性有明显提高。超细纤维面料可用于防护类医用纺织品的制备,也可用于血液过滤等特殊领域[9]。
2.2纳米技术与纳米纤维
纳米技术为医用纺织材料的研发提供了广阔的空间。作为功能性添加剂,纳米材料在抗菌及防静电性能、抗紫外线、防沾污性、抗皱性等领域有重要的应用价值,而基于天然和合成高分子的纳米纤维、纳米管、纳米棒等新材料也有特殊的应用价值,可以负载顺磁性粒子、抗菌药物、酶等生物活性材料,用于防护性服装、药物缓释、组织工程、再生医学等领域[10]。
2.3静电纺丝技术
静电纺丝是近年来得到迅速发展的一种纤维生产技术,可以通过溶剂的挥发制备具有纳米尺度的纤维材料。以水为溶剂可以制备聚氧化乙烯、聚乙烯醇等水溶性纤维,以有机溶剂可以制备聚乳酸、聚酰胺等超细纤维材料[11]。共静电纺丝把两组纺丝液通过同心环形喷嘴挤出成形,并通过喷丝孔的设计可以把一种高分子包埋在另一种高分子中形成复合纤维,由于成形速度快,两种高分子在形成纤维前尚未混合,处在核心部位的高分子可以负载药物等活性成分,而外层高分子可以起到缓控释放的功能[12]。
2.4中空纤维
以醋酸纤维素和铜氨人造丝为原料制备的中空纤维在医疗卫生领域中有很高的应用价值,可用于过滤及生物反应器。聚砜、聚酰胺、聚丙烯腈等合成高分子制备的中空纤维也具有很好的使用价值,在用含磷脂的高分子改性后可以有效改善其与血液的相容性,降低其对蛋白质的吸附和血小板的黏附。用磷脂类高分子与纤维素共混后制备的中空纤维膜具有很好的透气性、血液相容性和细胞相容性,在血液净化和肝脏辅助生物反应器中起重要作用[13-15]。
2.5成胶性纤维
成胶性纤维是一类在遇水湿润后能形成纤维状水凝胶的功能纤维材料,其纤维结构富含亲水性基团,能把大量的水分吸收进入纤维的结构中,在具有很高吸湿性的同时也具有很好的保湿性能,可为伤口的愈合提供一个湿润的环境,适用于功能性创面用敷料的制备。把棉花、黏胶纤维、甲壳胺纤维等含有羟基、氨基等活性基团的纤维与氯乙酸进行羧甲基化改性处理后,可以在纤维结构中加入亲水性的羧甲基钠基团,得到的羧甲基纤维素和羧甲基甲壳胺纤维具有优良的成胶性能,可以在吸收伤口渗出液后形成一个湿润但不潮湿的环境,有效促进伤口的愈合[16]。
3纺织材料的功能化成型技术
医用纺织材料具有批量小、结构复杂、性能多样等特点,在加工成型过程中适合使用个性化的成型技术以控制材料的形状、孔隙度、体积、纤维取向等结构特征,更好地满足其在医疗领域中应用的要求[17]。以下是一些应用于医用纺织材料中的纺织成型技术。
3.1间隔织物
具有三维立体结构的间隔织物包含大量的空间,有超强的吸湿、保湿功效,在医用敷料、卫生材料、吸湿垫等产品中有很高的应用价值。如图2所示,间隔织物由表面层和间隔纤维组成,后者一般由具有较强刚性的单丝制备,这样的结构在具有包容液体、隔热等性能的同时也具有较好的耐压性,可以通过控制纤维的种类、纤维在织物中的取向、针迹密度等工艺参数调控产品的性能。
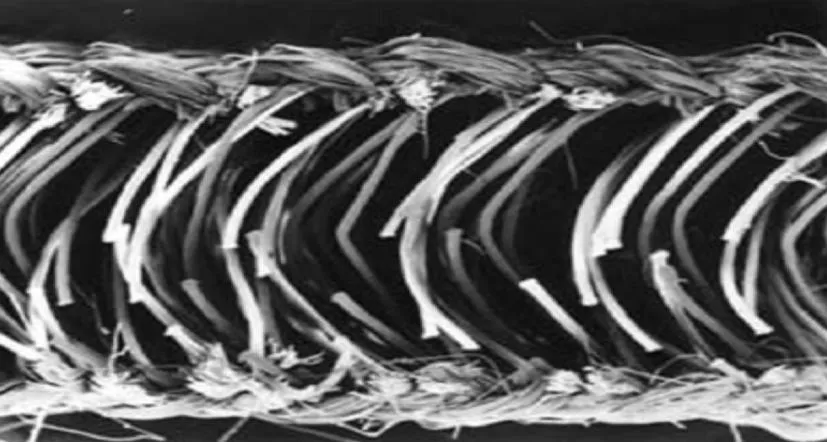
图2 间隔织物结构示意
3.2涂层和复合
对纺织材料进行涂层处理可以有效改变其表面性能。例如,用甲壳胺对非织造布进行后整理,可以使材料负载一层具有生物活性的甲壳胺薄膜,起到抑菌、促进伤口愈合等作用,有效阻止外源微生物的入侵[18];用多孔热塑性或热固性薄膜与纺织材料复合可以获得防水、透气、隔离微生物等功效,其中用聚四氟乙烯膜与纺织材料复合,可以把纺织材料的强度、柔顺性和膜的耐酸、耐碱、防水等特性有效结合,在卫生材料中有特殊的应用价值。
图3显示了一种用乙烯-丙烯酸甲酯共混膜与含银海藻酸盐非织造布复合后制备的抗菌医用敷料,其中隔离膜在降低敷料对创面黏附性的同时通过其多孔结构为伤口渗出液提供通透性,而非织造布中的镀银聚酰胺纤维可以持续释放出银离子,在海藻酸盐非织造布吸收大量渗出液的基础上为敷料提供抗菌性能[19]。

图3 一种复合抗菌敷料的示意
3.3表面处理
通过物理、化学、生物等改性处理可以改变纺织材料的表面结构,提高其亲水、抗菌、低黏等使用性能。通过电镀、等离子体喷雾等方法在织物表面负载一层金属银可以制备具有抗菌性能的医用敷料应用于烧伤创面的护理,利用纳米银对纺织材料处理后也可以得到具有抗菌和消毒功能的医用纺织材料,对细菌、真菌、微生物有很强的抑制作用[20]。为了改善医用纺织材料的亲水性能,可以对纺织材料进行等离子体表面处理,以改变其化学组成,增加亲水性基团,并由此改善其转送水蒸气和水的性能[21- 22]。
3.4其他纺织技术
纺织材料结构和性能的多样化特性为其在医疗领域的应用提供了广阔的空间,在对纤维、纱线、织物的结构进行改性的基础上可以控制医用纺织材料对空气和水的渗透性以及对电、热、冷、暖的传递特性,有效控制医用防护服的透气性和舒适性能[23]。利用纤维在纺织材料中的取向可制备各向异性流体传输特性的产品,在垂直和横向具有不同的结构和性能,并通过控制织物孔隙度、纤维直径和取向分布可制备具有特殊性能的医用纺织材料。此外,利用刺绣技术可制备组织工程支架材料,通过负载辅助记录和传输信号的微电子智能材料可用于医疗诊断中生物生理信号的转送[24]。
4复合技术在纺织材料中的应用
复合技术涉及两种及两种以上具有不同理化性能的材料在纤维、纱线、织物等各个层次上的结合,可以更好地满足医用卫生领域中复杂的终端需求。例如,含银抗菌材料与纺织材料复合后制备的含银医用敷料目前被广泛应用于功能性医用敷料的制备[25],而微尺寸的生物传感器在与纺织材料结合后可以跟踪患者体温和心脏活动,用于病人的动态跟踪。以下是医用纺织材料中使用的几种复合技术。
4.1高分子共混
高分子材料的共混包括相容高分子共混、互不相容高分子共混和高分子的混溶等三种状态,其中纳米技术的进展使共混高分子材料的制备获得新的发展动力,传统高分子材料与纳米化粉体在溶液、熔体中共混后可以制备具有全新结构和性能的纤维材料[26]。在医用敷料领域,通过水溶性的羧甲基纤维素钠(CMC)与海藻酸钠的共混及纺丝成形,可以制备具有很高吸湿性能的海藻酸与CMC共混纤维[27]。表1显示了海藻酸盐/CMC共混敷料与纯海藻酸盐敷料的性能比较。由于CMC破坏了海藻酸盐纤维的结构规整性,含CMC的共混纤维在与生理盐水接触后很容易形成高度膨胀的凝胶结构,由其制备的医用敷料的吸湿性比纯海藻酸盐的高30%。
表1海藻酸盐/CMC共混敷料与纯海藻酸盐敷料的性能比较
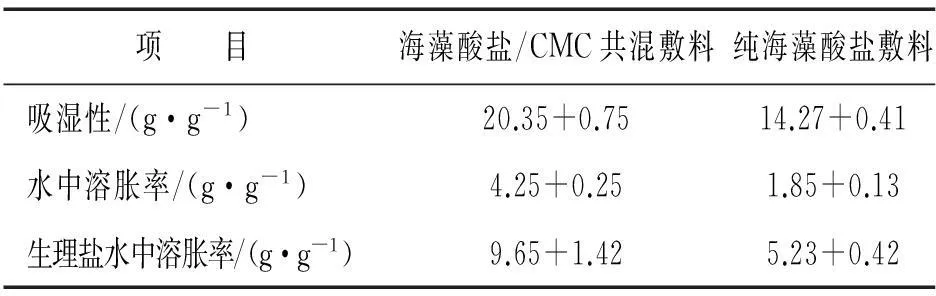
项 目海藻酸盐/CMC共混敷料纯海藻酸盐敷料吸湿性/(g·g-1)20.35+0.7514.27+0.41水中溶胀率/(g·g-1)4.25+0.251.85+0.13生理盐水中溶胀率/(g·g-1)9.65+1.425.23+0.42
4.2微胶囊
微胶囊可以负载液体或固体状态的活性物质,并通过压力、摩擦、扩散、囊壁的解散和生物降解等方式释放出香料、皮肤软化剂、杀虫剂、抗菌药物等物质。在负载驱蚊剂、抗螨剂、驱虫整理剂等材料后,直径1~10 μm的微胶囊可以通过多种方式结合到直径为5~30 μm的纺织纤维上,其中基于甲醛与尿素或三聚氰胺的微胶囊在医用纺织材料中广泛应用,该系统可以把液态的活性成分与预聚体混合后制备微胶囊,然后用黏结剂结合到纺织材料上[28]。
4.3药物缓释
纤维材料为药物的控制释放提供了一个理想的载体,特别是静电纺丝技术的发展为载体材料的选择提供了更大的范围。抗生素、抗癌药物、蛋白质、DNA等活性物质可以与各种高分子结合后加工成纤维材料,应用于透皮给药、医用敷料以及其他许多应用领域[29-30]。浸轧、竭染等传统纺织工艺也可以把活性物质结合到纺织材料上。在浸轧工艺中,包埋有活性物质的微胶囊与软化剂、润湿剂等助剂一起分散在整理浴中,与交联剂一起进入烘箱,在105~140 ℃下处理1~2 min,使活性成分结合在纺织材料上。活性成分也可以通过喷涂、印刷、涂层等方法负载在纺织材料上。
4.4组织工程
通过细胞生物学、材料科学、医疗技术的结合可以在人造支架上培养人造组织后应用于医疗领域,其中天然或合成高分子制备的具有三维结构的纺织材料为人体组织的体外培养提供了合适的环境[31]。在此领域中,刺绣技术可以精确控制纺织支架的三维立体结构,具有很高的应用价值。由海藻酸盐纤维制备的机织、针织、编织及非织造材料具有很好的成胶性能,可以为细胞的繁殖提供良好的环境,有利于细胞与支架的融合。目前组织工程技术已被用来培养皮肤、血管、骨骼、神经和软骨组织,由静电纺丝制备的纳米纤维具有超细的直径,可以更好地模拟人体的细胞外基质,在组织工程中有很高的应用价值。图4显示了一种组织工程支架的结构。
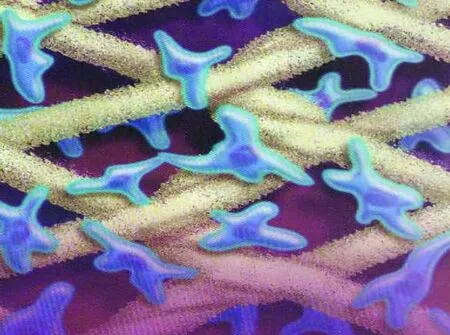
图4 组织工程支架的结构示意
4.5人造器官
利用现代生物技术制备的人工肾可以起到代谢、内分泌、免疫等生理功能,以及透析、超滤等基本的理化作用[32-34]。人造肾与血液透析器基本相似,但在毛细管外空间负载的活细胞具有人体特有的生理功能,细胞可以包埋在凝胶中或固定在高分子微载体上,以避免堵塞中空纤维膜的交换功能。把人类和猪肾细胞收获后种植在中空纤维生物反应器上可以起到肾的功能,而负载活的肝细胞的中空纤维可以制备人工肝,血液中的毒性成分在中空纤维中通过时被包埋的肝细胞代谢[35-37]。中空纤维生物反应器也被应用于其他的体外装置,如人工肺和体外血液氧合器,在体外循环时为血液补充氧气。人工胰腺可以被用来辅助糖尿病的治疗[38-39],把胰岛、郎格罕氏岛结合在中空纤维膜中后,通过控制膜的结构使其渗透葡萄糖和胰岛素,但不渗透免疫球蛋白和淋巴细胞,由此起到胰腺的功能。
5结语
作为一种功能多样、技术复杂、应用专一的特殊材料,医用纺织材料的制备具有很强的个性化特征,涉及对终端需求的科学研判及对各种材料加工技术的合理应用。高分子、纤维、纺织及材料领域的技术进展为医用纺织材料的研究和开发提供了新的动力,将有效推动纺织新材料及先进加工技术在关节置换、人工韧带和肌腱、伤口敷料、人造血管、心脏瓣膜、组织工程支架、防护服装、患者动态监控等医疗卫生领域中的应用。
参考文献
[1]CZAJKA R. Development of medical textile market[J]. Fibres & Textiles in Eastern Europe, 2005,13(1):13-15.
[2]ANAND S. Medical Textiles[M]. Cambridge: Woodhead Publishing Ltd.,2001:30-35.
[3]BARTELS V T. Handbook of medical textiles[M]. Cambridge: Woodhead Publishing Ltd.,2011:3-37.
[4]RAJENDRAN S, ANAND S. Contribution of textiles to medical and healthcare products and developing innovative medical devices[J]. Indian Journal of Fibre and Textile Research,2006,31:215-229.
[5]RIGBY A J, ANAND S C, HORROCKS A R. Textile materials for medical and healthcare applications[J]. Journal of the Textile Institute,1997,88(Part 3):83-93.
[6]SHONAIKE G O, ADVANI S G. Advanced polymeric biomaterials[M]. Boca Raton: CRC Press,2003:40-48.
[7]CHILARSKI A, KRUCINSKA I, KIEKENS P, et al. Novel dressing materials accelerating wound healing made from dibutyrylchitin[J]. Fibres & Textiles in Eastern Europe,2007,15:77-81.
[8]BLACKBURN R S. Biodegradable and sustainable fibres[M]. Cambridge: Woodhead Publishing Ltd.,2005:52-65.
[9]LARRONDO L, MANLEY R S. Electrostatic fiber spinning from polymer melts 1. Experimental observations on fiber formation and properties[J]. Journal of Polymer Science, Part B: Polymer Physics,1981,19:909-915.
[10]BUCHENSKA J. Polyamide fibers with antibacterial properties[J]. Journal of Applied Polymer Science,1996,61:567-576.
[11]GRAHAM K, SCHREUDER-GIBSON H, GOGINS M. Incorporation of electrospun nanofibers into functional structures[J]. INJ,2004,13:21-27.
[12]MIN B M, LEE G, KIM S H, et al. Electrospinning of silk fibroin nanofibers and its effect on the adhesion and spreading of normal human keratinocytes and fibroblasts in vitro[J]. Biomaterials,2004,25:1289-1297.
[13]ZHANG Q, LU X, ZHAO L. Preparation of polyvinylidene fluoride (PVDF) hollow fiber hemodialysis membranes[J]. Membranes,2014,4(1):81-95.
[14]MENNE D, PITSCH F, WONG J E, et al. Temperature-modulated water filtration using microgel-functionalized hollow-fiber membranes[J]. Angew Chem Int Ed Engl,2014,53(22):5706-5710.
[15]INABA Y, TERAOKA F, NAKAGAWA M, et al. Development of a new direct core build-up method using a hollow fiber-reinforced post[J]. Dent Mater J,2013,32(5):718-724.
[16]QIN Y, HU H, LUO A, et al. The effect of carboxymethylation on the absorption and chelating properties of chitosan fibers[J]. Journal of Applied Polymer Science,2006,99(6):3110-3115.
[17]ANAND S C. Medical Textiles 96[M]. Cambridge: Woodhead Publishing Ltd.,1997:15-20.
[18]EHRET P, LAHTEENKORVA K. Nonwoven/film biodegradable composite structure:US, 5783504[P].1998-4-18.
[19]MEAUME S, VALLET D, MORERE M N, et al. Evaluation of a silver-releasing hydroalginate dressing in chronic wounds with signs of local infection[J]. J Wound Care,2005,4(9):411-419.
[20]LEE H J, YEO S Y, JEONG S H. Antibacterial effect of nanosized silver colloidal solution on textile fabrics[J]. Journal of Material Science,2003,38:2199-2204.
[21]GULRAJANI M L. Nano finishes[J]. Indian Journal of Fibre and Textile Research,2000,31:187-201.
[22]TAMURA H, TSURUTA Y, TOKURA S. Preparation of chitosan-coated alginate filament[J]. Materials Science and Engineering,2002,20(1-2):143-147.
[23]CIECHANSKA D. Multifunctional bacterial cellulose chitosan composite materials for medical applications[J]. Fibres & Textiles in Eastern Europe,2004,12:69-72.
[24]PETRULYTE S. Advanced textile materials and biopolymers in wound management[J]. Danish Medical Bulletin,2008,55(1):72-77.
[25]QIN Y. Silver containing alginate fibres and dressings[J]. International Wound Journal,2005,2(2):172-176.
[26]WANG J, SMITH J, BABIDGE W, et al. Silver dressings versus other dressings for chronic wounds in a community care setting[J]. Journal of Wound Care,2007,16:352-356.
[27]QIN Y, GILDING D K. Fibres of co-spun alginates:US,6080420[P].2000-6-27.
[28]GRECHIN A G, BUSCHMANN H J, SCHOLLMEYER E. Quantification of cyclodextrins fixed onto cellulose fibers[J]. Textile Research Journal,2007,77:161-164.
[29]MATHIOWITZ E. Encyclopaedia of controlled drug delivery[M]. New York: Wiley Interscience,1999:45-60.
[30]CHASIN M, LANGER R. Biodegradable polymers as drug delivery systems[M]. New York: Marcel Dekker,1990:1-41.
[31]PATRICK C W, MIKOS A G, McINTIRE L V. Frontiers in tissue engineering[M]. Oxford: Pergamon Press,1998:52-75.
[32]ZHU W, LI J, LIU J. The cell engineering construction and function evaluation of multi-layer biochip dialyzer[J]. Biomed Microdevices,2013,15(5):781-791.
[33]OO Z Y, DENG R, HU M, et al. The performance of primary human renal cells in hollow fiber bioreactors for bioartificial kidneys[J]. Biomaterials,2011,32(34):8806-8815.
[34]FISSELL W H, FLEISCHMAN A J, HUMES H D, et al. Development of continuous implantable renal replacement: past and future[J]. Transl Res,2007,150(6):327-336.
[35]HILAL-ALNAQBI A, MOURAD A H, YOUSEF B F, et al. Experimental evaluation and theoretical modeling of oxygen transfer rate for the newly developed hollow fiber bioreactor with three compartments[J]. Biomed Mater Eng,2013,23(5):387-403.
[36]PALAKKAN A A, RAJ D K, ROJAN J, et al. Evaluation of polypropylene hollow-fiber prototype bioreactor for bioartificial liver[J]. Tissue Eng:Part A,2013,19(9-10):1056-1066.
[37]AMIMOTO N, MIZUMOTO H, NAKAZAWA K, et al. Hepatic differentiation of mouse embryonic stem cells and induced pluripotent stem cells during organoid formation in hollow fibers[J]. Tissue Eng:Part A,2011,17(15-16):2071-2078.
[38]GUNDERSEN S I, CHEN G, POWELL H M, et al. Hemoglobin regulates the metabolic and synthetic function of rat insulinoma cells cultured in a hollow fiber bioreactor[J]. Biotechnol Bioeng,2010,107(3):582-592.
[39]SILVA A I, MATEUS M. Development of a polysulfone hollow fiber vascular bio-artificial pancreas device for in vitro studies[J]. J Biotechnol,2009,139(3):236-249.
The application of advanced technologies in
medical textile materials
QinYimin1,LiKechang2,DengYunlong2,ShenShengbiao2,HaoYuna2ShaoJianhua2
(1. College of Material and Textile Engineering, Jiaxing College;
2. Qingdao Brightmoon Seaweed Group Co., Ltd.)
Abstract:The research progress in the functional modifications of polymer, fiber and textile materials was described, and the processing technologies for the manufacture of medical textile materials and the properties and applications of the resultant products were introduced. By applying chemical, physical and biological modifications to polymer, fiber, fabric, and composite materials, the functional performances of textile materials can be effectively enhanced, and can be used to develop new medical textile materials with high absorbency, antimicrobial, anti-ultraviolet, drug releasing, protection and other functions, which are highly valuable in the fields of biomedical materials and functional medical textiles.
Kaywords: medical textile material, biomedical material, functionalization, modification technology, research progress

