消化道溃疡患者奥美拉唑代谢相关基因CYP2C19的多态性分布
消化道溃疡患者奥美拉唑代谢相关基因CYP2C19的多态性分布*
**通信作者 E-mail:junyuan99430@163.com
网络出版时间:2015-09-11网络出版地址:http://www.cnki.net/kcms/detail/52.5012.R.20150911.2240.004.html
任凌雁, 袁军**, 陈琨, 骆姝琳, 李伟, 令狐克燕
(贵州省人民医院 中心实验室, 贵州 贵阳550002)
[摘要]目的: 分析奥美拉唑代谢相关基因CYP2C19基因在消化道溃疡患者中的多态性分布。方法: 选取消化道溃疡患者23例为研究对象,采用基因芯片的方法检测CYP2C19的基因多态性,并分析CYP2C19基因型总体分布和性别分布。结果: CYP2C19基因型(636GG,681GG)、(636GG,681GA)、(636GA,681GG)、(636GG,681AA)、(636GA,681GA)及(636AA,681GG)携带率分别为39.1%、30.4%、13%、8.7%、8.7%、0;CYP2C19基因快代谢型占39.1%,中代谢型占43.5%,慢代谢型占17.4%;不同性别在CYP2CI9基因分型上差异无统计学意义。结论: 检测CYP2C19基因型可为奥美拉唑个体化用药提供指导。
[关键词]消化性溃疡; 奥美拉唑; CYP2C19基因; 多态性,单核苷酸
[基金项目]*黔科平台[2010]4005;[2010]筑科技合同字3-1号;黔科合sy[2010]3132号
[中图分类号]R34-33; R573.1
The Polymorphism Distribution of Omeprazole Mechanism
Related CYP2C19 Gene in Patients of Peptic Ulcer
REN Lingyan, YUAN Jun, CHEN Kun, LUO Shulin, LI Wei, LINGHU Keyan
(CentralLaboratory,People'sHospitalofGuizhouProvince,Guiyang550002,Guizhou,China)
Abstract[] Objective: To investigate the polymorphism distribution of omeprazole mechanism related CYP2C19 gene in patients of peptic ulcer. Method: Twenty-three patients of peptic ulcer were selected, then adopting gene chip to test the polymorphism of CYP2C19. Analyzing the general distribution and gender distribution of CYP2C19 genotype. Results: CYP2C19 genotype(636GG,681GG),(636GG,681GA),(636GA,681GG),(636GG,681AA) ,(636GA,681GA) and (636AA,681GG) carrier rates were respectively 39.1%, 30.4%, 13%, 8.7%, 8.7%, 0;the extensive metabolizer, intermediate metabolizer, poor metabolizer of CYP2C19 gene were 39.1%, 43.5% and 17.4%; the gender differences in CYP2C19 had no statistical significance. Conclusion: Testing of CYP2C19 might be useful in suggesting medication of omeprazole.
[Key words] peptic ulcer; omeprazole;CYP2C19 gene; polymorphism,single nucleotide
奥美拉唑是目前针对消化道溃疡应用最早且最广泛的有效药物,但是不同患者使用奥美拉唑的效果大相径庭,遗传背景差异可能是造成这一结果的主要因素[1-2]。CYP2C19作为细胞色素氧化酶P450超家族的主要药物代谢酶,影响奥美拉唑、氯吡格雷等众多药物在人体内的代谢速度。由于奥美拉唑在体内经肝细胞微粒体中CYP2C19代谢,生成羟基奥美拉唑而失去活性[3],而CYP2C19 基因又具有明显的种族和地域的多态性分布[4]。因此本研究选择消化道溃疡患者为对象,检测其CYP2C19的基因型,从而分析CYP2C19与奥美拉唑治疗效果的相关性,旨在更好的为临床用药提供指导。
1对象与方法
1.1对象
采集消化科胃十二指肠溃疡患者23例 ,平均年龄(61.8±3.73)岁,性别不限。经医院伦理委员会批准,并经研究对象签署知情同意书。
1.2标本采集
采集肘静脉血标本2 mL,加入含EDTA抗凝剂的真空抽血管中,颠倒数次混匀,放置-20 ℃冰箱保存备用,使用百傲生物技术(上海)有限公司的全血DNA快速提取试剂盒提取人全血DNA。
1.3PCR扩增
25 μL PCR反应体系组成为:CYP2C19扩增反应液1和2各19 μL, 1 μL反应液A,样本DNA 5 μL; PCR循环条件:50 ℃ 5 min;94 ℃ 5 min;94 ℃ 25 s,48 ℃ 40 s,72 ℃ 30 s,35个循环,72 ℃ 5 min。
1.4杂交显色
在百傲全自动杂交仪中设置程序后进行自动杂交。反应结束后取出芯片,将其放入生物芯片识读仪中,用百傲基因芯片图像分析软件进行图像扫描,软件自动分析判定所检测基因的基因型(图1)。
1.5观察指标
观察CYP2C19基因型的总体分布和性别分布,根据文献[5]将CYP2C19基因分为快代谢型即基因型(636GG,681GG),中代谢型基因型(636GG,681GA) 、(636GA,681GG),慢代谢型基因型(636GG,681AA) 、(636GA,681GA)及(636AA,681GG) ,分析各种代谢基因型分布及性别分布。

图1 芯片探针阵列图 Fig.1 Chip probe array
1.6统计学方法
将数据采用SPSS 17.0软件进行统计学分析,组间比较采用χ2检验,P<0. 05为差异有统计学意义。
2结果
CYP2C19基因型(636GG,681GG)、(636GG,681GA) 、(636GA,681GG)、(636GG,681AA) 、(636GA,681GA)及(636AA,681GG)芯片图见图2。男性和女性CYP2C19基因型频率分布大致相同,差异无统计学意义(χ2=0.538,P>0. 05)。CYP2C19基因代谢类型的性别分布差异也无统计学意义(χ2=0.518,P>0. 05)。见表1。

图2 CYP2C19基因型芯片分型结果 Fig.2 The results of the chip probe array of CYP2C19 genotype
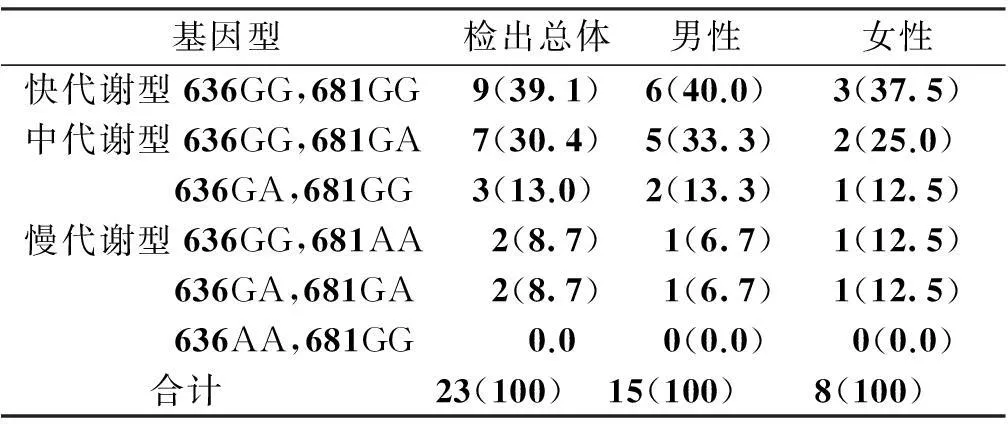
基因型检出总体男性女性快代谢型636GG,681GG9(39.1)6(40.0)3(37.5)中代谢型636GG,681GA7(30.4)5(33.3)2(25.0) 636GA,681GG3(13.0)2(13.3)1(12.5)慢代谢型636GG,681AA2(8.7)1(6.7)1(12.5) 636GA,681GA2(8.7)1(6.7)1(12.5) 636AA,681GG0.00(0.0)0(0.0) 合计23(100)15(100)8(100)
3讨论
质子泵抑制剂(proton pump inhibitors,PPIs)是目前治疗消化道溃疡最有效的一类药物,它通过高效快速抑制胃酸分泌和清除幽门螺旋杆菌达到快速治愈溃疡的目的。质子泵抑制剂包括奥美拉唑、埃索美拉唑、泮托拉唑、兰索拉唑等,其中又以奥美拉唑最为常用。有活性的奥美拉唑在人体内可经CYP2C19酶代谢生成无活性的羟基奥美拉唑,由于CYP2C19酶的表达具有遗传多态性,因此不同基因型的人群对PPI的代谢速度可能有所不同。若患者携带CYP2C19突变基因,对奥美拉唑代谢能力弱,药物容易在体内积累,治愈率较好,但产生不良反应风险可能增高;若患者携带野生型基因,对奥美拉唑代谢能力强,易造成疗效不佳。因此CYP2C19的基因型检测对奥美拉唑个体化的指导用药是十分重要的。
CYP2C19 基因多态性分布具有明显的种族和地域差异[6]。本研究对23例消化道溃疡患者进行了CYP2C19基因检测,从基因型的分布中可以看出男性和女性患者在(636GG,681GG)基因型的检出率最多,分别为40%和37.5%;在(636GG,681AA)、(636GA,681GA)基因型中都分别有1例检出,没有发现(636AA,681GG)基因型。此外不同性别CYP2C19基因多态性分布差异无统计学意义,推测在分析CYP2C19基因多态性对药物代谢的影响时,可能可以不必过多地考虑性别因素。
对于不同代谢型的患者其临床用药也有所差异,对于快代谢型患者,代谢能力强,奥美拉唑在体内暴露量偏低,适当增加剂量或增加每日服药次数,可显著提高患者体内药物暴露量及疾病治愈率。对于中间代谢型患者代谢能力中等,奥美拉唑在体内暴露量处于快慢代谢之间,可按常规剂量用药,并监测血药浓度,必要时可按照上述快代谢患者方案适当增加剂量。对于慢代谢型患者,代谢能力差,奥美拉唑在体内暴露量高,按常规剂量用药即可,并应加强临床关注以防患者体内药物积累量高导致不良反应。本研究的23例病例中,中代谢类型检出率最高达43.5%,在男、女性中分别占46.7%、37.5%,这与中国人群CYP2C19代谢类型分布相似[7]。本次研究的慢代谢型检出率为17.4%,高于白种人慢代谢检出率(3%~5%)[8],与东方人检出率为13%~23%一致[9]。本次研究对这23例消化道溃疡患者进行回访,发现临床医生对快代谢患者增加了用药剂量,疗效较好。
CYP2C19基因检测的开展将有效提高临床用药有效性,可以最大限度的提高药物的安全性,真正意义上做到合理用药、个性化用药。
4参考文献
[1] 张鉴,彭向,李军,等.质子泵抑制剂的代谢与细胞色素P450[J].山东医药, 2005(2):20.
[2] 牛春燕,罗金燕.CYP2C19 基因多态性与质子泵抑制剂对消化性溃疡患者抑酸效应的关系[J].世界华人消化杂志, 2007(19):2551-2155.
[3] 江尔胜,汪涓,孙启泉,等. 奥美拉唑体内药物分析[J].山东医药工业, 2003(4):12.
[4] 谢婧,胡欣,杨丽萍. CYP2C19* 17多态性对氯吡格雷临床疗效影响的系统评价[J].中国循证医学杂志, 2014(3):271-276.
[5] 李鹏飞,杨海波, 赵荫涛, 等.冠心病介入患者氯吡格雷药物代谢相关基因CYP2C19的多态性分布[J].中国实用医刊, 2014(10):64-65.
[6] Hulot JS, Hajjar R, Montalescot G. Clopidogrel and CYP2C19 testing: ready for clinical prime time[J], Clin Chem, 2012(1):154-157.
[7]梁艳, 刘振华, 白清清, 等.CYP2C1基因型与奥美拉唑治疗消化道溃疡疗效的相关性[J].武警医学, 2014(2):142-147.
[8] 陈珲,蔡泓敏,冯端浩,等.CYP2C9和CYP2C19基因多态性对药物代谢的影响及个体化用药研究进展[J].中国药物应用与检测, 2014(4):240-243.
[9] 严非,夏春华,熊玉卿.CYP2C19 基因多态性对药物代谢的影响及其个体化用药[J]. 中国临床药理学与治疗学, 2010(8):949-953.
(2015-05-26收稿,2015-07-10修回)
中文编辑: 周凌; 英文编辑: 赵毅

