离子色谱法测定米线中甲醛次硫酸氢钠的含量
廖予琦,侯英,杨燕,杨蕾,3,许志成,李璐芸
[1.云南瑞升烟草技术(集团)有限公司,昆明 650106;2.云南同创检测技术股份有限公司,昆明 650106;3.昆明理工大学环境科学与工程学院,昆明 650500]
甲醛次硫酸氢钠俗称吊白块,分子式为NaHSO2·CH2O·2H2O,分子量为154.13。甲醛次硫酸氢钠属细胞原浆毒,对人体细胞功能损害较大,已被国际上列为能引起致癌作用的物质[1],因具有潜在的毒性而禁止在食品中使用。甲醛次硫酸氢钠在酸性或受热条件下可分解产生甲醛与亚硫酸氢钠,其主要危害来自于分解放出的甲醛。同时甲醛次硫酸氢钠分解产物之一为亚硫酸氢钠,亚硫酸钠具有漂白作用。食品中掺入甲醛次硫酸氢钠可达到防腐增白,改善食品口感的目的[2],但其会破坏食品的营养成分,可使蛋白质凝固[3]。
米线是云南人的传统饮食,据调查,市场上某些食品中有出现加入甲醛次硫酸氢钠的情况[4]。长期食用掺有甲醛次硫酸氢钠的食品,会损坏人体的皮肤粘膜、肾脏、肝脏及中枢神经系统,严重的会导致癌症和畸形病变等,直接危害消费者的健康。为保证食品安全,测定食品中甲醛次硫酸氢钠的含量对维护人体的健康有着重要作用。
目前检测甲醛次硫酸氢钠的方法有分光光度法,包括盐酸苯肼法[5]、乙酰丙酮法[6]、变色酸法[7];也有用AHMT法及直接蒸馏滴定–AHMT法[8]进行测定的报道。这些测定方法是通过检测甲醛次硫酸氢钠中的甲醛或二氧化硫的含量来间接计算甲醛次硫酸氢钠的含量。此外,近年发展起来的检测甲醛次硫酸氢钠的方法还有化学发光分析法[9]和高效液相色谱法[10]。
以上方法中,分光光度法和AHMT法间接测定甲醛次硫酸氢钠,有些样品本身就含有这两种物质,容易产生假阳性;直接蒸馏滴定–AHMT法费时费力;化学发光法容易产生污染;高效液相色谱法需要衍生化。近年来,用离子色谱法检测甲醛次硫酸氢钠已经成为趋势。如赵士权等[11]以稀碱提取水发食品中的甲醛次硫酸氢钠,过C18小柱除杂后,以KOH水溶液为流动相,进行离子色谱法测定;赵新颖等[12]将样品经固相萃取柱处理后用离子色谱法测定食品中的甲醛次硫酸氢钠;张建平等[13]建立了测定烟用添加剂中甲醛次硫酸氢钠的离子色谱方法;黄凤妹[14]采用IonPac ASl8作为分离柱,在线发生KOH淋洗液,离子色谱法测定了食品中的甲醛次硫酸氢钠含量。
笔者采用离子色谱法测定米线中的甲醛次硫酸氢钠,利用浓度为0.03 mol/L的NaOH溶液直接振荡萃取,离心后过滤膜进离子色谱仪系统分析,建立了米线中甲醛次硫酸氢钠含量的测定方法,该法前处理简单,结果准确,灵敏度高。
1 实验部分
1.1 主要仪器与试剂
离子色谱分析仪:ICS–2000型,配有电导检测器(CD),柱温箱,KOH自动淋洗液发生器,AS40自动进样器,美国戴安公司;
超纯水仪:Milli-QA型,美国Millipore公司;
振荡器:SHA–B型,中国金南仪器制造有限公司;
离心机:3K15型,15 000 r/min,德国Sigma公司;
甲醛次硫酸氢钠标准品:98.0%,美国Sigma公司;
甲醛次硫酸氢钠的储备液:1 000 μg/mL,使用时逐级稀释;
米线样品:昆明农贸市场;
实验用水:电阻率为18.2 MΩ·cm的超纯水。
1.2 样品处理
准确称取样品5.000 g,置于100 mL PET样品瓶中,加入50 mL 0.03 mol/L的NaOH溶液,振荡萃取30 min,放置30 min后以10 000 r/min的转速离心8 min,萃取液过0.45 μm水系滤膜,进离子色谱仪进行分析检测。
1.3 色谱条件
色谱柱:IonPac AS1l-HC型阴离子分离柱(250 mm×4 mm,),IonPac AG11–HC 阴离子保护柱(50 mm×4 mm),美国戴安公司;ASRS 300型抑制器;淋洗液:KOH溶液,流量为1.2 mL/min;抑制模式:自动抑制电流为179 mA;柱温:30℃;进样体积:20 μL;检测器:抑制型电导检测器;检测池温度:40℃;淋洗梯度见如表1。

表1 淋洗液的淋洗梯度
1.4 色谱图
由于所采集的米线样品中未检出有甲醛次硫酸氢钠,因此在样品中加入甲醛次硫酸氢钠标准品,米线样品加标的离子色谱图如图1所示。由图1可知,样品中的其它杂质对甲醛次硫酸氢钠无影响,甲醛次硫酸氢钠的分离度较好。采用的淋洗方式为梯度淋洗,在13 min后基线有向上飘的趋势,但不影响甲醛次硫酸氢钠的定性、定量,甲醛次硫酸氢钠出峰的位置(5 min左右)基线较平稳。
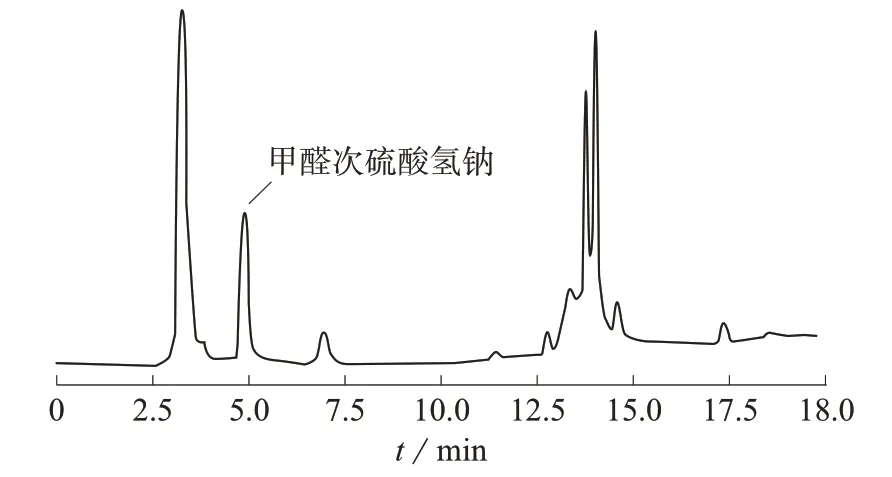
图1 米线样品加标的离子色谱图
2 结果与讨论
2.1 萃取条件的选择
2.1.1 萃取溶液
为选择适宜的萃取溶液提取米线中的甲醛次硫酸氢钠,分别用0.01,0.03,0.05 mol/L的NaOH溶液及超纯水对米线进行萃取试验(样品中甲醛次硫酸氢钠含量低于检出限,故在样品处理的过程中加入微量甲醛次硫酸氢钠标品)。当萃取溶液为超纯水、0.01,0.03,0.05 mol/L NaOH溶液时,不同浓度萃取液的萃取效果见图2。由图2可知,0.03 mol/L NaOH溶液的萃取效果更好,故选择0.03 mol/L的NaOH溶液作为萃取溶液。

图2 不同萃取溶液的萃取效果
2.1.2 萃取时间
将米线切细后,分别称取几份5.0 g左右的样品,同时加入微量甲醛次硫酸氢钠标准品。加入一定量的超纯水作为萃取剂,分别振荡器上振荡10,20,30,30,40 min,不同萃取时间的萃取效果见图3。由图3可知,振荡30 min 能达到最好的萃取效果。因此选择萃取时间为30 min。

图3 不同萃取时间的萃取效果
2.1.3 淋洗液流速、柱温和检测池温度
淋洗液流速、柱温和检测池温度是影响分离效果的3个主要因素。淋洗液流速的增大和柱温的升高可以使出峰提前,分析时间缩短,但系统压力增大,造成灵敏度下降及分离度降低。考虑到分离柱的使用寿命,选择的仪器条件为:淋洗液流量为1.2 mL/min,柱温为30℃,检测池温度为40℃。
2.2 标准工作曲线、线性范围与检出限
配制质量浓度分别为2.00,5.00,10.00,20.00,50.00 μg/mL的系列标准工作溶液,按优化的离子色谱条件进行测定,甲醛次硫酸氢钠的质量浓度在2.0~50 μg/mL范围内线性关系良好,标准曲线方程为Y=0.044 3X+0.001,相关系数r2=0.999 7,检出限(LOD)和定量检测限(LOQ)分别由3倍和10倍信噪比来确定,通过计算得出甲醛次硫酸氢钠的检出限为0.007 μg/mL,定量限为0.024 μg/mL。
2.3 重复性试验
分别在不同3个工作日处理相同的样品,所选样品中甲醛次硫酸氢钠含量低于检出限,向每个样品当中加入相同体积的甲醛次硫酸氢钠标准溶液。前处理条件相同,每天处理6 份样品,在1.3色谱条件下进行分析,测定结果见表2。

表2 米线样品的测量重现性
由表2可知,样品的日内精度不大于2.72%,样品的日间精密度为0.82%,说明采用1.2方法处理样品,重现性良好。
2.4 加标回收试验
根据所测得的米线中甲醛次硫酸氢钠的含量,依次加入高、中、低三个水平浓度的标准溶液之后,采用相同的处理方法对样品进行处理。对加有标准溶液的样品进行分析测定,计算回收率,结果见表3。由表3可知,加标准米线样品的回收率在91.4%~110.7%之间,不同水平的平均回收率在95.1%~101.2%之间,说明此方法测定米线中甲醛次硫酸氢钠的含量准确度较高。

表3 米线样品甲醛次硫酸氢钠的回收率
2.5 稳定性试验
将处理好的样品(在样品处理的过程中加入微量甲醛次硫酸氢钠标准样品),置于冰箱0~5℃条件下分别保存6,12,24,48 h后进行测试,考察样品溶液的稳定性,结果见表4。由表4可知,萃取液在48 h内稳定,因此样品在处理后48 h内进样即可。

表4 样品稳定性试验结果
2.6 样品测定
配制10.00 μg/mL的浓度的甲醛次硫酸氢钠标准溶液作为质控样,每隔10次样品检测一个质控样,以保证方法的可靠性。在样品测定过程中检测质控样6次,结果见表5。由表5可知,质控样检测平均值为10.10 μg/mL,测定结果的相对标准偏差为1.23%。

表5 质控样品的测定结果
3 结语
以0.03 mol/L的NaOH溶液提取米线样品中的甲醛次硫酸氢钠,利用离子色谱抑制电导检测法测定云南传统食品–米线中的甲醛次硫酸氢钠。该方法具有前处理简单、稳定性好、准确度高的特点。该法不需要过固相萃取小柱除杂也能使目标物与其它杂质得到很好的分离。该方法可在食品安全检验工作中(特别是水发食品中甲醛次硫酸氢钠的检测方面)发挥重要作用,具有较高的推广应用价值。
[1]王丽娟,王恒.甲醛次硫酸氢钠的危害及定性检测[J].科技情报开发与经济,2005,15(17): 289–290.
[2]周颖,朱伟,杜琰琰,等.甲醛次硫酸氢钠急性毒性作用研究[J].癌变.畸变.突变,2007,19(5): 416–417.
[3]Vincent J C,Yann G,Robert A B,et al. Meeting Report: Summary of IARC Monographs on Formaldehyde,2-Butoxyethanol and 1-tert-Butoxy-2–Propanol[J]. Environ Health Perspect,2005,113(9): 1 205–1 208.
[4]何继波,沈其萍,王建华.昆明市食品中甲醛次硫酸氢钠及甲醛现状调查报告[J].预防医学情报杂志,2004,20(2): 198–199.
[5]秦启发.盐酸苯肼比色法测定食品中甲醛次硫酸氢钠[J].湖北预防医学杂志,2002(4): 27.
[6]谢宏斌,刘建湘,董文波,等.乙酰丙酮法测定米粉中的甲醛次硫酸氢钠[J].中国公共卫生,2002,18(8): 94–95.
[7]杜利敏,赵建民,高中灿.变色酸法定性测定食品中的甲醛次硫酸钠[J].中国卫生检验杂志,2004,14(6): 735.
[8]何小青,罗美中,蓝勇波,等.直接蒸馏滴定–AHMT法联合测定食品中的甲醛次硫酸氢钠[J].冶金丛刊,2004(3): 16–18.
[9]王冬梅,李保新,章竹君.化学发光法测量食品中残留甲醛次硫酸氢钠的含量[J].西南农业大学学报:自然科学版,2006,28(5): 817–819.
[10]霍权恭,范璐,张浩,等.小麦粉中甲醛(甲醛次硫酸氢钠)的测定方法研究[J].分析试验室,2007,26(2): 33–36.
[11]赵士权,查河霞,林明珠.离子色谱法测定水发食品中甲醛次硫酸氢钠残留量[J].中国卫生检验杂志,2007,17(10): 1 787–1 788,1 804.
[12]赵新颖,焦霞,盖学武,等.离子色谱法测定食品中的甲醛次硫酸氢钠[J].现代科学仪器,2009(5): 77–79.
[13]张建平,黄朝章,邓其馨.离子色谱法测定烟用添加剂中的甲醛合次硫酸氢钠[J].烟草科技,2013(10): 55–58.
[14]黄凤妹.食品中甲醛次硫酸氢钠的离子色谱法检测[J].计量技术,2013(1): 42–44.

