纳米SiO2 /[BMIm]BF4 剪切增稠液的制备及性能研究
陶敏,张广成,秦建彬,谢忠曦
(西北工业大学 应用化学系,陕西 西安 710129)
剪切增稠液体(STF)是指当剪切速率达到一定值时,体系粘度突然增加,表现为剪切增稠现象,当剪切速率降低,粘度又可以恢复的固体粒子分散液。近年来,剪切增稠液体开始应用到人体防护材料[1]、阻尼设备[2]、防震领域[3]等。
目前,剪切增稠液体的分散相粒子一般为SiO2,分散介质大多是水、乙二醇、丙二醇、丁二醇、聚乙二醇等。离子液体具有熔点低、液态温度范围宽、物理和化学稳定性良好、蒸气压几乎为零、电化学窗口宽、不易燃、可设计性等优点,是许多有机物、无机物的优良溶剂。
本文合成了离子液体1-丁基-3-甲基咪唑四氟硼酸盐离子液体[BMIm]BF4,并将其作为分散介质,与纳米SiO2组成分散体系,制备一种新型的离子型剪切增稠液体,研究了纳米SiO2/[BMIm]BF4分散体系的流变性和粘弹性,为进一步发展剪切增稠液提供新思路。
1 实验部分
1.1 试剂与仪器
纳米SiO2(粒径50 nm 左右),阿拉丁试剂;N-甲基咪唑(阿拉丁试剂)、正溴丁烷、四氟硼酸钠(NaBF4)均为分析纯;乙腈、乙酸乙酯、丙酮、二氯甲烷均为化学纯。
RE-52AA 型旋转蒸发仪;DZF-6051 型真空干燥箱;AVANCE400 型核磁共振波谱仪;TENSOR27 型红外光谱仪;MCR302 型流变仪。
1.2 [BMIm]BF4离子液体的合成与表征
用乙腈作溶剂,将摩尔比1∶1.1 的1-甲基咪唑与溴代正丁烷依次加入到三口烧瓶中,在氮气保护下,在70 ℃水浴中磁力搅拌反应24 h,减压蒸馏,用乙酸乙酯洗涤中间粗产物3 次,每次20 mL,60 ℃真空干燥24 h,得到[BMIm]Br。
将等摩尔的[BMIm]Br 与NaBF4加入到单口烧瓶中,以丙酮为溶剂,室温下磁力搅拌反应24 h,过滤,用二氯甲烷洗涤,减压蒸馏,60 ℃真空干燥,得到淡黄色粘稠液体1-丁基-3-甲基咪唑四氟硼酸盐([BMIm]BF4)。

1.3 SiO2/[BMIm]BF4分散体系的制备
称取一定量的纳米SiO2和[BMIm]BF4,加入试剂瓶,滴加适量无水乙醇,100 Hz 超声分散2 h。60 ℃干燥,除去无水乙醇。60 ℃真空干燥24 h,除去其中的气泡和部分可能剩余无水乙醇,得到稳定的分散体系。配制纳米SiO2分散体系。
1.4 SiO2/[BMIm]BF4 分散体系流变性能和粘弹性能测试
用流变仪测试,使用椎板夹具,锥弧度1°,直径为50 mm。
2 结果与讨论
2.1 [BMIm]BF4离子液体的结构表征
离子液体[BMIm]BF4的FTIR 见图1。
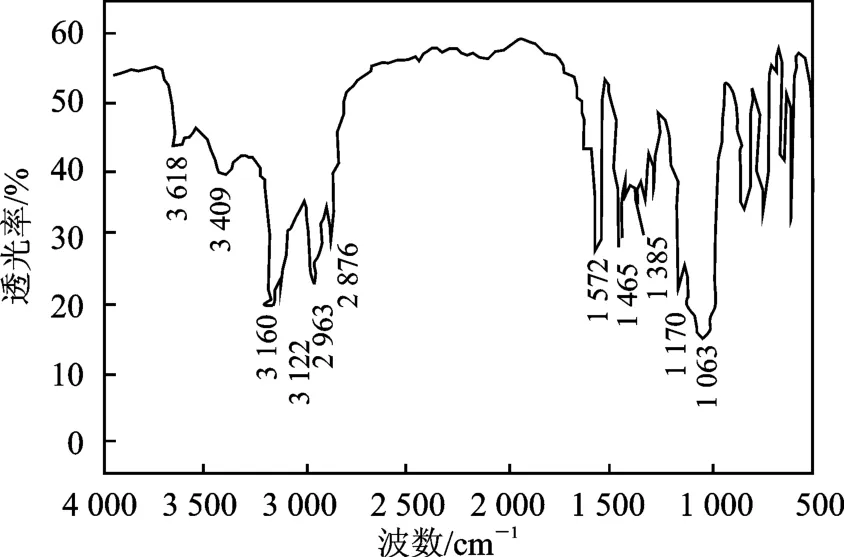
图1 [BMIm]BF4的FTIRFig.1 The FTIR of[BMIm]BF4
由图1 可知,3 617 cm-1和3 409 cm-1是—OH的伸缩振动,3 160 cm-1和3 122 cm-1是咪唑环CC 双键上C—H 的伸缩振动,2 963 cm-1和2 876 cm-1是 侧 链 饱 和 C—H 的 伸 缩 振 动,1 572 cm-1和1 465 cm-1是咪唑环的骨架振动,1 385 cm-1是CH3中C—H 的变形振动,1 170 cm-1为咪唑环C—H 面内变形振动,1 063 cm-1是BF4-的B—F 伸缩振动。FTIR 表明,合成产物为1-丁基-3-甲基咪唑四氟硼酸盐,与参考文献[4]一致。
[BMIm]BF41H NMR 见图2。
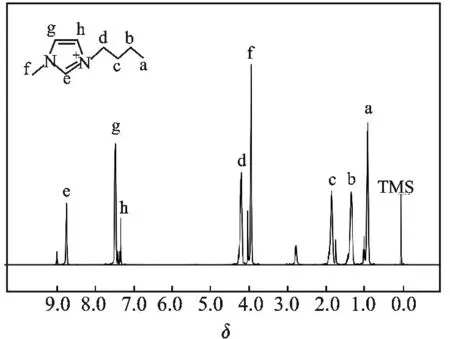
图2 [BMIm]BF4的1H NMRFig.2 The 1H NMR of[BMIm]BF4
质子化学位移δ:0.87(3H,t,a),1.29(2H,m,b),1.81(2H,t,c),3.90(3H,s,f),4.15(2H,t,d),7.42(2H,s,g,h),8.69(1H,s,g),8.38(1H,s,e)。1H NMR分析表明,合成产物为1-丁基-3-甲基咪唑四氟硼酸盐,与参考文献[4]一致。
2.2 SiO2/[BMIm]BF4分散体系的流变性能
2.2.1 浓度对SiO2/[BMIm]BF4分散体系流变行为的影响 由图3 可知,初始剪切,体系粘度略有下降,达到临界剪切速率后,体系出现剪切增稠现象,随着体系浓度增大,粘度增大,增稠现象越来越明显,临界剪切速率也逐渐减小。这可能是分散相浓度的增加,一方面粒子间空间减小,粒子相互碰撞几率增加,粘度变大,体系更易形成粒子簇[5]。另一方面,随着SiO2含量的增多,形成的粒子簇变多、变大。当剪切速率继续增大,体系又变为剪切变稀流体,可能是由于剪切应力过大,使得粒子簇被破坏。
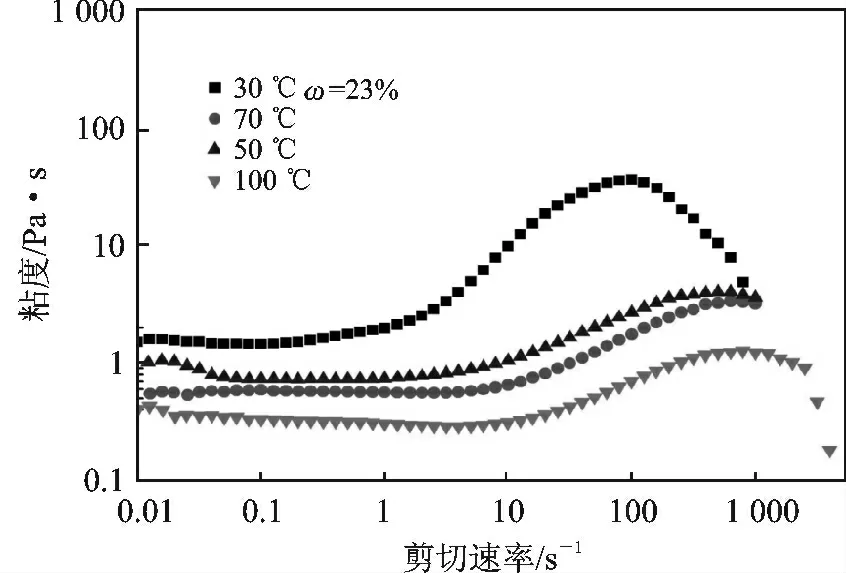
图3 浓度对SiO2/[BMIm]BF4的流变性能的影响Fig.3 The influence of the concentration on the rheological properties of SiO2/[BMIm]BF4
对于浓度较大的(25%,27%)分散体系,剪切增稠后,随剪切速率继续增加,粘度出现趋于平稳后继续增加,粘度的增加不连续。这可能由于分散体系中SiO2有一定的团聚,只有剪切应力增加到一定程度,才能使团聚体解体,粘度增加程度降低,出现一个平稳区,之后粒子簇继续形成并增大,粘度继续增加。
2.2.2 温度对SiO2/[BMIm]BF4分散体系流变性能的影响 由图4 可知,SiO2/[BMIm]BF4分散体系在不同温度下均出现了明显的剪切增稠现象,随温度增加,临界剪切速率增加,临界剪切粘度降低,剪切增稠作用降低。
温度升高,一方面分散介质的粘度下降、氢键作用减弱,另一方面,SiO2粒子吸收能量,粒子间碰撞几率增加,但是SiO2粒子运动更加剧烈,形成的粒子簇变小,体系剪切增稠趋势减弱。临界剪切速率增大,可能是因为随着体系温度升高,布朗运动加剧,粒子间斥力增加,形成粒子簇所需要的剪切速率会更大[6-7]。

图4 温度对SiO2/[BMIm]BF4的流变性能影响Fig.4 The influence of the temperature concentration on rheological properties of SiO2/[BMIm]BF4
2.3 SiO2/[BMIm]BF4分散体系粘弹性能
2.3.1 SiO2/[BMIm]BF4分散体系粘弹性能 见图5。
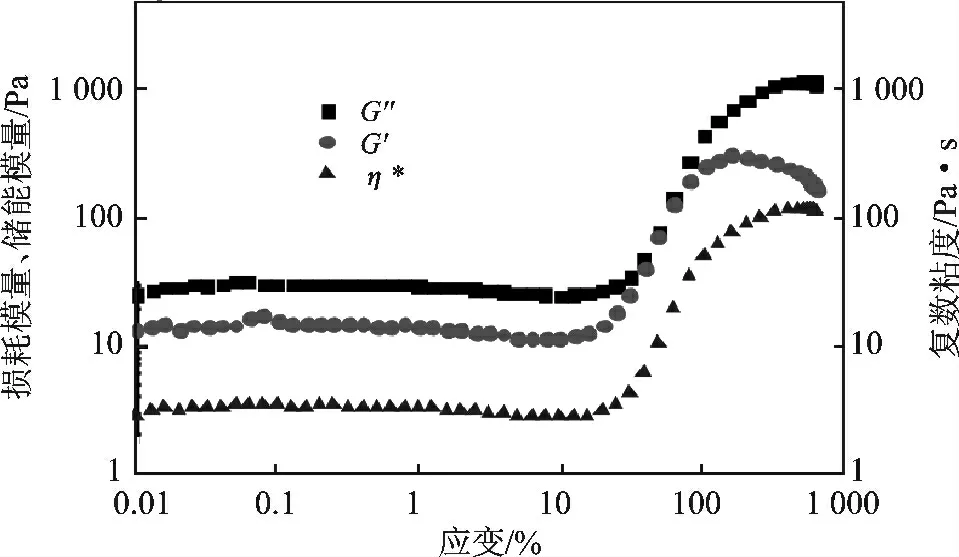
图5 SiO2/[BMIm]BF4动态粘弹性能曲线Fig.5 The viscoelastic properties curve of SiO2/[BMIm]BF4
由图5 可知,随着剪切应变增大,初始储能模量G'、耗能模量G″和复数粘度η* 都稍有下降,当达到一定剪切应变时,储能模量、损耗模量、复数粘度均出现急剧增加,粘弹性能出现突变。整个动态剪切过程中,损耗模量始终大于储能模量,体系表现为粘性。
初始储能模量和损耗模量有所下降,可能由于粒子间有序度增加,粒子间碰撞减少,损耗降低。随剪切应变增加,溶剂层被破坏,粒子间接触,形成粒子簇,使损耗模量和储能模量增加。应变继续增加,粒子簇可能被破坏,粒子间摩擦减少,损耗模量下降,粘度下降。
2.3.2 浓度对SiO2/[BMIm]BF4分散体系粘弹性能的影响 由图6 可知,随分散体系的浓度增加,储能模量(a)和耗能模量(b)都增大,剪切增稠现象更加明显,体系临界剪切应变下降。分散体系的浓度增加,有利于粒子间更容易发生碰撞,更利于形成更大更多粒子簇,因此储能模量和损耗模量都随浓度的增加而增加,增稠后储能模量和损耗模量增幅更明显,说明浓度对体系的储能模量和损耗模量的变化影响很大。临界剪切应变下降,可能是因为随着浓度增加,粒子间距离减小,分散体系更容易形成粒子簇。

图6 浓度对SiO2/[BMIm]BF4粘弹性能的影响Fig.6 The influence of the concentration on the viscoelastic properties of SiO2/[BMIm]BF4
2.3.3 温度对SiO2/[BMIm]BF4分散体系粘弹性能的影响 由图7 可知,随着温度升高,储能模量(a)和耗能模量(b)都下降,临界剪切应变增加。温度增加,分散介质的粘度下降,整个分散体系的储能模量下降,粒子运动所受摩擦阻力下降,损耗模量降低。临界剪切应变增大,可能是因为随着体系温度升高,布朗运动加剧,不利于粒子簇的形成,需要在较大的剪切应变下形成。
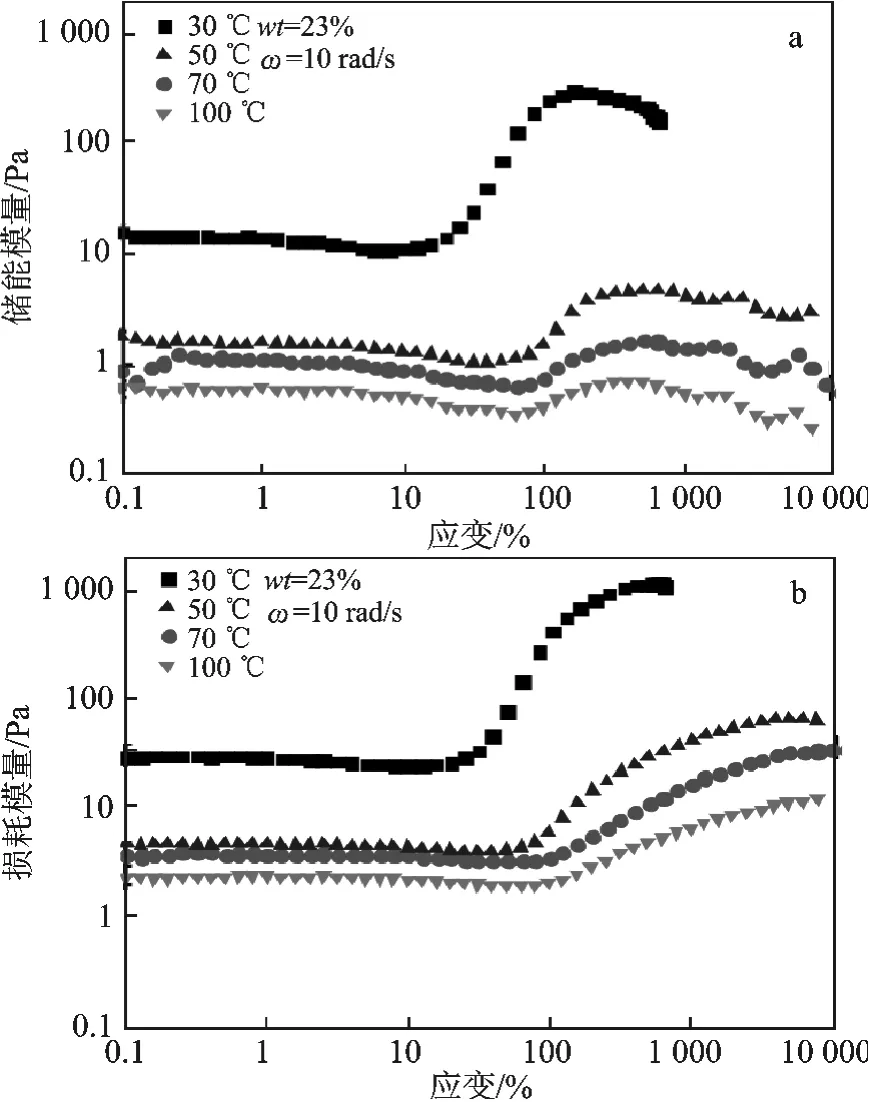
图7 温度对SiO2/[BMIm]BF4粘弹性能的影响Fig.7 The influence of the temperature on the viscoelastic properties of SiO2/[BMIm]BF4
2.3.4 角频率对SiO2/[BMIm]BF4分散体系粘弹性能的影响 见图8。
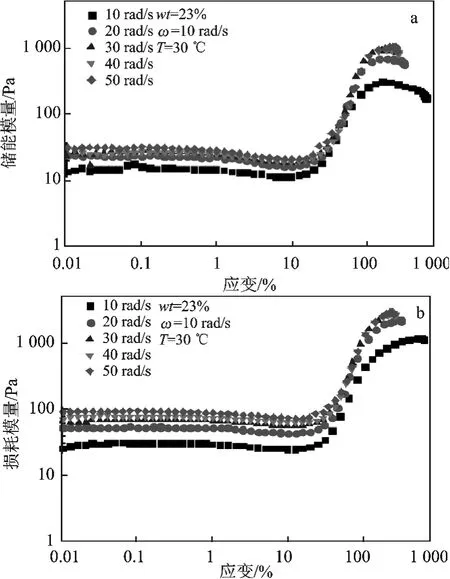
图8 角频率对SiO2/[BMIm]BF4粘弹性能的影响Fig.8 The influence of the angular frequency on the viscoelastic properties of SiO2/[BMIm]BF4
由图8 可知,随着频率增加,储能模量(a )和耗能模量(b)增大,剪切增稠现象更明显,临界剪切应变并未发生明显的变化。可能是因为随剪切频率增加,在初始剪切过程中,粒子间碰撞的机率增加,分散体系的储能模量和损耗模量都增加[8],达到临界剪切应变,溶剂层更容易被破坏,形成更大的粒子簇,增稠现象更明显。
2.3.5 SiO2/[BMIm]BF4分散体系与SiO2/PEG400分散体系流变性能比较 在体系SiO2含量相同条件下,PEG400 分散介质与[BMIm]BF4的对比见图9。

图9 SiO2/[BMIm]BF4 与SiO2/PEG400 流变性能比较Fig.9 The comparison of rheological properties between SiO2/[BMIm]BF4 and SiO2/PEG400
由图9 可知,以离子液体[BMIm]BF4作为分散介质,增稠效果要比PEG400 更加显著。对于PEG400 体系,可能是由于存在大分子链间的缠结,固液间的作用力较强,不利于SiO2摆脱液相束缚参与粒子簇的生成,所以增稠之后,粘度增幅较小[9]。
2.4 SiO2/[BMIm]BF4分散体系的增稠机理
在SiO2/[BMIm]BF4分散体系中,离子液体的BF4-中氟原子可与SiO2表面的—OH 形成氢键,由于静电作用,阳离子分散在BF4-周围,并在SiO2表面形成溶剂层,见图10。
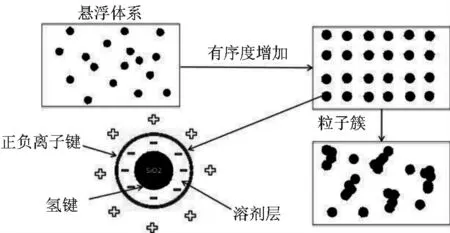
图10 SiO2/[BMIm]BF4分散体系的增稠机理模型Fig.10 The shear thickening mechanism model of SiO2/[BMIm]BF4 dispersions
由图10 可知,由于离子液体的溶剂力和空间位阻,使得SiO2能够更加稳定的分散在[BMIm]BF4中[10-13]。初始剪切时发生剪切变稀,可能是由于受剪切作用,体系中SiO2粒子的有序度增加,导致宏观粘度下降。随着剪切速率的增加,剪切应力可能克服离子液体的溶剂力和空间位阻,使得SiO2粒子间更加容易接触、聚集,形成了亚稳态的粒子簇[13-14],导致分散体系的粘度增加,体系出现剪切增稠现象。
3 结论
(1)SiO2/[BMIm]BF4分散体系具有剪切增稠现象,并随分散体系浓度增加,临界剪切速率下降,临界剪切粘度增加,剪切增稠越显著;随温度增加,临界剪切速率增加,临界剪切粘度下降,剪切增稠趋势减弱。
(2)SiO2/[BMIm]BF4分散体系的损耗模量大于其储能模量,为一耗散体系,并随分散体系的浓度增加、频率增加和温度降低,临界剪切应变下降,损耗模量、储能模量增加。
(3)SiO2/[BMIm]BF4是一种新型的剪切增稠液,其增稠效果要明显优于含量相同的SiO2/PEG400 体系。
[1] Wagner N,Wetzel E D. Advanced body armor utilizing shear thickening fluids:US,7498276[P].2009-03-03.
[2] Zhang X Z,Li W H,Gong X L. The rheology of shear thickening fluid (STF)and the dynamic performance of an STF-filled damper[J]. Smart Materials and Structures,2008,17(3):27-35.
[3] Fischer C,Braun S A,Bourban P E,et al.Dynamic properties of sandwich structures with integrated shear-thickening fluids[J]. Smart Materials & Strutures,2006,15(5):1467-1475.
[4] 刘红霞,徐群.1-丁基-3-甲基咪唑四氟硼酸盐离子液体的合成研究[J].化学世界,2007,47(11):679-681.
[5] Novak J,Britton M M.Magnetic resonance imaging of the rheology of ionic liquid colloidal suspensions[J]. Soft Matter,2013,9(9):2730-2737.
[6] Tian T,Li W,Ding J,et al.Study of the temperature effect of shear thickening fluid[C]//Advanced Intelligent Mechatronics (AIM),2013 IEEE/ASME International Conference on.IEEE,2013:833-837.
[7] Franks G V,Zhou Z,Duin N J,et al.Effect of interparticle forces on shear thickening of oxide suspensions[J].Journal of Rheology (1978-present),2000,44(4):759-779.
[8] Raghavan S R,Khan S A. Shear-thickening response of fumed silica suspensions under steady and oscillatory shear[J].Journal of Colloid and Interface Science,1997,185(1):57-67.
[9] 伍秋美,阮建明,黄伯云,等. 分散介质和温度对SiO2分散体系流变性能的影响[J].中南大学学报:自然科学版,2006,37(5):862-866.
[10]Kazuhide Ueno Ueno K,Imaizumi S,Hata K,et al.Colloidal interaction in ionic liquids:Effects of ionic structures and surface chemistry on rheology of silica colloidal dispersions[J].Langmuir,2008,25(2):825-831.
[11]Raghavan S R,Walls H J,Khan S A. Rheology of silica dispersions in organic liquids:new evidence for solvation forces dictated by hydrogen bonding[J]. Langmuir,2000,16(21):7920-7930.
[12]Ueno K,Watanabe M.From colloidal stability in ionic liquids to advanced soft materials using unique media[J].Langmuir,2011,27(15):9105-9115.
[13]Hoffman R L.Explanations for the cause of shear thickening in concentrated colloidal suspensions[J]. Journal of Rheology (1978-present),1998,42(1):111-123.
[14]Wagner N J,Brady J F.Shear thickening in colloidal dispersions[J].Physics Today,2009,62(10):27-32.

