孔雀石绿-碘化钾体系共振光散射法测定水中痕量汞
杨胜园,徐小娜,于军晖,杨慧仙,唐璐
(南华大学 公共卫生学院,湖南 衡阳 421001)
汞及其化合物属于剧毒物质,进入体内的汞可以在体内蓄积,进而危害身体健康[1],因此汞是环境监测中的一项重要污染指标。汞的传统测定方法通常有分光光度法[2]、冷原子吸收光谱法[3]和冷原子荧光法[4]等,近年来也有不少文献报道基于有机生色团、纳米材料、功能核酸检测汞的新方法[5]。共振光散射法是近年来发展的一种新技术,由于具有灵敏度高、简便、快速等特点,已在药物[6]、核酸[7]、蛋白质[8]以及其他环境污染物检测中得到了广泛应用。
本 文 发 现,I-能 与 Hg2+形 成 配 阴 离 子[HgI4]2-,与碱性阳离子染料孔雀石绿(MG)结合形成的离子缔合物能使反应体系共振光散射(RLS)强度明显增强,且在一定浓度范围内散射强度与Hg2+浓度呈线性关系,据此建立共振光散射法测定水中痕量汞的新方法。
1 实验部分
1.1 试剂与仪器
HgCl2、碘化钾、二烷基硫酸钠(SDS)、孔雀石绿(MG)、硫酸等均为分析纯;实验用水为超纯水。Hitachi F-4500 荧光分光光度计;UV-2550 紫外/可见分光光度计;AB204-S 型电子分析天平。
1.2 HgCl2 标准溶液的配制
准确称取0.271 6 g HgCl2于小烧杯中,加水溶解后,转移至100 mL 容量瓶中,用水稀释至刻度,溶液浓度为1.00 ×10-2mol/L。标准应用液由标准储备液逐级稀释至1.00 ×10-6mol/L。
1.3 实验方法
在10 mL 比色管中,加入一定量的1. 00 ×10-6mol/L HgCl2标准应 用液,2. 0 × 10-3mol/L H2SO41.2 mL,加水至5 mL 左右,加入1.00 mol/L KI 标准溶液1.5 mL,摇匀,置暗处放置5 min。依次加入1. 00 × 10-3mol/L SDS 0. 8 mL,1. 00 ×10-3mol/L MG 1.0 mL,定容,摇匀,10 min 后将溶液置于荧光分光光度计上以λex= λem进行同步扫描,得到RLS 光谱。在最大RLS 峰344 nm 处,测定溶液的RLS 强度I 和试剂空白的RLS 强度I0,ΔIRLS= I-I0。激发和发射狭缝宽度均为10 nm,光电倍增管负电压400 V。
2 结果与讨论
2.1 光谱特征
在实验条件下,分别测定体系的紫外/可见吸收光谱和RLS 光谱,结果见图1。
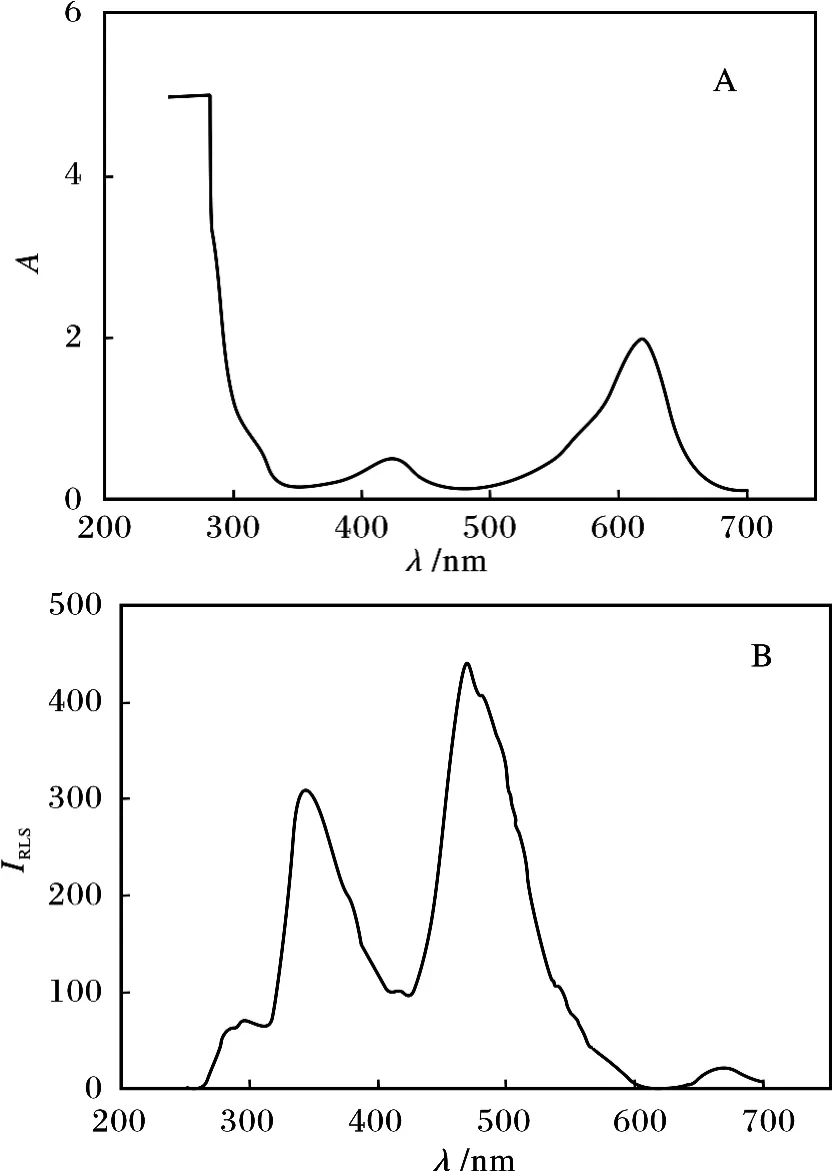
图1 吸收光谱与散射光谱Fig.1 Absorption and resonance light scattering spectra of the systerm
由图1A 可知,吸收峰分别位于426,618 nm 处,在344,468 nm 处吸收最弱。由图1B 可知,其散射峰分别位于344,468 nm 处,而在426,618 nm 处散射强度较弱。可知在250 ~600 nm 波长范围内,体系散射光谱均位于其分子吸收带中。体系吸收强时,散射光弱;体系吸收弱时,散射光强。这是瑞利散射位于其分子吸收带中产生的共振瑞利散射[9]。
Hg2+-KI-MG 体系的RLS 光谱见图2。

图2 Hg(Ⅱ)-KI-MG 体系的共振散射光谱Fig.2 RLS spectra of Hg(Ⅱ)-KI-MG system
由图2 可知,在本实验条件下,MG 自身的散射光很弱,其最大散射峰位于468 nm 波长处。随着Hg2+的加入,[HgI4]2-与MG 形成离子缔合物,在284,344 nm 处产生新的强RLS 峰。原因可能是:随着MG 溶液的加入,在弱酸性条件下,MG 分子形成阳离子MG+,与[HgI4]2-反应,形成离子缔合物,大大增加了分子的体积。而共振光散射的强度与所形成的颗粒的大小有关,且正比于分子体积的平方。因此,体系中有新的分子体积比较大的离子缔合物的形成,导致体系的IRLS明显增强。实验发现,体系在波长344 nm 处产生的共振散射强度更大,灵敏度更高,故实验选择344 nm 作为检测波长。加入不同浓度的Hg2+后,体系的RLS 强度逐渐增强,且在一定浓度范围内,RLS 强度增加值ΔI(λmax=344)与Hg2+浓度呈良好的线性关系。
2.2 酸度的影响
实验研究了H3PO4、H2SO4和HCl 对体系共振光散射强度的影响。发现在H2SO4介质中,ΔIRLS强度最大,并且随着Hg2+浓度的变化产生的光强度的变化最稳定。因此,采用加入1. 2 mL 2. 0 ×10-3mol/L的硫酸调节体系酸度。
2.3 KI 用量的影响
实验表明,体系ΔIRLS值随KI 用量增加而逐渐增大,当1.00 mol/L KI 用量在1.5 mL 时,ΔIRLS达到最大,且基本恒定。KI 量继续增加,ΔIRLS值有所下降,但基本保持恒定,表明该离子缔合物已完全形成。所以,选择1. 00 mol/L KI 溶液加入量为1.5 mL。
2.4 孔雀石绿用量的影响
实验表明,MG 用量少时,[HgI4]2-与MG 反应不完全,体系ΔIRLS偏低;MG 用量1.0 mL 时,反应完全,ΔIRLS达到最大值;继续增加MG 浓度,不再有利于增大ΔIRLS值。因此,选用1.00 ×10-3mol/L MG 1.0 mL。
2.5 表面活性剂的选择及用量的影响
表面活性剂对体系有增敏和增稳作用,研究了SDS、SDBS、SLS、CTMAB 对体系的影响。发现加入以上4 种表面活性剂,均可使体系RLS 强度增强,但空白值也均随之增加,对ΔIRLS值影响不大。但考虑到表面活性剂对本体系的增稳作用,选择加入1.0×10-3mol/L 的SDS 0.8 mL 增强体系稳定性。
2.6 反应时间与反应温度的影响
多次实验表明,试剂完全混合均匀后,体系迅速发生反应。室温下放置10 min,体系的△IRLS已基本上达到最大值,且1 h 内体系共振光散射强度基本保持不变。所以,选择试剂混合后10 min 开始测定。
在10 ~45 ℃的温度范围,考察反应温度对△IRLS的影响。结果表明,适宜的反应温度在20 ~25 ℃,体系相对稳定且△IRLS较大。温度高于30 ℃,随着温度的升高,△IRLS值逐渐减小,可能是升温导致分子热运动增加,分子间作用力和疏水作用力减弱,使得离子缔合物离解,稳定性降低;当温度低于15 ℃时,△IRLS值较小,有可能是因为低温条件下,反应进行比较缓慢。故选择室温(约20 ℃)下进行,试剂混合10 min 后开始测定。
2.7 标准曲线的建立
在最佳实验条件下,按照实验法分别加入不同浓度的Hg2+标准溶液,分别测定空白和体系RLS 强度。结 果 表 明,汞 浓 度 在4. 2 × 10-8~8. 0 ×10-7mol/L 范围内与△I 呈现良好的线性关系,线性回归方程△I =70.82C(×10-7mol/L)+11.87,相关系数r=0.999 1。按实验方法测定11 次空白值,依据其标准偏差的3 倍除以斜率(3Sd/K)计算出检出限为1.26 ×10-8mol/L。分别对Hg2+含量为0.75 ×10-7mol/L(低浓度)、1.5 ×10-7mol/L(中浓度)和4.5 ×10-7mol/L(高浓度)的溶液进行7 次平行测定,相对标准偏差分别为2.47%,1.08% 和2.49%。
2.8 共存离子的影响
在最优实验条件下,以2. 0 × 10-7mol/L 的Hg2+标准溶液进行干扰实验,研究水中常见离子对Hg2+测定的影响,控制相对误差在±5%以内,共存离子最大允许倍数为:500 倍量的F-、K+、Cl-、Na+、NH4+、Al3+、Fe2+、NO3-,100 倍量的Ca2+、Cu2+、Mn2+、Zn2+、Cr3+,50 倍量的Mg2+,5 倍量的Fe3+、Pb2+。可见,水中常见K+、Na+、Cl-、NO3-对测定结果干扰非常小,但Fe3+、Pb2+具有一定程度的干扰。在测定前可对水样进行简单预处理,选用掩蔽剂进行掩蔽,加入2%抗坏血酸和2%柠檬酸三铵各1.0 mL,可消除干扰。
2.9 样品分析及回收率测定
分别取湘江水样、池塘水样各50 mL 于100 mL烧杯中,加入H2SO4、KMnO4各1.0 mL,缓慢加热,并不断均匀搅拌至约20 mL。冷却后移入50 mL 容量瓶,加入2% 抗坏血酸和2% 柠檬酸三铵各1.0 mL,超纯水定容至刻度。取5.0 mL 预处理的水样进行测定,每份样品做3 次平行测定,并进行加标回收实验,结果见表1。

表1 样品测定结果及回收率Table 1 Determination results of the samples
3 结论
对Hg2+-KI-MG 体系的RLS 光谱特征、反应条件、影响因素以及一些共存物质的影响进行了研究。结果表明,在该体系中,共振光的强度变化与Hg2+的浓度变化有良好的线性关系,该方法可用于环境水样中Hg2+的测定,方法简便、快速、结果准确可靠。
[1] 周斌,史林飞,刘璐,等. 非标记金纳米粒子共振光散射法检测汞离子[J].应用化工,2012,41(2):344-346.
[2] 王文忠.分光光度法测定水中微量汞[J].化学分析计量,2002,11(5):24-25.
[3] 赵延庆.微型氢化物发生装置在冷原子吸收分光光度法测汞中的应用[J].岩矿测试,2008,27(1):69-70.
[4] 孙引,郑建明.原子荧光法检测鸡肉中铅、砷、汞[J].广州化工,2011,39(6):117-119.
[5] Wu D H,Zhang Q,Chu X,et al. Ultrasensitive electrochemical sensor for mercury (Ⅱ)based on target-induced structure-switching DNA[J]. Biosens Bioelectron,2010,25(5):1025-1031.
[6] 江虹,舒亚林,张秀菊.亚甲基蓝共振瑞利散射法测定阿莫西林的含量[J]. 理化检验:化学分册,2011,47(9):1063-1065.
[7] Qi H,Bi N,Chen Y H,et al.Determination of DNA based on localized surface plasmon resonance light scattering using unmodified gold bipyramids[J]. Spectrochim Acta,2011,81(1):769-773.
[8] 张亚南,冯素玲.表面活性剂和染料探针共振光散射法测定蛋白质[J].化学研究与应用,2012,24(11):1624-1628.
[9] Cui F L,Yun Y R,Hui G Q,et al.Determination of lead at nanogram level in water samples by resonance light scattering technique using tetrabutyl ammonium bromide as a molecular probe[J]. Chemical Society of Ethiopia,2012,26(1):1-8.

