肿瘤患者化疗相关性肠梗阻程序化内科综合治疗的探讨
肿瘤患者化疗相关性肠梗阻程序化内科综合治疗的探讨
何续逊,严文跃,陈艳,杨荣,董正宇
(盐城市肿瘤医院肿瘤内科,江苏 盐城 224003)
[摘要]目的探讨提高肿瘤患者化疗相关性肠梗阻内科治疗疗效的方法。方法学习《晚期癌症患者合并肠梗阻治疗的专家共识》,结合临床经验,对19例化疗相关性肠梗阻患者采用10项措施程序化内科综合治疗。结果全组19例患者中,治愈18例(94.74%),于1~11 d肠梗阻解除,中位时间5 d;死亡1例(5.26%),为延误诊治3 d者。结论肿瘤患者化疗相关性肠梗阻多为不完全性肠梗阻,程序化内科综合治疗尤为重要,只要给予及时合理的内科综合治疗绝大多数可于1周内恢复。
[关键词]肿瘤;化疗;肠梗阻;专家共识;综合治疗
作者简介:何续逊(1951-),男,主任医师,主要从事肿瘤内科诊疗工作。E-mail:hexuxun@csco.org.cn
DOI:10.3969/j.issn.1673-5412.2015.01.026
[中图分类号]R730.53;R730.6
收稿日期:(2014-08-06)
Sequencing Combined Modality Therapy for
Chemotherapy-related Intestinal Obstruction in the Patients with Tumor
He Xuxun,Yan Wenyue,Chen Yan,Yang Rong,Dong Zhengyu
(DepartmentofMedicalOncology,YanchengTumorHospital,Yancheng224003,China)
Abstract[]ObjectiveTo probe the method improving the efficacy of modality therapy for chemotherapy-related intestinal obstruction.MethodsNineteen patients with chemotherapy-related intestinal obstruction received the sequencing combined modality therapy according to the expert consensus and clinical experience.ResultsOf the 19 patients,18 patients (94.74%) relieved in 1-11 days (the median time was 5 days),while 1 patient (5.26%) died of the three-day delayed diagnosis and treatment.ConclusionMost of chemotherapy-related intestinal obstruction are incomplete intestinal obstruction,it could be relieved in one week by using timely and reasonable sequencing combined modality therapy measure.
[Key words]tumor; chemotherapy; intestinal obstruction; experts consensus; combined modality therapy
恶性肠梗阻是指原发性或转移性恶性肿瘤造成的肠道梗阻,是晚期恶性肿瘤患者的常见并发症,国外报道其发生率为5%~43%[1]。由癌性原因所致的恶性肠梗阻早为人们熟知,但对非癌性原因所致的恶性肠梗阻尚认识不足、重视不够。其实非癌性原因所致的恶性肠梗阻并不少见,国外报道约占恶性肠梗阻的3%~48%,其中化疗药物神经毒性所致的麻醉性肠梗阻为恶性肠梗阻中一种特殊的类型,属功能性肠梗阻,又称动力性肠梗阻[1]。其在肿瘤内科时有发生,一旦发生使化疗不能正常进行,同时给患者带来躯体、生理和心理上的痛苦,严重影响患者生活质量。作者通过学习《晚期癌症患者合并肠梗阻治疗的专家共识》(下称专家共识)[1],结合临床经验,对19例化疗相关性肠梗阻患者采用程序化内科综合治疗,现报道如下。
1资料与方法
1.1一般资料入组2006年10月至2012年6月我院收治的肿瘤化疗相关性肠梗阻患者19例。男13例,女6例。年龄27~76岁,中位年龄57岁。原发病:肺癌、结直肠癌各5例,胃癌3例,贲门癌2例,胰腺癌、乳腺癌、胆管癌及腹腔内小圆细胞肿瘤各1例。除1例肺癌外,其余均有原发癌的手术史。临床分期:Ⅱ期1例,Ⅲ期4例,Ⅳ14例。使用的化疗药物:长春瑞滨、紫杉醇、多西紫杉醇、奥沙利铂、培美曲赛、伊立替康、5-氟尿嘧啶、顺铂、吉西他滨。使用的止呕药:格拉司琼16例,甲氧氯普胺3例。
1.2临床特征1)初期临床表现:恶心、呕吐12例,腹胀8例,腹痛5例,腹泻6例,停止排便、排气仅4例;2)影像学征象:19例X线腹部立位平片均见不同程度肠腔胀气、扩张、多个液气平面。临床诊断为不完全性肠梗阻(麻痹性肠梗阻);3)肠梗阻发生时间:发生于化疗第4~7天者10例、第8~14天者9例;4)合并的毒副反应:Ⅰ~Ⅳ度骨髓抑制6例,最低者白细胞0.41×109·L-1,血小板0.76×109·L-1;低血钾1例(3.20 mmol·L-1)。
1.3诊断依据以临床症状及体征为线索,以X线腹部立位平片见肠内多个液气平面为确诊依据。
1.4治疗方法10项措施程序化综合治疗:1)禁食、禁水;2)鼻胃管胃肠减压;3)经中心静脉置管(CVC)途径给药治疗,维持水电解质、酸碱平衡及营养支持;4)抗分泌:奥曲肽或生长抑素24 h持续静脉输注(CIV);5)抗水肿:最初3~5 d内使用激素地塞米松或甲泼尼龙;6)解痉序贯促进胃肠排空:先使用抗胆碱能类解痉剂山莨菪碱10~20 mg·d-1静脉滴注(上午),后予胃动力剂甲氧氯普胺20~30 mg·d-1静脉滴注(下午);并配合脐部贴敷麝香壮骨膏+按摩和(或)腹部高频热疗促进胃肠蠕动及排空;7)预防应激性溃疡:奥美拉唑、西咪替丁1~2次/d;8)防治感染:酌情使用抗生素;9)润肠通便:植物油(香油)灌肠通便及停胃肠减压前胃管内注入;10)对症处理:白细胞减少者即予rhG-CSF升白治疗;低血钾者静脉补钾;伴有癌痛者将口服吗啡类镇痛剂转换为芬太尼透皮贴,若阵发性加剧或暴发痛时,临时加用布桂嗪肌注补救。本组给药途径:17例为经锁骨下CVC、2例为外周静脉植入的中心静脉导管(PICC)。
1.5疗效评估以症状及体征缓解或消失为复查指征,以X线腹部立位平片液气平面消失为梗阻解除标准。
2结果
全组19例患者中,治愈18例(94.74%),于1~11 d肠梗阻解除,中位时间5 d;死亡1例(5.26%),为延误诊治3 d者(表1)。1例死亡患者的演变过程:2006年10月首次纳入该研究,胃癌术后DPF方案化疗结束后,症状仅有腹胀及腹泻稀便少许,未予特殊处理,3 d后腹胀加重伴发热、呼吸急促。经床边X线胸腹部平片发现肠内大量积气、肠腔扩张并多个液气平面才确诊。经胃肠减压胃内吸出咖啡色液体,山莨菪碱解痉、抗生素、激素、奥美拉唑、西咪替丁、补液等治疗无效,发热2 d后死亡。
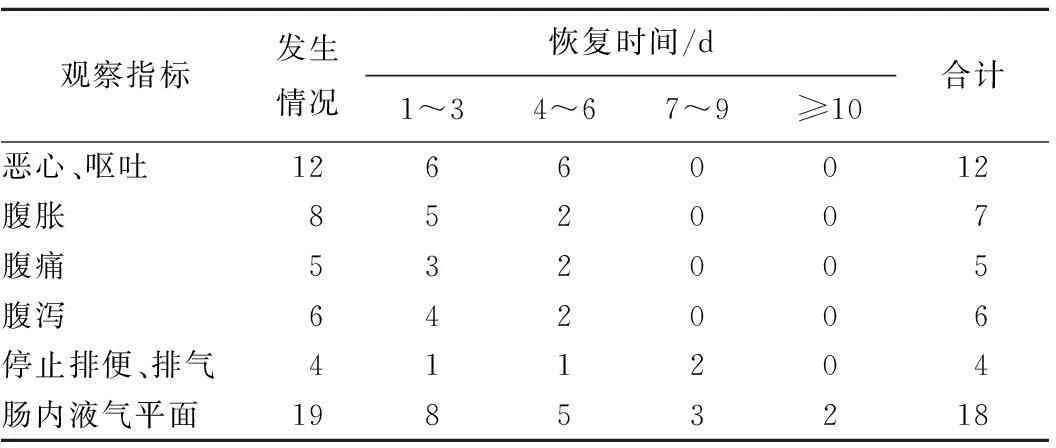
表1 19例化疗相关性肠梗阻患者的治疗转归 n
3讨论
化疗相关性肠梗阻的诊治经验国内文献报道较少,2007年以前作者对此缺乏认识,更无经验,故首例延误诊治即为惨痛教训。自2007年仔细学习专家共识[1],并在临床中不断探索,对肿瘤患者化疗相关性肠梗阻加深了认识并积累了一定的经验。
3.1诱因或高危因素分析专家共识强调明确病因对恶性肠梗阻的治疗有重要意义[1],对于化疗相关性肠梗阻的防治更为重要。化疗者并发麻痹性肠梗阻多与如下因素有关:1)使用了具有神经毒性的化疗药物(尤其是长春碱类、紫杉类、奥沙利铂等)。有学者指出长春碱类大约1/3神经受损害的患者会出现自主神经损伤的症状,表现为便秘、腹痛、尿频、阳痿、起立性低血压等,有时甚至会出现致命的肠梗阻[2];2)便秘及其他所有诱发便秘的因素均为重要诱因,诸如:同时使用5-HT3受体拮抗剂类强力止呕药;同时使用强阿片类镇痛剂;长期卧床,活动过少;体质虚弱无力;同时使用其他减弱胃肠蠕动的药,如麻醉药、抗抑郁药、镇静剂等;脱水,含纤维素性粗糙食物摄入不足等。有学者认为长春碱及长春新碱大剂量给药可降低神经活性,从而抑制胃肠蠕动发生肠麻痹。因此有时与其说是便秘倒不如说是麻痹性肠梗阻[3];3)伴低血钙、血钾等电解质紊乱;4)伴有骨髓抑制,尤其是白细胞减少显著者;5)胃肠道肿瘤术后,有腹腔内转移、有腹腔内灌注化疗史。
3.2治疗措施的探讨及体会1)禁食、禁水并鼻胃管引流胃肠减压应尽早实施,不可因梗阻为不完全性而忽视。专家共识指出鼻胃管引流仅推荐用于需要暂时性减少胃潴留的恶性肠梗阻患者[1]。本组病例中位缓解时间为5 d,表明化疗药物所致的肠梗阻即为仅需短期鼻胃管引流的适应证并应及时实施。早期的胃肠减压对于促进肠梗阻的尽早恢复非常重要[4];2)经CVC途径给药治疗及营养支持为首选最佳途径。专家共识指出大多数恶性肠梗阻患者不能口服给药,静脉给药最好经PICC[1]。本组17例为经锁骨下CVC、2例为PICC,确保了多种药物给药的畅通,尤其是奥曲肽的CIV,并避免了患者外周静脉反复穿刺并长时间输液之苦及四肢活动受限的不便。不建立CVC的途径几乎无法满足多种特殊药物及营养支持的需求,而在CVC中又以经锁骨下CVC为最佳途径。医院感染管理预防与控制措施中也提倡应首选锁骨下静脉[5]。在营养支持中除大量补液促进排泄,维持水和电解质、酸碱平衡外,需注意补充维生素C、B6、B1、B12,以营养神经;补充氨基酸、脂肪乳及白蛋白,以维持患者较好的体能及其精神状态,增强耐受性,有利于病情恢复。反之,一旦全身衰竭梗阻急趋直下将无法逆转;3)解痉序贯促进胃肠排空措施实用而有效。先使用山莨菪碱类解痉剂抑制肠平滑肌的蠕动使梗阻部位松弛,而后使用胃肠动力剂,并配合脐部贴敷具有活血化瘀止痛功效的麝香壮骨膏+按摩促进胃肠排空,有条件加用腹部高频热疗者更佳。热疗40 ℃左右即可,0.5~1 h/次,1次/d。因为热疗通过辐射水肿病灶肠管,进行透热加温,扩张毛细血管,改善局部微循环,增强新陈代谢,提高组织的再生修复能力[6],故更有助于促进排空及有利于不完全性梗阻的疏通;4)抗分泌和抗水肿为重要措施,应用越早越好。有文献[7]报道生长抑素能显著减少消化道分泌,这一抑制作用包括整个消化系统的胃、肠、胆、胰腺等,其减少分泌可达正常分泌的50%以上,故理应对各种类型的肠梗阻均有作用,作者观察本组病例发现生长抑素或奥曲肽以CIV优于皮下注射。激素类药物对梗阻部位的水肿有良好的抗炎、抗水肿作用,发病初期的3~5 d内应用甲泼尼龙或地塞米松冲击未见毒副反应。专家共识认为奥曲肽与促胃肠动力药联用可能逆转恶性肠梗阻恶性进展[1]。早期联用甲氧氯普胺、地塞米松不仅可缓解症状,而且可协同促进肠运动功能快速恢复,逆转肠梗阻,推荐早期应用奥曲肽。学习专家共识,并结合临床效果,作者分为早期联合应用生长抑素类药(奥曲肽或生长抑素)、激素(地塞米松或甲泼尼龙)+抗胆碱能类解痉剂序贯胃肠动力剂是化疗相关性肠梗药物治疗的最佳组合模式,是综合治疗最重要的部分;5)预防应激性溃疡防患于未然。化疗相关性肠梗阻者常伴骨髓抑制、腹胀、腹痛、恶心、呕吐等,使患者处于应激状态,加之使用激素,故加用奥美拉唑及西咪替丁预防应激性溃疡有益无害;6)预防性使用抗生素需酌情而定。对于伴白细胞减少者、发热者应尽早应用。对肠梗阻3 d以上仍未解除者最好也应用;7)植物油(香油)灌肠简便易行。植物油灌肠可促进梗阻以下部分肠内容物尽早排出,胃肠减压前胃管内注入,有利于胃肠道全线润滑,以防再度便秘、梗阻;8)有严重白细胞减少者及时使用rhG-CSF强力升白治疗;9)止痛治疗应尽量避免强阿片类吗啡制剂,以防加重便秘、恶心、呕吐,必须使用者以转换为等效剂量的芬太尼贴剂为宜。伴有暴发痛者以布桂嗪肌注为妥;10)病例死亡原因及其教训:对DPF方案化疗的神经毒性,尤其是易致肠麻痹的高风险警惕性不够;仅有腹胀,且有排便,症状轻微不典型易忽视;腹部X线平片检查为时偏晚,延迟诊断3 d;已并发应激性残胃溃疡出血,发热预示肠管缺血坏死,难以逆转;当时治疗经验缺乏,未及时使用生长抑素或奥曲肽CIV以加强抗分泌治疗;对化疗后或化疗中只要出现无法解释的恶心、呕吐,或腹胀、腹痛,即使有排便排气也应高度警惕麻痹性肠梗阻的可能,应立即行腹部X线平片检查,这样可避免延误诊断;11)化疗相关性肠梗阻若延误诊治3 d以上,一旦伴发热则难以逆转,只要遵循专家共识处理原则及时采取内科综合治疗多可于1周内较顺利恢复。总之,本组程序化内科综合治疗措施及体会也许对临床有一定参考价值。
参考文献:
[1]于世英,王杰年,王金万,等.晚期癌症患者合并肠梗阻治疗的专家共识[J].中华肿瘤杂志,2007,29(8):637-640.
[2]孔莉,于金明.肿瘤化疗不良反应与对策[M].济南:山东科学技术出版社,2002:195-196.
[3]韩少良,邵永孚.癌症化学治疗的毒副反应及其处理[M].上海:复旦大学出版社,2001:133.
[4]陆宇晗,国仁秀.消化道肿瘤合并肠梗阻患者程序化护理中存在的问题及对策[J].护士进修杂志,2009,24(5):475-476.
[5]张苏明.医疗机构医务人员三基训练指南:医院感染管理[M].南京:东南大学出版社,2011:33.
[6]刘乃元,王峰,伊庭海.针刺配合微波热疗治疗粘连性肠梗阻[J].中国针灸,2003,23(5):309.
[7]陈腊旺,周文波.生长抑素治疗急性肠梗阻的临床研究[J].中外医学研究,2010,8(4):34-35.

