朗格汉斯细胞肉瘤的临床病理学观察
俞 岚 周 蕾 武世伍 宋文庆 李涤臣 郭冰沁
(蚌埠医学院第一附属医院临床病理科,蚌埠医学院病理学教研室,安徽省感染与免疫重点实验室,安徽233030)
朗格汉斯细胞肉瘤(Langerhans cell sarcoma,LCS)指具有明确恶性细胞学特征的朗格汉斯细胞(Langerhans cell,LC)呈肿瘤性增生。常多器官累犯,包括淋巴结、肝脏、脾脏、皮肤、肺及骨骼[1]。LC增生在组织学上包括了朗格汉斯细胞组织细胞增生症的临床症候群;另一类即为朗格汉斯细胞肉瘤[2]。LCS罕见,文献鲜有报道。本文报道2例,并复习有关文献。
材料和方法
1.临床资料
病例1,患者男性,31岁。颈部右侧肿块逐渐增大3年余,就诊时肿块长径15cm,部分皮肤已破溃,约3cm。腹壁、胸壁先后出现多个斑块和硬结,稍隆起,质稍硬,暗红色。右侧头皮上亦见一硬结,直径约1cm。右腋下肿块长径1.5cm,切除送检。体检发现巨脾,肝脏肋下4cm。患者无发热、乏力、疼痛等不适感。确诊后2月余患者即死亡。病例2,患者女性,23个月。枕部肿块进行性增大4个月。MRI显示枕部颅内外等低密度混杂影,相应颅骨侵蚀消失。术中查见肿块界限不清。
2.试剂
所用抗体 CD1α(O10)、S-100蛋白(4C4.9)、CD68(KP1)、CD45(PD7/26+2B1)、CD3(SP7)、CD45RO(UCHL-1)、CD45RA (111-1C5)、CD20(L26)、CD99(D13)、CD15(Carb-3)、SMA(1A4)、CK(AE1/AE3)、Ki-67(MIB-1)、Vimentin(V9)、Syn(SP11)、Lysozyme(多克隆),ElivisionTMplus试剂盒及DAB显色试剂盒均购自福州迈新公司。
3.方法
手术标本经10%福尔马林液固定,常规脱水,石蜡包埋,组织切片,HE染色,光镜观察。同时组织块连续切片行免疫组织化学ElivisionTM法染色。S-100蛋白及Ki-67阳性染色为肿瘤细胞胞核呈现棕黄色颗粒或团块,其余各种抗体阳性染色均为肿瘤细胞胞浆内出现棕黄色颗粒或团块。结果判定采取二次计分法:每张切片随机计数5个高倍视野(×400),计数每个高倍视野中阳性细胞所占百分比并计分。首先将染色强度计分:0分为无色,1分为淡黄色,2分为棕黄色,3分为棕褐色。再将阳性细胞百分比计分,0分为阴性,1分为阳性细胞为<10%,2分为11%-50%,3分为51%-75%,4分为>75%。用染色强度得分和细胞数得分的乘积作为判断表达结果,若积分≤2为阴性,>2为阳性。
结 果
1.大体检查
病例1:灰红色结节一个,1.5cm×1.5cm×0.7cm,切面大部分灰红、灰白色,质嫩。病例2:灰红色组织一块,5.0cm×4.5cm×1.5cm,切面灰红、灰白色。
2.镜检
两例LCS的瘤细胞均弥漫排列,瘤细胞体积大,核呈圆形或椭圆形,核沟易查见,可见核仁,核分裂象多见,异型性明显(图1)。病例2于肿瘤间质内尚可见少量嗜酸性粒细胞浸润(图2)。
3.免疫表型
两例CD1α(图3)、S-100蛋白(图4)、CD68(图5)均阳性、Ki-67增殖指数40%-50%(图6)。病例1,CD45、CD45RO、CD45RA、CD20阳性,CD3弱阳性表达,CD99、CD15、SMA、CK 均阴性。病例2,Vimentin阳性,Lysozyme及Syn阴性。
讨 论
1868年,德国病理学家Paul Langherans首先对Langerhans细胞进行了描述,并以此命名。正常情况下,朗格汉斯细胞在体内的分布很局限,主要见于皮肤的复层鳞状上皮;电镜下观察,该细胞还可见于淋巴结、胸腺上皮、支气管黏膜内[3]。Langhans细胞属于辅助免疫系统细胞(单核细胞及其相关细胞)系统,参与免疫反应。辅助免疫系统细胞(表1)分为两大类,一类是抗原递呈细胞(antigen-presenting cells),即各种树突状细胞;另一类是抗原处理细胞(antigen-processing cells),即吞噬/组织细胞。树突状细胞又包括LC、指状交错突细胞(Interdigitating dendritic cell,IDC)、滤泡树突细胞(Follicular dendritic cell,FDC)和纤维母网织细胞(Fibroblast reticulocyte,FRC)。LC和IDC来自骨髓,FDC和FRC来自问叶组织。吞噬细胞来源于单核母细胞和前单核细胞,这些细胞进入血液后游走到组织内,分化成巨噬细胞。LC和IDC是S-100阳性细胞,将抗原递呈给T淋巴细胞,而FDC是S-100阴性细胞,将抗原递呈给B淋巴细胞。组织细胞和树突状细胞增殖性病变十分罕见,历史上对于这类病变的界定不断变动,文献报道也多不一致,导致一些术语的混淆,并且在获取这类病变的生物学行为和组织学特征上存在一定困难。2001年,世界卫生组织将组织细胞和树突状细胞的肿瘤进行了分类:组织细胞肉瘤、Langerhans细胞组织细胞增生症、Langerhans细胞肉瘤、指间树突状细胞肉瘤/肿瘤、滤泡树突状细胞肉瘤/肿瘤、树突状细胞肉瘤(未确定类型)[4]。
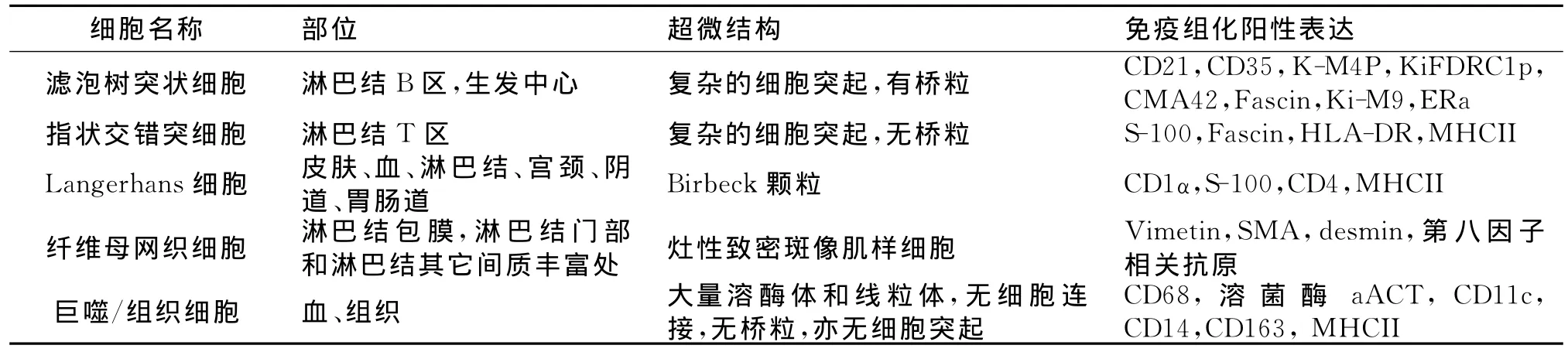
表1 辅助免疫系统细胞Table 1 Auxiliary cells of the immune system
Langerhans细胞直径约12mm,胞质丰富,核形不规则,有切迹或分叶状。在电镜下可见特征性的细胞器,Birbeck颗粒。这是一种呈杆状的管状结构,中央有一纵行条纹和平行排列的周期性条纹,形似一条小拉链。有时一端有泡状膨大似网球拍状。Langerhans细胞表达 HLA-DR、CD1α和S-100蛋白[5]。
3.1 病理学特征 典型的LCS最主要的形态学特点是出现明确恶性细胞学特征的肿瘤细胞:瘤细胞核染色质异常显著,核仁清晰,核分裂比例高,通常>50个/10HPF。部分异型细胞可见核沟,也偶见嗜酸性粒细胞浸润。LCS常为多系统、多器官、多部位累犯,如本例所见。当病变累及淋巴结时常侵犯淋巴窦。免疫表型:瘤细胞S-100蛋白和CDlα均阳性(多为灶性),通常也有CD68、CD45和溶菌酶的表达,Ki-67增殖指数10%-60%,中位数22%。电镜下,瘤细胞胞质内可找到Birbeek颗粒。
3.2 鉴别诊断 ①朗格汉斯细胞组织细胞增生症(Langerhans cell histiocytosis,LCH):LCH 也是Langerhans细胞的肿瘤性增生,可多系统、多器官累犯,也可表现为单灶性。LCH临床多见于儿童,男性多发,常累及骨,也可累及皮肤、肺、淋巴结等部位。镜检LCH常伴有特征性的嗜酸细胞浸润,并夹杂少量淋巴细胞、中性粒细胞及多核袋巨细胞。病变主要累及淋巴窦,其次为副皮质区。表现为淋巴窦的高度扩张,窦腔内充以大量增生的LCH细胞,其细胞核有明显核沟或折叠、凹陷、分叶状,核染色质细腻,核膜较薄,核分裂象不易查见,此细胞学特征与LCS有一定的相似性,但形态温和,异型性不明显。病变中可见到广泛的坏死及纤维化,后者尤其多见于时间长的病变中。免疫组化,朗格汉斯组织细胞通常表达 CD1α、S-100、vimentin、HLADR、peanut agglutinin lectin和胎盘碱性磷酸酶,可不同程度的表达CD45、CD68及溶菌酶,不表达B细胞和T细胞的标记物。超微结构,朗格汉斯组织细胞在细胞质内可出现网球拍状的Birbeck颗粒。②霍奇金淋巴瘤(Hodgkin’s disease,HL):HL多发生于淋巴结,发生于结外者少见。镜检,淋巴结结构消失,RS细胞体积大,胞质丰富,嗜酸性或嗜双色性,核大,常为双核,并有嗜伊红的大核仁。另外,间质常伴有嗜酸性粒细胞、浆细胞和淋巴细胞浸润,部分病例可伴有坏死和纤维化,这与大细胞为主、细胞异型明显伴有坏死的LC肉瘤相似。但LCS不见典型的R-S细胞,并且 HD的免疫组化:CD15、CD30阳性而S-100蛋白、CDlα阴性。③间变性大细胞性淋巴瘤:瘤细胞体积大,圆形或者椭圆形。胞质丰富,嗜双色性或偏淡,可见核旁空晕。间变性大细胞性淋巴瘤的免疫表型:CD30、EMA、ALK-1及T淋巴细胞标记阳性,而S-100、CDlα阴性。④恶性黑色素瘤:免疫表型除S-100阳性外,而且还表达HMB45和 Melan-A。
3.3 临床特点LCS的发病年龄比较广泛,包括成人和儿童(中位年龄41岁)。肿瘤以多脏器累犯为特征,包括皮肤、淋巴结、肝、脾、肺和骨。此型发病者,如仅有单灶性病变,存活率较高[6]。LCS在临床上的变化谱系很大,可以由无痛性发展为侵袭性很强的病灶,常最终导致患者死亡[7]。LCS的肿瘤细胞异型性较小而增殖比率较高并不一定预后不良,恰恰相反,其临床参数却显示预后较好[8]。有报道[9]称所有发生在骨的孤立性病损患者均获得无瘤生存率,相反,20%的患者伴有多系统的累犯,尽管进行了广泛的治疗仍发生了进行性的疾病过程。而异型性显著的病例常伴有进行性临床过程及远处转移[10-12]。所以,当 LCH 伴有显著异型性的肿瘤细胞时,可称为LCS。Kawase等[13]在研究中发现了CD56/NCAM表达的LCS,这种CD56阳性的LCS显示了侵袭性的临床行为,预后较差。国际淋巴瘤研究组织[14]对61例怀疑组织/树枝状细胞类型的淋巴瘤进行了15个抗体的染色,包括标记组织细胞的CD68(lysozyme,Lys),朗格汉斯细胞(CD1α),滤泡树突状细胞(FDC:CD21/CD35)和S-100。其中朗格汉斯细胞肿瘤(LCT)26例:表达结果为CD68 96%,Lys 42%,CD1α100%,S-100 蛋 白100%,CD21/CD35 0%。包括两种类型:典型细胞样LCH(17例)和恶性细胞样(9例),即朗格汉斯细胞肉瘤(LCS)。LCH和LCS的平均年龄分别为33和41岁。男女比率分别为317∶1和1∶2,死亡率为(31%和50%DOD)。4例LCH患者有系统典型损害(Letterer-Siwe disease)。
LCS发病罕见,迄今为止,国内外仅有26例报道。患者年龄17~74岁,13例男性,14例女性;皮肤、淋巴结、肝、脾、肺和骨均见发病,并有1例胆囊受累的报道。本例患者于头部、颈部、胸壁、腋下皮肤出现多发性肿瘤病灶且有内脏累犯,极为罕见。
3.4 治疗 关于LCS尚无公认的完全有效的治疗方案。目前仅以手术切除为主。对于复发性或者进展性病变,单独采用强的松龙或者长春新碱和阿糖胞苷联合化疗较为满意[15]。还有人建议用环孢霉素进行治疗。对于局限性病变者如皮肤病变可用氮芥进行治疗。累及椎体可分次局部放疗(300~600Cgy)。
[1]Bohn O L,Ruiz-Argüelles G,Navarro L,et al.Cutaneous Langerhans cell sarcoma:a case report and review of the literature.Int J Hematol,2007,85(2):116-120
[2]Ferringer T,Banks P M,Metcalf J S.Langerhans cell sarcoma.Am J Dermatopathol,2006,28(1):36-39
[3]Favara B F,Feller A C,Pauli M,et a1.Contemporary classifieat on of histiocyte disorders.Med pediatr Onco1,1997,29(3):157-166
[4]刘彤华.组织细胞/树突状细胞肿瘤的分类和进展.中华病理学杂志,2005,34(6):373-374
[5]Lauritzen A F,Ralfkiaer E.Histiocytic sarcomas.Leuk Lymphoma,1995,18(1-2):73-80
[6]龚西騟.朗格罕斯细胞增生症的病理与临床.临床与实验病理学杂志,2000,16(2):149-153
[7]Frederiksen P,Thommesen P.Histiocytosis X:II.Histologic appearance correlated to prognosis and extent of disease.Acta Radiol Oncol Radiat Phys Biol,1978,17(1):10-16
[8]Risdall R J,Dehner L P,Duray P,et al.Histiocytosis X (Langerhans’cell histiocytosis).Prognostic role of histopathology.Arch Pathol Lab Med,1983,107(2):59-63
[9]Howarth D M,Gilchrist G S,Mullan B P,et al.Langerhans cell histiocytosis:diagnosis,natural history,management,and outcome.Cancer,1999,85(10):2278-2290
[10]Tani M,Ishii N,Kumagai M,et al.Malignant Langerhans cell tumor.Br J Dermatol,1992,126(4):398-403
[11]Itoh H,Miyaguni H,Kataoka H,et al.Primary cutaneous Langerhans cell histiocytosis showing malignant phenotype in an elderly woman:report of a fatal case.J Cutan Pathol,2001,28(7):371-378
[12]Misery L,Godard W,Hamzeh H,et al.Malignant Langerhanscell tumor:a case with a favorable outcome associated with theabsence of blood dendritic cell proliferation.J Am Acad Dermatol,2003,49(3):527-529
[13]Kawase T,Hamazaki M,Ogura M,et al.CD56/NCAM-positive Langerhans cell sarcoma:a clinicopathologic study of 4cases.Int J Hematol,2005,81(4):323-329
[14]Pileri SA,Grogan TM,Harris NL,et al.Tumours of histiocytes and accessory dendritic cells:an immunohistochemical approach to classification from the International LymphomaStudy Group based on 61cases.Histopathology,2002,41(1):1-29
[15]纪小龙.尹彤,申明识.朗格汉斯细胞组织细胞增生症的临床病理.临床与实验病理学杂志,2000,16(2):154-155
图 版 说 明
图1 瘤细胞在真皮内弥漫分布,异型明显(HE×400)
图2 瘤细胞间可见少量嗜酸性粒细胞浸润(红色箭头)(HE×400)
图3 瘤细胞CD1α阳性,箭头示细胞膜表达(ElivisionTM×400)
图4 瘤细胞S-100蛋白阳性,箭头示细胞核表达(ElivisionTM×400)
图5 瘤细胞CD68阳性,箭头示细胞质和膜表达(ElivisionTM×400)
图6 瘤细胞Ki-67阳性,箭头示细胞核表达(ElivisionTM×400)
EXPLANATION OF FIGURES
Fig.1Diffusing arrangement of tumor cells in superficial
Fig.2Interstitial of tumor cells,we can see dermal,with marked atypia(HE×400)eosinophils(red arrow)infiltrating(HE×400)
Fig.3Expression of CD1αwas observed in cell membrane
Fig.4Expression of S-100protien was observed in cell nucleus(red arrow)(ElivisionTM×400)(red arrow)(ElivisionTM×400)
Fig.5Expression of CD68was observed in cytoplasm
Fig.6Expression of Ki-67was observed in cell nucleus and cell membrane(red arrow)(ElivisionTM×400)(red arrow)(ElivisionTM×400)

