B2O3对CaO-MgO-Al2O3-SiO2体系玻璃的结构和析晶性能的影响
徐心怡,顾少轩,夏素旗,顾安娜
(武汉理工大学材料科学与工程学院,湖北 武汉 430070)
B2O3对CaO-MgO-Al2O3-SiO2体系玻璃的结构和析晶性能的影响
徐心怡,顾少轩,夏素旗,顾安娜
(武汉理工大学材料科学与工程学院,湖北 武汉 430070)
采用溶胶-燃烧法制备了CaO-MgO-Al2O3-SiO2体系玻璃的粉体,粉体的颗粒细小均匀,其平均颗粒粒径在80 nm左右。采用X射线衍射分析、傅里叶变换红外光谱分析、差热分析等方法研究了玻璃粉体样品的结构和析晶性能。研究结果表明,加入B2O3后,样品中形成由[SiO4]四面体网络和[BO3] 三角体链共同构成的结构骨架,使玻璃结构更加紧密,并增强了阴离子结构基团与Ca2+、Mg2+等网络外体离子之间的静电作用;B2O3的加入显著降低了样品的玻璃转变温度,明显抑制CaOMgO-Al2O3-SiO2玻璃体系的析晶能力,经过1150 ℃热处理后的样品基本保持非晶态结构。
硼硅酸盐玻璃;无碱,烧结助剂;结构;析晶性能
0 引 言
电介质陶瓷元件是电子器件中的重要无源元件,具有旁路、耦合、鉴频、滤波、储能交换、吸收浪涌等广泛的用途。当前,电子器件日益向微小型化、集成化、模块化和低维化方向发展。与之相应,要求采用低温烧结技术制备电介质陶瓷元件。加入烧结助剂是降低电介质陶瓷元件的烧结温度的重要途径。加入适量的烧结助剂,不仅可以利用液相烧结机制来实现电介质陶瓷的低温烧结,而且可以优化电介质陶瓷的显微结构和介电性能[1-5]。无碱的CaO-MgO-Al2O3-SiO2体系玻璃具有优良的介电性能[6],是一种常用的电介质陶瓷的烧结助剂[7-9]。
通信联系人:顾少轩(1967-),女,教授。
当前,还需要对CaO-MgO-Al2O3-SiO2体系玻璃烧结助剂的制备技术和组成进行优化,以改善其使用效果。一方面,国外研究者大多采用熔融-淬冷法来制备玻璃烧结助剂,所制备的烧结助剂粉体的颗粒较大。采用超细微的玻璃粉体为烧结助剂,可以提高烧结助剂粉体与电介质粉体混合的均匀程度,改善电介质陶瓷的烧结性能和显微结构[1]。因此,探索制备玻璃烧结助剂的超细微粉体的新工艺具有重要意义。另一方面,CaO-MgO-Al2O3-SiO2体系玻璃在高温下产生析晶,形成堇青石、钙长石等晶相[10,11]。在作为电介质陶瓷的烧结助剂使用时,该体系玻璃在高温下的析晶不利于充分发挥其促进电介质陶瓷烧结的作用。有人研究了B2O3对CaO-MgO-Al2O3-SiO2体系玻璃陶瓷烧结性能的影响,发现加入少量B2O3可以降低该体系玻璃的软化温度和促进该体系玻璃陶瓷的烧结,同时抑制了堇青石、钙长石等晶相在高温下的析出[12]。由于该研究的目的是获得致密的玻璃陶瓷,为保证堇青石等晶相的析出,B2O3的加入量较低(≤6wt.%),对B2O3的抑制析晶效应的认识不够充分。当前,尚有待进一步考察B2O3抑制CaO-MgO-Al2O3-SiO2体系玻璃析晶的效果,并揭示这种抑制析晶效应的微观机制,为优化该体系玻璃烧结助剂的组成提供依据。
Correspondent author:GU Shaoxuan(1967-), female, Professor.
E-mail:gsx@whut.edu.cn
在本论文中,用B2O3代替CaO-MgO-Al2O3-SiO2玻璃中的部分Al2O3,采用溶胶-燃烧法制备该体系玻璃的粉体样品,并考察B2O3的加入对CaO-MgO-Al2O3-SiO2玻璃粉体结构和析晶性能的影响。
1 实 验
采用溶胶-燃烧法制备玻璃粉体样品,样品的名义组成为7wt.%CaO-5wt.%MgO-(26-x) wt.%Al2O3-xwt.%B2O3-62wt.%SiO2(x=0、5、10和15),所采用的原料为分析纯的柠檬酸、正硅酸四乙酯、硝酸镁、四水硝酸钙、九水硝酸铝、冰乙酸、乙醇和硼酸。将正硅酸四乙酯溶于无水乙醇中并加入去离子水,无水乙醇与去离子水的体积比为6:1,滴加冰乙酸调节溶液的pH值至1,在60 ℃下加热搅拌,得到澄清透明的溶液。将柠檬酸、硼酸和各种硝酸盐溶于无水乙醇中,在60 ℃下加热搅拌,得到澄清透明的溶液。然后,将两种溶液混合,在60 ℃下加热搅拌后形成透明的粘稠状溶胶。在本论文研究中,柠檬酸与各种反应物阳离子总量的摩尔比为1.5∶1。在300 ℃下对该溶胶进行加热,使之脱水、浓缩、膨化和燃烧,得到褐色的固态前驱体。固态前驱体经过研磨后,在650 ℃下保温2 h,得到白色的合成粉体。X射线衍射(XRD)分析结果表明,该合成粉体为非晶态。为考察合成粉体在高温下的析晶行为,在800 ℃-1200 ℃的温度范围内进行合成粉体的热处理,热处理时间为2 h。
采用Netzsch STA449C型同步热分析仪进行固态前驱体样品的失重-示差扫描量热(TG-DSC)分析和合成粉体样品的差热分析(DTA),TG-DSC分析和DTA分析均在空气气氛中进行,其升温速率均为10 ℃/min。采用Panalytical X’pert PBO X射线衍射仪分析合成粉体样品和热处理样品的物相组成。采用JEOL JSM-5610LV型扫描电子显微镜(SEM)观察合成粉体样品的颗粒形貌,测试前在合成粉体样品表面进行喷金处理,采用Image-ProPlus6.0图像分析软件计算合成粉体的颗粒粒度分布。采用Nicolet Nexus傅里叶变换红外光谱仪进行合成粉体样品的红外光谱(FT-IR)分析,采用KBr压片法制备测试样品,合成粉体与KBr的质量比为1:100。
2 结果与讨论
2.1 合成粉体的表征
图1为x=5的固态前驱体样品的TG-DSC曲线。在40 ℃-200 ℃的温度范围内,TG曲线上出现13.6 %的失重,在DSC曲线上对应产生吸热蜂(100 ℃附近),这可归于固态前驱体中吸附水的挥发和残余有机物的分解。在420 ℃附近,DSC曲线上出现强放热峰,同时在TG曲线上可观察到明显的失重现象(30.1%),这是由于固态前驱体中残余碳粉的燃烧所引起的。650 ℃以后,TG曲线保持稳定,DSC曲线上无放热峰或放热峰出现,表明固态前驱体的热分解过程基本结束。对其它组成的固态前驱体样品也进行了TG-DSC分析,其结果与在图1中观察到的变化基本一致。
图2为不同B2O3含量的合成粉体样品的XRD图谱。各样品的XRD图谱均呈现为弥散的漫峰,表明合成粉体均为非晶态结构。图3为不同B2O3含量的合成粉体样品的SEM照片。可以观察到,各样品均具有均匀细小的颗粒形态。图4为不同B2O3含量的合成粉体颗粒粒度的图像分析结果。可以看到,合成粉体样品的颗粒粒度主要在50-120 nm的范围内,颗粒粒度基本符合高斯分布,平均颗粒粒径为约80 nm。

图1 x=5的固态前驱体样品的TG-DSC曲线Fig.1 TG-DSC curves of the solid precursor with x=5
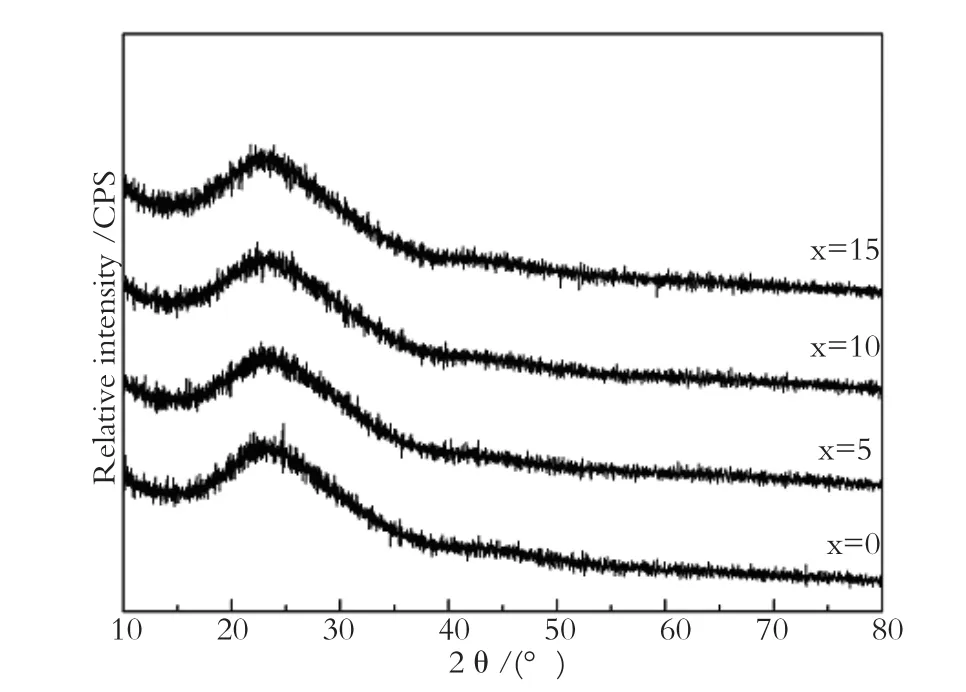
图2 不同B2O3含量的合成粉体样品的XRD图谱Fig.2 XRD patterns of synthesized powders with varied B2O3content
2.2 FT-IR分析
图5为不同B2O3含量的合成粉体样品的FT-IR图谱。表1列出各样品吸收谱线带的中心波数。x=0时,样品吸收谱带的中心波数位于460 cm-1、800 cm-1和1080 cm-1附近,其中以中心波数在1080 cm-1附近的吸收谱带最为明显。这与硅酸盐玻璃红外光谱的基本特征是相吻合的,表明该样品中形成[SiO4]四面体网络结构,三个吸收谱带分别对应于[SiO4]四面体结构基团中Si-O-Si的弯曲振动、对称伸缩振动和反对称伸缩振动等振动模式[13,14]。
对于加入B2O3的样品(x=5、x=10和x=15),除 [SiO4]四面体基团的吸收谱带外,在700 cm-1和1420 cm-1附近出现新的吸收谱带,且这些吸收谱带随B2O3含量的增加而趋于增强。这两个新的吸收谱带可分别归于[BO3]三角体中B-O的弯曲振动和伸缩振动[15-18],表明B2O3以 [BO3] 三角体链的形式存在于样品的玻璃结构中。
由表1中数据可知,随着B2O3含量的增加,[BO3]三角体中B-O伸缩振动所对应谱带的中心波数向高波数方向移动,这可能是由于[BO3]链状结构的聚合度增强的结果。可以注意到,B2O3的加入对[SiO4]四面体的振动产生影响,随着B2O3含量的增加,[SiO4]四面体中Si-O-Si的弯曲振动模式和反对称伸缩振动模式所对应的振动谱带(460 cm-1附近和1080 cm-1附近)的中心波数分别向高波数方向和低波数方向偏移,说明玻璃结构中[BO3]三角体链的形成对[SiO4]四面体网络的振动产生影响,反映出[BO3] 三角体链与[SiO4]四面体网络之间的相互作用。这种相互作用源于[SiO4]四面体和[BO3]三角体与网络外体离子(如Ca2+、Mg2+等)之间的静电作用,通过这种静电作用,不同类型的阴离子基团之间形成紧密的联系[19]。

图3 不同B2O3含量的合成粉体样品的SEM照片Fig.3 SEM images of synthesized powders with (a) x=0, (b) x=5, (c) x=10 and (d) x=15

图4 不同B2O3含量的合成粉体样品的SEM照片Fig.4 Particle size distribution of synthesized powders with (a) x=0 and (b) x=10

图5 不同B2O3含量的合成粉体样品的FT-IR图谱Fig.5 FT-TR spectra of synthesized powders with varied B2O3content

表1 不同B2O3含量的合成粉体的红外吸收谱带Tab.1 Infrared adsorption bands of synthesized powders with varied B2O3content
2.3 析晶行为
图6为不同B2O3含量的合成粉体样品的DTA曲线。可见,x=0的样品的玻璃转变温度(Tg)位于910 ℃附近。在960 ℃-1090 ℃的温度范围内,DTA曲线的基线明显降低,这是由于样品粘度降低,从而产生粘性流动所致[10]。在1140 ℃和1225 ℃附近,DTA曲线上分别出现两个放热峰,这是玻璃体系样品中部分氧化物产生析晶所引起的。在1306 ℃附近, DTA曲线上出现了一个尖锐的吸热峰,这可归于析出晶体的熔融。
与x=0的样品相比,加入B2O3的样品的玻璃转变温度降低至730 ℃附近,样品产生粘性流动的温度范围也向低温方向移动(760 ℃-870 ℃),这与加入B2O3的样品中 [BO3] 三角体链状结构的存在有关。此外,随着B2O3含量的增加,样品中Al2O3的含量相应减少,促进了样品中液相的形成,这也是样品的玻璃软化温度降低的重要原因[12,20]。当x=5时,DTA曲线上与析晶行为相对应的放热峰变弱。还可以看到,该样品的析晶温度明显降低,这与B2O3的加入促进了液相的形成有关[12]。对于x=10和x=15的样品,在其DTA曲线上未能观察与析晶行为相对应的放热峰。
图7为经热处理后不同B2O3含量的样品的XRD图谱。可以看到,当热处理温度为1000 ℃时,x=0的样品中开始有少量的晶相析出。随着热处理温度的提高,析出晶相所对应衍射峰的数量和强度都逐渐增加。经过查对JCPDS卡片确定,析出晶相为堇青石和钙长石,这与前人对CaO-MgO-Al2O3-SiO2玻璃体系的析晶产物的研究结果相符合[10-12]。可以注意到,加入B2O3的样品(x=5、x=10和x=15)的析晶能力明显变弱,析出的堇青石和钙长石所对应衍射峰的数量和强度都明显减少。当热处理温度为1150 ℃时,加入B2O3的样品的XRD图谱仍基本呈现出弥散的衍射特征,说明样品在整体上保持非晶态结构。热处理样品的XRD分析结果证实, B2O3的加入对CaO-MgO-Al2O3-SiO2玻璃体系粉体的析晶性能具有明显的抑制作用,这与合成粉体样品的DTA分析结果是相一致的。

图6 不同B2O3含量的合成粉体样品的DTA曲线Fig.6 DTA curves of synthesized powders with varied B2O3content
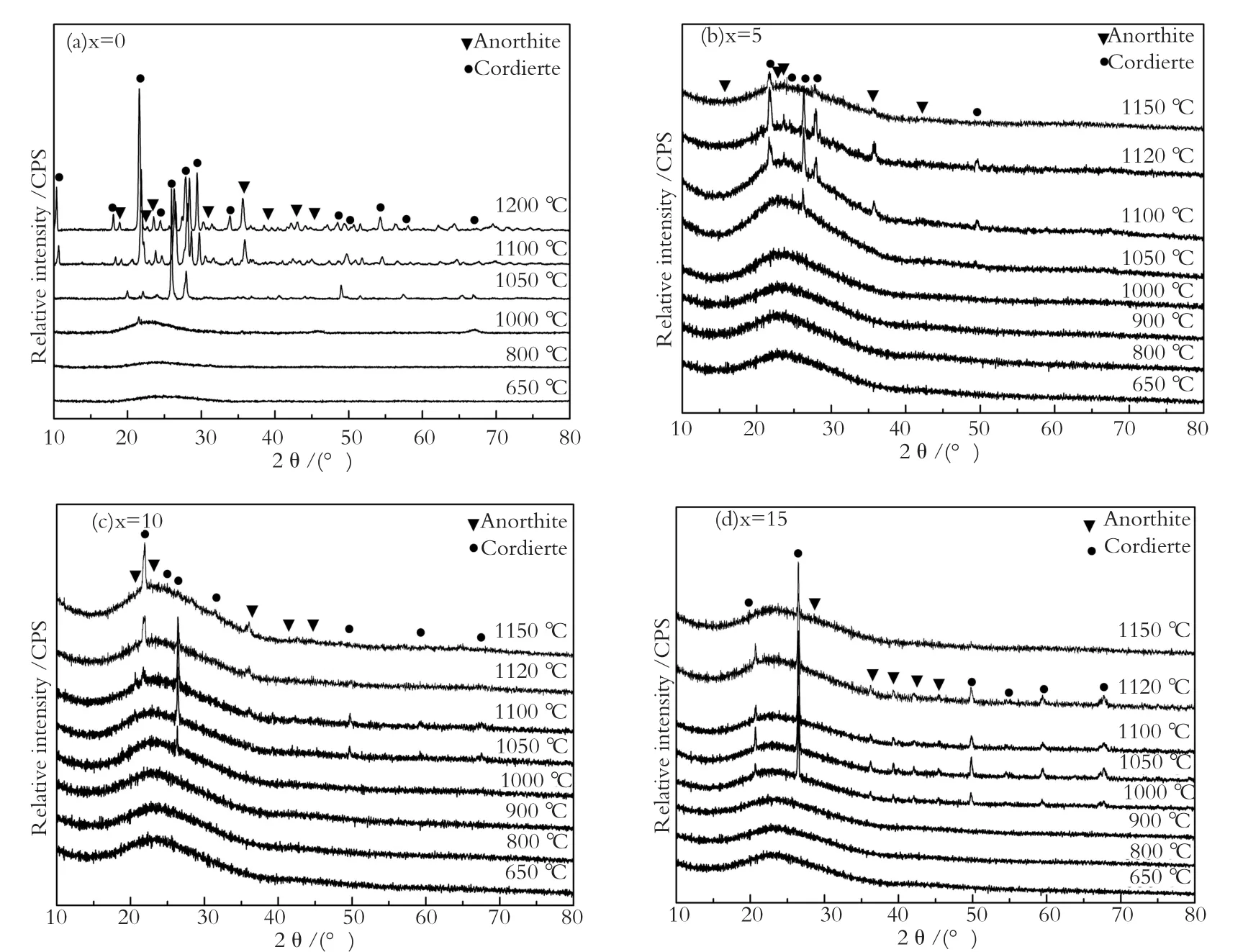
图7 经热处理后不同B2O3含量的样品的XRD图谱Fig.7 XRD patterns of the powders with varied B2O3content after calcination
CaO-MgO-Al2O3-SiO2玻璃体系中堇青石、钙长石等晶相的析出依赖于Ca2+、Mg2+、Al3+等参与晶相形成的金属离子的聚集,与这些金属离子在玻璃结构中的扩散行为紧密相关。对于x=0的样品,[SiO4]四面体通过共顶相连而形成网络结构,构成玻璃结构的骨架。加入B2O3后,样品中形成由[SiO4]四面体网络结构和[BO3] 三角体链状结构共同构成的结构骨架,[SiO4]四面体阴离子基团与[BO3]三角体阴离子基团之间通过与网络外体离子(如Ca2+、Mg2+等)的静电作用而产生相互联系,使玻璃结构更加紧密。此外,与[SiO4]四面体网络结构相比,[BO3]三角体链的形成能够提供更多的非桥氧,进一步增强了阴离子基团与Ca2+、Mg2+等网络外体离子之间的静电作用。加入B2O3后所导致的这些结构变化都有利于抑制金属离子在玻璃结构中的扩散和聚集,因而降低了样品的析晶能力。
3 结 论
(1)采用溶胶-燃烧法制备了名义组成为7wt.%CaO -5wt.%MgO-(26-x)wt.%Al2O3-xwt.%B2O3-62wt.%SiO2(x=0、5、10和15)的玻璃粉体,粉体的颗粒细小均匀,其平均颗粒粒径在80 nm左右。
(2)加入B2O3后,样品中形成由[SiO4]四面体网络和[BO3] 三角体链共同构成的结构骨架,使玻璃结构更加紧密,并增强了阴离子结构基团与Ca2+、Mg2+等网络外体离子之间的静电相互作用。
(3)B2O3的加入显著降低了玻璃转变温度,促进了液相的形成,有效抑制了CaO-MgO-Al2O3-SiO2玻璃体系的析晶能力,经过1150 ℃热处理后的样品基本保持非晶态结构。
[1] JAIN T A, FUNG K Z, HSIAO S, et al. Effects of BaO-SiO2glass particle size on the microstructures and dielectric properties of Mn-doped Ba(Ti, Zr)O3ceramics [J]. J. Eur. Ceram. Soc., 2010, 30: 1469-1476.
[2] WANG X R, ZHANG Y, SONG X Z, et al. Glass additive in barium titanate ceramics and its influence on electrical breakdown strength in relation with energy storage properties [J]. J. Eur. Ceram. Soc., 2012, 32: 559-567.
[3] WU T, PU Y P, CHEN K. Dielectric relaxation behavior and energy storage properties in Ba0.4Sr0.6Zr0.15Ti0.85O3ceramics with glass additives [J]. Ceram. Int., 2013, 39: 6787-6793.
[4] CHEN X Y, ZHANG W J, BAI S X, et al. Densification and characterization of SiO2-B2O3-CaO-MgO glass/Al2O3composites for LTCC application [J]. Ceram. Int., 2013, 39: 6355-6361.
[5] WANG P K, PU Y P, WU T. Microstructure and dielectric properties of Ba0.4Sr0.6Ti1-yZryO3sintered with SrO-B2O3-SiO2glass additive [J]. Ceram. Int., 2015, 41: 7261-7266.
[6] SMITH N J, RANGARAJAN B, LANAGAN M T, et al. Alkalifree glass as a high energy density dielectric material [J]. Mater. Lett., 2009, 63: 1245-1248.
[7] WEIR R D, NELSON C W, Electrical-energy-storage unit (EESU) utilizing ceramic and integrated-circuit technologies for replacement of electrochemical batteries [P]: US, 7033406 B2. 2006-04-25.
[8] DAI Y, Guo T, PEI X M, et al. Effects of MCAS glass additives on dielectric properties of Al2O3-TiO2Ceramics [J]. Mater. Sci. Eng. A, 2008, 457: 76-80.
[9] XU Q, ZHAN D, HUANG D P, et al. Effect of MgOCaO-Al2O3-SiO2glass additive on dielectric properties of Ba0.95Sr0.05Zr0.2Ti0.8O3ceramics [J]. J. Alloys Compd., 2013, 558: 77-83.
[10] TOYA T, TAMURA Y. Preparation and properties of CaOMgO-Al2O3-SiO2glass-ceramics from kaolin clay refining waste (Kira) and dolomite [J]. Ceram. Int., 2004, 30: 983-989.
[11] FU Y P, LIN C H. Synthesis and microwave characterization of 2(MgO,CaO)-2Al2O3-5SiO2glass ceramics from the sol-gel process [J]. J. Mater. Sci., 2003, 38: 3081-3084.
[12] YANG C F, CHENG C M. The influence of B2O3on the sintering of MgO-CaO-Al2O3-SiO2composite glass powder [J]. Ceram. Int., 1999, 25: 383-387.
[13] TOMOZAWA M, HONG J W, S. RYU R. Infrared (IR) investigation of the structural changes of silica glasses with fictive temperature. J. Non-Cryst. Solids., 2005, 35: 1054-1060.
[14] OKUNO M, ZOTOV N, SCHMUCKER M, et al. Structure of SiO2-Al2O3glass: Combined X-ray diffraction, IR and Raman studies [J]. J. Non-Cryst. Solids., 2005, 351: 1032-1038.
[15] UCHINO T, YOKO T. Vibration of alkali cations in borate glasses from molecular orbital calculations [J]. Solid State Ionics, 1998, 105: 91-95.
[16] STOCH L, SRODA M. Infrared spectroscopy in the investigation of oxide glasses structure [J]. J. Mol. Struct., 1999, 511-512: 77-84.
[17] 杜建波,范尚青,何璇, 等. 含Y2O3的ZnO-Bi2O3-B2O3系统玻璃热学与电学性能研究[J]. 陶瓷学报,2013,34(2):171-176.
DU Jianbo, et al. Journal of Ceramics, 2013, 34(2): 171-176.
[18] 何璇,杜建波,范尚青, 等. La2O3对ZnO-Bi2O3-B2O3系统玻璃结构和介电性能的影响[J]. 陶瓷学报,2013,34(4):443-449.
HE Xuan, et al. Journal of Ceramics, 2013, 34(4): 443-449.
[19] 王雯雯, 岳云龙, 杜钊, 等. 硼含量及配位对铝硼硅酸盐玻璃介电性能的影响[J]. 山东陶瓷, 2012, 35(3): 3-6.
WANG Wenwen, et al. Shangdong Ceramics, 2012, 35(3): 3-6.
[20] TORRES F J, DE SOLA E R, ALARCON J. Effect of boron oxide on the microstructure of mullite-based glass-ceramic glazes for floor-tiles in the CaO-MgO-Al2O3-SiO2system. J. Eur. Ceram. Soc., 2006, 26: 2285-2292.
Effects of B2O3Addition on Structure and Crystallization Ability of CaO-MgO-Al2O3-SiO2Glass Sintering Aids
XU Xinyi, GU Shaoxuan, XIA Suqi, GU Anna
(School of Materials Science and Engineering, Wuhan University of Technology, Wuhan 430070, Hubei, China)
The powders of CaO-MgO-Al2O3-B2O3-SiO2system glass with varied B2O3content were prepared by a sol-combustion method. The resulted powders exhibited an amorphous nature and uniform particle morphology, with the mean particle sizes around 80 nm. The structure and crystallization behavior of the powders were investigated as a function of B2O3content by employing XRD, FT-IR and DTA methods. The addition of B2O3led to coexistence of [SiO4] tetrahedral network and [BO3] triangle chains as the structural frameworks, producing a tighter glass structure while enhancing static electric interactions between the anion structural units and network-modifying cations such as Ca2+and Mg2+. As a result, the transition temperature Tgof the glass system was significantly decreased due to the addition of B2O3. Meanwhile, the crystallization ability of the glass powders at elevated temperatures was effectively suppressed. The borosilicate glass powders basically maintained an amorphous structure after calcining at 1150 ℃.
borosilicate glass system; alkali-free; sintering aids; structure; crystallization ability
date: 2015-03-27. Revised date: 2015-07-19.
10.13957/j.cnki.tcxb.2015.06.005
TQ174.75
A
1000-2278(2015)06-0594-07
2015-03-27。
2015-07-19。
国家自然科学基金项目(51172169);武汉理工大学自主创新研究基金项目(2015-CL-B1-19)。

