HPLC法测定多血康胶囊中6个成分
黄 宇, 王毓杰, 杨文娟, 张 艺, 赖先荣
(1.成都中医药大学民族医药学院,四川成都611137;2.四川新绿色药业科技发展股份有限公司,四川成都611193)
[质 量]
HPLC法测定多血康胶囊中6个成分
黄 宇1,2, 王毓杰1*, 杨文娟1, 张 艺1, 赖先荣1
(1.成都中医药大学民族医药学院,四川成都611137;2.四川新绿色药业科技发展股份有限公司,四川成都611193)
目的 建立HPLC法测定藏药多血康胶囊 (大花红景天、余甘子、沙棘、干姜)中红景天苷、没食子酸、柯里拉京、槲皮素、山柰素、异鼠李素等6种成分。方法 多血康胶囊70%甲醇提取液分析采用Wondasil C18-WR色谱柱 (4.6mm×250 mm,5μm),流动相Ⅰ为甲醇-0.2%磷酸溶液,梯度洗脱,检测波长275 nm,测定红景天苷、没食子酸和柯里拉京;流动相Ⅱ为甲醇-0.4%磷酸溶液 (48:52),检测波长370 nm,测定槲皮素、山柰素、异鼠李素。体积流量为1 m L/m in,柱温30℃,进样10μL。结果 各成分均达到基线分离,在其线性范围内呈现良好的线性关系,r≥0.999 7。加样回收率值为99.1%~101.7%,RSD值为0.69%~1.7%。结论 本方法以多血康胶囊的入血成分为指标,建立了简便、准确,专属性和重复性好的定量测定方法。
多血康胶囊;红景天苷;柯里拉京;异鼠李素;HPLC
高原红细胞增多症(high altitude polycythemia,HAPC)系由高原低氧引起红细胞增多、血液黏稠的常见高原病,又名 “多血症”。我国青藏高原人群患病率为2.5%[1]。随着海拔升高,HAPC患病
率明显增高,已成为严重威胁高原人群健康的常见慢性疾病之一。藏药复方多血康是著名藏医措如.才郎大师治疗多血症的经验方,疗效确切。该方以红景天为君药,活血清肺、滋补元气;以余甘子清热化瘀、沙棘活血散瘀为臣药;以干姜舒胸、润腔、生胃火为佐药[2]。现代药理研究表明其能缓解机体疲劳、提高缺氧耐受力[3]。在前期研究中,课题组选择血瘀证模型与高原缺氧多血症动物模型,从细胞及基因水平,阐明了多血康治疗高原多血症的分子机制;采用血清药物化学及体外化学指纹图谱方法,明确了藏药多血康的入血成分主要来源于红景天、余甘子、沙棘膏[3-5]。目前,对于该方还缺乏全面的质量控制研究。本实验以红景天、余甘子、沙棘中的主要入血成分为指标,建立多成分定量测定方法,为进一步提高多血康胶囊的质量控制水平提供参考依据。
1 材料
美国Aglient 1260高效液相色谱仪;Wondasil C18-WR(4.6 mm×250 mm,5μm);KQ-50B型超声波清洗器 (昆山市超声仪器有限公司);BP121S电子天平(德国Sartorius公司)等。对照品没食子酸、柯里拉京、红景天苷、槲皮素、山柰素、异鼠李素均购自于中国食品药品检定研究院,批号分别 为 110831-201204、111623-200301、110818-201206、100081-201408、110861-201310、110860-201109。乙腈、甲醇、磷酸为色谱纯,其余试剂均为分析纯。
多血康胶囊自制样品5批 (批次DXK1~DXK5)。原药材经成都中医药大学张艺研究员鉴定,为大花红景天Rhodiola crenulata(Hook.f.et Thoms.)H.Ohba的干燥根和根茎、余甘子Phyllanthus emblica L.的干燥成熟果实、中国沙棘H. rhamnoides L.subsp.sinensis Rousi.的干燥成熟果实、干姜Zingiber officinale Rosc.的干燥根茎,制备工艺参照专利方法[3]进行。
2 方法与结果
2.1 色谱条件 Wondasil C18-WR色谱柱(4.6 mm×250 mm,5μm)。流动相Ⅰ为甲醇 (A)-0.2%磷酸溶液 (B),梯度洗脱 (0~30 min,1%~14%A;30~65 min,14%~48%A);检测波长275 nm。流动相Ⅱ为甲醇(A)-0.4%磷酸溶液 (B)(48:52);检测波长370 nm;体积流量1 m L/min;柱温30℃;进样10μL。在上述色谱条件下,6个成分均能与相邻色谱峰达到基线分离,分离度均大于1.5,理论塔板数不低于5 000。对照品、供试品、阴性样品色谱图见图1。
2.2 对照品溶液的制备 混合对照品Ⅰ:精密称取一定量的没食子酸、红景天苷和柯里拉京对照品,分别用甲醇溶解,制成质量浓度为0.996、0.634、0.835 mg/mL的对照品溶液。精密量取各对照品溶液,置同一量瓶中,加甲醇分别制成没食子酸0.344 7 mg/m L、红景天苷0.101 1 mg/mL、柯里拉京0.056 3 mg/mL的混合对照品。混合对照品Ⅱ:精密称取一定量的槲皮素、山柰素和异鼠李素对照品,分别用甲醇溶解,制成质量浓度为0.481、0.10、0.095 mg/mL的对照品溶液。精密量取各对照品溶液,置同一量瓶中,加甲醇分别制成槲皮素4.81μg/mL、山柰素20.00μg/m L、异鼠李素5.70μg/mL的混合对照品溶液。
2.3 供试品溶液的制备 供试品溶液Ⅰ:取本品粉末约1 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇50 m L,密塞,称定质量,超声提取50 min,滤过,用少量甲醇分次洗涤容器及残渣,洗液与滤液合并,挥干,残渣加甲醇使溶解,转移至10 mL量瓶中,并稀释至刻度,摇匀,精密量取5 mL,置氧化铝柱 (中性氧化铝2 g,用水湿法装柱,加15 mL水预洗)上,用70%甲醇洗脱,收集洗脱液,置25mL量瓶中,至洗脱液近刻度时为止,加70%甲醇至刻度,摇匀,滤过,即得。供试品溶液Ⅱ:取本品粉末约1 g,精密称定,置具塞锥形瓶中,加甲醇50mL,加入盐酸3 mL,称定质量,80℃水浴回流1 h,冷却,再次称定质量,用甲醇补足减失的质量,摇匀,滤过,即得。
2.4 线性关系考察 分别精密吸取上述2个混合对照品溶液6、8、10、12、15、20μL,按各色谱条件分别进样,以峰面积为纵坐标,以对照品质量(μg)为横坐标,绘制标准曲线,得到回归方程和相关系数,见表1。
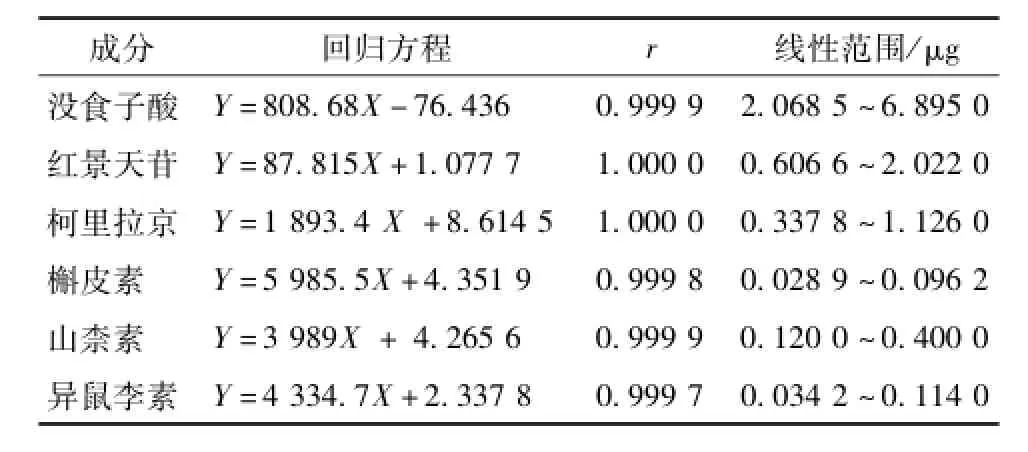
表1 多血康胶囊中6个成分的线性范围Tab.1 Linear ranges of six com ponents in Duoxuekang Capsu Ies

图1 多血康胶囊中6个成分的高效液相色谱图Fig.1 HPLC chromatogram s of six com ponents in Duoxuekang Capsu Ies
2.5 精密度试验 分别精密吸取混合对照品溶液Ⅰ、Ⅱ10μL,分别按流动相Ⅰ、Ⅱ色谱条件,连续进样6次,记录并分析色谱图。各成分峰面积RSD值分别为1.0%、0.16%、1.5%、0.69%、0.94%、1.1%,表明仪器精密度良好。
2.6 稳定性试验 分别精密吸取供试品溶液Ⅰ、Ⅱ (DXK-3,下同)10μL,于0、2、4、6、10、24 h,分别按流动相Ⅰ、Ⅱ色谱条件进样,记录色谱峰面积。各成分的 RSD值分别为1.1%、0.15%、1.7%、0.75%、1.0%、1.1%,表明供试品溶液24 h内稳定性良好。
2.7 重复性试验 取同一批样品12份,分别按供试品溶液Ⅰ、Ⅱ制备方法制样6份,分别进样测定,各成分的RSD值分别为1.0%、0.13%、1.6%、0.58%、1.0%、1.0%,表明该方法重复性良好。
2.8 加样回收率试验 取成分含有量已知的供试品(DXK-3)18份,每份0.5 g,精密称定,分别精密吸取0.996 mg/mL没食子酸对照品溶液6.5、8、10 mL,0.634 mg/mL红景天苷对照品溶液3.6、4.5、5.4 mL,0.835 mg/m L柯里拉京对照品溶液1.6、2、2.4 mL各3份,低温蒸干溶剂,按“2.3”项下供试品溶液Ⅰ制备方法制备;分别精密吸取混合对照品溶液0.8、1.0、1.2 mL(槲皮素0.135 mg/mL、山柰素0.630 mg/mL、异鼠李素0.149 mg/mL)各3份,低温蒸干溶剂,按 “2.3”项下供试品溶液Ⅱ制备方法制备。然后按 “2.1”项下色谱条件Ⅰ、Ⅱ分别测定,计算各对照品的平均加样回收率和RSD,结果见表2、3。
2.9 样品测定 取多血康胶囊样品 5批,按“2.3”项下方法制备供试品溶液Ⅰ、Ⅱ,按“2.1”项下色谱条件Ⅰ、Ⅱ分别测定,进样10μL,测定结果见表4。

表2 没食子酸、红景天苷、柯里拉京加样回收试验结果(n=9)Tab.2 Resu Its of recovery tests for gaIIic acid,saIidrosideand coriIagin(n=9)

表3 槲皮素、山柰素、异鼠李素加样回收试验结果 (n= 9)Tab.3 Resu Its of recovery tests for quercetin,kaem p feroIand isorhamnetin(n=9)

表4 样品测定结果(n=2)Tab.4 Resu Its of the determ ination of samp Ies(n=2)
3 讨论
藏药复方多血康胶囊,是措如.才郎大师治疗高原红细胞增多症(多血症)的经验方。课题组研究证实该方能够降低红细胞压积和纤维蛋白原浓度,抑制红细胞聚集[4],降低血清EPO含有量[5]。并结合体外化学及体内血清指纹图谱,发现入血成分主要来源于红景天、余甘子和沙棘膏[5]。因此,本研究选取了红景天、沙棘、余甘子中的入血成分为指标,开展了其质量控制研究。
本实验在对流动相Ⅰ筛选过程中,先后考察了乙腈-水、乙腈-0.2%磷酸溶液、甲醇-0.2%磷酸溶液3种系统,结果表明,采用甲醇-0.2%磷酸作流动相时,色谱峰基线稳定,分离度好[6-13]。提取方式和提取时间考察结果表明,选用70%甲醇溶液50 mL超声提取50 min,目标成分提取效率较高。另外,本实验测定槲皮素、山柰素、异鼠李素3个成分的方法与本实验室建立的沙棘[12]、沙棘膏质量标准测定方法一致,该法已收录至 《中国药典》2015年版中,故本研究未进行论述。
本研究结合血清药物化学的研究结果,以多血
康胶囊中的入血成分为指标,建立其定量测定方法,能够为进一步提高多血康胶囊及其他藏药复方的质量控制标准提供参考依据。
[1] 曹祯吾.红细胞增多症[M].北京:军事医学科学出版社,1996:8.
[2] 帝玛尔.丹增彭措.晶珠本草[M].上海:上海科学技术出版社,2012:84.
[3] 索朗其美,张 艺,松桂花,等.一种预防或/和治疗红细胞增多症的药物或保健食品组合物:中国,102526656 A[P].2012-07-04.
[4] 伍文彬,赖先荣,索朗其美,等.藏药多血康对家兔血瘀症模型全血黏度及红细胞流变性的影响[J].西藏科技,2009(2):39-40.
[5] 伍文彬,赖先荣,索朗其美,等.多血康对高原红细胞增多症的影响研究[J].中药药理与临床,2009,25(5):93-95.
[6] 冀 静,杨继家,廖 琦,等.藏药余甘子中三种酚酸类成分的HPLC含量测定研究[J].中药药理与临床,2012,3(4):14-16.
[7] 陈毓芳,林海丹,吴宏中,等.高效液相色谱法同时测定保健食品中11种功效成分[J].食品科学,2015,36(8):244-249.
[8] 冯 欣,周 刚,王 茜,等.HPLC法测定藏药五味甘露药浴颗粒中槲皮素、山柰素和盐酸麻黄碱[J].中成药,2015,37(1):120-123.
[9] 季宁平,徐晓秋,傅超美,等.HPLC法同时测定艾附暖宫丸中芍药苷、阿魏酸和川续断皂苷Ⅵ[J].中成药,2015,37(3):534-537.
[10] 田源红,张永萍,李 玮,等.HPLC法同时测定吉祥草中阿魏酸及芦丁[J].中成药,2015,37(3):603-606.
[11] 林 夏,胡军华,崔培超,等.HPLC同时测定大花红景天提取物中没食子酸、红景天苷、酪醇、对香豆酸的含量[J].中国实验方剂学杂志,2013,19(10):102-105.
[12] 杨 洋,苏永文,刘 悦,等.西藏沙棘质量标准研究[J].世界科学技术:中医药现代化,2014,16(1):146-150.
[13] 德 洛,姚 喆,冀 静,等.藏药三果汤散抗氧化有效成分的薄层色谱-生物自显影及HPLC指纹图谱[J].中国实验方剂学杂志,2012,18(12):98-102.
Determ ination of six com ponents in Duoxuekang Capsu Ies by HPLC
HUANG Yu1,2, WANG Yu-jie1*, YANGWen-juan1, ZHANG Yi1, LAIXian-rong1
(1.Gollege of Ethnic Medicine,Ghengdu University of Traditional GhineseMedicine,Ghengdu 611137,Ghina;2.Neo-Green PharmeutiralGo.Ltd.,Ghengdu 611193,Ghina)
AIM To establish a high-performance liquid chromatography(HPLC)method for simultaneously identifying the contents of salidroside,gallic acid,corilagin,quercetin,kaempferol and isorhamnetin in Duoxuekang Capsules(Rhodiolae Grenulatae Radix et Rhizome,Phyllaxthi Fructus,Hippophae Fructus,Zingiber Rhizome).METHODS 70%methanolic extractof Duoxuekang Capsules was performed on a Wondasil C18-WR column(4.6 mm×250 mm,5μm).Themobile phaseⅠ(methanol and 0.2%phosphoric acid solution)was in a gradient elution for the determination of salidroside,gallic acid and corilagin with a detection wavelength setat275 nm.Themobile phaseⅡ(methanol and 0.4%phosphoric acid solution[48:52])was for the determination of quercetin,kaempferol and isorhamnetin ata detection wavelength of370 nm.Their flow ratesweremaintained at1 m L/min at a column temperatures of30℃and a sample injection of 10μL.RESULTS Calibration curves of the six effective constituents revealed a good linear relationship(r≥0.999 7).The average recovery was within the range of 99.1%-101.7%,and RSD value was 0.69%-1.7%.CONCLUSION Based on the detectable active constituents in the blood stream,a simple,specific and good repeatablemethod for the quantitative determination of Duoxuekang Capsules has been established.
Duoxuekang Capsules;salidroside;corilagin;isorhamnetin;high-performance liquid chromatography(HPLC)
R927.2
A
1001-1528(2015)11-2418-05
10.3969/j.issn.1001-1528.2015.11.017
2015-02-27
江西中医药大学2011协同创新开放基金项目 (2011)
黄 宇(1990—),女,硕士,从事藏药药效物质基础研究。E-mail:xiaohuangdoudou12@163.com
*通信作者:王毓杰,男,博士,主要从事中药、民族药药效物质基础及作用机制研究。E-mail:superwangyj@126.com
——题《圣山系-金巅》

