亚铁盐添加的矿物聚合物对Cr(Ⅵ)的解毒与固化研究
陈方明,陈洁渝
1. 湖北大学资源环境学院,湖北 武汉 430062;2. 中国地质大学材料科学与化学工程学院,湖北 武汉 430074
亚铁盐添加的矿物聚合物对Cr(Ⅵ)的解毒与固化研究
陈方明1,陈洁渝2
1. 湖北大学资源环境学院,湖北 武汉 430062;2. 中国地质大学材料科学与化学工程学院,湖北 武汉 430074
中国铬盐生产量及消费量均居世界第一,铬盐生产排放的铬渣量很大,其中Cr(Ⅵ)是一种高毒性物质,是国家重点控制的重金属污染物之一,寻找经济、高效的Cr(Ⅵ)去除方法一直是研究的热点。以煤矸石为原料,以水玻璃和NaOH为碱性激发剂,合成矿物聚合物,用亚铁盐添加的矿物聚合物对Cr(Ⅵ)进行解毒与固化研究,并采用XRD、TEM/EDS、XPS对固化体进行检测。结果发现,当添加的Fe(Ⅱ)与Cr(Ⅵ)摩尔比大于3∶1时,矿物聚合物中总铬浸出的质量浓度小于1 mg·L-1,铬固化率大于99%。以亚铁盐FeSO4·7H2O作还原剂,矿物聚合物对Cr(Ⅵ)的最大固化量为0.8%。随着FeSO4·7H2O和Cr(Ⅵ)添加量按3∶1的摩尔比增加,矿物聚合物的抗压强度减小。XRD检测表明,FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物为非晶质结构。TEM/EDS检测表明,矿物聚合物的非晶质结构中含有Fe和Cr。XPS检测结果证明,矿物聚合物中Fe和Cr分别为Fe(Ⅲ)和Cr(Ⅲ)。亚铁盐添加的矿物聚合物对Cr(Ⅵ)的解毒与固化是基于氧化还原反应。在Fe(Ⅱ)和Cr(Ⅵ)添加的矿物聚合物合成过程中,Fe(Ⅱ)被氧化成了Fe(Ⅲ),Cr(Ⅵ)被还原成了Cr(Ⅲ),随后Fe(Ⅲ)和Cr(Ⅲ)被矿物聚合物中的-OAl(-)(OH)3吸引,并被固定在非晶质结构中。
矿物聚合物;亚铁盐;Cr(Ⅵ);解毒;固化
中国铬盐生产量及消费量均居世界第一。传统的铬盐工业为无机化工与冶金材料交叉的重污染行业,采用高温焙烧—水浸—多级蒸发结晶工艺,铬转化率仅75%,每吨铬盐产品要排放2.5 t高毒性铬渣,其中 Cr(Ⅵ)含量是国家排放标准的近万倍(Wei等,2010)。大量铬渣长期堆存,不但占用大量土地,而且细小粉尘随风飞散,对周围环境和水域造成污染。若遭受雨雪侵淋,Cr(Ⅵ)还会渗透到地下造成江河、湖泊和地下水污染,进而危害生物和人体健康(Jon等,2010)。
Cr(Ⅵ)对环境危害极大,是国家重点控制的重金属污染物之一。现有铬污染控制方法多种多样,归结起来可分为两大类:一类是解毒法;一类是固化法(Shi等,2007;Wu等,2010)。解毒法有化学法、物理法中的吸附法、微波法、生物法等,会留下大量的残渣堆积,若不及时处理,会再次被氧化而产生剧毒(Attia等,2010;梁咏梅等,2007)。固化法可将铬密封在材料中,处于一种厌氧的环境,可弥补解毒法的不足(Liu等,2008;Ji等,2011)。目前,固化法采用的材料主要为水泥,这种方法将铬渣粉碎后加入一定量还原剂,使其中Cr6+还原成 Cr3+,再加入大量的水泥,加水搅拌,随着水泥的水化与凝结硬化过程,铬化合物形成稳定的晶体结构或化学键,并被封闭在固化体中(Zhang等,2008;陈云等,2011)。水泥固化法还可以在制造过程中添加高炉矿渣和还原剂将水溶性Cr(Ⅵ)固定,但由于水泥自身耐酸性较差,难以抑制酸溶性Cr(Ⅵ)的淋滤(Bhattacharya等,2008;Li等,2010)。因此对酸溶性 Cr(Ⅵ)还没有行之有效的处理措施,寻找经济、高效的Cr(Ⅵ)去除方法一直是研究的热点(Zhang等,2007)。本文以煤矸石为原料,以水玻璃和NaOH为碱性激发剂,合成矿物聚合物,用亚铁盐添加的矿物聚合物对Cr(Ⅵ)进行解毒与固化研究,进而探讨矿物聚合物对Cr(Ⅵ)的解毒与固化机理。
1 材料与方法
1.1 实验原料和试剂
实验原料为山西朔州煤矸石,主要由高岭石组成,化学成分如表1。将煤矸石粉磨至10 μm以下,置于马弗炉中,于600 ℃煅烧4 h,得到偏高岭土,室温冷却备用。
工业水玻璃,模数为 3.1~3.4,质量分数为38%~40%。NaOH、K2Cr2O7和FeSO4·7H2O等化学试剂均为市售分析纯。
1.2 矿物聚合物的制备
以偏高岭土、水玻璃和NaOH为原料制备矿物聚合物,质量比为 m(偏高岭土)∶m(水玻璃)∶m(NaOH)=7∶4.5∶1。首先将水玻璃与NaOH混合,搅拌均匀,配成碱性激发剂;然后将偏高岭土分次加入,机械搅拌,同时滴加水至合适的稠度(以能流畅地流动为标准),倒入20 mm×20 mm×20 mm模具成型,60 ℃固化,脱模,用聚乙烯薄膜密封,60 ℃养护1 h。
1.3 亚铁盐添加的矿物聚合物对Cr(Ⅵ)的解毒与固化
还原剂采用亚铁盐 FeSO4·7H2O,实验方案有两种,一种是先用 FeSO4·7H2O将 Cr(Ⅵ)还原成Cr(Ⅲ),再用矿物聚合物对 Cr(Ⅲ)固化;另一种是将FeSO4·7H2O和Cr(Ⅵ)直接加进矿物聚合物的凝胶液中,充分搅拌,在搅拌过程中还原并固化Cr(Ⅵ)。本文采用第二种实验方案。
按7∶4.5∶1的质量比称取偏高岭土、水玻璃和NaOH,先将水玻璃和NaOH混合搅拌,配成凝胶液;然后将偏高岭土分次加入凝胶液中,充分搅拌,均匀混合;再加入FeSO4·7H2O和K2Cr2O7溶液,充分搅拌,均匀混合后倒入20 mm×20 mm×20 mm模具成型,60 ℃固化,脱模,用聚乙烯薄膜密封,60 ℃养护1 h。
1.4 铬的浸出试验
固化后的矿物聚合物粉碎至5 mm以下,采用美国EPA毒性特征浸出程序(Toxicity Characteristic Leaching Procedure,简称TCLP)对粉碎的固化体进行浸取,浸取液为0.1 mol·L-1的醋酸溶液,固液比为1∶20(质量比),震荡时间为(18±2) h,过滤,采用火焰原子吸收法(Flame Atomic Absorption Method,简称FAAM)检测滤液中铬的含量。铬固化率计算公式为:
S=(m-C×V)/m×100%
式中:S为铬固化率,C为滤液中铬浓度,V为滤液体积,m为总Cr的添加量。

表1 煤矸石的化学成分Table 1 Chemical composition of gangue
2 结果与讨论
2.1 FeSO4·7H2O和Cr(Ⅵ)添加量对固化率的影响
FeSO4·7H2O添加量为1.0%,以Cr(Ⅵ)添加量为变量进行试验,浸出液中总铬的质量浓度及矿物聚合物对铬的固化率如图1和图2。可以看出,随着Cr(Ⅵ)添加量的增加,总铬浸出的质量浓度明显增大,固化率大幅度降低。当Cr(Ⅵ)添加量≤0.05%时,总铬浸出的质量浓度小于 1 mg·L-1,远低于TCLP检测阈值 5 mg·L-1,固化率大于 99%;当Cr(Ⅵ)添加量>0.05%时,总铬浸出的质量浓度增大,超出TCLP检测阈值。即当FeSO4·7H2O∶Cr(Ⅵ)质量比≥20∶1(或Fe(Ⅱ)∶Cr(Ⅵ)摩尔比≥3∶1)时,固化效果较好。

图1 Cr(Ⅵ)添加量对总铬浸出质量浓度的影响Fig. 1 The effect of Cr(Ⅵ) amount to leaching concentration of chromium

图2 Cr(Ⅵ)添加量对铬固化率的影响Fig. 2 The effect of Cr(Ⅵ) amount to fixation rate of chromium
按照FeSO4·7H2O与Cr(Ⅵ)质量比20∶1(或者Fe(Ⅱ)∶Cr(Ⅵ)摩尔比3∶1),同比例放大进行试验,试验结果如表2。从表2可见,随着矿物聚合物中Cr(Ⅵ)添加量从0.05%增加到0.8%,FeSO4·7H2O添加量从1.0%增加到16.0%,矿物聚合物中总铬浸出的质量浓度均小于1 mg·L-1,固化率均大于99%。当Cr(Ⅵ)添加量增加到1.0%,FeSO4·7H2O添加量增加到20.0%时,凝胶体失去胶凝活性,不能固化。因此,以亚铁盐FeSO4·7H2O作还原剂,矿物聚合物对Cr(Ⅵ)的最大固化量为0.8%。
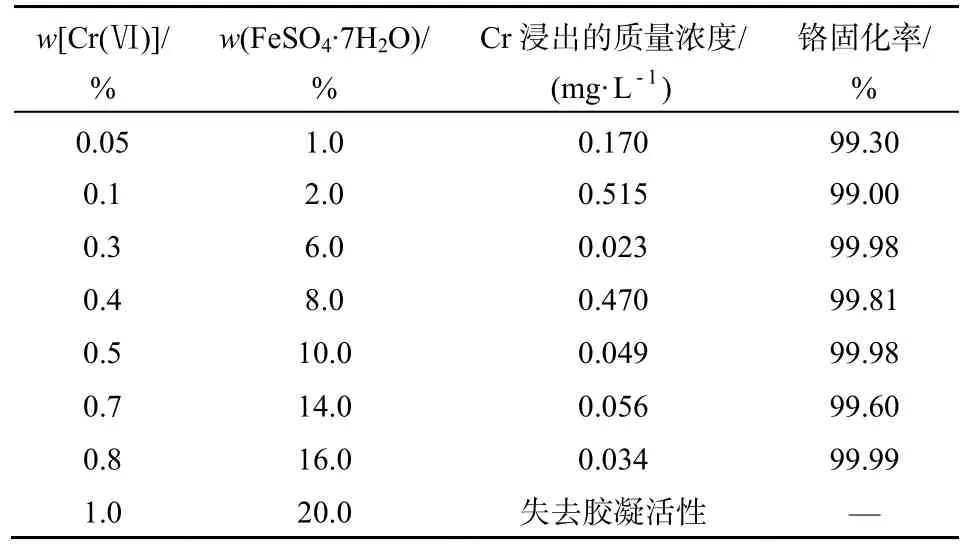
表2 FeSO4·7H2O与Cr(Ⅵ)添加量对固化率的影响Table 2 The effect of FeSO4·7H2O and Cr(Ⅵ) amount to fixation of chromium
2.2 FeSO4·7H2O和 Cr(Ⅵ)添加量对抗压强度的影响
抗压强度测试采用山东济南 WE-50万能试验机(最大量程为50 KN),取相同条件下3个检测结果的平均值。图3为Cr(Ⅵ)添加量与矿物聚合物抗压强度的关系曲线,当 FeSO4·7H2O添加量为1.0%,Cr(Ⅵ)添加量从0.025%增大到0.2%时,矿物聚合物的抗压强度没有明显的变化规律,变化率<5%。

图3 Cr(Ⅵ)添加量对矿物聚合物抗压强度的影响Fig. 3 The effect of Cr(Ⅵ) amount to compressive strength of geopolymers
表3为FeSO4·7H2O与Cr(Ⅵ))按质量比20∶1(或者Fe(Ⅱ)∶Cr(Ⅵ)摩尔比3∶1)同比例放大所得矿物聚合物的抗压强度,随着矿物聚合物中Cr(Ⅵ)添加量从0.05%增加到0.8%,FeSO4·7H2O添加量从1.0%增加到16.0%,矿物聚合物抗压强度大幅度降低,从58.23 MPa降低到20.33 MPa,降幅为65%。
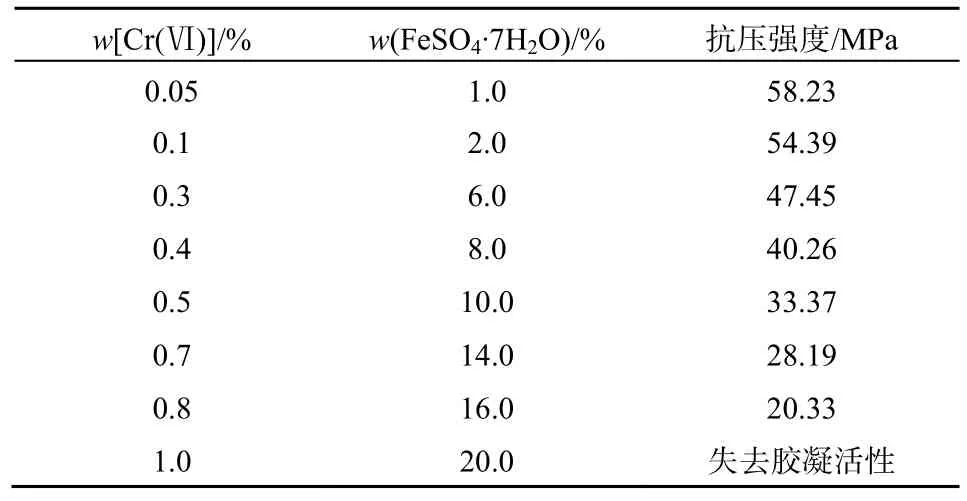
表3 FeSO4·7H2O与Cr(Ⅵ)添加量对抗压强度的影响Table 3 The effect of FeSO4·7H2O and Cr(Ⅵ) amount to compressive strength
2.3 FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物的表征
图4为矿物聚合物及FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物的XRD图谱,其中谱线1为矿物聚合物的XRD图谱,谱线2为FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物的XRD图谱。从图谱可以看出,矿物聚合物为非晶质结构,FeSO4·7H2O和 Cr(Ⅵ)添加的矿物聚合物亦为非晶质结构,即FeSO4·7H2O和Cr(Ⅵ)的添加并未形成新的晶相。

图4 矿物聚合物及FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物的XRD图谱Fig. 4 XRD pattern of geopolymers and geopolymers added by FeSO4·7H2O and Cr(Ⅵ)
为了检测矿物聚合物中是否存在 Cr或其他元素的结晶质,采用透射电子显微镜(TEM)对FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物进行检测,加速电压120 kV,同时用EDAX9100型X射线能谱仪对检测范围进行能谱分析,结果如图 5。在透射电镜下,矿物聚合物为非晶质结构,非晶质呈均匀细小的团聚体。非晶质区域能谱分析显示,主要元素为 Na、Al、Si、Cr和 Fe。其中 Na、Al、Si为矿物聚合物的主要元素,Cr、Fe为以K2Cr2O7和FeSO4·7H2O形式添加的元素,其衍射峰强度为Fe>Cr。

图5 FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物的TEM/EDS分析Fig. 5 TEM/EDS analysis results of geopolymers added by FeSO4·7H2O and Cr(Ⅵ)
图6为FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物的Cr2p和Fe2p的XPS图谱,在矿物聚合物的XPS图谱中出现了Cr和Fe,Cr2p电子结合能为576.07eV,判断为Cr(Ⅲ);Fe2p电子结合能为710.27eV,判断为Fe(Ⅲ)。这说明FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物在合成过程中,Cr(Ⅵ)被还原成了Cr(Ⅲ),而Fe(Ⅱ)被氧化成了Fe(Ⅲ),Cr(Ⅲ)和 Fe(Ⅲ)存在于矿物聚合物的非晶质结构之中。
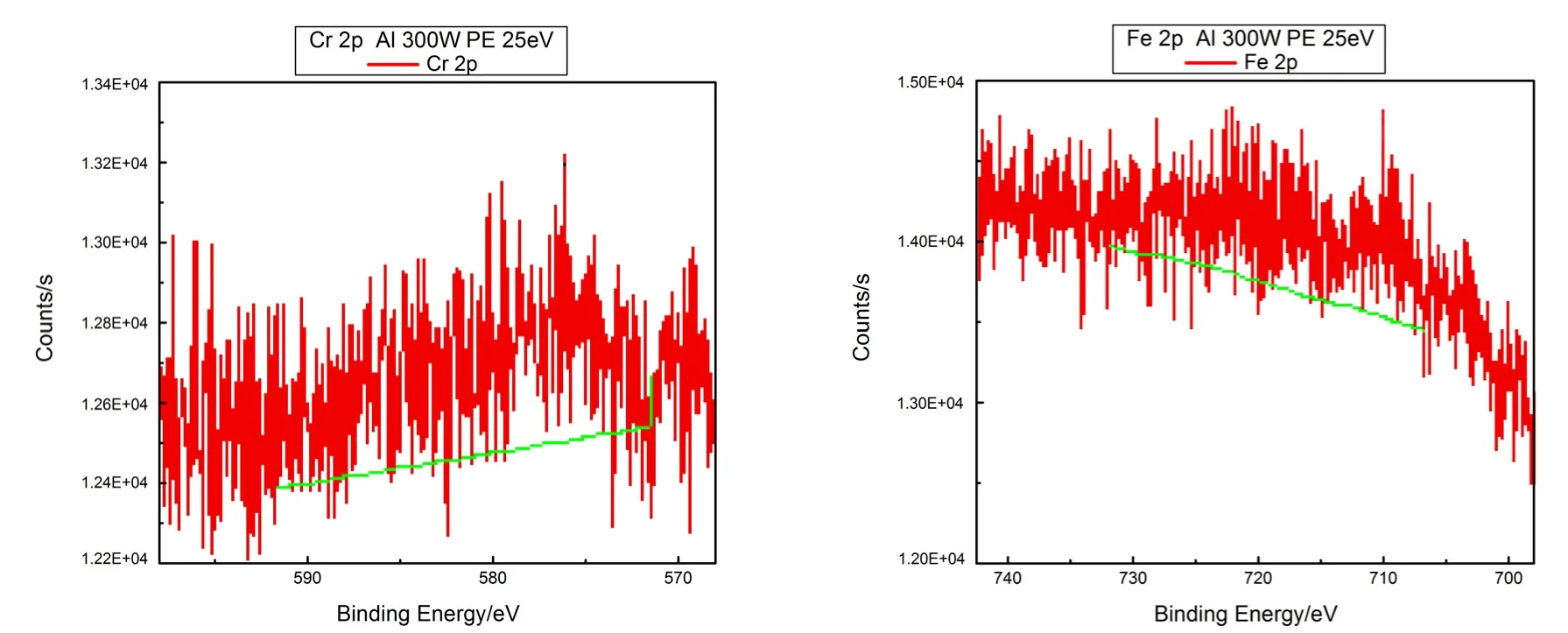
图6 FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物的Cr2p和Fe2p的XPS图谱Fig. 6 XPS pattern of Cr2p and Fe2p of geopolymers added by FeSO4·7H2O and Cr(Ⅵ)
2.4 解毒与固化机理
亚铁盐FeSO4·7H2O的添加促进了矿物聚合物对Cr(Ⅵ)的解毒与固化。在矿物聚合物合成过程中,少量水使 Fe2+、Cr(Ⅵ)以离子形式接触,具有还原性的 Fe2+首先将 Cr(Ⅵ)(Cr2O72-)还原成 Cr3+,同时Fe2+被氧化成Fe3+,然后Cr3+与Fe3+同时进入非晶质结构中,与带负电荷的[AlO4]四面体结合,中和负电荷,并随着矿物聚合物的固化而被固定。
以 FeSO4·7H2O作还原剂,当 Fe(Ⅱ)∶Cr(Ⅵ)最佳摩尔比为3∶1时,氧化还原反应式为:
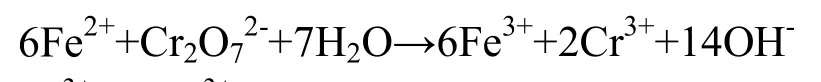
Fe3+和 Cr3+形成后,根据矿物聚合物的合成步骤,首先在碱作用下形成4次配位的铝:

在此产生带负电荷的-OAl(-)(OH)3,当无其他阳离子时,Na+填充其中,中和负电荷;当带正电荷的Fe3+和Cr3+进入其中时,同样会被负电荷吸引:

4次配位的铝可结合 Na+,也可以结合 Fe3+和Cr3+形成混合相,所以在TEM/EDS和XPS检测中均发现了Fe和Cr。
在碱的进一步作用下,混合相还可以形成带Fe3+和Cr3+的正铝硅酸盐:
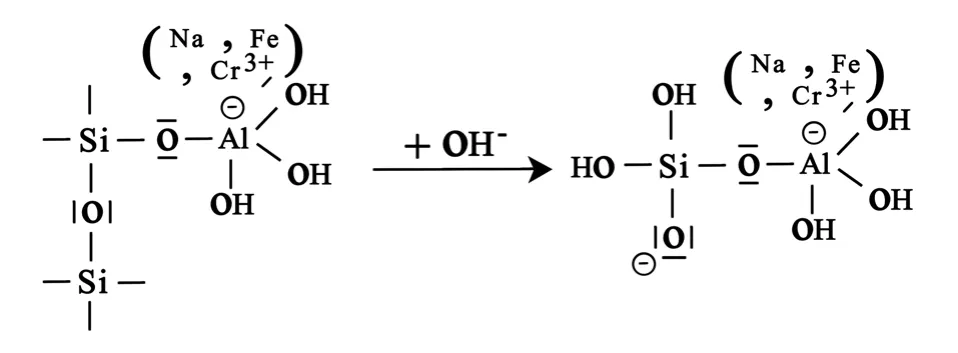
带 Fe3+和 Cr3+的正铝硅酸盐分子发生缩聚反应,Si-ONa与Al-OH缩合,形成带Fe3+和Cr3+的聚铝硅酸盐,同时生成NaOH。NaOH继续参加反应,使缩聚反应继续进行,生成-Si-O-Al(Cr,Fe)-聚铝硅酸盐网络状结构。

3 结论
1)当 Fe(Ⅱ)∶Cr(Ⅵ)摩尔比≥3∶1时,FeSO4·7H2O和 Cr(Ⅵ)添加的矿物聚合物中总铬浸出的质量浓度小于1 mg·L-1,固化率大于99%。以FeSO4·7H2O作还原剂,矿物聚合物对Cr(Ⅵ)的最大固化量为0.8%。
2)当FeSO4·7H2O添加量为1.0%,Cr(Ⅵ)添加量从0.025%增加到0.2%时,矿物聚合物的抗压强度较稳定。随着FeSO4·7H2O与Cr(Ⅵ)按质量比20∶1(或摩尔比 3∶1)同比例放大,矿物聚合物的抗压强度降低。当 Cr(Ⅵ)增加到 1.0%,FeSO4·7H2O增加到20.0%时,矿物聚合物失去胶凝活性,不能固化。
3)XRD检测表明,FeSO4·7H2O和Cr(Ⅵ)添加的矿物聚合物为非晶质结构。TEM/EDS检测表明,矿物聚合物的非晶质结构中含有Fe和Cr。XPS检测结果证明,矿物聚合物中Fe和Cr分别为Fe(Ⅲ)和Cr(Ⅲ)。
4)在合成过程中,Fe(Ⅱ)和Cr(Ⅵ)添加的矿物聚合物发生了氧化还原反应,Fe(Ⅱ)被氧化成了Fe(Ⅲ),Cr(Ⅵ)被还原成了 Cr(Ⅲ),随后 Fe(Ⅲ)和Cr(Ⅲ)被矿物聚合物中的-OAl(-)(OH)3吸引,并被固定在非晶质结构中。
ATTIA A A, KHEDR S A, ELKHOLY S A. 2010. Adsorption of chromium ion (Ⅵ) by acid activated carbon[J]. Brazilian Journal of Chemical Engineering, 27(1): 183-193.
BHATTACHARYA A K, NAIYA T K, MANDAL S N, et al. 2008. Adsorption,kinetics and equilibrium studies on removal of Cr(Ⅵ) from aqueous solutions using different low-cost adsorbents[J]. Chemical Engineering Journal, 137: 529-541.
JI B S, BEDABRATA S, GOPAl D. 2011. Efficient removal of chromate and arsenate from individual and mixed system by malachite nanoparticles[J]. Journal of Hazardous Materials, 186: 575-582.
JON R, BRUCE A. 2010. Reduction and immobilization of chromium(VI) by iron(II)-treated faujasite[J]. Journal of Hazardous Materials, 174: 167-174.
LIU S F, WANG P M, LI ZONG J. 2008. FTIR and XPS study of immobilization of chromium with fly ash based geopolymers[J]. Spectroscopy and Spectral Analysi, 28(1): 67-71.
LI Y, YUE Q Y, GAO B Y. 2010. Effect of humic acid on the Cr(Ⅵ) adsorption onto Kaolin[J]. Applied Clay Science, 48: 481-484.
SHI Y M, DU XINGHONG, MENG QINGJIA, et al. 2007. Reaction process of chromium slag reduced by industrial waste in solid phase[J]. Journal of Iron and Steel Research, 14(1): 12-15.
WEI Y L, HE H F, PENG Y S, et al. 2010. Thermal detoxification and bloating of chromium(VI) with bentonite [J]. Nuclear Instruments and Methods in Physics Research, 619: 108-111.
WU C L, ZHANG H, HE P J, et al. 2010. Thermal stabilization of chromium slag by sewage sludge: Effects of sludge quantity and temperature[J]. Journal of Environmental Sciences, 22(7): 1110-1115.
ZHANG Y S, SUN W, CHEN Q L, et al. 2007. Synthesis and heavy metal immobilization behaviors of slag based geopolymer[J]. Journal of Hazardous Materials, 143: 206-213.
ZHANG J G, JOHN L, FENG D, et al. 2008. The role of sulfide in the immobilization of Cr(VI) in fly ash geopolymers[J]. Cement and Concrete Research, 38: 681-688.
陈云, 于永鲜, 张金利, 等. 2011. 铁氧化物改性黏土对Cr(Ⅵ)的吸附性能研究[J]. 环境科学学报, 31(5): 905-911.
梁咏梅, 何利华, 仇荣亮, 等. 2007. 焙烧温度对铁覆膜砂 IOCS吸附Cr(Ⅵ)的影响[J]. 环境科学学报, 27(11): 1887-1891.
Detoxication and Immobilization of Chromium (VI) by Geopolymers Added by Ferrous Salts
CHEN Fangming1, CHEN Jieyu2
1. School of Resources and Environment, Hubei University, Wuhan 430062, China; 2. Institute of Materials Science and Chemical Engineering, China University of Geosciences, Wuhan 430074, China
Chromate production amount and consumption amount of our country are first in the world. The emission amount of Chromium residue is huge. It is well known that Cr(Ⅵ) is a highly toxic waste and one of the heavy metal pollutants controlled strictly by the country. So it is a research hot spot to look for a method in order to removal Cr(Ⅵ) economically and efficiently. In this paper, geopolymers have been synthesized using gangue as raw materials, water glass and sodium hydroxide as alkaline excitated agents. The geopolymers added by ferrous salts have been researched on detoxification and immobilization of Cr(Ⅵ). Then curing geopolymers have been tested by XRD, TEM/EDS and XPS. When the molar ratio of Fe(Ⅱ) and Cr(Ⅵ) is more than 3∶1, the leaching concentrations of total chromium are less than 1 mg·L-1and the fixation rates of chromium are above 99%. The best Cr(Ⅵ) fixation capacity of geopolymers is 0.8% when ferrous salt FeSO4·7H2O is used as reducing agent. The compressive strength of geopolymers decreases when the amount of FeSO4·7H2O and Cr(Ⅵ) increases accordinghe molar ratio of 3∶1. The XRD testing results show that geopolymers added by FeSO4·7H2O and Cr(Ⅵ) is non-crystaline structures. The TEM/EDS testing results show that the non-crystaline structures contain Fe and Cr. The XPS testing results show that the Fe is Fe (Ⅲ) and the Cr is Cr (Ⅲ). The mechanism of detoxification and immobilization of Cr(Ⅵ) is oxidation- deoxidation reaction. Fe(Ⅱ) has been oxidized to Fe(Ⅲ) and Cr(Ⅵ) has been deoxidized to Cr(Ⅲ) during the synthesis of the geopolymers added by FeSO4·7H2O and Cr(Ⅵ). Then Fe(Ⅲ) and Cr(Ⅲ) have been attracted by -OAl(-)(OH)3in the geopolymers and fixated in the non-crystaline structures.
Geopolymers; ferrous salts; chromium(VI); detoxification; immobilization
10.16258/j.cnki.1674-5906.2015.02.020
X705
A
1674-5906(2015)02-0310-06
陈方明,陈洁渝. 亚铁盐添加的矿物聚合物对Cr(Ⅵ)的解毒与固化研究[J]. 生态环境学报, 2015, 24(2): 310-315.
CHEN Fangming, CHEN Jieyu. Detoxication and Immobilization of Chromium (VI) by Geopolymers Added by Ferrous Salts [J]. Ecology and Environmental Sciences, 2015, 24(2): 310-315.
国家自然科学基金项目(41102025);中国地质大学生物地质与环境地质国家重点实验室开放基金(GBL21310)
陈方明(1970年生),男,副教授,博士,主要从事环境矿物学的教学和科研工作。E-mail:cfm@hubu.edu.cn或785398029@qq.com
2015-01-19

