高黏度与低黏度骨水泥在椎体成形术中应用的临床对比研究*
陈学忠,董 玮,奚江明,孟繁胜,朱肖奇
1.深圳市宝安区石岩人民医院 骨科(深圳518108);2.深圳市宝安区人民医院 脊柱与骨关节外科(深圳518101)
近年来,随着微创外科的发展以及新方法、新观念的涌现,出现了微创脊柱外科领域的新技术——经皮椎体成形术(percutaneous vertebroplasty,PVP)。PVP可有效解决患者骨折引起的疼痛和畸形,提高生活质量,是治疗骨质疏松性椎体压缩性骨折最成功的手术方法之一[1-2]。但是,术后骨水泥渗漏是PVP技术应用中困扰骨科医生的难题之一。据报道[3-4],骨水泥渗漏高达30%~70%。少量的骨水泥渗漏大多不会产生临床表现,但若渗漏到大血管部或神经根部,会造成脊髓压迫、神经损伤、血管热损伤和肺栓塞等严重并发症。目前,对于如何有效降低或避免骨水泥渗漏在学术界尚未达成共识[5]。除了骨水泥渗漏外,PVP术后发生手术椎体或非手术椎体再骨折的现象也引起了临床医生的重视。其中,以邻近椎体骨折(adjacent vertebral fracture,AVF)最为多见,其发生机制尚不明确,研究报道的发生率(8%~52%)差异也很大[6],在一定程度上说明了其相关因素的复杂性,而通过应用新型骨水泥能否降低AVF的风险有待进一步研究。
一些学者[7-9]报道,高黏度骨水泥在治疗骨质疏松性椎体压缩性骨折中均取得了较为满意的临床疗效,术后疼痛缓解率与传统的PVP比较,差异无统计学意义(P>0.05),但骨水泥渗漏发生率较传统的PVP明显降低。李春海等[10]研究表明,在应用高黏度骨水泥治疗椎体压缩性骨折31例中,2例发生椎体旁骨水泥渗漏,渗漏率仅为6.5%。尽管高黏度骨水泥具有潜在的应用前景,但目前相关研究较缺乏,尚需更多的临床应用研究和总结以进一步明确其有效性。因此,本研究回顾性分析近年来通过PVP治疗胸腰椎骨质疏松性压缩性骨折患者的临床数据,比较分析注入高黏度与低黏度骨水泥治疗骨质疏松性椎体压缩性骨折的临床疗效,现报道如下。
1 资料与方法
1.1 临床资料
选取2009年1月至2014年8月深圳市宝安区石岩人民医院骨科收治的椎体压缩性骨折患者40例,其中,男18例,女22例,年龄59~88岁。根据治疗措施,将患者分为低黏度骨水泥组(n=20)和高黏度骨水泥组(n=20)。高黏度骨水泥组随访时间为0.8~3.0年,低黏度骨水泥组随访时间为1.0~3.0年。所有患者均存在腰背部疼痛、不能站立、翻身疼痛、平卧时疼痛缓解、搬动时疼痛加重,查体胸椎或腰椎骨折部位压痛和叩击痛明显。纳入标准:1)经国际公认的影像学(X线片、CT和MRI)以及临床检查确诊为椎体压缩骨折;2)经骨密度(bone mineral density,BMD)检查确诊骨质疏松,BMD≤2.5SD,提示有骨质疏松改变;3)椎体压缩骨折急性疼痛(<3个月)明显;4)慢性疼痛(>3个月)伴骨折不愈合;5)胸椎及腰椎骨折均无脊髓和神经根受损的症状和体征。排除标准:1)凝血功能障碍,有出血倾向者;2)伴有脊髓损伤或马尾神经损伤等神经功能损伤者;3)伴有神经受压或椎管狭窄、脊柱结核、脊髓肿瘤等病变或风湿性、类风湿性关节炎的患者;4)伴有高血压、糖尿病及心、脑、肺、肝、肾等重大疾病者;5)伴有恶性疾病或骨转移性疾病;6)不能根据本研究要求进行相关检查者;7)随访期间不合作者以及失访者。本研究获得了医院伦理委员会批准,入选患者均知情同意签字。两组患者随访时间等临床基本资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 手术方法
患者在脊柱外科四点式支架上取俯卧位并使胸腹部悬空,头架支撑固定,在C型臂X线机透视下明确进针点并予以标记,常规皮肤消毒铺无菌巾,1%利多卡因于病椎处皮肤皮下局部麻醉,透视下将穿刺针插入至椎弓根外上缘并确定进针方向,继续缓慢进针至椎体前中1/3处,C型臂X线机透视位置满意。调好骨水泥,在持续C型臂X线机透视下注入至椎体中,骨水泥逐渐散开。术中取椎体内骨组织进行病理检查,以排除肿瘤导致的病理性骨折。
两组骨水泥的使用均根据说明书进行。患者术后取平卧位并密切观察情况,术后第1小时内每15min检查血压、心率以及氧饱和度。针对性治疗骨质疏松的患者,根据其恢复情况指导腰背肌肉功能锻炼,并帮助其在腰椎支具的保护下进行临床行走。术后1d行X线等影像学检查。
1.3 观测指标
1)骨水泥分布与渗漏评估:放射科医生对患者术后第1天的脊柱X线片以及CT检查进行读片,观察骨水泥是否同时接触上下终板以及偏一侧分布;骨水泥渗漏包括静脉渗漏、椎旁渗漏和椎间盘渗漏。2)疼痛缓解评估:采用视觉模拟评分法(VAS)对术前和末次随访进行评分。3)脊柱功能改善情况评估:采用Oswestry功能障碍指数问卷表(ODI评分)对术前和末次随访进行评分。4)伤椎高度恢复情况评估:在椎体侧位X线片上测量Cobb角以评估病椎前缘高度和后凸畸形恢复情况。5)术后骨水泥肺栓塞发生率。6)X线及CT复查评估术后手术椎体或非手术椎体再骨折的情况。
1.4 统计学方法
应用SPSS 17.0统计软件进行分析,所有数据采用均数±标准差(±s)表示。VAS评分、ODI评分和Cobb角比较采用t检验,渗漏率、骨水泥肺栓塞发生率以及邻近椎体骨折发生率比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组骨水泥注入量比较
所有患者均顺利完成手术。高黏度组骨水泥注入量为2.0~5.0mL,平均(2.7±0.8)mL,低黏度组骨水泥注入量为2.0~5.0mL,平均(2.6±0.7)mL,两组骨水泥注入量比较,差异无统计学意义(P>0.05)。
2.2 两组患者VAS评分、ODI评分以及Cobb角的比较
两组患者术前VAS评分、ODI评分以及Cobb角比较,差异无统计学意义(P>0.05)。末次随访高黏度骨水泥组的VAS评分、ODI评分以及Cobb角,与低黏度骨水泥组比较,差异有统计学意义(P<0.05)(表1)。
表1 两组患者VAS评分、ODI评分和Cobb角的比较(n=20,±s)
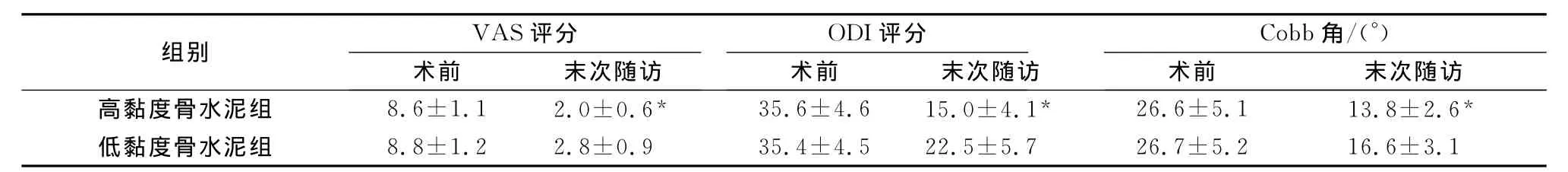
表1 两组患者VAS评分、ODI评分和Cobb角的比较(n=20,±s)
注:与低黏度骨水泥组比较,*P<0.05
组别 VAS评分ODI评分Cobb角/(°)术前 末次随访高黏度骨水泥组 8.6±1.1 2.0±0.6* 35.6±4.6 15.0±4.1* 26.6±5.1 13.8±2.6术前 末次随访 术前 末次随访*6.6±3.1低黏度骨水泥组 8.8±1.2 2.8±0.9 35.4±4.5 22.5±5.7 26.7±5.2 1
2.3 两组骨水泥渗漏率及椎体内骨水泥分布的比较
高黏度组术后CT未发现骨水泥静脉渗漏;术后X线片发现1个椎体椎间盘渗漏,1个椎体旁渗漏,但无临床表现;骨水泥偏向一侧分布者有3个椎体渗漏,骨水泥未同时接触上下终板者有5个椎体。低黏度组术后CT未发现静脉渗漏;术后X线片发现1个椎间盘渗漏,3个椎体旁渗漏,1个椎体椎管内渗漏,除椎管内渗漏病例仍有轻度腰背痛外,其他均无明显临床表现;骨水泥偏向一侧分布者有6个椎体渗漏,骨水泥未同时接触上下终板者有9个椎体渗漏。两组患者术后椎间盘渗漏率比较,差异无统计学意义(P>0.05);而静脉渗漏率、椎旁渗漏率、椎管内渗漏率及合计骨水泥渗漏率比较,差异有统计学意义(P<0.05)。高黏度骨水泥组中的骨水泥未同时接触上下终板的发生率及偏向一侧分布的发生率,与低黏度骨水泥组比较,差异有统计学意义(P<0.05),提示高黏度骨水泥组中椎体内骨水泥的分布更均匀,优于低黏度骨水泥组(表2)。

表2 两组骨水泥渗漏情况比较[n(%)]
2.4 两组术后手术椎体或非手术椎体再骨折的发生率与骨水泥肺栓塞的发生率比较
两组术后随访均无手术椎体再骨折发生,而高黏度骨水泥组中,仅有1例高龄重度骨质疏松性椎体压缩性骨折(T12)患者,术后次日下地即发生远隔椎体(L4)骨折;低黏度骨水泥组中,则有1例患者术后发生邻近椎体骨折。两组手术椎体或非手术椎体再骨折的发生率比较,差异无统计学意义(P>0.05)。两组患者术后均无骨水泥肺栓塞情况发生。
3 讨论
骨质疏松症已成为严重危害老年人健康的一种常见疾病[11]。在全球范围内,1名妇女一生中发生骨质疏松性骨折的危险性为30%~40%。60岁以上者骨质疏松发生率约60%,其中,约80%为女性患者。我国是骨质疏松症的高发病国家之一,据2002年统计,骨质疏松患者近820万,占总人口7%[12]。有研究[13]表明,40%骨质疏松人群会经历骨质疏松相关椎体骨折。随着人口老龄化的增加,由骨质疏松引起的椎体压缩性骨折患者逐渐增加,尤其是绝经后的老年女性。统计表明,70岁以上老年人中,约20%患有椎体压缩性骨折,这些患者常产生剧烈的腰背痛、后凸畸形、丧失劳动力甚至生活自理能力,生活质量明显下降[14-16]。骨折为骨质疏松症的主要严重并发症,骨质疏松性椎体压缩性骨折是其中之一[17-18]。
PVP是目前临床上常用的手术治疗措施,但是骨水泥渗漏是其所面临的难题之一。有研究[19-20]报道,与高黏度骨水泥比较,低黏度骨水泥的椎旁渗漏与静脉渗漏发生率高。低黏度骨水泥凝固时间较短,操作不方便,注入时容易出现渗漏,并随静脉扩散,可能导致肺栓塞,其聚合产热会对周围组织造成热损伤,尤其是神经根和脊髓,同时也会损伤椎体内的骨细胞,影响骨质愈合。
有研究发现,骨水泥渗漏的主要影响因素是骨水泥黏度,高黏度骨水泥能显著降低术后渗漏率。Habib等[19]研究显示,与低黏度骨水泥比较,高黏度骨水泥在椎体内分布更均匀,这可能也是高黏度骨水泥渗漏率明显降低的重要原因之一。Bhatia等[21]报道,高黏度骨水泥的静脉渗漏率显著降低,且在PVP术中注射高黏度骨水泥时间较短,并不增加手术步骤。本研究结果显示,高黏度骨水泥组术后渗漏率明显低于低黏度骨水泥组,这可能是因为高黏度骨水泥是在低黏度骨水泥的基础上改进的,改善了骨水泥混合过程中的液态期,因此降低了渗漏以及其它并发症的发生率,提高了PVP的安全;高黏度骨水泥组末次随访的VAS评分、ODI评分和Cobb角明显低于低黏度骨水泥组,这是由于高黏度骨水泥具有瞬间高黏度,可注射时间长,凝固温度低以及低聚温度等特点,减少了对周围组织的不可逆热损伤及神经损伤。
然而,本研究中,高黏度骨水泥组与低黏度骨水泥组术后的手术椎体或非手术椎体再骨折发生率比较,差异无统计学意义(P>0.05),可能是因为PVP术后发生手术椎体再骨折或非手术椎体新发骨折的原因非常复杂。范顺武等[22]在文献综述中总结认为,PVP术后手术椎体再骨折的危险因素主要是手术椎体骨坏死、椎体内裂隙样变、无骨水泥区、椎体高度恢复过度及脊柱后凸不足;而非手术椎体再骨折的危险因素主要是骨密度低、椎间隙骨水泥渗漏、体质量指数低、椎体高度纠正过度、年龄以及药物治疗。尽管,目前并无研究表明高黏度骨水泥能显著降低PVP术后手术椎体或非手术椎体再骨折的发生率,但笔者认为,由于高黏度骨水泥能明显降低术后渗漏率,其在椎体内分布更均匀并具有足够的力学强度,因此能更好地恢复椎体的负载能力。若能在术前对患者骨质疏松严重程度进行充分评估的基础上,进一步规范高黏度骨水泥的使用及PVP手术中的操作,并在围手术期及术后予以规范的抗骨质疏松药物治疗,因人而异执行术后卧床时间及下地活动程度,将有可能在一定程度上降低PVP术后椎体再骨折发生风险。
综上所述,高黏度骨水泥能够显著降低PVP术后的骨水泥渗漏率,其在PVP治疗骨质疏松性椎体压缩性骨折的效果方面优于低黏度骨水泥。因此,采用高黏度骨水泥的PVP手术可望成为治疗骨质疏松性胸腰椎压缩性骨折更有效、更安全的方法。
[1]刘文贵,吕锦瑜,孙建华,等.PVP与保守方法治疗骨质疏松性胸腰椎椎体压缩骨折的疗效比较[J].中国脊柱脊髓杂志,2012,22(10):914-918.
[2]Evalls AJ,Jensen ME,Kip KE,etal.Vertebral compression fractures:pain reduction and improvement in functional mobility after percutaneous polymethylmethacrylate vertebroplasty retrospective report of 245cases [J].Radiology,2003,226(2):366-372.
[3]潘永谦,李健,杨波,等.经皮椎体成形术治疗不同程度骨质疏松椎体压缩性骨折的疗效分析[J].中华创伤骨科杂志,2012,14(3):220-224.
[4]Venmans A,Klazen CA,van Rooij WJ,etal.Postprocedural CT for perivertebral cement leakage in percutaneous vertebroplasty is not necessary:results from VERTOS Ⅱ[J].Neuroradiology,2011,53(1):19-22.
[5]潘俊,杨惠林,孟斌,等.经皮椎体成形术及椎体后凸成形术骨水泥的研究进展[J].中国脊柱脊髓杂志,2012,22(1):81-84.
[6]Lee KA,Hong SJ,Lee S,etal.Analsysis of adjacent fracture after percutaneous vertebroplasty:does intradiscal cement leakage really increase the risk of adjacent vertebral fracture[J].Skeletal Radiol,2011,40(12):1537-1542.
[7]陈晓东,易小波,王洪,等.高粘度骨水泥治疗胸腰椎骨质疏松性轻度爆裂性骨折疗效观察[J].中国骨与关节损伤杂志,2010,25(2):134-135.
[8]Anselmetti GC,Zoarski G,Manca A,etal.Percutaneous vertebroplasty and bone cement leakage:clinical experience with a new high-viscosity bone cement and delivery system for vertebral augmentation in benign and malignant compression fractures[J].Cardiovasc Intervent Radiol,2008,31(5):937-947.
[9]李波,王群波,余雨,等.Confi dence高黏度骨水泥椎体成形系统结合体位复位治疗急性重度骨质疏松性椎体压缩骨折[J].中国修复重建外科杂志,2011,25(3):307-310.
[10]李春海,刘尚礼,叶伟,等.高黏度骨水泥在经皮椎体成形术中的应用[J].中华骨科杂志,2007,27(4):259-260.
[11]Legroux-Gérot I,Lormeau C,Boutry N,etal.Long-term follow-up of vertebralosteoporotic fractures treated by percutaneous vertebroplasty[J].Clin Rheumatol,2004,23(4):310-317.
[12]Nakano M,Hirano N,Matsuura K,etal.Percutaneous transpedicular vertebroplasty with calcium phosphate cement in the treatment of osteoporotic vertebral compression and burst fractures[J].J Neurosurg,2002,97(3):287-293.
[13]Rao RD,Singrakhia MD.Painful osteoporotic vertebral fracture.Pathogenesis,evaluation and roles of vertebroplasty and kyphoplasty in its management[J].J Bone Joint Surg:Am,2003,85(10):2010-2022.
[14]LeCeors RZ.Properties of osteoeonductive biomateirla:clacium phosphates[J].Clin Orthop Relat Res,2002(395):81-98.
[15]Laredo JD,Hamze B.Complications of percutaneous verte roplasty and their Prevention[J].Semin Ultrasound CT MR,2005,26(2):65-80.
[16]刘尚礼,郑召民,吕维加,等.注射性锶羟磷灰石在椎体成形术中的临床应用[J].中华骨科杂志,2004,24(11):653-656.
[17]Ha KY,Lee JS,Kim KW,etal.Percutaneous vertebroplasty for vetebral compression fractures with and without intravenebral clefts[J].J Bone Joint Surg(Br),2006,88(5):629-633.
[18]Singh AK,Pilgram TK,Gilula LA.Osteoporotic compression fractures:outcomes after single versus multiple-level percutaneous vertebroplasty[J].Radiology,2006,238(1):211-220.
[19]Habib M,Serhan H,Marchek C.Cement leakage and filling pattern study of low viscous vertebroplastic versus high viscous confidence cement[J].SAS J,2010,4(1):26-33.
[20]Baroud G,Crookshank M,Bohner M.High-viscosity cement significantly enhances uniformity of cement filling in vertebroplasty:an experimental model and study on cement leakage[J].Spine,2006,31(22):2562-2568.
[21]Bhatia C,Barzilay Y,Krishna M,etal.Cement leakage in percutaneous vertebroplasty:effect of preinjection gelfoam embolization[J].Spine,2006,31(8):915-919.
[22]范顺武,万双林,马彦.骨质疏松性骨折椎体成形术后再骨折与新发椎体的相关问题[J].中华骨科杂志,2014,34(1):86-91.

