重组人鼠嵌合抗CD20单克隆抗体免疫原性检测方法的建立
孟庆芳 ,马志强,陈知航,李丽,刘运龙,单成启,钱小红,程远国
1.北京理工大学 生命学院,北京 100081;2.军事医学科学院 微生物流行病研究所,北京 100071;3.军事医学科学院 放射医学研究所,国家蛋白质组学重点实验室,北京蛋白质组研究中心,北京 102206
CD20是B淋巴细胞表面特异性抗原之一,在淋巴细胞分化早期表达并且能激活淋巴细胞,导致淋巴细胞增殖分化。CD20 分子在95%以上的B 细胞性非霍奇金淋巴瘤(NHL)中均有表达,是治疗B 细胞淋巴瘤的理想靶点[1]。人鼠嵌合抗CD20抗体由鼠抗CD20抗体可变区肽段和人抗体IgG1恒定区肽段组成,临床实验证明治疗效果明显且副反应小,已经被美国FDA批准投入市场,商品名为Rituximab[2]。
本研究选择实验室构建并表达的重组抗CD20人鼠嵌合单克隆抗体TSLXK 进行。这种嵌合抗体虽然通过人源化改造,减少了鼠源组分,但给药后仍然存在一定程度的免疫反应,导致抗药物抗体(antidrug antibody,ADA)产生,尤其是在临床前动物实验中,由于种属差异,抗体更易产生。在治疗性蛋白质药物临床应用过程中,应对免疫原性给予关注,多家国际权威机构就蛋白质药物免疫原性的评价发布了指导原则[3-5]。美国FDA 建议采用多重检测法评价抗体药物的免疫原性,建立一种灵敏度高、操作简单快捷、通量高的筛选法,对临床样品进行初步筛选,筛选呈阳性结果的样品还须进一步采用确证法确定检测抗体特异性结合药物抗体[6-7]。目前,抗体药物免疫原性检测方法很多,如桥连ELISA法、间接ELISA 法、放射免疫沉淀法(RIP)、表面等离子共振法(SPR)等,各种方法都具有其优缺点。
为评价TSLXK 的免疫原性,我们建立了桥连ELISA法,对TSLXK临床前样品进行筛选,再以免疫清除法和交叉试验进行确证,实验结果显示该检测体系灵敏度高、重复性好、通量高,有望进一步应用于将来的临床试验研究。
1 材料和方法
1.1 材料
供试品重组人鼠嵌合抗CD20 单克隆抗体(TSLXK,批号20140402)及原研对照品利妥昔单抗注射液(Rituximab Injection Mabthera,批号H0135/SH0078)均由正大天晴药业集团股份有限公司提供,每瓶100 mg/10 mL,2~8℃避光保存;阳性抗药物抗体(鼠抗Rituximab 单抗,批号300914)购自BIO-RAD 公司,-20℃保存;空白食蟹猴血清由北京协尔鑫生物资源研究所提供;生物素标记试剂盒购自Dojindo Molecular Technologies 公司;辣根过氧化物酶标记链霉亲和素(Streptavidin-HRP)购自R&D Systems公司;其他试剂均为国产分析纯产品。
磷酸盐 缓冲液(PBS,pH7.4):16 g NaCl、0.4023 g KCl、2.84 g Na2HPO4、0.544 g KH2PO4,溶解于2 L ddH2O;封闭液:用PBS配置5%脱脂奶粉;稀释液:用PBS 配制1%牛血清白蛋白(BSA)溶液;显色液:TMB 底物液A 液与B 液等体积混合;1 mol/L 硫酸终止液:将20.8 mL 硫酸缓慢加入100 mL 蒸馏水中,边加边搅拌;PBST 洗板液:将0.5 mL Tween-20加入999.5 mL PBS中。
1.2 对照品及血清样本制备
用含10%食蟹猴空白血清的PBS稀释液将鼠抗Rituximab 抗体分别稀释至320、80、10 ng/mL,作为高、中、低浓度阳性对照样品;空白猴血清用PBS 稀释至1/10 作为阴性对照样品;血清样本用PBS 稀释至1/10待测。
1.3 筛选法(桥连ELISA法)
用PBS 磷酸盐缓冲液将TSLXK 或Rituximab 稀释至5 μg/mL,100 μL/孔,4℃包被过夜;PBST 洗板3 次,用5%脱脂奶粉封闭,300 μL/孔,室温孵育2 h;PBST洗板3次,拍干,分别加入100 μL待测样品、阴性对照品及阳性对照品各3~6 孔,室温孵育1 h;PBST洗板3次,用1% BSA稀释生物素标记TSLXK/Rituximab 至1/10 万,100 μL/孔,室温孵育1 h;PBST洗板3次,用1% BSA稀释Streptavidin-HRP至1/200,100 μL/孔,室温孵育20 min;PBST洗板4次,TMB 显色,100 μL/孔,室温反应15 min;加终止液100 μL/孔,终止反应;酶标仪测定D450/560mm值。
1.4 确证法(免疫清除法)
筛选法检测结果为阳性的样本进一本采用此法进行确证。用PBS 将TSLXK 或Rituximab 稀释至5 μg/mL,100 μL/孔,4℃包被过夜;PBST 洗板3 次,用5%脱脂奶粉封闭,300 μL/孔,室温孵育2 h;TSLXK初筛为阳性的食蟹猴血清样品分别用PBS 和900 μg/mL 的TSLXK 或Rituximab 稀释至1/10,待 测;PBST洗板3次,拍干,分别加入100 μL待测样品、阴性对照品及阳性对照品,室温孵育1 h;PBST 洗板3次,用1% BSA 稀释生物素标记TSLXK/ Rituximab至1/10 万,100 μL/孔,室温孵育1 h;PBST 洗板3次,用1% BSA 稀释Streptavidin-HRP 至1/200,100 μL/孔,室温孵育20 min;PBST洗板4次,TMB显色,100 μL/孔,室温反应15 min;加终止液100 μL/孔,终止反应;酶标仪测定双波长D450/560mm值。
1.5 免疫交叉
为了考察ADA 对TSLXK 和Rituximab 的免疫反应有无差异,将初筛结果呈阳性的血清样品交换包被药物,重新测定。在筛选法中,TSLXK 和Rituximab 给药组动物血清分别采用TSLXK 和Rituximab包板进行检测;在免疫交叉反应中,则采用TSLXK包板检测Rituximab 给药组动物血清,采用Rituximab包板检测TSLXK给药组动物血清,进而与初筛结果进行对比。
2 结果
2.1 筛选(桥连ELISA法)
2.1.1 临界值的确定 临界值(cut-off)是判定样品阴阳性的临界点,高于临界值判定为阳性,低于临界值则判定为阴性。对32 只健康正常食蟹猴血清样品进行桥连ELISA法测定,样品平行测定3次,结果见图1。临界值等于每批测定的血清样品平均值加2 倍标准差。由3 批供试品TSLXK 测得的数据得到的临界值分别为0.0143、0.0142、0.0144,取其均值,临界值设为0.0143;3 批原研对照品Rituximab 测得的数据得到的临界值均为0.0124,其临界值设为0.0124。
2.1.2 临界值的归一化 不同检测批次的临界值不尽相同,为了得到更准确的判定结果,FDA建议对临界值进行归一化。根据Anthony介绍的归一化方法,临界值可进行归一化的必要条件是每批测定的血清样本信号值(即D450/560mm值)标准偏差一致。对32 只食蟹猴血清样品进行3次平行检定,经方差分析,各组间的P值均大于0.05(置信区间95%),说明不同批次测定的血清样品信号值标准偏差一致,满足归一化条件。单一检测批次临界值等于本批次阴性对照样品平均D450/560mm值+归一化因子。其中归一化因子为上述临界值减去阴性对照品平均D450/560mm值,TSLXK 检测的临界值为0.0143,阴性血清D450/560mm值为0.0107,归一化因子为0.0036;Rituximab检测的临界值为0.0124,阴性血清D450/560mm值为0.0097,归一化因子为0.0027。
2.1.3 检测灵敏度 本实验采用鼠抗Rituximab 抗体作为阳性对照品,以反映该方法的灵敏度。用含10%食蟹猴空白血清的PBS缓冲液将鼠抗Rituximab抗体分别稀释为400、200、100、50、25、12.5、6.25 ng/mL。取100 μL上述标准样品加入预先处理的酶标板中(方法详见1.3),根据标准曲线计算临界值所对应的阳性抗体浓度,即为该方法的检测限。
以浓度为横坐标、D450/560mm值为纵坐标,双对数作图,线性回归得到标准曲线(图2)。TSLXK 临界值(0.0143)所对应抗体浓度为0.35 ng/mL,因为血清样品测定时须稀释至1/10,故该方法测定血清中实际抗TSLXK抗体的检测灵敏度为3.5 ng/mL;对照品Rituximab 临界值(0.0124)所对应的浓度也是0.35 ng/mL,故该方法测定血清中实际抗Rituximab 抗体的检测灵敏度为3.5 ng/mL。
2.1.4 精密度与准确度 精密度表示测定值之间的一致性或接近程度,一般用相对标准偏差(CV)表示;准确度表示测定值与真实值之间的符合程度,一般用相对误差(RE)表示。对阳性高、中、低对照进行3 次重复检测,每个浓度6 个平行孔,经计算不同浓度样本的板内或板间的CV均小于10%,板内或板间的RE均介于±10%之间(表1),说明该方法具有较高的精密度与准确度,满足方法学要求
2.1.5 血药浓度对检测方法的影响 血样中存在的药物(TSLXK 或Rituximab)有可能会影响ADA 的检测,因此需要考察样品中存在的TSLXK或Rituximab对免疫原性检测方法的影响程度。用含10%猴血清的PBS 将TSLXK 分别稀释至5000、1000、200、40、8、1.6 μg/mL,将Rituximab 分别稀释至320、64、12.8、2.56、0.512、0.102 ng/mL,进而用梯度稀释的上述含药溶液将鼠抗Rituximab 阳性抗体稀释至320、80 和10 ng/mL,取100μL 加入已包被的酶标板孔中。图3 为不同浓度的TSLXK 和Rituximab 对检测方法的影响。结果显示,二者的影响趋势基本相同,随着血中TSLXK或Rituximab浓度的增高,含有阳性抗体的样品的检测信号值逐渐降低,当药物浓度增加到一定程度时,检测信号值突降至临界值以下,产生假阴性结果(本批次临界值分别为0.0194和0.0148)。阳性样本所含ADA 浓度越高(从10、80 到320 ng/mL),能够耐受的血清药物浓度越高(分别对应12.8、64和320 ng/mL),血清药物浓度一旦超过耐受浓度,则检测结果转为阴性。

图1 食蟹猴血清样品不同检定批次的D450/560mm值波动及分布图(n=32)
2.2 筛选法检测结果
表2 为食蟹猴TSLXK 重复静脉给药4 周、停药恢复8 周毒性实验中动物的分组情况,给药期每组10 只动物(d29 前),恢复期每组4 只动物(d29 后)。表3为毒代样本中ADA检测结果,测定D450/560mm值大于本批次临界值时,结果判定为阳性(+),否则判断为阴性(-)。结果显示TSLXK低剂量给药组从给药后第15 d开始陆续检测到ADA,且动物抗体产生率达到90%;中剂量组仅有1 只在药后22 d 开始检测到抗体,另有2 只在最后一个检测时间点产生抗体(d119);高剂量组无抗体产生。Rituximab 阳性对照组也有1 只动物在药后22 d 开始出现抗体,一直维持到实验结束。
2.3 确证法检测结果
采用免疫清除法确证筛选法检测结果呈阳性的血清样品中是否确实含有抗药物抗体。在检测结果呈阳性的血清样品中加入过量TSLXK,若样品中含有ADA,则过量的TSLXK与包被的TSLXK竞争结合ADA,洗涤过程可将该部分液相中的结合抗体去除,包被TSLXK上结合的ADA减少,最终导致信号值降低。若加入过量TSLXK后信号值无显著差异,阳性结果可能是血清基质非特异性结合所致。

图2 供试品与对照品桥连ELISA法检测的标准曲线
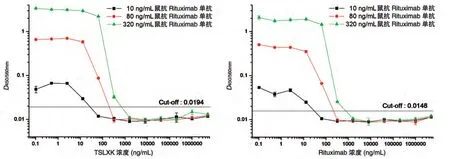
图3 TSLXK及Rituximab血药浓度对桥连ELISA法检测抗药物抗体的影响

表1 桥连ELISA法检测的板内和板间精密度与准确度
对筛选法检测结果呈阳性的各采血点血清样品进行免疫清除试验,结果见图4,以不加TSLXK的检测孔所得D450/560mm值为横坐标,以同一样本加入过量TSLXK后所得D450/560mm值为纵坐标,绘制全部44个初筛为阳性样本的散点图。结果显示,不加TSLXK时,初筛为阳性的全部44个样品点D450/560mm值均大于临界值(0.0145),介于0.189到3.648之间;当加入过量TSLXK后,信号值均显著降低,仅有3个样本点略高于临界值,其余均转为阴性。证实阳性样品中确实含有抗TSLXK或Rituximab的特异性抗体。
2.4 免疫交叉反应
TSLXK 和Rituximab 给药组动物血清在筛选法中分别采用TSLXK和Rituximab包板进行检测,初筛结果呈阳性的血清样品进一步交换包被药物,重新测定,考察ADA 对TSLXK 和Rituximab 的免疫反应有无差异。以TSLXK 包被并检测所得D450/560mm值为横坐标,同一样本用Rituximab 包被并检测所得D450/560mm值为纵坐标绘图(图5),结果显示供试品/原研对照品连续给药在食蟹猴体内均可以引发抗体产生,且二者与二者产生的抗体间存在交叉反应。2种检测方法均可以检测抗体,检测数值比较接近,在散点图上呈现一定的线性回归趋势。
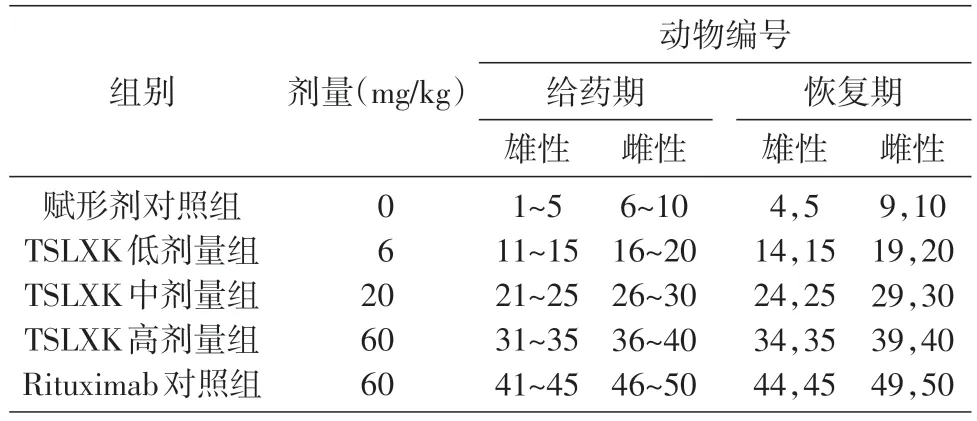
表2 TSLXK重复静脉给药4周、停药恢复8周毒性实验动物分组
2.5 抗体滴度检测
将经免疫确证后的阳性样本进行一系列梯度稀释,直至稀释至检测结果为阴性,则前一个滴度即为血清中抗TSLXK 和Rituximab 抗体的滴度。结果显示食蟹猴血清抗体的滴度从1∶40~1∶1280 不等,随时间延长,抗体滴度逐渐升高,给药后第119 d(最后一个检测时间点)抗体滴度达到最高值1∶1280。
3 讨论
随着基因重组技术的引入,将抗体可变区转移至另一个抗体,使克服或减少鼠克隆抗体的某些局限性成为可能,将鼠抗体的可变区转移至人抗体的恒定区可以明显减少鼠源组分(大约减少2/3),从而生产一种被称为嵌合单克隆抗体的抗体。这种嵌合抗体尽管大大减少了鼠源部分,但仍然存在免疫反应。本研究建立了检测食蟹猴血清中抗CD52 单克隆抗体免疫原性的检测方法并进行了确证,结果显示TSLXK与Rituximab连续给药后,部分个体产生针对TSLXK和Rituximab的特异性抗体,且随时间延长抗体滴度逐渐增高。低、中、高剂量组随剂量的增加,抗体产生率明显降低,说明连续静脉给予抗CD20单克隆抗体后,剂量对抗体的产生存在较大影响,低剂量连续给药更易诱发抗体产生。TSLXK 和Rituximab 相同剂量给药后,TSLXK 没有抗体产生,而对照品Rituximab 却有1 只动物出现抗体,考虑到动物样本数有限且动物本身存在较大的个体差异,要判断差异存在,尚须进一步研究。

表3 TSLXK重复静脉给药4周、停药恢复8周抗药物抗体检测结果
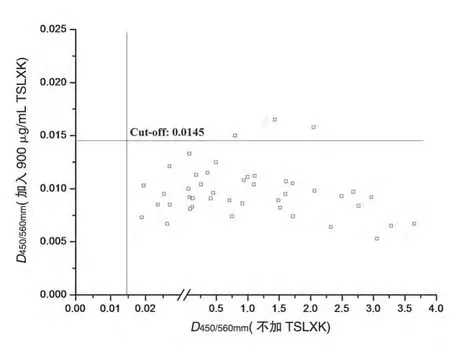
图4 食蟹猴给药4周恢复8周抗体阳性采血点确证法检测结果(n=44)
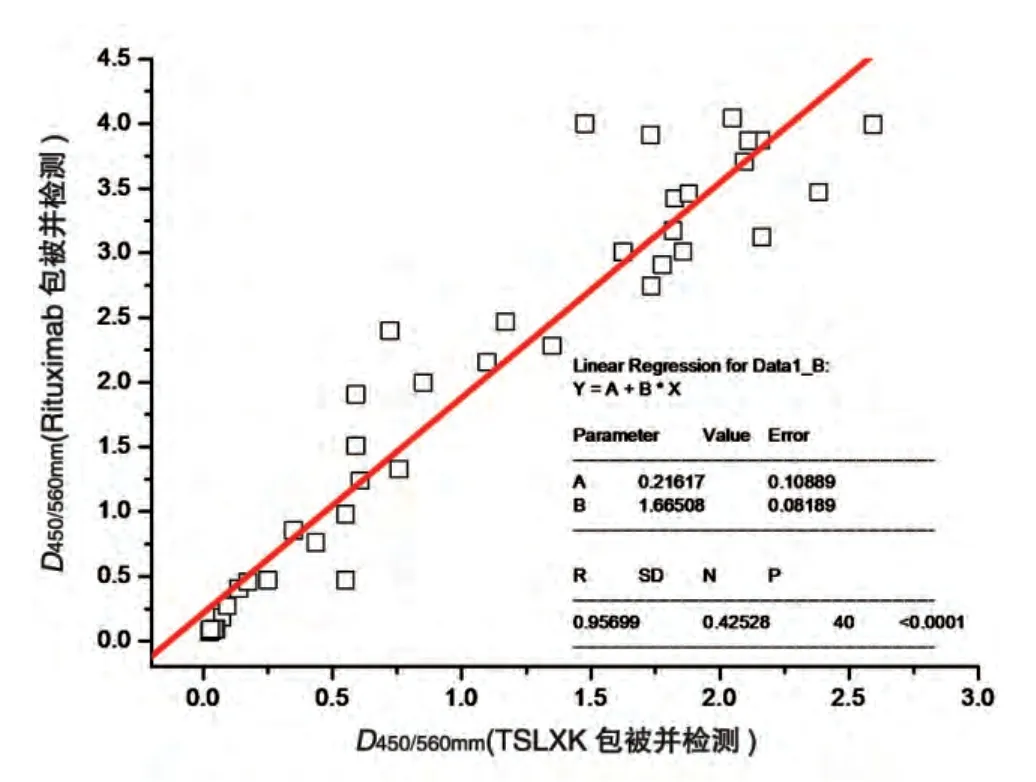
图5 食蟹猴给药4周恢复8周抗体阳性采血点免疫交叉反应(n=44)
由于抗CD20单抗在体内半衰期较长,一段时期内猴体内会存在较高的血药浓度,需要考察血药浓度对ADA检测的影响。方法学确证表明,供试品和原研对照品血清中的药物浓度对抗体检测的影响水平一致,阳性样本所含ADA 浓度越高,能够耐受的血清药物浓度越高,血清药物浓度一旦超过耐受浓度,则检测结果转为阴性。药物与ADA本质上均为抗体,两者分子大小接近,提示体外ELISA 实验中,药物与ADA 的结合比例接近1∶1,一旦血清中所含药物超过所含ADA,即可干扰ADA 的检测,产生假阴性结果。血药浓度较高时虽然对抗体检测有影响,但只是增加了假阴性率,不会增加假阳性率,所以检测结果为阳性的样本是可信的。
桥连ELISA法只是作为大量临床样品免疫原性的初筛,若样品检测结果为阳性,还须采用确证法确证血清中抗CD20 单抗特异性抗体的存在。本实验采用免疫清除作为确证方法,降低了假阳性的发生。桥连ELISA 和免疫清除法的联合,可以更好更客观地评价药物的免疫原性,也是目前国内临床常用的方法之一。根据新的指导原则,免疫原性检测过程中需要加入免疫交叉试验,本实验将实验中检测并确证为阳性抗体的样本进行了免疫交叉试验,结果表明,供试品/原研对照品连续给药在食蟹猴体内均可以引发抗体产生,且二者与二者产生的抗体间存在较高的交叉反应率,这从另一方面证实供试品与原研对照品的结构和免疫反应性高度一致。
[1]Jemal A,Siegel R,Ward E,et al.Cancer statistics,2008[J].CA Cancer J Clin,2008,58(2):71-96.
[2]Pescovitz M D.Rituximab,an anti-CD20 monoclonal antibody:history and mechanism of action[J].Am J Transplantation,2006,6:859-866.
[3]Guidance for industry:assay development for immunogenicity testing of therapeutic proteins[EB/OL].http://www.fda.gov/downloads/drugs/guidancecomplianceregulatoryinformation/guidances/ucm192750.pdf,2009.
[4]Guidance on immunogenicity assessment of biotechnology-derived therapeutic protein[EB/OL].http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2009/09/WC500003 46.pdf,2007.
[5]周海钧.药品注册的国际技术要求(安全性部分)[M].北京:人民卫生出版社,2001:121-134.
[6]Kelley M,Ahene A B,Gorovits B,et al.Theoretical considerations and practical approaches to address the effect of antidrug antibody on quantification of biotherapeutics in circulation[J].AAPS J,2013,15(3):646-658.
[7]Guidance for industry:bioanalytical method validation[EB/OL].http://www.fda.gov/ucm/groups/fdagov-public/@fdagov-drugs-gen/documents/document/ucm368107.pdf,2013.

