替卡格雷的合成研究进展
张银
(青岛科技大学化工学院,山东青岛266042)
替卡格雷的合成研究进展
张银
(青岛科技大学化工学院,山东青岛266042)
替卡格雷是一种新型选择性小分子抗凝血药物,能可逆性地作用于血管平滑肌细胞上的嘌呤2受体亚型P2Y12,明显抑制二磷酸腺苷(ADP)引起的血小板聚集。对替卡格雷的合成方法进行了归纳和比较,以期为进一步研究及工业化生产提供参考。
替卡格雷;直接凝血酶抑制剂;抗凝血药;合成
替卡格雷(Ticagrelor),化学名为(1S,2S,3R,5S) -3-[7-[(1R,2S)-2-(3,4-二氟苯基)环丙氨基]-5-(硫丙基)-3H-[1,2,3]三唑[4,5-d]嘧啶-3-基]-5-(2-羟基乙氧基)环戊烷-1,2-二醇,是由美国阿斯利康(AstraZeneca)公司研发的一种新型的、具有选择性的小分子抗凝血药,于2010年和2011年分别通过欧盟药品管理局(EMEA)和美国食品药品管理局(FDA)的审批在欧盟和美国上市,其进口制剂已获得中国食品药品监督管理总局(CFDA)批准上市[1]。该药能可逆性地作用于血管平滑肌细胞(VSMC)上的嘌呤2受体(purinoceptor 2,P2)亚型P2Y12[2],对ADP引起的血小板聚集有明显的抑制作用,且口服使用后起效迅速,因此能有效改善急性冠心病患者的症状。因为替卡格雷的抗血小板作用是可逆的,所以对于那些需在前期进行抗凝治疗后再进行手术的病人尤为适用,可有效改善急性冠状动脉综合征患者的中风和心脏病风险[3]。
有关替卡格雷的合成路线和工艺改进的研究报道较多,迄今为止已公开的替卡格雷的制备文献大部分是通过嘧啶环、三元环、五元环及相关重要中间体的制备、保护、链接和反应而进行的,本文对其合成路线的报道进行了综述,以期为替卡格雷合成的进一步研究和工业化生产提供参考依据。
1 替卡格雷的合成
1.1 原研厂家阿斯利康公司报道的合成路线
1.1.1 阿斯利康公司专利WO9905143中报道的合成路线[4]
该路线步骤长,且其中涉及锇酸氧化、DIBAL-H还原、铁粉还原等步骤,采用的部分原料有剧毒,容易造成大量工业三废的产生,加大了工业化生产的难度,合成路线如图1所示。
1.1.2 原研厂家阿斯利康公司专利WO0192263报道的合成路线
本专利在反应中先完成五元环的2-乙醇官能团的引入以及先将嘧啶环中的硝基还原生成氨基[5-7],具体合成路线如图2所示。

图1 专利WO9905143报道的合成路线
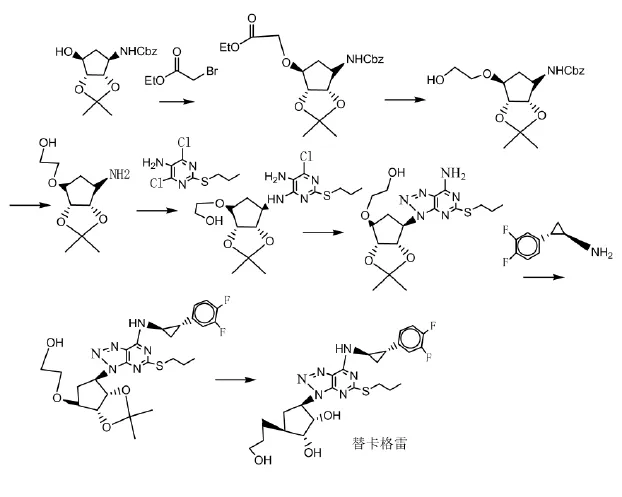
图2 专利WO0192263报道的合成路线
该路线同样存在路线较长,反应步骤较多的缺点,也不适宜作为大规模工业化生产的优选路线。
1.2 美国专利US6525060报道的合成路线
本专利公开了由2-丙巯基-4,6-二氯-5-硝基嘧啶在N,N-二异丙基乙胺的作用下缩合,然后经过铁粉/乙酸还原、亚硝酸异戊酯环合、胺化得到8-氮杂腺嘌呤类衍生物,在丁基锂存在下与2-三氟甲磺酰基乙酸甲酯反应,再经溴代、与手性中间体缩合,最后经DIBAL-H还原酯基,脱丙酮叉保护得到替卡格雷[8-9],具体合成路线如图3所示。
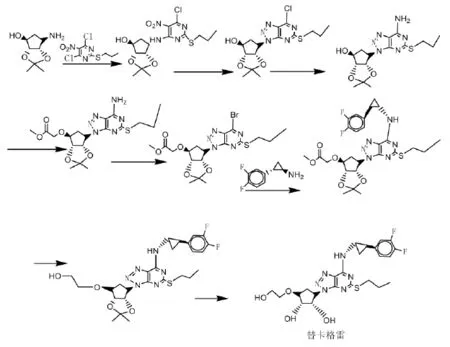
图3 专利US6525060报道的合成路线
该路线的不足之处是中间体中由于受到强吸电子基团硝基的影响,邻位上的两个氯原子活性很高,并且同时含有胺基和羟基,反应极易发生副反应,给后续中间体的纯化带来很大困难。反应中采用正丁基锂,明显加大了工业化生产的危险性。此外,经过反应得到的各步中间体都需要采用柱层析纯化,不利于规模化生产的实施。
1.3 专利WO2006001905报道的合成路线
本专利采用五元环和嘧啶环缩合的方法,通过环丙胺上的氨基保护,增加了缩合反应的选择性[10],具体合成路线如图4所示。
该路线合成步骤较少,药物前体分别分开单独反应,不同于其他专利的反应路线,提高了反应收率,降低了纯化难度,从而降低了该反应的生产成本,更加利于工业化的生产。
1.4 专利US2003/0148888报道的合成路线
本专利采用硫代巴比妥酸为原料,经过烷基化、缩合、三氯氧磷氯化以及催化氢解反应,在三乙胺下缩合,再与亚硝酸钠/乙酸环合形成氮杂嘌呤类衍生物,继续经环合和酸解脱除丙酮叉得到替卡格雷[11],具体合成路线如图5所示。
该路线的反应步骤比较短,对已有路线中裸露羟基进行适当的保护之后,使反应的产率得到大幅的提升,极大地降低了生产成本。不足之处是原料嘧啶环上的两个氯基团活性小,与五元环缩合时需要100℃高温长时间反应,并且五元环中含有胺基和羟基,高温长时间反应容易发生副反应,颜色加深,为后续中间体的纯化带来困难,收率难以保证。
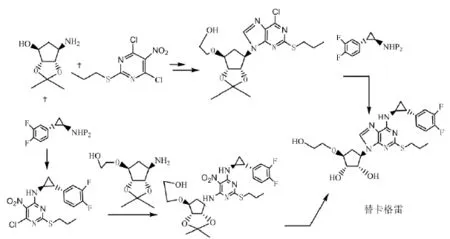
图4 专利WO2006001905报道的合成路线

图5 专利US2003/0148888报道的合成路线
1.5 专利CN102675321报道的合成路线
本专利先经过亲核取代反应,再氢化脱Cbz保护,然后与4,6-二氯-2-(丙巯基)-5-氨基嘧啶反应后,经碱金属的亚硝酸盐,再与(1R,2S)-2-(3,4-二氟苯基)环丙胺反应脱保护基后得到替卡格雷[12-13],具体合成路线如图6所示。
该路线考虑到2-乙醇官能团在后续反应中可能存在副反应,因而先将其羟基进行保护,再进行胺取代反应,最终再通过脱保护生成替卡格雷,反应路线相对较短。
1.6 专利WO2012172426报道的合成路线
本专利先在五元环上保留乙酸甲酯官能团,在完成三个中间体的链接后,最后将酯基还原成醇[14],具体合成路线如图7所示。
该路线首先保留了乙酸乙酯官能团,最后再将酯基水解成醇,主要是因为羟基和氨基容易发生脱水反应,减少了羟基对后续反应的干扰,为替卡格雷实现低成本的工业化生产提供了一种方法。
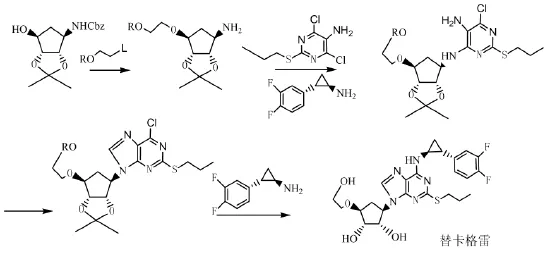
图6 专利CN102675321报道的合成路线

图7 专利WO2012172426报道的合成路线
1.7 专利CN10331266.5报道的合成路线[15]
本专利提供了一种新的工业上容易实现的、简便的建立在新的中间体上的制备方法,具体合成路线如图8所示。
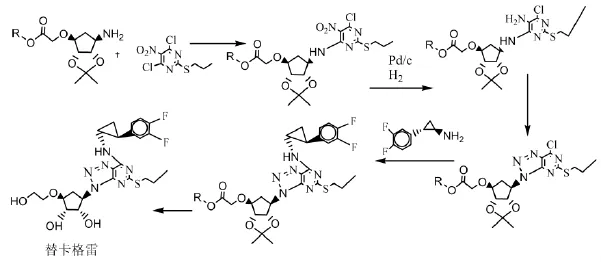
图8 专利CN10331266.5报道的合成路线
该路线可有效减少反应过程中的副反应,提高了中间体的纯度,简化了中间体的纯化方式,通过该合成方法可以经济的、高质量的得到替卡格雷产品。
1.8 专利CN 201010214993.4报道的合成路线[16]
本专利针对五元环与嘧啶环并三氮唑的链接方法上提出了另一种思路,通过五元环上的羟基和三氮唑上的氮原子在三苯基磷和偶氮二羧酸二乙酯的作用下实现耦合。具体合成路线如图9所示。
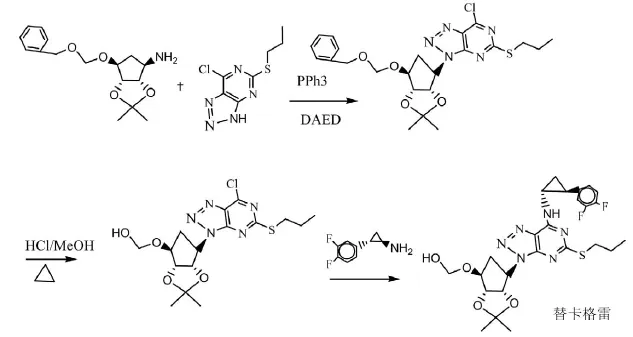
图9 专利CN 201010214993.4报道的合成路线
该路线提供了一种环保、纯度高、收率好、成本较低的制备方法,该方法使用了不对称合成手段,原料来源便捷,产品质量容易控制,不足之处是由于三氮唑环的方向性,使得耦合位置较难控制,总收率为59.2%。
1.9 专利CN 201210138562.3报道的合成路线[17]
本专利以天然D-核糖为原料,经多步反应制得具有复杂手性中间体A,以A为初始反应物,经一系列反应得替卡格雷,具体合成路线如图10所示。
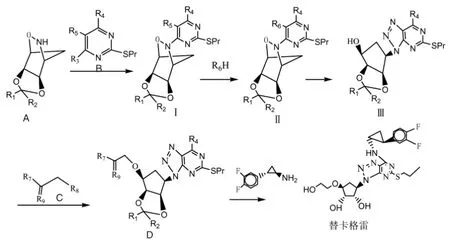
图10 专利CN 201210138562.3报道的合成路线
该路线在合成替卡格雷的过程中涉及到多个全新中间体,技术路线新颖,最后考虑到将替卡格雷做成盐结晶,降低了纯化难度,总收率为36.5%,比较适合工业化大生产。
1.10 专利CN 103304567报道的合成路线
本专利用5-胺基-1,4-二取代基-1,2,3-三氮唑(Ⅱ)和含硫环化剂(Ⅲ)发生环化反应,中间体(Ⅳ)与卤代丙烷(Ⅴ)发生取代反应,中间体(Ⅵ)经氯代反应并与反式-(1R,2S)-2-(3,4-二氟苯基)环丙胺(Ⅶ)发生胺化反应,和中间体(Ⅷ)脱去叉丙酮保护基得到替卡格雷[18-19],具体合成路线如图11所示。

图11 专利CN 103304567报道的合成路线
该路线按照绿色化学的合成理念,提供了一种改进的替卡格雷制备方法,克服了现有路线长、原料不稳定等缺点,该制备方法简便、经济、环保,有利于该药品的工业化生产,总收率可达38.9%。
2 结语
在目前现有技术下,替卡格雷有多条合成路线,每条合成路线各有优缺点。本文对替卡格雷专利合成路线的反应过程进行了综述,以期能为本领域的研究人员提供参考,相信通过科研人员的不断努力,替卡格雷的合成工艺将会更先进、更绿色。
[1]Storey R F.New developments in antiplatelet therapy[J]. Eur Heart J,2008,10(Suppl D):30-37.
[2]Michelson A D.New P2Y12 antagonists[J].Curr Opin Hematol,2009,16(5):371-377.
[3]杨臻峥编译,晋展审校.抗凝血药替卡格雷[J].药学进展,2008,32:426-427.
[4]Simon G,Anthony I,Brian S,et al.Novel compounds:WO, 9905143[P].1999-02-04.
[5]Ulf L,Mattias M,Tibor U,et al.Novel triazolo pyrimidine compounds:WO,0192263[P].2001-12-06.
[6]David H,Anthony I.Novel ribose compounds:WO,2001/ 36438[P].2001-05-25.
[7]SimonG,Brian S.Novel[1,2,3]-triazolo[4,5-D]pyrimidine compounds:WO,2001/36421[P].2001-05-25.
[8]David H,Brian S.Triazolo(4,5-D)pyrimidine compounds: US,6525060[P].2003-02-25.
[9]科克斯D,加尔A,维利斯P.新的血小板凝集抑制剂: WO,9703084[P].1998-10-07.
[10]Kansal V K,Mistry D,Pandey G.New intermediates and processes for preparing ticagrelor:WO,2012138981[P].2012-10-11.
[11]Bjorn J.A multilayer composite vascular access graft:WO, 2006001905[P].2006-01-05.
[12]许学农.替卡格雷中间体4,6-二氯-2-(丙巯基)-5-氨基嘧啶的制备方法:CN,103130726[P].2013-06005
[13]郑保富,薛吉军,高强,等.一种替卡格雷的制备方法: CN,102675321[P].2012-09-19.
[14]Anil S K,Vignesh N,Nikhil T.Improved process for preparing cyclopentylamine derivatives and intermediates thereof:WO,2012172426[P].2012-12-20.
[15]王兵,孙光祥,顾斌,等.一种新的抗血栓药物的制备方法:CN,2010331266.5[P].2013-01-16.
[16]马超,黄箭,马静.一种抗血小板凝集药替卡格雷的制备方法:CN,201010214993.4[P].2012-01-11.
[17]安荣昌,董学军,王伟华,等,一种制备选择性抗凝血药替卡格雷及其中间体的方法:CN,201210138562.3[P]. 2012-09-12.
[18]许学农.一种替卡格雷的制备方法:CN,103304567 A[P]. 2013-06-27.
[19]许学农.替卡格雷的制备方法:CN,103288836 A[P]. 2013-06-27.
Synthesis Progress of Ticagrelor
ZHANG Yin
(Chemical Engineering College,Qingdao University of Science and Technology,Qingdao, Shandong 266042,China)
Ticagrelor is a novol selective antithrombotic agent that reversibly binds to P2Y12 receptors and inhibits adenosine diphosphate-induced platelet aggregation.This paper is summarized and compared of Ticagrelor synthesis method,in order to further research and provide a reference for industrial production.
Ticagrelor;directthrombin inhibitors;antithrombotic agent;synthesis
1006-4184(2015)1-0008-08
中科院大连化物所纳米碳材料催化研究取得重要进展
10.1002/anie.201409524)在线发表,并被该期刊选为“热点文章(Hot Paper)”。以上研究得到了国家自然科学基金委、中国科学院纳米先导专项和教育部能源材料化学协同创新中心(2011·iChEM)的资助。
2014-06-16
国家自然科学基金:粉红粘帚霉固体发酵孢子生长动力学及新型固体发酵反应器研究(编号:21376129)。
张银(1989-),女,硕士研究生,研究方向:药物合成研究方向,E-mail:1172519049@qq.com。
1月12日,中科院大连化物所催化基础国家重点实验室邓德会副研究员和包信和院士带领的研究团队在长期深入研究纳米碳材料催化的基础上,通过创新二维纳米碳材料(类石墨烯材料)的制备策略和合成方法,成功实现了均一的超薄石墨烯壳层(一般为1-3碳层)对3 d过渡金属纳米粒子的包裹和封装。理论模拟和实验研究表明,在催化反应过程中,活性金属纳米粒子催化剂在纳米碳空腔中的封装阻断了其与苛刻反应环境(如酸性、碱性和强氧化性等)的直接接触,有效地延缓和阻止了催化剂的失活;同时,被包裹的纳米金属的活性价电子通过与类石墨烯碳层的相互作用“穿透(penetration)”到外表面,实现了高效催化反应。基于这一原理制备得到的石墨烯碳层封装的纳米钴-镍催化剂应用于强酸性条件下电解水制氢反应(HER),表现出了优异的催化活性和稳定性,在电流密度为10 mA/cm2条件下,电解水阴极过电位仅为142 mV,性能接近于通常采用的40%Pt/C催化剂,相关结果于近日在《德国应用化学》(Angew.Chem.Int.Ed.,2015,
(来源:http://news.sciencenet.cn/htmlnews/2015/1/311446.shtm)

