脂肪族取代脲的合成研究
丁晨 郑添裕 蔡波(中国药科大学,江苏南京 211198)
脂肪族取代脲的合成研究
丁晨 郑添裕 蔡波(中国药科大学,江苏南京 211198)
脂肪族二取代脲是一种绿色环保的合成碳二亚胺的前体。本文主要论述了利用脂肪伯胺和三光气反应合成对称的脂肪族二取代脲以及利用伯胺和N,N’-羰基二咪唑合成不对称脂肪族二取代脲的方法。该实验方法简单,时间短,产率高,具有很高的理论和实际应用价值。
伯胺;二取代脲;碳二亚胺;N,N’-羰基二咪唑;三光气;合成
碳二亚胺化合物(Carbodiimides)[1],就是结构中含有碳二亚胺基团的化合物,其通式如下:R1-N=C=N-R2
分子结构中的累积二烯结构使碳二亚胺具有很强的化学活泼性,不仅可以和许多酸性化合物反应,也可以和醇、胺及含活泼亚甲基等活泼氢一类化合物起反应,其参与的反应具有条件温和、操作简便和收率高的特点。碳二亚胺化合物不如含有N=C=O,O=C=C,S=C=S等基团的相似结构的化合物活泼,其参与的化学反应的动力主要来源于结构中N=C=N双键的不饱和性,作为一种良好的有机试剂。它在非催化条件下很稳定,而在催化条件下表现出很强的反应性。碳二亚胺化合物最早用作酯化反应以及氨基酸合成多肽的脱水剂。
此外DCC和DMSO亦可对醇就行的Pfitzener-Moffatt氧化反应[2]。
1 实验部分
1.1 合成路线
所设计的合成路线如图2-1所示:
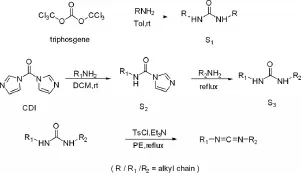
图1-1 二取代脲及对应碳二亚胺的合成路线
1.2 合成化合物
1.2.1 合成对叔丁基脲
反应方程式如图1-2:
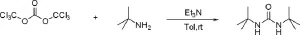
图1-2 对叔丁基脲的合成路线
实验步骤:
于500 mL四颈瓶中依次加入450 mL甲苯、叔丁胺94 g(1293 mmol,6 e.q.)、三乙胺130 g(1293 mmol,6 e.q.)后加塞,电动搅拌冰水浴冷却。于恒压滴液漏斗中缓慢加入54 g(215.5 mmol,1 e.q.)三光气的400 mL甲苯溶液。控制内温不得超过20℃,滴毕rt反应3h,TLC追踪反应。
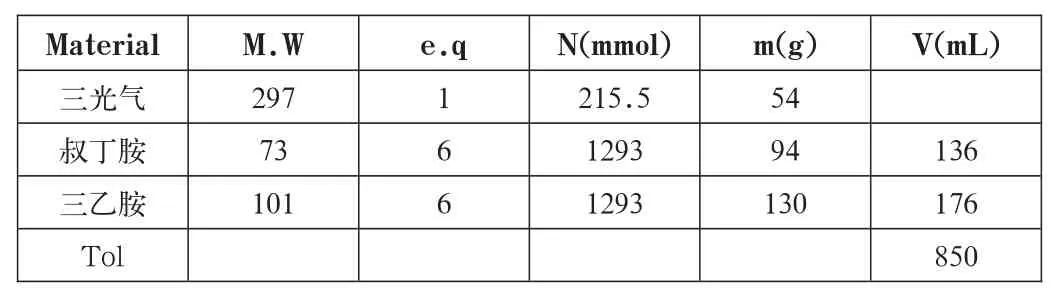
表1-1 合成S1a实验的投料状况
TLC如图(展开剂:P/E=1:2,显色剂:磷钼酸)

图1-3 对叔丁基脲反应液的TLC示踪
反应结束后取250 mL水淬灭反应,转移至分液漏斗中,分出水相后用甲苯反萃取,合并有机相,有机相用水洗两次,然后用5%盐酸洗一次,再用饱和NaCl aq洗两次。浓缩溶剂,加水浆洗后减压过滤,固体用无水乙醇重结晶,收集白色针状晶体68.04 g(72.52%)。
mp:199.6-202.1℃..IR(KBr):3352.11,2964.53,1638.22,1381.61,1360.82 cm-1.1H NMR(CDCl3,300 MHz):δ5.82-5.74(m,2H),3.09(td,J=7.0,2.3 Hz,2H),2.92(dd,J=6.9,2.4 Hz,2H),1.67(dtd,J=13.4,6.7,2.4 Hz,1H),1.45-1.19(m,4H),0.86(td,J=6.6,2.1 Hz,9H).
1.2.2 合成1-正丁基-3-异丁基脲
反应方程式如图1-4
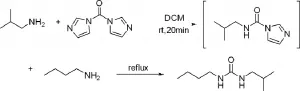
图1-4 1-正丁基-3-异丁基脲的合成路线
实验步骤:
在50 mL圆底烧瓶中依次N,N’-羰基二咪唑20.03 g(123.6 mmol,1.17e.q.)和20 mL二氯甲烷使成浆状,磁力搅拌,在冰水浴条件下滴加异丁胺2.0 mL(20.55 mmol,1 e.q.),滴毕加2.5mL二氯甲烷洗涤恒压滴液漏斗,rt反应20 min,留样β并TLC示踪。加入15 mL水搅拌30 min,分去水相后继续在冰水浴条件下滴加异戊胺3.6 mL(30.62 mmol,1.49 e.q.),滴毕加2.5 mL二氯甲烷洗涤恒压滴液漏斗,回流反应1h,TLC示踪。
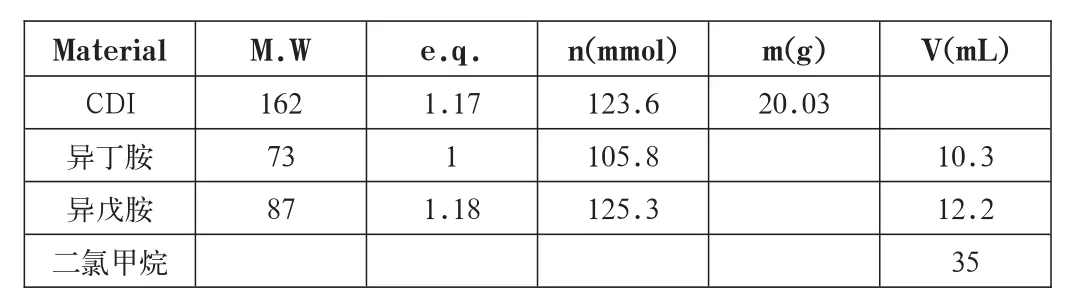
表1-2 合成实验的投料状况
TLC如图(展开剂:P/E=1:3,显色剂:磷钼酸)

图1-5 1-正丁基-3-异丁基脲反应液的TLC示踪
反应结束后,转移至分液漏斗中用20 ml 10%HCL洗,分液水相用10mL二氯甲烷反萃取,合并有机相后再用饱和食盐水洗两次,最后有机相用无水硫酸镁干燥30min,减压过滤后浓缩溶剂收得白色蜡状固体粗品S3b(13.86 g)。
mp:48.4-50.2℃..IR(KBr):3342.05,,1637.53,1573.86 cm-1.1H NMR(CDCl3,300 MHz):
产物提纯后TLC如图(展开剂:P/E=1:3,显色剂:磷钼酸)

图1-6 1-正丁基-3-异丁基脲提纯后的TLC图

图1-7 三光气发生SN2反应的机理
不对称产物的红外光谱与核磁图谱:
图1-8 1-正丁基-3-异丁基脲的H1-HMR图谱
2 实验结果
鉴于此次对碳二亚胺前体对称和不对称二取代脲合成的研究,分别选择了较为温和反应条件的Triphosgene法和CDI法,比之于工业上的异氰酸酯与胺的亲核取代及CO2or CO与胺在金属催化剂及高温高压条件下显得更为绿色低毒,且温和而产率较高。
[1]Williams,A.;Ibrahim,I.T.;Carbodiimide Chemistry:Reagent Advances,Chem,Rev.1981,81.589-636.
[2]Pfitzner,K.E.;Moffatt,J.G.;A New and Selective Oxidation of Alcohols,J,Am,Chem,Soc.1963,85.3027-3028.

