环境因素对单增李斯特菌inlB毒力基因表达的影响
桑 雪,朱耀磊,朱雅慧,张公亮,侯红漫(大连工业大学食品学院,辽宁大连116034)
环境因素对单增李斯特菌inlB毒力基因表达的影响
桑雪,朱耀磊,朱雅慧,张公亮,侯红漫*
(大连工业大学食品学院,辽宁大连116034)
针对单增李斯特菌毒力基因inlB设计五对引物,从中筛选出一对特异性强的引物,利用反转录荧光定量PCR技术来考察毒力基因表达的强弱。在不同环境因素条件下培养单增李斯特菌,分别提取菌体RNA,继而合成cDNA,以管家基因16S rRNA为内参基因,利用循环阈值(Ct)的变化计算inlB基因的相对表达量。结果表明,毒力基因inlB在温度为15℃、pH为6、氯化钠浓度为1.5%~2.0%、蔗糖浓度为0.75%~1.25%时能高效表达;温度为0℃和45℃、pH为4和9、氯化钠浓度为3.5%以上以及蔗糖浓度为0%~0.25%和2.25%以上时,对毒力基因inlB的表达起明显的抑制作用;在pH为6的条件下,酸的种类对毒力基因inlB的表达影响不大。
单增李斯特菌,毒力基因inlB,环境因素,基因表达
李斯特氏菌是兼性厌氧的革兰氏阳性杆状菌[1],其中单增李斯特菌是一种可导致食源性疾病的致病菌,广泛存在于蛋、禽、水产品、乳制品、肉、蔬菜等我们日常的食品中[2-3]。食物较易被单增李斯特菌污染,其中乳制品及肉中的污染检出率最高。目前在世界的很多国家都发生过因该菌引起的中毒事件,感染该菌后临床表现多样化,其病的主要表现为败血症、脑膜炎和单核细胞增多,该菌的致病率远远超过其他食源性细菌[4]。
致病的毒力基因常成簇状,扎堆形成毒力岛[5]。单增李斯特菌即由100个大小不一的毒力岛组成,其中单增李斯特菌的内化素岛主要参与诱导、粘附、侵袭,构成了一个基因家族系:inlA~inlH,基因家族系中inlA和inlB基因有着重要的作用,它们是最早鉴定出的与细菌侵袭相关的毒力因子,是被非吞噬细胞内化所必需,为单增李斯特菌特有,其对单增李斯特菌具有鉴别意义[6]。毒力基因inlB属于内化素家族,具有受体特异性,能与肝细胞生长因子受体结合,是肝细胞、成纤维细胞、上皮细胞的介导因素等。缺失inlB基因的单增李斯特菌毒力株的毒力严重下降。国内外在环境因素对致病菌毒力影响方面也有了一定的研究[7-8],本文选取的inlB基因,是单增李斯特菌很重要的产毒基因之一,且国内外对其研究较少,但其表达的强弱也直接影响了单增李斯特菌的毒性强弱。本文主要研究常见食品加工条件,如温度、pH、氯化钠浓度、蔗糖浓度和酸的种类对inlB基因表达量的影响,以期能初步了解食品加工环境因素的变化对单增李斯特菌毒力的影响。
1 材料与方法
1.1材料与仪器
菌种单增李斯特菌ATCC 19111、ATCC 19112、ATCC 19115、ATCC 15313、威氏李斯特菌CICC 21672和格氏李斯特菌CICC 21670;副溶血性弧菌、大肠杆菌、产气杆菌、沙门氏菌、金黄色葡萄球菌本实验室保存菌株;SYBR®Premix Ex TaqTM、Oligo(dT)15Primer、5×M-MLV Buffer、dNTP Mixture、RNase Inhibitor、RTase M-MLV(RNase H-)等购自宝生物工程(大连)有限公司;20×PBS缓冲溶液、RNase Free dH2O、荧光定量PCR用引物等购自生工生物工程(上海)股份有限公司;细菌总RNA提取试剂盒以及溶菌酶等购自北京天根生化有限公司;胰蛋白胨、磷酸氢二钾、大豆蛋白胨、酵母膏、氯化钠、葡萄糖、醋酸、乳酸、柠檬酸、盐酸等购自博诺试剂。
荧光定量PCR仪美国BIO-RAD公司;高速离心机德国Eppendorf公司;水浴锅上海精宏实验设备有限公司。
1.2实验方法
1.2.1单增李斯特菌的培养含0.6%酵母浸膏的胰酪胨大豆肉汤培养基(TSB-YE)[9]:胰蛋白胨1.7 g,磷酸氢二钾0.25 g,大豆蛋白胨0.3 g,酵母膏0.6 g,氯化钠0.5 g,葡萄糖0.25 g,去离子水100 mL,pH7.5。培养条件为37℃,160 r/min培养20 h。
1.2.2引物的设计及筛选利用NCBI与FastPCR软件相结合,要满足如下条件:21~26个碱基;前面以G/C开头(数值在45%~60%),A/T结尾;Tm=50~60且一对引物的Tm值相差不超过3℃;检测时不产生二级结构;Quality值较理想。
根据以上条件设计了五对引物,见表1,再将每对引物分别与单增李斯特菌、格氏李斯特菌、威氏李斯特菌、大肠杆菌、沙门氏菌、金黄色葡萄球菌、副溶血性弧菌、产气杆菌这几株细菌分别进行特异性检测,最终筛选出了一对特异性强的引物用于后续实验。
1.2.3模板的制备
1.2.3.1细菌RNA的提取取适量菌液按照细菌总RNA提取试剂盒说明书步骤进行RNA提取,于-80℃条件下保存。
1.2.3.2cDNA的合成反应体系6 μL,包括:模板RNA(RNA定量到1 ng),Oligo(dT)Primer 1 μL,RNase free dH2O,混匀;反应条件:70℃10 min;4℃2 min。
反应体系10 μL,包括:以上模板RNA变性溶液6 μL,5×M-MLV Buffer 2 μL,dNTP Mixture 0.5 μL, RNase Inhibitor 0.25 μL,RTase M-MLV(RNase H-)0.5 μL,RNase Free dH2O 0.75 μL,反应条件:42℃60 min;70℃15 min;4℃2 min;4℃保存。
1.2.4荧光定量PCR检测反应体系及条件25 μL扩增体系:2倍浓度的SYBR®Premix Ex TaqTM12.5 μL;浓度为10 μmol/L的引物对各0.5 μL;Cdna模板2 μL;灭菌双蒸水9.5 μL。
反应参数:95℃30 s;95℃5 s,63.3℃25 s;72℃15 s;80℃15 s,40个循环;60~95℃建立熔解曲线。
1.2.5环境因素对毒力基因inlB表达的影响为了研究毒力基因inlB的表达,在不同环境因素条件下培养单增李斯特菌,每个条件作三个平行样本和一个对照样本,继而分别提取RNA,并对所有样品RNA均一化处理,合成cDNA,以管家基因16S rRNA为内参基因。方程2-ΔΔCt用来作为判定inlB表达量的依据,其中37℃、pH7.5、葡萄糖0.25%、氯化钠0.5%作为对照。本文环境因素的选择均是事先经过实验验证的在单增李斯特菌能够良好生长的条件范围内选取,利用荧光定量PCR技术分别得到每一个环境因素的循环阈值(Ct)的变化,从而计算inlB基因的相对表达量。

1.2.5.1温度对inlB基因表达的影响分别在0、5、10、15、20、25、30、37、40、45℃条件下,培养单增李斯特菌20 h,其他条件见1.2.1,继而分别提取RNA、合成cDNA,最后进行荧光定量PCR检测。
1.2.5.2pH对inlB基因表达的影响分别在pH=4、5、5.5、6、6.5、7、7.5、8、8.5、9条件下,培养单增李斯特菌20 h,每个条件作三个平行样本,其他条件见1.2.1,继而分别提取RNA、合成cDNA,最后进行荧光定量PCR检测。
1.2.5.3氯化钠浓度对inlB基因表达的影响分别在氯化钠浓度为0.25%、0.5%、1%、1.5%、2%、2.5%、3%、3.5%、4%(即加入氯化钠0.25、0.5、1、1.5、2、2.5、3、3.5、4 g)条件下,培养单增李斯特菌20 h,每个条件作三个平行样本,每个条件作三个平行样本,其他条件见1.2.1,继而分别提取RNA、合成cDNA,最后进行荧光定量PCR检测。
1.2.5.4蔗糖浓度对inlB基因表达的影响分别在蔗糖浓度为0%、0.25%、0.75%、1.25%、1%、1.75%、2.25%、3%、5%、7%、9%、11%、13%、15%、17%、19%、21%(不加葡萄糖且分别加入蔗糖0、0.25、0.75、1.25、1、1.75、2.25、3、5、7、9、11、13、15、17、19、21 g)条件下,培养单增李斯特菌20 h,每个条件作三个平行样本,其他条件见1.2.1,继而分别提取RNA、合成cDNA,最后进行荧光定量PCR检测。
1.2.5.5酸的种类对inlB基因表达的影响分别选取醋酸(6 mol/L)、乳酸(85%~90%)、柠檬酸(1%)和盐酸(0.1 mol/L)调节培养基pH为6,对单增李斯特菌培养20 h,每个条件作三个平行样本,其他条件见1.2.1,继而分别提取RNA、合成cDNA,最后进行荧光定量PCR检测。
2 结果与分析
2.1引物设计
以单增李斯特菌毒力基因inlB为靶基因设计了五对引物,引物由生工生物工程(上海)股份有限公司合成,所用引物序列见表1。

表1 目的基因与对应引物序列Table 1 Target gene and corresponding primer sequences
2.2引物的特异性检测
用5对引物分别对单增李斯特菌ATCC 19111、ATCC 19112、ATCC 19115、ATCC 15313、威氏李斯特菌CICC 21672、格氏李斯特菌CICC 21670、副溶血性弧菌、大肠杆菌、产气杆菌、沙门氏菌、金黄色葡萄球菌共11株细菌进行荧光定量PCR扩增,经过筛选,引物inlB1、inlB2特异性较强,如图1所示,只有单增李斯特菌ATCC 19111、单增李斯特菌ATCC 19112、单增李斯特菌ATCC 19115和单增李斯特菌ATCC 15313有扩增曲线,其他7株细菌没有扩增曲线,说明可以用于后续实验。

图1 引物inlB1、inlB2扩增结果Fig.1 The amplification results of primer inlB1 and inlB2
2.3温度对inlB基因表达的影响
由图2可知,温度为15℃条件下的相对表达量显著高于其他不同温度条件下的相对表达量(p<0.01),inlB基因的表达较好;温度为0、45℃条件下相对表达量显著低于其他不同温度条件下的相对表达量(p<0.05),对inlB基因的表达量较低。实验结果表明,在低温条件下,inlB基因表达量较高,并不会影响单增李斯特菌的产毒性能。在温度对毒力基因inlB表达的影响方面,Gonzalez-Serrano等[10]也指出低温条件下毒力基因的表达量是高于28℃和37℃条件下的毒力基因表达量的,其结论与本文得到的结果是一致的。

图2 温度对inlB基因表达的影响Fig.2 Effect of temperature on inlB expression
2.4pH对inlB基因表达的影响
由图3可知,pH=6条件下的相对表达量极显著高于其他pH条件下的相对表达量(p<0.01),inlB基因的表达较好;pH=4和pH=9条件下的相对表达量明显低于其他pH条件下的相对表达量(p<0.05),对inlB基因的表达起抑制作用。实验结果表明,在酸碱性较强的条件下,inlB基因相对表达较弱。

图3 pH对inlB基因表达的影响Fig.3 Effect of pH on inlB expression
2.5氯化钠浓度对inlB基因表达的影响
由图4可知,氯化钠浓度在0%~1.5%所对应的inlB基因表达量是递增的,而氯化钠浓度由1.5%~4.0%对应的inlB基因表达量是递减的。氯化钠浓度为1.5%和2.0%条件下的相对表达量极显著高于其他氯化钠浓度条件下的相对表达量(p<0.01),inlB基因的表达较好;氯化钠浓度为4.0%条件下的相对表达量(相对表达量为0.016034)显著低于其他氯化钠浓度条件下的相对表达量(p<0.05),对inlB基因的表达起抑制作用。实验结果表明,低盐度的条件下,能一定程度的促进inlB基因的表达,高盐度条件下抑制inlB基因的表达。

图4 氯化钠浓度对inlB基因表达的影响Fig.4 Effect of NaCl concentration on inlB expression

图5 蔗糖浓度(0%~2.25%)对inlB基因表达的影响Fig.5 Effect of saccharose concentration(0%~2.25%)on inlB expression
2.6蔗糖浓度对inlB基因表达的影响
由图5可知,蔗糖浓度为0.75%和1.25%条件下的相对表达量高于其他蔗糖浓度条件下的相对表达量,inlB基因的表达较好;蔗糖浓度为0%、0.25%和2.25%条件下的相对表达量低于其他蔗糖浓度条件下的相对表达量,对inlB基因的表达有一定的抑制。

图6 蔗糖浓度(1%~21%)对inlB基因表达的影响Fig.6 Effect of saccharose concentration(1%~21%)on iinlB expression
在单增李斯特菌能够良好生长的条件范围内,选取了1%~21%的蔗糖浓度进行对inlB基因表达情况的研究,由图6可知,蔗糖浓度为1%条件下的相对表达量极显著高于其他蔗糖浓度条件下的相对表达量(p<0.01),inlB基因的表达较好;而蔗糖浓度为3%~21%条件下的相对表达量均较低。
实验结果表明,低蔗糖浓度条件下,能够一定程度的促进inlB基因的表达,高蔗糖浓度的条件下抑制inlB基因的表达。
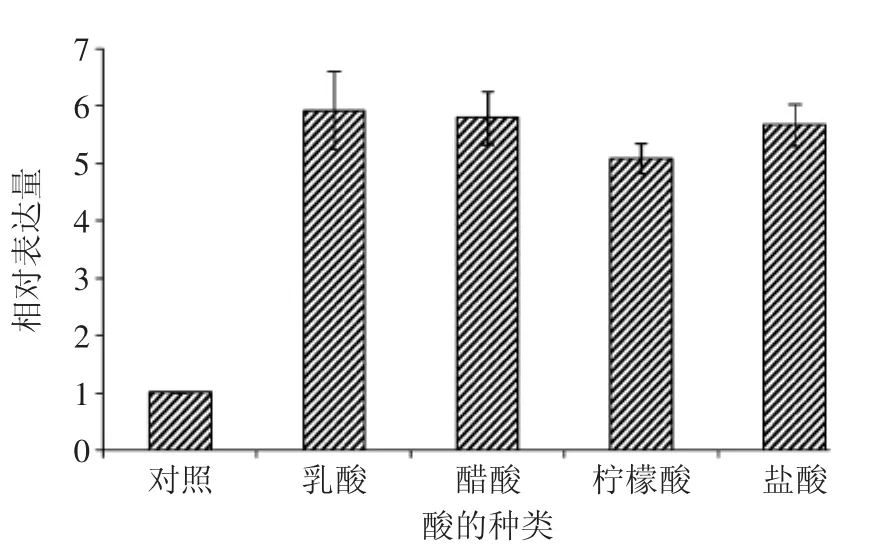
图7 酸的种类对inlB基因表达的影响Fig.7 Effect of various acids on inlB expression
2.7酸对inlB基因表达的影响
分别选取醋酸、乳酸、柠檬酸和盐酸调节培养基pH为6,其中,乳酸、醋酸、柠檬酸为有机酸,盐酸为无机酸。由图7可知,在pH为6的条件下,酸的种类对inlB的表达没有显著的差异性。有关酸的种类对毒力基因表达的研究也有相关报道,Scott E Hanna等[7]报道,选取醋酸、乳酸和盐酸调节培养基pH为5,其对毒力基因inlA表达没有差异性,其结论与所得结果一致。
3 结论
inlB基因高效表达的pH为6的条件下,酸的种类对毒力基因inlB的表达没有明显的差异。毒力基因inlB在温度为15℃、pH为6、氯化钠浓度为1.5%~2.0%、蔗糖浓度为0.75%~1.25%时能高效表达;温度为0℃和45℃、pH为4和9、氯化钠浓度为3.5%以上以及蔗糖浓度为0%~0.25%和2.25%以上时,对毒力基因inlB的表达起明显的抑制作用;在pH为6的条件下,酸的种类对毒力基因inlB的表达影响不大。
[1]Gamble R,Muriana PM.Microplate fluorescence assay for measurement of the ability of strains of Listeria monocytogenes from meat and meat-processing plants to adhere to abiotic surfaces[J].Appl Environ Microbiol,2007,73(16):5235-5244.
[2]Englyst H N,Kingman S M,Cummings J H.Classification and measurement of nutritionally important starch fractions[J].Eur J Clin Nutr,1992,46(2):S33-S50.
[3]Chan Y C,Wiedmann M.Physiology and genetics of Listeriamonocytogenes survival and growth at cold temperature[J].Crit Rev Food Sci Nutr,2009,49(3):237-253.
[4]Hein I,Klein D,Lehner A,et al.Detection and quantification of the iap gene of Listeria monocytogenes and Listeria innocua by a new real-time quantitative PCR assay[J].Res Microbiol,2001,152(1):37-46.
[5]Xiao L L,Hua L Z,Wang H.Critical issue in detecting viable Listeria monocytogenes cells by real-time reverse transcriptase PCR[J].Journal of Food Protection,2012,75(3):512-517.
[6]Rudol M,Scherer S.High incidence of Listeria monocytogenes in European red smear cheese[J].Int J Food Microbiol,2001,63(1-2):91-98.
[7]Scott E.Hanna,Wang H H.Assessment of Environmental Factors on Listeria monocytogenes Scott A inlA Gene Expression by Relative Quantitative Taqman Real-Time Reverse Transcriptase PCR[J].Journal of Food Protection,2006,69(11):2754-2757.
[8]陈星.副溶血弧菌毒力基因的表达变化研究[D].上海:上海海洋大学,2011.
[9]王昊宇,张公亮,侯红漫.应用SYBR GreenⅠ溶解曲线检测食源性单增李斯特菌[J].食品工业科技,2013,34(10):77-79.
[10]Gonzalez-Serrano C J,Santos J A,Garcia-Lopez M L,et al. Virulence makers in Ameromonas veronii biovar sobria isolates from fresh water fish and from a diarrhea case[J].J Appl Microbiol,2002,93(3):414-419.
Effect of environmental factors on Listeria monocytogenes inlB gene expression
SANG Xue,ZHU Yao-lei,ZHU Ya-hui,ZHANG Gong-liang,HOU Hong-man*
(School of Food Science and Technology,Dalian Polytechnic University,Dalian 116034,China)
Five pairs of primers were designed based on Listeria monocytogenes virulence genes inlB and a pair of well specific primers were selected for this study.The Listeria monocytogenes virulence factor expression was studied by real-time reverse transcriptase PCR.RNAs were extracted from Listeria monocytogenes culture solution under the different environmental factors conditions,and then cDNAs were synthesized respectively. The housekeeping gene 16S rRNA was used as an internal standard.The changes of the Ct value could mirror the relative expression levels of inlB gene.Our data suggested that inlB gene expression was efficient when the temperature was 15℃,pH was 6,the NaCl concentration was 1.5%to 2%,and the concentration of sucrose was 0.75%to 1.25%.When the temperature was 0℃ or 45℃,pH was 4 or 9,the NaCl concentration was more than 3.5%,and the concentration of sucrose was 0%to 0.25%,or more than 2.25%,inlB gene expression was suppressed.What’s more,the kinds of acid had little effect on the inlB gene when the pH was 6.
Listeria monocytogenes;virulence genes inlB;environmental factors;gene expression
TS201.1
A
1002-0306(2015)20-0175-05
10.13386/j.issn1002-0306.2015.20.028
2015-01-06
桑雪(1990-),女,硕士研究生,研究方向:食品安全与检测,E-mail:sangxue116@sina.com。
侯红漫(1964-),女,教授,研究方向:微生物技术,E-mail:houhongman@dlpu.edu.cn。
辽宁省高校重大科技平台(辽教发[2011]191号);辽宁省特聘教授(辽教发[2012]145号)。

