电子垃圾中金的生物浸取技术研究进展
梁昌金
(韩山师范学院陶瓷学院,广东潮州 515633)
随着经济的增长和电子、电器设备领域科技的进步,电子产品在促进工业和商业发展的同时,大量的电子垃圾也随之产生.据估计,全球每年所产生的电子垃圾多达2000 万~5 亿吨,而且以每年3%-5%的速度增长,被认为是当前增长最快的垃圾[1].电子垃圾中含有各种各样的有毒有害物质,如Hg、Ni、Sn、Pb、Cr等重金属以及氯氟碳化物、卤素阻燃剂等[2].这些金属与液体废物或污水接触,会产生有毒溶液,渗入到土壤中会污染土壤、水,危害动植物及人类,使人体器官产生内分泌或遗传方面的病变[3].然而从循环经济的角度来看,电子垃圾又是一种有用物质含量极为丰富的资源.据分析[4],个人电脑的印刷线路板中含有20.13%铜,3.59%铝,2.78%锌,2.10%铅,3.27%锡,7.19%铁及0.66%镍,很多重要的有机元素也可以在废弃印刷线路板中找到[5].1吨电子垃圾中含金量是普通金矿的17倍,含铜量是普通铜矿的40倍,因此,有人也把电子垃圾称为“城市矿山”[6].
随着全球高品位金矿资源的日益枯竭,以及工业化推动下人们对黄金需求的逐渐增大,从大量增长的电子垃圾中寻求金资源显得尤为火热.用环境友好的方式对电子垃圾中的金进行回收,既获得了宝贵的稀贵金属,又有效地防止了电子垃圾对环境的污染,达到双赢的目的.
1 生物处理技术
目前,从电子垃圾中回收金属的技术主要有机械处理技术、热处理技术、湿法冶金技术及生物处理技术等[7].机械处理技术只能是将金属浓缩、分选高分子聚合物以及陶瓷等,无法将各种金属彻底分离,且在分选过程中容易造成金属损失[8,9];热处理技术消耗大量的能源,且电子垃圾中的阻燃剂燃烧会释放二噁英、呋喃及粉尘,造成大气污染,同时温度过高会造成金属资源挥发,因此使用时尾气处理是先决条件[10];湿法冶金技术选择性差,往往是多种金属一起浸出,分离困难,且工艺复杂,使用大量的有毒、易燃或高酸碱性化学试剂,易腐蚀设备[11].
生物处理技术基于微生物(细菌、真菌等)能将固体物质转化为可溶化合物的特性,在处理过程中的产物都溶解于水溶液中,易于储存、处理和回收,不需要添加任何有毒化学物质,且在温和的条件下就能进行[12,13].一种回收技术,只有回收成本比金属的原有价值低才在情理之中.像热处理及机械处理这种传统的处理方法不但成本高,经济性低,而且高污染.随着能源成本的不断攀升,加工成本的大幅增长以及环境准入政策的收紧,其它回收技术越来越受到限制.生物技术表现出的低成本,对难处理矿物适应性好,最大限度利用现有投资资本以及其在环境保护等方面的优势,越来越受到人们的青睐[14].
生物处理技术在电子垃圾处理过程中主要应用在两个方面:生物浸出和生物吸附.
1.1 生物浸出
酸解、络合、还原、生物富集等都是生物浸出中常用的机制[15].异养菌在代谢过程中会产生有机酸、氨基酸及其它代谢物质,这些代谢产物能够用氢离子取代线路板中的金属或与金属形成可溶性络合物或螯合物[16].
生物浸出又分为直接浸出和间接浸出两种过程[17].
直接浸出时,微生物吸附在颗粒表面,进行生长代谢,利用自身的氧化或还原性发生电化学反应,将颗粒中的金属氧化成可溶性离子,这个过程中微生物生长与金属浸出同时发生,易于执行,但是溶解的金属离子会对微生物的生长及代谢产生抑制,限制生物浸出效率.
间接浸出分两步来完成:第一步,微生物在适当的环境中生长,产生对浸出过程有活性的代谢产物;第二步,微生物的这些代谢产物作为浸出剂与金属反应,将金属络合或螯合后溶于溶液中.
1.2 生物吸附
生物吸附过程是在带电的生物表面及溶液离子之间的被动的物化交换过程.溶液中的可溶性金属离子被生物富集后,再通过解吸、焚烧、熔融等技术从生物体内获取金属.
在之前的研究中主要是嗜酸性细菌在金属的浸出中发挥着重要的作用,如,嗜酸性氧化硫硫杆菌、嗜酸性氧化亚铁硫杆菌、氧化铁钩端螺菌、硫化叶假单胞菌等[18].利用微生物的氧化作用从矿石中提炼金属已经得到很好的商业化应用,但是利用微生物从电子垃圾中提炼金属的报道还很少,主要集中在利用微生物从电子垃圾中浸取铜的研究上.
2 生物浸金
氰化法以其实用、经济、有效的浸出特征仍被全球90%的金矿企业所采用[19].但是,迫于氰化法对环境的影响,近年来,人们又开始关注硫脲法、硫代硫酸盐法、卤化法等非氰化法,但是都受到各种各样的限制[20].生物法在金属回收中的优点已经显现出来,其在金的提炼中也有着同样的优势,细菌冶金这种绿色工艺将成为颇具希望的新型提金工艺[21].
2.1 生物预处理
利用微生物从难冶矿石中浸金从20世纪70年代开发至今已被大量报道过,且逐渐走向成熟,效果显著[22].微生物的作用主要体现在从含金矿石将包裹在金表面的其它金属氧化物或金属硫化物破坏掉,是浸金前的预处理过程.这样的微生物一般是化能自养菌,这些细菌能从氧化二价铁离子或还原态硫化物的过程中获取能量,以三价铁离子或硫酸为最终代谢产物,包裹在金外面的其它金属氧化物及硫化物被氧化成能容易水的无机盐,在此过程中溶液的pH值会不断降低,更有利于金属硫化物的溶解[23],如利用氧化亚铁硫杆菌氧化矿石中的贱金属矿物,将其剥离掉,使被矿物包裹的金颗粒裸露,这样就能充分与浸出剂接触反应,增加浸出速率,提高金的浸出率.由于微生物直接吸附在颗粒的表面,产生电化学反应,因此是“直接浸金”过程.微生物的预处理率受到pH值、矿浆浓度、接触时间[24]、粉末粒度、细菌接种量、反应温度、通气量及矿物成分的比例[25]等众多因素的影响,因此,微生物处理是一个十分复杂的过程.伍赠玲先对含砷微细浸染型难处理金矿采用细菌预氧化与化学预氧化,然后再采用氰化法对金的浸出率比较:化学预氧化可使金的浸出率提高60%,达到65.4%;而细菌预氧化可使金的浸出率提高到89.2%.[26]
2.2 产氰生物浸金
近年来,利用产氰微生物浸金开始受到人们的关注.微生物在生长代谢过程中利用营养物质中的C、N元素生成次生代谢产物CN-.据推测,微生物的产氰作用是为了抑制与其共同生长的同一环境中的其他生物的生长[27].
利用微生物的产氰作用从废弃印刷线路板中提取金,实际上是利用氰化法浸金的原理将印刷线路板中的金资源提取出来,是“间接浸金”.在处理过程中,金不像有机物那样被微生物矿化,而是被微生物氧化或还原,转化为其它氧化还原态,或与微生物的有机代谢产物形成络合物[14].这种细菌多为异养型细菌,它们利用其它有机物作为生长需要的碳源,在代谢过程中产生的代谢产物CN-可以与金络合,从而将金等金属浸出[12].微生物的浸金机理包括两步:(1)微生物在适当的条件下生长,甘氨酸等有机物营养物质在相关的酶的作用下转化成中间代谢产物HCN;(2)金单质与氰根离子的反应生成可溶性络合物.[28]
尽管很久以前人们就已经发现了微生物的产氰作用,但是关于微生物的产氰能力的数据资料还不多,用产氰微生物来浸取金的研究就更少了.已被报道用于浸金的的细菌主要有:紫色色杆菌(Chromobacterium violaceum)、荧光假单胞菌(Pseudomonas fluorescens)、铜绿假单胞菌(Pseudomonas aeruginosa)、变形假单胞菌(Pseudomonas plecoglossicida),绿针假单胞菌(Pseudomonas Chlorora⁃phis)等.[29,30]
紫色色杆菌利用甘氨酸生成氢氰酸的途径如下[31]:
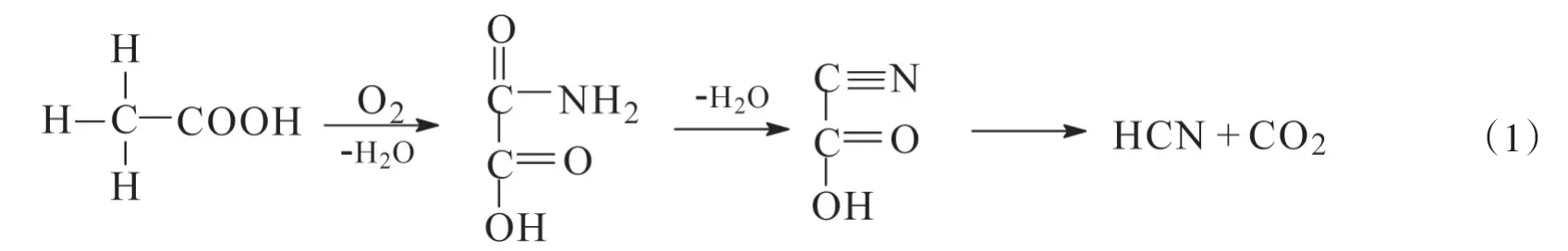
一些假单胞菌通过甘氨酸的氧化脱羧作用可以产生多达300 μM的氰化物[32].假单胞菌属的生氰作用主要发生在其对数生长期,是其次生代谢的主要特征.这种作用受到氧气、铁和磷等浓度的影响.假单胞菌的生氰作用对与其生长在同一生境(如根系环境),与对其生存环境有竞争作用的植物致病菌以及真菌有抑制作用[33].据报道,荧光假单胞菌的产氰能力虽然没有紫色色杆菌强,但是在浸取电子垃圾中的金时,它的能力要比紫色色杆菌高,这是因为荧光假单胞菌有较高的生长率以及高的金属耐受性,比紫色色杆菌拥有更好的浸出动力学过程.[34]
这些产氰细菌除了能在代谢过程中产生中间代谢产物氢氰酸外,还可以在营养物质缺乏时,将CN-分解供给自身生长所需的碳源和氮源[35].因此,利用产氰菌浸出含金材料中的金是一种相对环保的方法.
3 生物浸金的影响因素
生物浸金过程是一个复杂的过程,受菌种、O2、pH值、温度、生长环境的等多种因素的影响[36].例如,紫色色杆菌的产氰能力比荧光绿假单胞菌强,但是在浸取电子垃圾中的金时,由于荧光假单胞菌对金属的耐受能力强,使得这种细菌的生长率及浸金率都比较高.因此,研究浸金微生物的生理特性及生长条件对浸金效率有很大的影响.
(1)微生物性质:氰化物的产生跟细菌自身的性质有关,实验发现,紫色色杆菌在培养到第二天时进入对数生长期,到第五天达到最大值,氰化物的产量也达到最大值,五天之后细菌数量开始下降,氰化物的浓度也开始下降,这主要是因为随着时间的增长,新陈代谢的能力开始降低.[37]细菌也有可能将产生的CN-重新作为碳源或氮源而利用掉[38].
无论是对难处理矿石的预处理还是废弃印刷线路板的直接浸金,微生物与颗粒间的细微的的反应过程,目前了解的很少,但是微生物的吸附作用是其与颗粒进行反应的第一步,只有微生物吸附于颗粒表面,才能更好的利用自身代谢过程中产生的代谢产物将难溶物质氧化溶解,吸附作用决定了溶解率的好坏.Tan和Chen研究了氧化亚铁硫杆菌在多种矿石表面的吸附作用,细菌对亲水矿物有较高的吸附能力,而且细菌的吸附作用具有点位选择性,在适于细菌生成的点位有较高的吸附能力.[35]孙理鑫等分别对无菌、嗜酸性氧化亚铁硫杆菌游离于培养基、吸附于矿石表面等三种情况下矿石氧化过程的基本工学特征做了研究,发现细菌吸附时氧化矿石的能力要高于细菌游离于培养基时和无菌时.[39]
(2)营养物质:细菌的产氰量主要依赖于其生长的介质.细菌要想在代谢过程中产生氰化物,C、N 是必需的,甘氨酸通常被用来为细菌提供这些元素,甘氨酸在酶的作用下脱羧生成CN-[40],其次,蛋白胨、谷氨酸、蛋氨酸等有机物都可以拿来作为细菌的营养物质.除了有机物外,一些低浓度的金属离子(如Mg2+、Na+等)对细菌的产氰能力也有催化和加强作用,但浓度过高会对微生物的数量产生影响.Chi 等向培养紫色色杆菌的培养基中分别加入NaCl、MgSO4、FeSO4及三种物质的混合物,发现细菌的数量都有所减少,而加入NaCl及三种物质的混合物的培养基中,减少更明显,这主要归因于Cl-和高浓度的金属离子对细菌产生毒性,抑制其生长,而且在pH>7.4 时,Fe2+会产生沉淀,吸收一部分细菌;相比较细菌数量的下降,这些物质的加入强化了产氰酶的催化作用,促进了氰的产生,其中Fe2+和Mg2+的强化作用更加明显,经过5天的培养,加入这两种物质的培养基中氰的浓度分别达到61 mg/L和59 mg/L.[38]他们还研究了Pb(NO3)2和Na2HPO4的加入对紫色色杆菌产氰量的影响,在培养基中分别加入低浓度的两种物质都能促进氰化物的产生,而高浓度的两种物质都会抑制氰化物的产生.
(3)氧:氧在生物浸金中有两种作用,一种是供给微生物呼吸用;另一种是作为金与氰化物反应时的电子受体.提高溶液的含氧量,可以加速氰化反应的过程,能提高金的浸出率10%-15%[11].产氰细菌对金属的浸出受到培养液中DO 的限制,因为好养细菌在生长相中呼吸需要消耗大量的溶解氧,经过一天的培养,几乎全部的溶解氧都被细菌呼吸消耗掉[41].Kita等采用曝气的方式,为培养基补充氧气,废弃印刷线路板粉末经过细菌重复批处理后,金的浸出率可达60%.[42]
(4)金/铜的比例:废弃印刷线路板中铜的含量可达70%,铜及其氧化物能与氰化物发生反应而生成铜氰络盐而消耗氰化物.高溶解氧的条件下,Cu 比Au 优先溶解,因为Cu 还原电势比金的低(E0Au3+/Au=1.52 V,E0Cu2+/Cu=0.34 V),要想提高金的浸出量,必须在细菌浸金之前减少铜的含量.Pham和Ting利用氧化亚铁硫杆菌对电子垃圾进行了预处理,去除掉其中80%的Cu,增加了Au/Cu的比例,然后再用紫色色杆菌和荧光假单胞菌分别进行浸金试验发现金的浸出率都有所提高,尤其是使用紫色色杆菌时,浸出率提高更加明显.[43]Dangton 和Leepowpanth 使用硝酸对电子垃圾中的铜进行预处理后采用紫色色杆菌浸出金,含铜率从33%降到了3.67%,而金的浸出率从1.63%上升到了13.62%.[44]
(5)氰化物浓度:有文献显示,当溶液中氰化钠不超过0.03%~0.05%的低浓度时,金溶解的较完全、速度也较快,当浓度提高到0.05%~0.15%时,金的溶解速度增加,当溶液氰化钠浓度增高到0.20%~0.25%时,金的溶解度缓慢增加,当浓度超过此范围时,金的溶解度有所降低.[11]当溶液中的氰化物为低浓度时金的溶解度比较大,而矿石中其他的铜、铁、锌的溶解度比较小,而利用产氰微生物的产氰作用浸取含金资源中金时,微生物产生的氰正好是低浓度的,这样就增加了金的浸出,减少了贱金属的浸出,降低了氰化物的消耗.而氰化物的产生浓度跟细菌种类和数量[37]以及营养物质的种类和数量有关.
(6)pH值:研究发现,紫色色杆菌菌经过8天的培养,pH值从8增加到11时,数量降低,但金的浸出率由7.78%增加到10.80%.[45]这是因为当pH值<9时,Cu(CN)2-稳定,不易分解,消耗了CN-,减少了金的浸出量;当pH值>9时,会使Au(CN)2-生成,促进金的溶解.但是pH值>9会抑制细菌的生长,Natarajan和Ting通过基因突变选择,培养出对碱性环境有耐受性的紫色色杆菌,可在pH值>10的环境下生长,且金的浸出率是pH值为7时的两倍.[46]
(7)粒度:细菌与含金颗粒进行反应时有直接浸金与间接浸金两种方式.研究表明,细菌与颗粒接触的直接浸金方式效果更好.[43]因此颗粒的粒径越小,表面积越大,越容易与细菌接触.但是粒径过小同样会影响浸出效率,因为粒径过小会影响吸附到颗粒上的细菌数量[26].
(8)矿浆浓度:由于电子垃圾含有有毒物质,矿浆浓度的增加会抑制细菌生长,降低细菌的产氰量;但是过低的矿浆浓度也会增加成本.Pham 和Ting研究发现,废弃印刷线路板粉末的加入明显降低了细菌的产氰率,并且随着矿浆浓度的增长(从0.5%到8%),细菌对金的浸出率在下降.[43]Ar⁃shadi和Mousavi采用巨大芽孢杆菌(Bacillus megaterium)浸金时,所采用的最佳矿浆浓度为2 g/L,此时金的最高浸出率可达63.8%.[47]
Li等分别考虑了上述几种因素,先用氧化亚铁硫杆菌对废弃印刷线路板中的贱金属进行预处理,然后再用紫色色杆菌浸出金:在曝气条件下,当pH值为9,粉末粒径为200目,添加营养盐时,最高浸金率可达70.6%.[48]是所有采用紫色色杆菌浸出废弃印刷线路板中金的报道中浸出率最高的.
4 生物浸金的限制
生物法浸金技术被看成是最为绿色、最有广阔前景的技术.目前生物法浸金能被利用到工业上的还仅存在于难冶金矿的预处理技术上,而从废弃印刷线路板中直接生物浸金还局限于实验室里,没有应用到大规模的工业化运行中.这主要是因为生物浸金受到以下几个方面的限制:
(1)时间:生物技术本身就是一个耗时很长的过程,从研究、发展、试验直至到商业化应用少则需要几年,有时会长达10年,甚至是20年,而且这个过程中需要大量人力、物力和财力的支持.
(2)条件控制上:细菌生长受多种因素的限制,如温度、pH值、营养物质等,而且用于浸金的细菌竞争力不强,易于受杂菌的干扰而降低浸取效率甚至死亡,大规模的工业化应用,条件难以控制.
(3)竞争:生物技术需要与其它传统技术进行技术以及成本上的竞争.鉴于生物技术还不成熟,在浸取率、浸取时间以及条件控制方面没有其它传统技术在利润上表现的那么直接,因此,很多企业宁可选择操作条件易于控制、提取率高的高污染高成本的传统工艺.
(4)原料供应:碍于时间及技术上的短板,许多企业(尤其是小作坊)依旧走高耗能、高污染的传统道路.为提高自己的产能,不惜花高价收购电子垃圾,致使大量电子垃圾流入到这些企业中,造成真正有环保技术的大企业没有垃圾可以处理,形成“大企业吃不饱,小作坊吃不了”的局面.
(5)资本:一项新技术研发通常需要大量的资金支持,没有几家企业愿意为此承担过多的资金.
(6)知识产权:新技术的诞生往往是在前人研究的基础上或者几家单位联合研究而成功,在专利申请上容易产生纠纷.而且各自为使自己的知识产权产生经济利益,会阻碍新技术的传播与推广.
5 结 论
生物浸金是一个跨学科的技术,利用化学知识(金属跟氰的相互作用)与微生物特性(代谢过程中产生氰)相结合,使固体中的金属变成可溶的金属氰化络合物将是一个行之有效的新方法.尽管这种方法受到多种因素的限制,目前的研究还不成熟,金的浸出也没有直接添加氰化物的方法那么快,浸出率不高,但微生物浸金被看做是一种环境友好型的方法.物理方法无法获取纯的金属,化学方法实验条件容易控制但容易产生有毒有害废水等二次污染,将物理、化学等方法与生物法相结合,可以取长补短,将是未来废弃线路板利用的发展趋势.
[1]BRETT H ROBINSON.E-waste:An assessment of global production and environmental impacts[J].Science of the Total Envi⁃ronment,2009,408:183-191.
[2]宋闯,袁野.电子废弃物的环境污染及回收利用概述[J].环境保护与循环经济,2015(3):26-28.
[3]居颖.电子垃圾污染对当地居民内分泌干扰效应研究[D].武汉:华中科技大学,2008:5.
[4]SADIA ILYAS,MUNIR A,ANWAR,SHAHIDA B N.Bioleaching of metals from electronic scrap by moderately thermophilic acidophilic bacteria[J].Hydrometallurgy,2007(88):180-188.
[5]DAVIS C,HEART S.Electronic waste:the local government perspective in Queensland,Australia[J].Resources Conservation and Recycling,2008,52(8/9):1031-1039.
[6]钱伯章.国内外电子垃圾回收处理利用进展概述[J].中国环保产业,2010(8):18-23.
[7]YANG J,WU Y,LI J.Recovery of ultrafine copper particles from metal components of waste printed circuit boards[J].Hydro⁃metallurgy,2012,121-124:1-6.
[8]TUNCUK A, STAZI V, AKCIL A, et al.Aqueous metal recovery techniques from e-scrap: Hydrometallurgy in recycling [J].Minerals Engineering,2012(35):28-37.
[9]CUI J, ZHANG L.Metallurgical recovery of metals from electronic waste: a review [J].Journal of Hazardous Materials,2008,158:228-256.
[10]王玉林,齐森,胡海娟,等.废弃印刷电路板回收拆解过程中的气体排放物分析[J].环境化学,2015,34(1):83-88.
[11]KOYAMA K, TANAKA M, LEE J.Copper leaching behavior from waste printed circuit board in ammoniacal alkaline solu⁃tion[J].Mater.Trans,2006,47:1788-1792.
[12]ANJUM F,SHAHID M,AKCIL A.Biohydrometallurgy techniques of low grade ores:A review on black shale[J].Hydrometal⁃lurgy,2012,117-118:1-12.
[13]BRIERLEY C L.Biohydrometallurgical prospects[J].Hydrometallurgy,2010,104:324-328.
[14]REN W,LI P,GENG Y,et al.Biological leaching of heavy metals from a contaminated soil by Aspergillus niger[J].Journal of Hazardous Materials,2009,167(1-3):164-169.
[15]ANJUM F,BHATTI H N,GHAURI M A,et al.Bioleaching of copper,cobalt and zinc from black shale by Penicillium nota⁃tum[J].Afr.J.Biotechnol,2009,19(8):5038-5045.
[16]马荣骏.湿法冶金新发展[J].湿法冶金,2007,26(1):1-12.
[17]MISHRA D, RHEE Y H.Current research trends of microbiological leaching for metal recovery from industrial wastes [J].Current Research, Technology and Education Topics in Applied Microbiology and Microbial Biotechnology, 2010,2:1289-1292.
[18]WATLING H R.The bioleaching of sulphide minerals with emphasis on copper sulphides- A review [J].Hydrometallurgy,2006,84:81-108.
[19]黄海辉,王云,袁朝新,等.从提金渣中回收金银[J].有色金属:冶炼部分,2011,10:37-39.
[20]鲁顺利.非氰化法提金工艺研究现状[J].云南冶金,2011,40(3):32-36.
[21]杨洪英,范金,崔日成,等.难处理高砷金矿的细菌氧化-提金研究[J].贵金属,2009,30(3):1-3.
[22]ANJUM F, BHATTI H N, AMBREEN A.Bioleaching of black shale by Acidithiobacillus ferrooxidans[J].Asian J.Chem,2009,7(21):5251-5266.
[23]崔日成,杨洪英,张谷平,等.pH值对浸矿细菌的活化以及金精矿脱砷的影响[J].东北大学学报:自然科学版,2008,29(11):l597-1600.
[24]佟琳琳,姜茂发,杨洪英,等.湖南某高砷难处理金精矿的细菌氧化-氰化提金实验研究[J].贵金属,2008,29(1):15-18.
[25]杨玮,覃文庆,刘瑞强,等.高砷难处理金精矿细菌氧化-氰化提金[J].中国有色金属学报,2011,21(5):1151-1158.
[26]伍赠玲.高砷微细浸染型难处理金矿细菌预氧化-氰化提金试验研究[J].矿冶工程,2010,30(1):54-61.
[27]CRECZYNSKI-PASA T B,ANTÔNIO R V.Energetic metabolism of Chromobacterium violaceum[J].Genetics and Molecular Research.2004,26(3):162-166.
[28]BRANDL H,LEHMANN S,MOHAMMAD A F,et al.Biomobilization of silver,gold,and platinum from solid waste materials by HCN-forming microorganisms[J].Hydrometallurgy,2008(94):14-17.
[29]LIANG C, LI J, MA C.Review on cyanide-generating bacteria for gold recovery from E-waste [J].Advanced Materials Re⁃search,2014,878:355-367.
[30]RUAN J, ZHU X, QIAN Y, et al.A new strain for recovering precious metals from waste printed circuit boards [J].Waste Management,2014,34(5):901-907.
[31]KNOWLES C J,BUNCH A W.Microbial cyanide metabolism[J].Adv.Microb.Physiol.1986,27:73-111.
[32]CIPOLLONE R,ASCENZI P,TOMAO P,et al.Enzymatic detoxification of cyanide:clues from Pseudomonas aeruginosa rho⁃danese[J].J Mol Microbiol Biotechnol.2008,15:199-211.
[33]FARAMARZI M A, BRANDL H.Formation of water-soluble metal cyanide complexes from solid minerals by Pseudomonas plecoglossicida[J].FEMS Microbiol.Lett.2006,259:47-52.
[34]KUNZ O, NAGAPPAN J, SILVA-AVALOS G T.Utilization of cyanide as a nitrogenous substrate by Pseudomonas fluore⁃scens NCIMB 11764: Evidence for multiple pathways of metabolic conversion [J].Appl.Environ.Microbiol., 1992,58:2022-2029.
[35]TAN S N, CHEN M.Early stage adsorption behaviour of Acidithiobacillus ferrooxidans on minerals I: An experimental ap⁃proach[J].Hydrometallurgy,2012,119-120:87-94.
[36]SHIN D, JEONG J, LEE S, et al.Evaluation of bioleaching factors on gold recovery from ore by cyanide-producing bacteria[J].Minerals Engineering,2013,48:20-24.
[37]SUNIL H.Sustainable management of electronic waste(e-waste)[J].Clean,2007,35:305-310.
[38]TRAN C D,LEE J,PANDEY B D,et al.Bacterial cyanide generation in the presence of metal ions(Na+,Mg2+,Fe2+,Pb2+)and gold bioleaching from waste PCBs[J].Journal of Chemical Engineering of Japan,2011,44(10):692-700.
[39]孙理鑫,张旭,谭文松,等.金精矿生物氧化过程中菌体吸附的重要性研究[J].金属矿山,2012(1):92-96.
[40]URÁN M D,ALJONI-ALARIO A F,URÁN N D.Chromobacterium violaceum and its important metabolites-review[J].Folia Microbiol.2010,55(6):535-547.
[41]TRAN C D,LEE J,PANDEY B D,et al.Bioleaching of gold and copper from waste mobile phone PCBs by using a cyanogen⁃ic bacterium[J].Minerals Engineering,2011,24:1219-1222.
[42]KITA Y, NISHIKAWA H, IKE M, et al.Low environmentally impact recovery of gold using cyanide producing bacteria[J].Environmentally Conscious Design and Inverse Manufacturing,2005:935-938.
[43]PHAM V A,TING Y P.Gold bioleaching of electronic waste by cyanogenic bacteria and its enhancement with bio-oxidation[J].Biohydrometallurgy,2009,71-73:661-664.
[44]DANGTON J, LEEPOWPANTH Q.A study of gold recovery from e-waste by bioleaching using Chromobacterium violaceum[J].Applied Mechanics&Materials,2014,548-549:280-283.
[45]LIU Y, SU G, ZHANG B, et al.Nanoparticle-based strategies for detection and remediation of environmental pollutants [J].Analyst,2011,136:872-877.
[46]NATARAJAN G, TING Y.Pretreatment of e-waste and mutation of alkali-tolerant cyanogenic bacteria promote gold biore⁃covery[J].Bioresource Technology,2014,152:80-85.
[47]ARSHADI M, MOUSAVI S M.Enhancement of simultaneous gold and copper extraction from computer printed circuit boards using Bacillus megaterium[J].Bioresource Technology,2015,175:320-324.
[48]LI J, LIANG C, MA C.Bioleaching of gold from waste printed circuit boards by Chromobacterium violaceum [J].Journal of Material Cycles and Waste Management,2014,DOI:10.1007/s10163-014-0276-4.

