SAMRT IV检测葡萄糖、糖化血红蛋白、糖化白蛋白的性能评估
贾江花,谢远敏,汪 屹
(宁波美康生物科技股份有限公司,浙江宁波315104)
SAMRT IV检测葡萄糖、糖化血红蛋白、糖化白蛋白的性能评估
贾江花,谢远敏,汪屹
(宁波美康生物科技股份有限公司,浙江宁波315104)
目的探讨SMART IV检测葡萄糖(GLU)、糖化血红蛋白(HbA1c)、糖化白蛋白(GA)的性能。方法根据美国临床实验室标准化协会(CLSI)EP15-A2文件,选取低、高2个浓度水平质控品,采用SMART IV检测GLU、HbA1c、GA等3个项目,每个浓度水平质控品每日测定3次,连续测定5d,进行精密度评价。每天收集不同浓度新鲜样本5份,连续4d,共20份,在SMART IV和日立7180生化仪两台仪器上分别对上述3个项目进行测定,各重复2次,对测定结果进行准确度评价。结果SMART IV测定GLU、HbA1c、GA等3个项目的批内精密度(Sr)、总精密度(Sl)均小于厂家声明的批内精密度(σr)、总精密度(σl)。SMART IV测定GLU、HbA1c、GA等3个项目的相对偏倚均小于厂家允许偏倚。结论SMART IV测定GLU、HbA1c、GA等3个项目的精密度和准确度结果均在厂家允许范围内,SMART IV检测糖尿病三项满足临床需求。
葡萄糖;糖化血红蛋白;糖化白蛋白;精密度;准确度
糖尿病(Diabetes Mellitus,DM)是继肿瘤、心血管病变之后第三大疾病,严重威胁着人类健康。DM治疗关键是血糖水平的控制与稳定。目前临床监测DM最常用指标是血糖(GLU),但是GLU具有波动性、瞬间性等特点,易受饮食、药物、情绪等诸多因素影响[1],因此它属于短期血糖控制监测指标。糖化蛋白可为较长时间段的血糖浓度提供回故性评估,其中糖化血红蛋白(HbA1c)能反映患者过去8~l2周的平均血糖水平[2],已被糖尿病控制和临床实验协会(DCCT)推荐为血糖控制及监测的“金标准”[3];糖化白蛋白(GA)能反映患者过去2~3周的平均血糖浓度,尤其适用于血糖波动较大的初诊患者降糖治疗时的疗效观察[4,5]。由此可见,将上述三者同时检测在提高DM的诊断准确度的同时还可以提高监控血糖控制水平的准确性[6-8]。SMART IV是一款基于分光光度的POCT体外诊断仪器,其体积小,操作方便,可以应用于基层医院或者专业诊所,且其可以同时测定DM的三个指标:GLU、HbA1c、GA。本文对SMART IV测定GLU、HbA1c、GA的性能进行评估,现报道如下。
1 材料与方法
1.1标本来源所有标本均来自于美康中医院的门诊病人,所选标本无溶血、无脂浊。
1.2仪器和试剂宁波美康盛德生物科技有限公司生产的SMART IV仪器,宁波美康生物科技股份有限公司生产的GLU(氧化酶法)、HbA1c(酶比色法)、GA(酶比色法)、白蛋白(溴甲酚绿法)试剂盒及配套质控品,日立7180生化仪,所有操作均按说明书进行。
1.3精密度评价根据EP15-A2[9]方案要求,对2个不同水平的质控品每个每天测定3次,共测定5d。按照以下公式分别计算:
D=测定的天数;n=每天测定的次数;xdi=第d天第i个测定值;d=同一水平质控品第d天的测定均值;C=根据自由度和测定的浓度水平数查χ2分布表所得百分位。测定结果的批内精密度(Sr)和总精密度(Sl),分别与厂家声称的批内精密度(σr)和总精密度比较(σl)比较,若实验室测定的精密度比厂家声称的相应精密度小,则认为SMART IV测定三种试剂精密度达到厂家声称的精密度;若实验室测定的精密度比厂家声称的精密度大,再与相应的验证值进行比较,若比相应的验证值小则认为仪器的精密度与厂家声称的精密度无差异。
1.4准确度评价根据EP15-A2方案要求,每天收集不同浓度新鲜样本5份,连续4d,共20份,浓度范围尽可能覆盖分析测量范围,但不超过线性范围。每天用SMART IV、日立7180生化仪以常规操作在2h内检测标本,各重复2次。评价质量控制确保稳定的操作条件和有效的实验结果。以日立7180生化仪测定的值作为参考值(X轴),以SMART IV仪器的测定结果与日立7180生化仪测定值差值为对比值(Y轴)作偏倚图,并计算相对偏倚与偏倚验证值进行比较,判定差异是否显著。
bi=第i天偏倚;n=样本总量;=偏倚平均值;%b=百分比偏倚平均值;β=允许偏倚百分比。若实验室测定的偏倚(%)比厂家声称的相对偏倚小,则认为SMART IV测定三种试剂准确度达到厂家声称的准确度;若实验室测定的(%)比厂家声称的相对偏倚大,再与相应的验证值进行比较,若比相应的验证值小则认为仪器的准确度与厂家声称的准确度无差异。
2 结果
2.1精密度评价SMART IV测定GLU、HbA1c、GA等3个项目的批内精密度(Sr)、总精密度(Sl)均小于厂家声明的批内精密度(σr)、总精密度(σl),见表1。
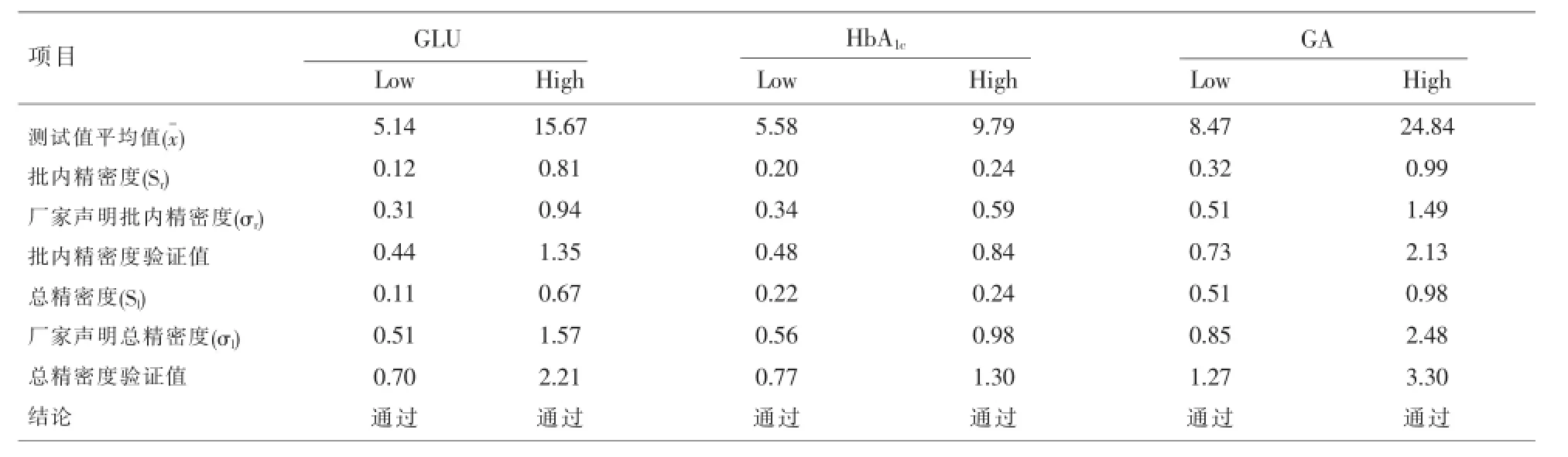
表1 SMART IV测定三种试剂精密度结果
2.2SMART IV和日立7180测定三种试剂偏倚分析见表1~表3。
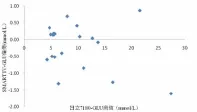
图1 SMART IV和日立7180两台仪器测定GLU偏倚图
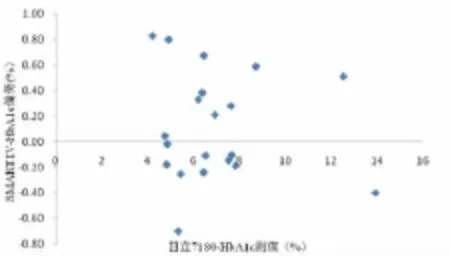
图2 SMART IV和日立7180两台仪器测定HbA1c偏倚图
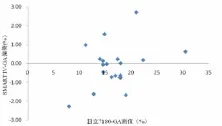
图3 SMART IV和日立7180两台仪器测定GA偏倚图
2.3准确度评价根据说明书要求,厂家允许偏倚5%。由表2可见,SMART IV测定GLU、HbA1c、GA三种试剂,相对偏倚均小于厂家允许偏倚及偏倚验证值,准确度符合厂家要求。
3 讨论
中国已成为DM第一大国,DM不断上升的患病率及随之增加的致残率和死亡率严重威胁着人们的生命健康。目前,国内监测DM最常用的指标是GLU,由于GLU含量易受各种因素影响,对确诊具有局限性,但是血糖仪的发展使得自我血糖监测成为可能,并在血糖控制中发挥重要的作用[10,11]。HbA1c是DM研究领域中备受瞩目的指标,作为血糖监测的“金标准”在临床中已广泛应用,但其准确性也会受许多因素影响(如因红细胞寿命、基因、年龄等一些非糖类作用因素的影响)[12]。对于那些HbA1c水平不能真实反应平均血糖水平或存在糖基化差距(glycation gap,GG)的DM患者[13,14],发达国家已逐渐将GA作为DM检测的补充。
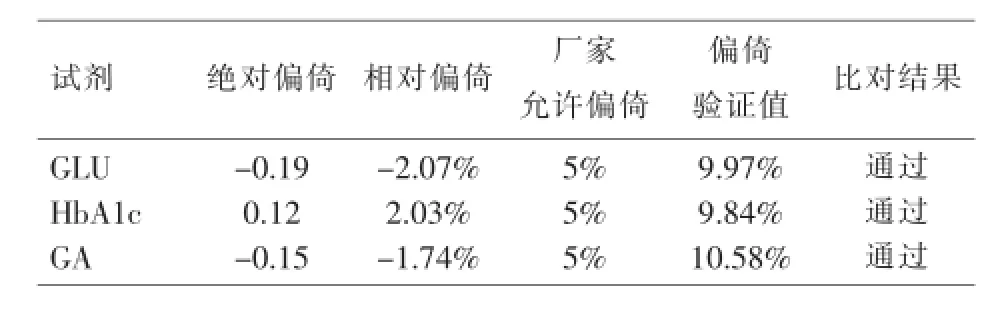
表2 SMART IV测定三种试剂准确度结果
目前国内测定患者HbA1c和GA大多在大型全自动生化仪上进行,而广大的社区医院、乡镇卫生院等基层医院由于大型生化仪价格昂贵、操作人员技术水平要求高等因素,没有能力开展此项工作,使得基层医院在DM这种慢性疾病的管理中失去了应有的作用,因此小型化、床边化、多功能化发展是DM检测技术的发展趋势之一。之前有学者报道过POCT测定HbA1c的研究[15,16],而将GLU、GA、HbA1c在同一台POCT上测定未见报道。
SMART IV是最适合基层慢性病诊断与管理的移动医疗系统,其中的一款DM检测仪可同时测定GLU、HbA1c、GA三种指标,从而满足日益扩大的DM监测需求,其搭载数字化云端数据,不但能够将检测数据以短信息的方式发送至患者手机,同时患者也可在手机中安装APP软件,实现档案数据查询及健康管理;其搭建的远程诊疗技术,使患者可以通过网络视频与语音等方式与专家交流,不出门不排队即可得到慢性病专家资源。
本文根据EP15-A2方案要求,通过对SMARTⅣ与日立7180生化仪测定GLU、GA、HbA1c,发现SMARTⅣ精密度及准确度均能满足临床的需求,因此SMARTⅣ仪器有望成为基层医院的常规使用仪器。
[1]沈秀金.同时测定血糖,糖化血清蛋白与糖化血红蛋白对糖尿病监测的重要性[J].实用医技杂志,2008,15(26):3633-3634.
[2]中华医学会糖尿病学分会.中国血糖监测临床应用指南(2011年版)[J].中华糖尿病杂志,2011,3:13-21.
[3]中华医学会糖尿病学分会.中国2型糖尿病防治指南(2013年版)[J].中华糖尿病杂志,2014,6(7):447-498.
[4]薛声能,程桦.糖化血红蛋白的研究进展[J].国际内科学杂志,2008,35(10):586-588.
[5]Koga M,Kasayama S.Clinical impact of glycated albumin as another glycemic control marker[J].Endocr,2010.57(9):751-762.
[6]陈锦,黄存敏,冯广贵,等.糖尿病三项检测的临床应用[J].实验与检验医学,2013,31(3):264-266.
[7]Masafumi Kogaa,Calculation of HbA1c and glycated albumin from serially measured self-monitored blood glucose in patients with type 1 diabetes mellitus[J].Clinica Chimica Acta,2013,425(21):188-191.
[8]陈凯,辛晓兰,陈佩琴,等.空腹血糖联合糖化血红蛋白检测对糖尿病筛查的临床意义[J].实验与检验医学,2012,30(3):267-268.
[9]Clinical and Laboratory Standards Institute.User verification of performance for precision and trueness approved guideline-second edition[S].EP15-A2(e),CISI,2005.
[10]García dela Torre N,Early management of type 2 diabetes based on a SMBG strategy:the way to diabetes regression-the St Carlos study:a 3-year,prospective,randomized,clinic-based,interventional study with parallel groups[J].Acta Diabetol,2013,50(4):607-14.
[11]Harashima S,Self-monitoring of blood glucose(SMBG)improves glycaemic control in oral hypoglycaemic agent(OHA)-treated type 2 diabetes(SMBG-OHA study)[J].Diabetes Metab Res Rev,2013,29(1):77-84.
[12]Ahmada J,Rafatb D.HbA1c and iron deficiency:A review[J]. Diabetes&Metabolic Syndrome:Clinical Research&Reviews,2013.7(2):118-122.
[13]David B,Sack S.Gaps in the glycation gap hypothesis[J].Clin Chem,2011.57(2):150-152.
[14]Santiago RS,Javier R,Jose M,et al.Progression of Nephropathy in Type 2 Diabetes:The Glycation Gap Is a Significant Predictor after Adjustment for Glycohemoglobin(HbA1c)[J].Clin Chem,2011,57(2):264-271.
[15]虞芳.一种新型全自动糖化血红蛋白POCT检测仪器的临床应用评估[J].西南军医,2011,13(6):1030-1031.
[16]Haliassos A,Drakopoulos I,Katritsis D,et al.Measurement of glycated hemoglobin(HbA1c)with an automated POCT instrument incomparisonwithHPLCandautomatedimmunochemistry method:evaluation of the influence of hemoglobin variants[J].Clin Chem Lab Med,2006,44(2):223-227.
R446.11+2,R587.1
A
1674-1129(2015)05-0607-03
10.3969/j.issn.1674-1129.2015.05.025
2015-04-13;
2015-09-17)
宁波市重大攻关项目(编号:2012B10005)

