醋酸乙酯加氢合成乙醇反应器的模型化
孙帆,程双,于小芳,张新平,张春雷,周兴贵
醋酸乙酯加氢合成乙醇反应器的模型化
孙帆1,2,程双1,于小芳1,张新平1,张春雷1,周兴贵2
(1上海华谊集团技术研究院,上海 200241;2华东理工大学化学工程联合国家重点实验室,上海 200237)
根据实验室数据对醋酸乙酯加氢制乙醇宏观动力学方程进行参数估计,得到宏观动力学模型。根据动力学模型,同时考虑内扩散的影响以及物料、热量和动量衡算方程建立了醋酸乙酯加氢制乙醇固定床反应器的一维拟均相模型,并分别得到不同氢酯比、不同控制温度、不同压力下的多种工况的模拟结果。模拟结果与实际生产数据吻合。该模型可用于指导工业反应器的设计和操作优化。
醋酸乙酯;固定床;反应器;乙醇;动力学;一维拟均相
引 言
乙醇是重要的化工原料和燃料。关于乙醇的制备技术,目前我国主要采用粮食发酵以及乙烯水合法[1],也有采用天然气为原料制备的报道[2-4],国外近几年有较多以天然气为原料制备乙醇的专利报道[5-7]。近年来,醋酸酯加氢制备乙醇技术越来越受到人们的重视,一方面可以缓解目前国内醋酸行业处于产能严重过剩、市场持续低迷的困境,开发其下游产业链[8],另一方面由于石油的不可再生和石油产区的不稳定性,燃料能源安全问题在全球范围内引起了越来越多的关注,因此,大力发展燃料乙醇、乙醇柴油等以乙醇为原料的能源产业已经成为国际燃料能源产业的一大亮点[9]。与其他技术相比,采用醋酸乙酯加氢合成乙醇,催化剂价格较低、单程转化率高、择性好且副产物少,可以大大降低后续分离的难度[10]。
加氢反应器是醋酸乙酯加氢制乙醇生产中的重要装置,目前国内外文献还没有关于该反应器模型的相关报道,仅有关于催化剂的文献[11-13]。本研究首先根据实验室数据建立动力学模型,然后根据动力学模型,同时考虑内扩散的影响以及物料、热量和动量衡算方程建立了反应器模型,模型结果与单管实际工况较吻合。
1 宏观动力学模型
原料氢气(H2)和汽化的醋酸乙酯(EA)在固定床反应器中与铜基催化剂接触,进行加氢反应,生成乙醇(EtOH)。反应过程可以描述为
为便于工程设计应用,宏观动力学方程模型一般用幂函数形式,反应速率常数采用修正的阿伦尼乌斯方程[14],反应动力学方程形式如下
采用非线性最小二乘法对实验数据进行参数估值[15],实验结果和参数拟合可见文献[16],经计算得到动力学参数为
01.585 Pa-1·s-1,6.056×104J·mol-1,
2 反应器模型
2.1 内扩散的影响
内扩散效率因子计算式为
气相反应物A在固相中的有效扩散系数由式(6)~式(9)计算[17]
所用催化剂的物理参数为:粒径0.003 m,长度0.003 m,颗粒密度1.6×103kg·m-3,颗粒平均孔径260×10-10m,颗粒孔隙率0.61,曲节因子1.35。
2.2 数学模型
建立醋酸乙酯加氢合成乙醇固定床反应器模型时,采用一维拟均相平推流模型[18],做如下假设:①流体在反应器中温度、浓度径向均一,仅沿轴向变化;②流体与催化剂在任一与流体流动方向垂直的横截面处的温度、反应物浓度相同;③流体在床层中以平推流流动。
在反应器床层高度上取微元d进行物料、热量和动量衡算,得到模型数学表达式如下。
物料衡算方程为
H2和EA在反应过程中的摩尔分数均用生成乙醇的摩尔分数表示
热量衡算方程为
动量衡算采用厄根(Ergun)方程[19]
气体混合物的混合规则采用Kay规则[20],该规则提出的虚拟临界参数为
混合气体的密度、比热容等参数也均采用此混合规则。
3 模型计算结果
在模拟计算时,采用Runge-Kutta积分算法对反应器模型沿轴向积分求解反应结果。在不同工况条件下运行模型,得到模型的模拟结果,与实际工况下的乙酯转化率、反应器热点温度和热点位置等主要指标进行对比。
3.1 不同氢酯比下的模拟结果
在压力为5.5 MPa、控制温度为204℃时,对不同氢酯比下的5组工况(氢酯比分别为7.5、10、13、20和30时)进行模拟,乙酯转化率模拟值与实际值的对比如图1所示。

图1 不同氢酯比时的乙酯转化率
氢酯比分别为7.5、13、20和30时的床层温度分布模拟值与实际值的对比如图2所示。其中,模拟转化率与实际转化率的平均相对误差为0.32%,模拟热点温度与实际热点温度的平均相对误差为0.20%。从模拟结果可以看出,随着氢酯比的增大,反应器出口的乙酯转化率逐渐增大,热点温度逐渐降低,热点位置略微提前。
3.2 不同控制温度下的模拟结果
在压力为5.5 MPa、氢酯比为13~14时(模拟时氢酯比取为13.5),对不同控制温度下的7组工况进行模拟,乙酯转化率模拟值与实际值的对比如图3所示,床层温度分布实际值和模拟结果如图4所示。其中,模拟转化率与实际转化率的平均相对误差为0.18%。从模拟结果可以看出,随着进口温度的增大,反应器出口的乙酯转化率逐渐增大,热点温度逐渐增大,热点位置略微提前。

图3 不同进口温度时的乙酯转化率

图4 不同进口温度时的床层温度分布
3.3 不同压力下的模拟结果
在控制温度为204℃、氢酯比为13时,对不同压力下的3组工况进行模拟,压力分别为5.5、4.8、4 MPa时的乙酯转化率模拟值与实际值的对比如图5所示。
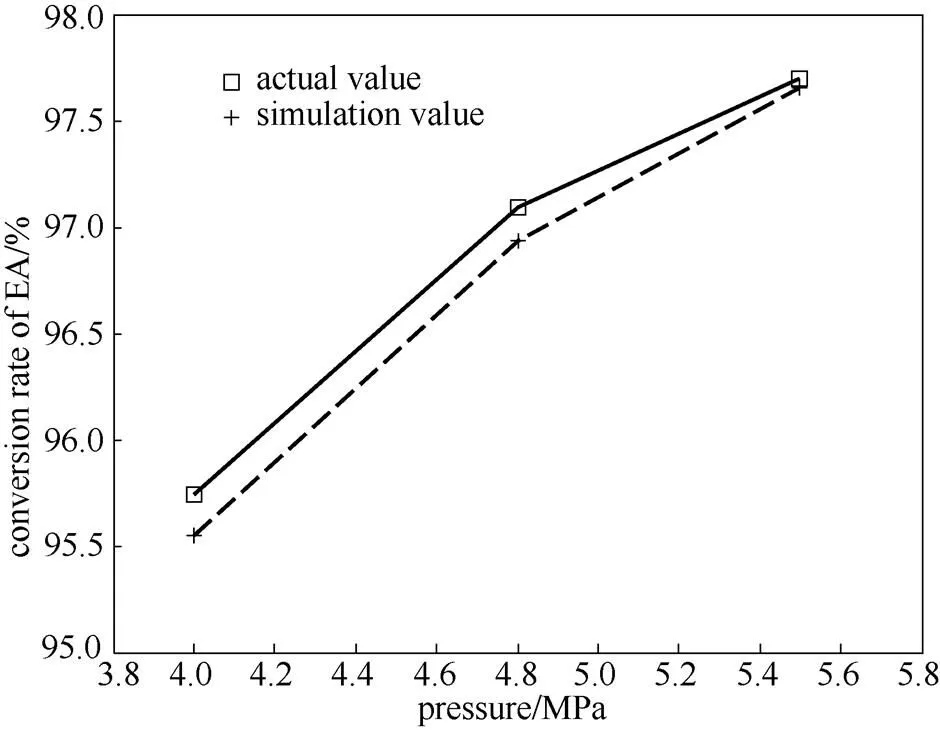
图5 不同压力下的乙酯转化率
床层温度分布模拟值与实际值的对比如图6所示。其中,模拟转化率与实际转化率的平均相对误差为0.34%,模拟热点温度与实际热点温度的平均相对误差为0.47%。从模拟结果可以看出,随着压力的增大,反应器出口的乙酯转化率逐渐增大,热点温度基本不变,热点位置略微提前。

图6 不同压力时床层温度分布
4 结 论
(1)针对醋酸乙酯加氢制乙醇反应体系建立了醋酸乙酯加氢合成乙醇固定床反应器的一维拟均相模型。模拟计算结果表明,增大氢酯比、增加反应器进口温度以及增加反应器压力均可以增大反应器出口的乙酯转化率,氢酯比和反应器进口温度对反应器热点温度影响较大,反应器压力则对热点温度影响较小。
(2)模型计算结果与单管装置实际生产数据吻合度较好,偏差较小,表明所建立的反应器模型及其他数据的计算和处理是合适的,所建模型可用于醋酸乙酯加氢合成乙醇固定床工业反应器的模拟、设计和操作优化。
符 号 说 明

Am——催化剂颗粒外表面面积,m2 cp——混合气体比热容,J·mol-1·K-1 cpc——导热油比热容,J·mol-1·K-1 DA,Knu——Knudsen扩散系数,m2·s-1 DA,mol——分子扩散系数,m2·s-1 DA,pore——孔扩散系数,m2·s-1 Deff,A——气体反应物A在固相的有效扩散系数,m2·s-1 dpore——颗粒平均孔径,m

ds——颗粒当量直径,m E——活化能,J·mol-1 F——混合气体流量,kg·m-2·s-1 Fc——导热油流量,kg·m-2·s-1 H——反应热,J·mol-1 K——管程传热系数,J·m-2·K-1·s-1 k——反应速率常数,Pa-1·s-1 k0——指前因子,Pa-1·s-1 l——床层位置,m M——组分相对分子质量 p——气体总压,Pa pci——组分i的临界压力,Pa pcm——虚拟临界压力,Pa pEA——EA的分压,Pa R——气体常数,J·mol-1·K-1 Rem——Reynolds数 S——反应管内截面积,m2

T——温度,K Tc——导热油温度,K Tci——组分i的临界温度,K Tcm——虚拟临界温度,K t——反应时间,s um——混合气体质量流速,kg·m-2·s-1 V——分子扩散体积 yi——组分i的摩尔分数 α——H2的反应级数 β——EA的反应级数 εB——床层孔隙率 εp——催化剂颗粒孔隙率 η——内扩散效率因子 ρB——催化剂床层密度,kg·m-3 ρg——混合气体密度,kg·m-3 τp——曲节因子 ——Thiele模数
References
[1] Li Fang, Zhang Ke, Ma Hongfang, Zhang Haitao, Ying Weiyong, Fang Dingye. Thermodynamic analysis of different routes of ethanol synthesis [J]., 2013, 30 (3): 256-260
[2] Sun Lujing (孙陆晶). Alcohol fuel industry prospect [J].(化学工业), 2011, 29 (1): 8-12
[3] Wang Peng (王鹏),Wang Xiangui (王宪贵),Guo Zhanying (郭战英). Research progress in producer gas to ethanol technology [J].(洁净煤技术), 2010, 16 (1): 55-58
[4] Phillips J, Clausen E, Gaddy J. Biological production of ethanol from coal synthesis gas [J]., 1993, 40 (1): 559-571
[5] Johnston V, Chapman J, Chen L. Ethanol production from acetic acid utilizing a cobalt catalyst [P]: US, 7608744. 2009
[6] Wollrab R, Johnston V, Warner R. Process for producing ethanol by hydrogenation of acetic acid [P]: WO, 2011140468. 2011
[7] Johnston V, Kimmich B, Waal J. Ethanol production from acetic acid utilizing a molybdenum carbide catalyst [P]: US, 8350098. 2013
[8] Hu Yurong (胡玉容), Wang Ke (王科), Li Yang (李扬), Fan Xin (范鑫), Yuan Xiaojin (袁小金), Xu Hongyun (许红云). Simulation of synthesizing ethanol by hydrogenation of ethyl acetate [J].(化学工程师), 2011 (9): 25-27
[9] Yang Jie (杨洁), Ding Mingzhu (丁明珠), Li Bingzhi (李炳志), Yuan Yingjin (元英进). Phospholipidome alterations ofin bioethanol fermentation process [J].(化工学报), 2012, 63 (6):1830-1835
[10] Wang Biao (王彪), Wang Xiting (王熙庭), Xu Guohui (徐国辉). Advances in technologies for hydrogenation of acetic acid and acetates to ethanol [J].(天然气化工), 2013, 38 (3): 79-83
[11] Song Qingfeng (宋庆锋),Zhang Yong (张勇),Zeng Qinghu (曾清湖). Techno-economic analysis of production process of syngas to ethanol [J].(工业催化), 2013, 21 (6): 17-21
[12] Yang Yong (杨勇), Wang Yangdong (王仰东), Liu Su (刘苏). Mo-Co-K sulfide-based catalysts promoted by rare earth salts for selective synthesis of ethanol and mixed alcohols from syngas [J].(催化学报), 2007, 28 (12): 1028 -1030
[13] Pan Hui (潘慧), Bai Fenghua (白凤华), Su Haiquan (苏海泉). Research progress of Rh-based catalyst for conversion of syngas to ethanol [J].(化工进展), 2010, 29 (2): 157-161
[14] Xia Xinyu (夏新宇), Zhang Wenzheng (张文正). A kinetic study on closed-system petroleum generation simulations under constant temperature and its significance [J].(石油勘探与开发), 2000, 27 (5): 22-26
[15] Roger F, Sven L. Solving mathematical programs with complementarity constraints as nonlinear programs [J]., 2004, 19 (1): 15-40
[16] Yu Xiaofang (于小芳), Cheng Shuang (程双), Sun Fan (孙帆), Zhang Xinping (张新平), Zhang Chunlei (张春雷), Tang Yi (唐颐). The macro-kinetics of ethyl acetate hydrogenation to ethanol [J].:(复旦学报:自然科学版), 2014, 53 (1):77-83
[17] Zhang Xinping (张新平), Sui Zhijun (隋志军), Zhou Xinggui (周兴贵). Modeling of coke burning off regeneration for coked propane dehydrogenation catalyst [J].(化工学报), 2009, 60 (1): 163-167
[18] Ling Zeji (凌泽济). Mathematical simulation of synthetic reactor of ethylene oxide [J].(江苏化工), 2005, 33 (5): 54-57
[19] Xiong Wei (熊玮), Bi Xuegong (毕学工), Zhou Guofan (周国凡). Simulation study on gas pressure drop characteristics in the lower zone of blast furnace [J].(高校化学工程学报), 2007, 21 (2): 233-238
[20] An Chao (安超), Guo Xiao (郭肖), Zhang Yong (张勇), Li Gang (李刚), Ma Jun (马军). Calculation methods optimization of deviation factor for overpressure gas reservoir [J].:(重庆科技学院学报: 自然科学版), 2010, 12 (5): 92-94
Modeling of ethyl acetate hydrogenation reactor
SUN Fan1,2, CHENG Shuang1, YU Xiaofang1, ZHANG Xinping1, ZHANG Chunlei1, ZHOU Xinggui2
(Technology Research Institute of Shanghai Huayi GroupShanghaiChinaState Key Laboratory of Chemical EngineeringEast China University of Science and TechnologyShanghaiChina
A kinetic model of synthesizing ethanol by hydrogenation of ethyl acetate was developed based on laboratory data, and then corrected by taking into consideration the pore diffusion effect. With the correction, the results could conform with actual operation. Based on the principles of material balance, energy balance, momentum balance and kinetics of the reactions, an one-dimensional pseudo-homogeneous model of the ethanol synthesis reactor by hydrogenation of ethyl acetate using fixed bed was established. The simulation results of a variety of conditions were obtained by the model with different H2/EA molar ratios, different temperatures and different pressures. The model could reflect the performance of the hydrogenation reactor and provide guidance for the design and operation optimization of industrial reactor.
ethyl acetate; fixed bed; reactor; ethanol; kinetics; one-dimensional pseudo-homogeneous
2014-08-11.
10.11949/j.issn.0438-1157.20141217
TQ 021.8
A
0438—1157(2015)02—0561—06
2014-08-11收到初稿,2014-09-30收到修改稿。
联系人:张春雷,周兴贵。第一作者:孙帆(1985—),男,博士。
Prof.ZHANG Chunlei, clzhang@shhuayitec.com; Prof. ZHOU Xinggui, xgzhou@ecust.edu.cn

