铜合金中低含量银的快速测定
范珍媛
(江苏包罗铜材集团股份有限公司,江苏海门226103)
铜合金中银的测定方法一般有原子吸收法、电位滴定法、硫氰酸盐容量滴定法、EDTA间接结合滴定法等。在这些方法中,除仪器分析(原子吸收法)外,其他方法只适用于较高含量银的测定,而不适用于低含量银的测定。
在一些合金中,用化学分析法测定低含量银,一般都需经过萃取分离手续,然后进行光度测定,例如,用双硫腙-四氯化碳萃取,用1.10-菲啰啉-溴邻苯三酚红使Ag+形成三元络合物后,以硝酸苯萃取或者用乙基紫使Ag+络合以甲苯萃取,或用喹哪啶红使Ag+络合以甲基异丁酮-乙酸异戊酯混合溶剂萃取等。总之,这些方法都要用到有机试剂,不但工序繁琐,测定周期长,且有毒性,污染水源。为此,查阅国外资料并结合本公司实际生产需要(银量0.03%~0.60%),制定出铜合金中低含量银的快速测定经多次试验,从实践中制订出本分析方法,以硝酸溶解样品,在0.35~0.40mol/L的酸度下,以氯离子和银离子作用使生成不溶性的氯化银乳浊液,然后进行比浊测定。
1 分析方法
1.1 方法提要
用硝酸溶解试样,在0.35~0.40mol/L的酸度下,以氯离子和银离子作用使生成不溶性的氯化银乳浊液,于分光光度计、波长440nm处进行比浊测定。
本分析方法的特点是:快速,无需任何萃取等分离手续;节能降耗,整个分析过程只需少量的两种试剂,大大提高经济效益;操作方法简便,因酸度及沉淀剂的加入量合适,较好的解决了氯化银露于空气中被还原为黑色金属银的缺点,因而在整个测定过程中无需避光,无需用黑布或黑纸遮住,操作过程顺利,比浊液稳定;环保、无污染。
1.2 试剂
(1)(1+1)(优级纯)的硝酸;
(2)1mol/L(优级纯)的盐酸;在500ml容量瓶中,加入约400ml纯水,加入41.7ml比重为1.19的盐酸,摇匀,冷至室温后以水稀至刻度,混匀;
(3)称取 0.1000g纯银(纯银 99.95% 以上),置于125ml小锥形烧杯中,加入20ml硝酸(1+1),微热溶解完全,并除去氮的氧化物,冷却移入500ml容量瓶中,以水稀释至刻度,混匀,此溶液1ml=200μg银,制成银标准溶液。
1.3 分析步骤
按表1称取试样(银量在200~1000μg),把试样置于100ml容量瓶中,按表1加入硝酸(1+1)溶解,加热溶解完全并除去氮的氧化物,冷却至室温,加入纯水使总体积在80ml,加5ml盐酸溶液(1mol/L),立即以水稀释至刻度,混匀,用力摇匀约1min,放置15min后比色。

表1 试样称取量Tab.1 Weight of working sample
称取同量的纯铜打底,按试样操作步骤作试剂空白,移取部分溶液于3cm比色皿中,于分光光度计波长440nm处对试剂空白测量吸光度在工作曲线上查得相应的银量。
1.4 工作曲线的绘制
称取与试样相同的纯铜六份,置于一组100ml容量瓶中,按试样所述步骤进行溶解并除去黄烟后冷却至室温,分别向上述溶液中加入 0、1.00、2.00、3.00、4.00、5.00ml银标准液;分别加入纯水使体积至80ml。按试样操作步骤进行,用3cm比色皿以补偿溶液为参比于分光光度计波长440nm处测量吸光度,以银量为横坐标,吸光度为纵坐标,绘制工作曲线。
1.5 分析结果的计算
2 试验内容
2.1 铜量的影响
称取不同量的纯铜数份置于一组100ml容量瓶中,分别加入硝酸(1+1)(按表1)微热溶解完全并除去氮的氧化物,各加入400μg银标准溶液,分别加入纯水使体积均约为80ml,按试样分析步骤进行操作,结果如表2所示。
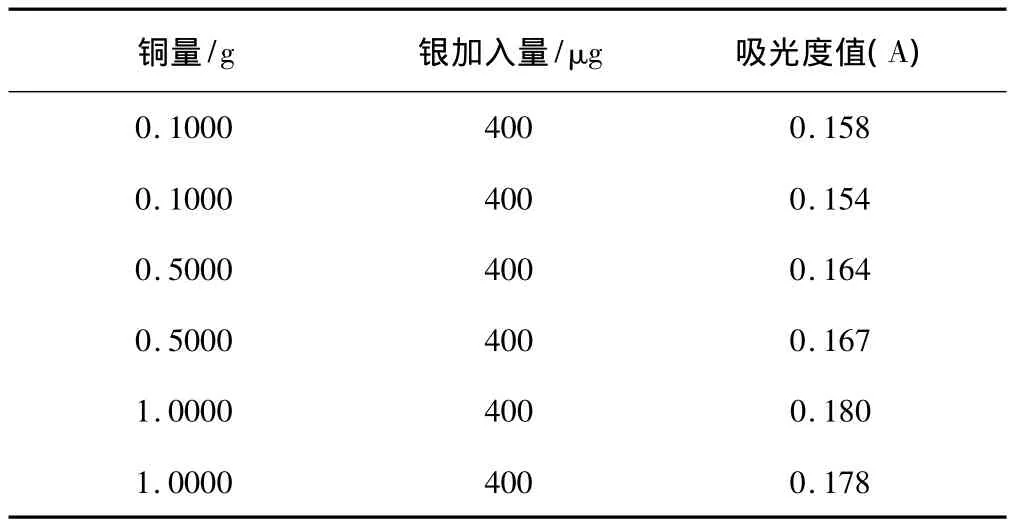
表2 铜量的影响Tab.2 Effect of copper content
从表2可知,铜量稍有影响,因此工作曲线应取相当于试样的含铜量打底绘制。
2.2 沉淀剂加入量
称取0.5000g纯铜数份置于100ml容量瓶中,各加入5.0ml硝酸(1+1),按试样分析步骤进行溶解冷却后,各加入400μg银并分别加入不同量的盐酸(1mol/L),按试样分析步骤进行操作测定吸光度,结果如表3所示。
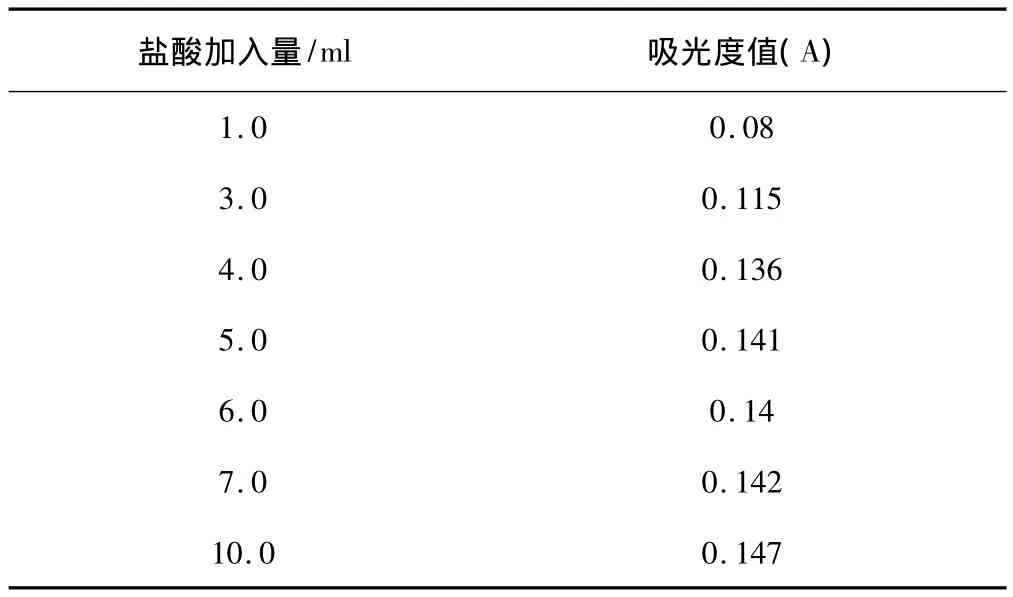
表3 沉淀剂加入量试验Tab.3 Effect of adding varying amounts of precipitating agent
由表3可见,盐酸(1mol/L)加入5ml即可。
2.3 硝酸的加入量
称取的试样量不同,因而硝酸的加入量也不同。根据相关资料并结合多次生产实践,认为0.1~0.2g试样加入硝酸(1+1)5.0ml,0.5g 试样加入 7.0ml,1g试样则加入10.0ml。总之,使酸度控制在0.35~0.40mol/L左右,测定的效果良好、稳定。
2.4 乳浊液稳定性
含600μg Ag+、其Agcl乳浊液吸光度变化如表4所示(放置时间是指从摇匀后放置至读取吸光度为止的这一段时间)。由表4可见,乳浊液放置15min后至1h内,吸光度值基本不变。

表4 乳浊液稳定性Tab.4 Emulsion stability test
2.5 试样分析结果
(1)工作曲线
称取0.2000g纯铜六份置于一组100ml容量瓶中,加入5.0ml硝酸(1+1),微热溶解完全除去氮的氧化物,冷却至室温,分别向上述溶液中加入0、1.00、2.00、3.00、4.00、5.00ml银标准液,各加入水使体积均约为80ml,不断摇晃并加入5.0ml盐酸(1mol/L),立即以水稀至刻度,摇匀,用力摇晃1min,放置15min,以补偿溶液为参比于分光光度计波长440nm处3cm比色皿测得吸光度,测得结果如表5所示,绘制工作曲线。

表5 Tab.5
(2)试样分析结果
取0.20000g试样分析,按上述步骤进行操作,结果表6所示。

表6 Tab.6
3 注意事项
(1)要用两次蒸馏水,水中不允许有Cl-,检查方法为:在两支比色管中装入待用的纯水,一管加入5ml AgNO3溶液(1%),另一管不加,两管均用同样的水稀至刻度,摇匀,在黑色纸的底色上由管上方观察比较,加入AgNO3溶液是否有混浊现象,如有,则此水不能用;
(2)用过的比色皿应在稀氨水(1+3)中浸泡一些时间,使附在器壁上的AgNO3沉淀物溶解;
(3)应在稀释至约80ml的稀溶液中,边摇晃边加入Cl-,加完后应立即稀释至刻度并大力摇动约1min;
(4)工作曲线为直线,每点均在曲线上,但曲线不通过“原点”,这可能是比浊法的一种通常现象(快速法测定铜合金中的砷也有类似的工作曲线)。乳浊液的形成,除本身浓度外,还与多种因素有关,此解析应从物质结构和胶体化学的角度进行阐述;
(5)CrO42、Br-、I-会妨碍测定;
(6)比浊法的特点是使被测物质形成极细小的粒子均匀分布于另一物质中,从而形成胶体微粒,其是分子或成千万离子的聚集体。胶体微粒直径(1~100μm)为胶体溶液,微粒<1μm时为真溶液(普通溶液),微粒 >100μm是悬浮液(泥水)或乳浊液(牛奶)。胶体溶液符合比耳定律,被测物质应为痕量较好(曲线通过 0 点),0 ~ 0.6μg/25ml中,为了解决生产需要快速不分离铜,产品在0.03% ~0.90%Ag时,所以本方法只考虑此范围;
(7)光的吸收-比耳定律,胶体溶液应稳定,由于温度(室温不同)影响,所以应用合成标样三点校正,工作曲线稳定,但由于不通过零点,所以如果带标样应与试样含银量相当的标准同时操作,以减少误差。
——一个解释欧姆表刻度不均匀的好方法

