定量蛋白质组学揭示三角鲂和团头鲂响应嗜水气单胞菌侵染机制变化
方献平, 朱丽敏, 刘凯, 阮松林, 许宝青, 谢楠, 蔡丽娟, 刘新轶, 戴瑜来, 冯晓宇, 李忠全*
(1.杭州市农业科学研究院生物技术研究所,杭州310024;2.杭州市农业科学研究院水产研究所,杭州310024)
定量蛋白质组学揭示三角鲂和团头鲂响应嗜水气单胞菌侵染机制变化
方献平1, 朱丽敏2, 刘凯2, 阮松林1, 许宝青2, 谢楠2, 蔡丽娟2, 刘新轶2, 戴瑜来2, 冯晓宇2, 李忠全2*
(1.杭州市农业科学研究院生物技术研究所,杭州310024;2.杭州市农业科学研究院水产研究所,杭州310024)
细菌性败血症对鱼类危害严重,为探究鲂属鱼类不同抗性品种响应病原菌嗜水气单胞菌的抗性机制,以三角鲂(高抗)和团头鲂(易感)肝组织为材料,采用非标记定量蛋白质组学技术分析其在嗜水气单胞菌侵染胁迫后3、10和24 h与对照组0 h(未感染)肝组织蛋白质组的变化,对差异表达蛋白质进行质谱鉴定、相对定量和生物信息学分析。结果显示:三角鲂和团头鲂在嗜水气单胞菌侵染下,分别有46个和29个蛋白质在侵染后各时期的表达丰度相比对照都发生了显著变化。通过基因本体(gene ontology,GO)功能注释发现,相对于团头鲂,三角鲂中氧化还原蛋白质比例从7%增加到13%,且发现一类新的β-免疫球蛋白(β-globin)在各时期分别上调表达了1.64、3.44和1.93倍。生物信息学分析进一步表明,三角鲂在响应嗜水气单胞菌侵染过程中可能特异性地启动了包括戊糖磷酸途径、脂肪酸代谢、亮氨酸代谢途径和β-globin高表达的协同抗性机制,从而抵御病原菌入侵。该研究成果为后续深入揭示鱼病互作分子机制及鲂属鱼类抗病新品种选育提供了重要的前期理论研究基础。
三角鲂; 团头鲂; 嗜水气单胞菌; 定量蛋白质组学
鲂属(Megalobrama)鱼类隶属鲤形目(Cypriniformes)、鲤科(Cyprinidae)、鲌亚科(Culterinae),主要包括三角鲂(Megalobramaterminalis)、团头鲂(Megalobramaamblycephala)、厚颌鲂(Megalobramapellegrini)和广东鲂(Megalobramahoffmanni)4种。三角鲂为鲂属最大个体种类(2+龄),它主要分布于南岭以北至黑龙江各淡水水系,栖息于中下水层,在自然条件下以黄蚬、螺蛳、小虾等为食,为偏肉食的杂食性鱼类,在人工养殖条件下可摄食人工配合饲料。目前,团头鲂为鲂属鱼类中养殖量最大种类。近年来,团头鲂细菌性败血症频发,严重影响养殖效益,而三角鲂养殖过程中未发现有大规模病害出现。因此,三角鲂越来越受到养殖户的青睐,在全国推广面积不断扩大,而团头鲂抗病性差,养殖治病成本高,难以实现无公害养殖。
细菌性败血症是团头鲂的主要病害,流行季节长,发病时往往造成鱼大批病死,病死率高达70%以上。据报道,此病在湖北、湖南、江西、福建、江苏和上海等省市均有流行。鱼体长2.5~15 cm均有发病,2龄以上的团头鲂也有发病,在水温20~33 ℃时发生流行,最适流行水温为27~30 ℃。当水质恶化,水中溶氧低,透明度低,水中总氮、有机氮、亚硝酸态氮和有机物耗氧量高时最为流行,即使水温在12 ℃或34 ℃时也发病。团头鲂感染败血症一般分3个阶段:一是潜伏期。在此期间,鱼的外表未显示出任何症状,活动与摄食正常。潜伏期的长短与水温及细菌浓度有密切关系,水温高,细菌浓度高,潜伏期短;反之,则长。二是前趋期。时间短,仅1~2 d左右,鱼的体色发暗变黑,离群独游,停止摄食。三是发展期。时间长短不一,一般为2~3 d,病鱼表现充血、出血症状而病死。
随着研究的日渐深入及其相关技术的不断完善,蛋白质组学作为当今生命科学的研究热点,已经成为生物学中破译基因功能、贡献于育种程序和探讨相关病害抗性机制的重要途径。如今,蛋白质组学技术已经成为研究外界胁迫诱导动植物响应机制的强有力工具[1-2]。陈强等[3]利用双向电泳技术对陆封型和洄游型香鱼体肾组织进行差异蛋白质组学分析,发现环境应激和能量代谢等层面有明显的蛋白质表达差异;朱佳杰等[4-5]建立和优化了吉富罗非鱼肝蛋白质组双向电泳技术体系,并进一步研究了吉富罗非鱼肝在无乳链球菌胁迫下发生的蛋白质组变化;李明云等[6]研究了低温胁迫下大黄鱼肝蛋白质组变化。由此可见,蛋白质组学技术已经被广泛用于各种鱼类的生长发育和抗逆机制研究,在鱼类的生物化学及其分子机制解析中发挥了重要的作用。
三角鲂和团头鲂同为鲂类,亲缘关系相近,但两者的抗病性差异却很大。因此,本研究试图利用非标记定量蛋白质组学技术比较三角鲂和团头鲂对细菌性败血症病菌响应的蛋白质组表达差异,找出三角鲂对细菌性败血症病菌特异响应的蛋白质,以期阐明其抗病性机制,为今后抗病基因克隆和分子育种及生物抗病制剂研发提供重要研究基础。
1 材料与方法
1.1 实验材料
实验用三角鲂和团头鲂由浙江省杭州市农业科学研究院水产研究所提供,嗜水气单胞菌株分离来自江苏武进某养殖场(经过回归再分离),采用VITEK-32全自动细菌鉴定仪鉴定。
1.2 致病性实验
选择体表无伤的健康三角鲂和团头鲂作为实验对象,分别设5组,每组10尾。将分离纯化的24 h培养物,用无菌0.75%氯化钠溶液洗下菌苔,制成含量为5.0×1010、5.0×108、5.0×106和5.0×104CFU/mL的菌悬液,进行腹腔注射感染,注射剂量0.1 mL/尾。同时设对照组,注射0.1 mL/尾的0.75%氯化钠溶液。置水族玻璃缸饲养24 h,水温控制在(20±2) ℃,观察结果,计算半数致死量LD50,用SPSS 13.0统计软件进行分析。经实验计算确定菌株对三角鲂和团头鲂的半数致死量LD50分别为1.05×108和5.90×106CFU/mL。解剖观察病死鱼,发现肝肿大,肾、肠道充血,与养殖中发病症状基本相同,对照组未见明显异常症状,试验鱼活动、摄食正常。选择健康体形大小均一的三角鲂和团头鲂各20尾,体质量130.5~150.5 g,对鱼体进行嗜水气单胞菌腹腔注射。实验所用致病菌剂量为108CFU/mL,注射量为0.1 mL/尾,分别于感染0、3、10和24 h各取1次样,每次(每个时间点)各取鱼5尾(具体实验线路见图1),在冰上进行活体解剖后取肝组织,放入冻存管称量,液氮冻存带回实验室-80 ℃保存备用。
1.3 肝蛋白质的提取及定量
分别将每次样的5尾鱼的肝组织混合剪碎,尽量去除脂肪组织和结缔组织等非目的组织,加入适量的冰冷磷酸盐缓冲液洗涤2次后,4 ℃,800 r/min离心2 min,去上清液,取沉淀组织放入研钵中,加入适量液氮进行研磨至粉末状。称取0.1 g粉末,加入1 mL裂解液(8 mol/L尿素、10 mmol/L二硫苏糖醇、2 mmol/L乙二胺四乙酸和1 mmol/L苯甲基磺酰氟)中,振荡混匀,4 ℃放置1 h,期间取出振荡3~5次;再于4 ℃,13 000 r/min高速离心20 min以沉淀组织碎片,取上清液后用预冷的丙酮沉淀,再用裂解液复溶即为肝组织总蛋白质,用考马斯亮蓝法蛋白质定量并用聚丙烯酰胺凝胶电泳检测总蛋白质提取质量,分装并保存于-80 ℃备用。
1.4 蛋白质溶液内酶解与除盐
取约100 μg蛋白质样本酶解,按1/10体积加入100 mmol/L二硫苏糖醇(Sigma公司)至最终为10 mmol/L,56 ℃还原反应1 h。冷却至室温后,按1/10体积加入500 mmol/L碘乙酰胺(Sigma公司)至最终为50 mmol/L,避光反应45 min。按1/10体积加入100%的三氯乙酸(Sigma公司)至最终为10%,4 ℃沉淀2 h,用冷丙酮洗3次后离心得沉淀颗粒,溶于100 mmol/L NH4HCO3,超声5 min。在此蛋白质混合物中,按酶与蛋白质质量比1∶50加入胰酶(Promega公司),37 ℃反应12 h,为保证充分酶解,12 h后再按上述比例加入胰酶,37 ℃反应4 h。酶解后的肽段经凯杰公司的C18柱除盐,后进行真空干燥。
1.5 液质鉴定与差异蛋白质相对定量分析
将真空干燥后的肽段,用0.1%甲酸的水溶液复溶至0.5 μg/μL,在转速为13 000 r/min下离心10 min,除去不溶物质,每个组分上样4 μL(约2 μg蛋白质)。采用EASY-nLC 1000纳升级液相色谱和Q-Exactive高分辨率质谱液质联用系统(Thermo Fisher公司),对各个时期的样品肽段进行LC-MS/MS鉴定。流动相A液:含0.1%甲酸(Thermo Fisher公司)的水溶液;B液:含0.1%甲酸的乙腈(Thermo Fisher公司)。线性洗脱梯度(B液):1%~40%,120 min;40%~65%,5 min;65%,保持5 min;65%~1%,1 min;1%,20 min平衡。流速为200 nL/min。Q-Exactive质谱扫描范围m/z为350~1 800,每个一级谱图自动选择3个最强母离子进行二级扫描,每个样品质谱鉴定为3次重复。
鉴于三角鲂和团头鲂为非模式生物,基因组序列未知,所以蛋白质搜库为NCBI中斑马鱼模式生物数据库(http://www.ncbi.nlm.nih.gov/protein,Daniorerio,81514 sequences)进行同源搜库比对,搜库鉴定软件为Proteome Discoverer 1.4,借助Thermo Fisher Sieve 2.2软件对差异表达的蛋白质谱峰强度比对,进行相对定量分析(P<0.05)。
1.6 实时荧光定量PCR分析
为了进一步了解通过蛋白质组学筛查得到的蛋白质对应的mRNA表达情况,我们选取了蛋白质组学中4个蛋白质(NCBI搜库编号分别为18858695、56744251、41056111和50539724)对应的基因进行了mRNA表达水平的分析。在NCBI中利用BLASTp比对挑选每个蛋白质的同源序列,利用CODEHOP软件在保守区设计简并引物(GDP),扩增cDNA中间片段,使用软件Primer 5.0设计5′端和3′端的RACE扩增特异性引物(GSP)。所有引物均由生工生物工程(上海)有限公司合成。本实验中所用到的引物序列及相应的退火温度(Tm)见表1。
提取鱼肝总RNA,合成cDNA第1链,分别采用各基因的简并引物GDP-S和GDP-A扩增cDNA中间片段。利用基因特异性引物5′-GSP和3′-GSP继续进行5′端和3′端的RACE反应。对PCR产物进行电泳、切胶纯化、连接、转化和测序,利用软件拼接各基因全长cDNA序列。根据拼接序列设计全长特异上下游引物GFP-S和GFP-A,PCR扩增各基因全长cDNA序列。
分别提取不同病菌处理样本总RNA,反转录得到cDNA模板。以磷酸甘油醛脱氢酶基因(登记号:BC083506)作为内参,根据内参基因序列和各基因cDNA全长序列设计定量PCR引物GRTP-S和GRTP-A,利用SYBR Green Realtime PCR Master Mix Kit (Toyobo, Japan)在ABI PRISM 7500实时定量PCR仪上进行PCR反应。样本和内参分别设定3个重复,以0 h处理作为对照,以各取样时间点内参基因的表达量为标准来确定目标基因的相对表达量。根据测得的CT值,利用2-ΔΔCT法计算不同侵染时期各基因的相对表达量。

表1 基因RT-PCR引物
1.7 生物信息学分析
利用Uniprot蛋白质数据库(http://www.ebi.uniprot.org)对所鉴定的各蛋白质进行基因本体(gene ontology,GO)注释,依据细胞学组分、分子功能及生物学过程属性,对三角鲂和团头鲂不同时期表达的共性差异蛋白质分别进行GO分析。用MultiExperiment Viewer 4.3软件对差异蛋白质进行差异表达图谱聚类分析。利用KEGG的网络信号数据库(http://www.genome.jp/kegg/pathway.html)对鉴定到的重要差异蛋白质进行匹配,挖掘在病菌侵染下,由差异蛋白质表达变化导致发生改变的重要代谢信号通路(P<0.05)。总体实验方案设计思路如图1。
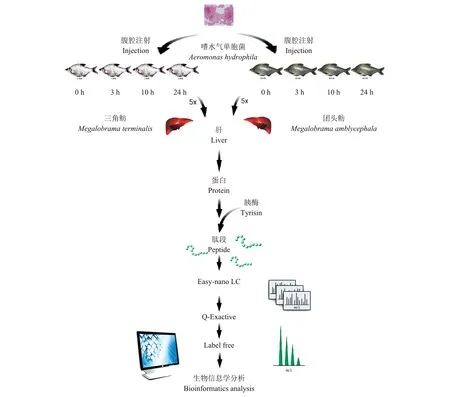
图1 实验设计流程图Fig.1 Flow chart of experimental design
2 结果
2.1 嗜水气单胞菌胁迫下三角鲂和团头鲂肝组织蛋白质组变化
在嗜水气单胞菌的侵染下,三角鲂肝组织蛋白质在侵染后0、3、10和24 h检测匹配鉴定到的蛋白质数分别为138、274、243和152个。其中由于病菌侵染,造成4个时期发生表达变化的共性差异蛋白质为46个(图2A,表2)。相应在嗜水气单胞菌的侵染0、3、10和24 h后,团头鲂肝组织检测鉴定到的蛋白质数分别为192、194、271和125个,其中不同时期共性应答差异蛋白质29个(图2B和表3)。从三角鲂和团头鲂应答蛋白质的分子质量分布范围来看,两者应答蛋白质的分子质量大小分布类似,分子质量大部分也都集中在pI 5~11之间;三角鲂中应答蛋白质则更多倾向于碱性蛋白质,较为明显地聚集成pI 7~9和pI 9~10的2个类群,而团头鲂中应答蛋白质在此范围等电点分布较为均匀(图2C,D)。

A:三角鲂在病菌侵染后鉴定到的蛋白质个数韦恩图;B:团头鲂在病菌侵染后鉴定到的蛋白质个数韦恩图;C:三角鲂不同时间点的46个共性应答蛋白质分子质量及等电点分布示意图;D:团头鲂不同时间点的29个共性应答蛋白质分子质量及等电点分布示意图。 A: Venn chart of the identified proteins in M. terminalis; B: Venn chart of the identified proteins in M. amblycephala; C: Schematic diagram of 46 proteins in M. terminalis based on molecular mass and isoelectric point; D: Schematic diagram of 29 proteins in M. amblycephala based on molecular mass and isoelectric point.图2 三角鲂和团头鲂肝在嗜水气单胞菌侵染不同时间点应答蛋白质鉴定个数情况图Fig.2 Summary charts of total identified responsive proteins of M. terminalis and M. amblycephala infected with A. hydrophila at different time points

表2 三角鲂肝感染嗜水气单胞菌不同时间点的46个共性差异蛋白质表达变化情况
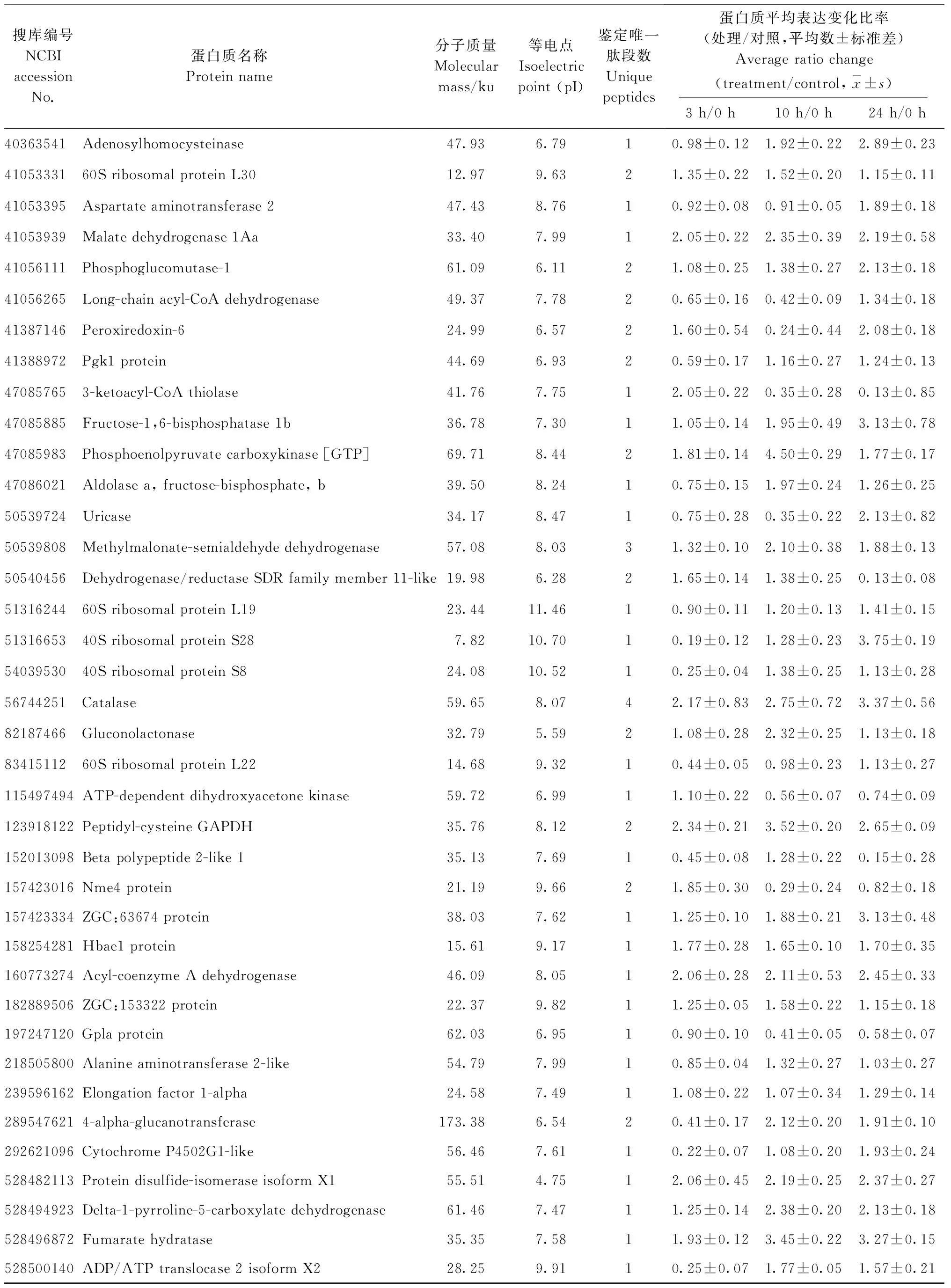
续表2 三角鲂肝感染嗜水气单胞菌不同时间点的46个共性差异蛋白质表达变化情况

表3 团头鲂肝感染嗜水气单胞菌不同时间点的29个共性差异蛋白质表达变化情况
2.2 部分蛋白质mRNA在不同侵染时期的表达情况
为了进一步探索和验证部分发育相关蛋白质mRNA在不同侵染时期的表达变化,我们选取了4个蛋白质进行对应mRNA表达水平分析。实验表明,在不同发育阶段,丙酮酸羧化酶(图3A)、过氧化氢酶(图3B)和尿酸氧化酶(图3D)在转录水平上的变化趋势与蛋白质表达水平呈现较好的一致性,而葡萄糖磷酸异构酶(图3C)在蛋白质和mRNA的表达变化趋势上并不很一致,甚至出现转录水平持续增高,而蛋白质却有表达程度下调的情况。出现这一现象原因可能是部分mRNA经过转录后调控、降解和翻译后修饰等的影响,从而导致了后期蛋白质翻译表达水平的降低。
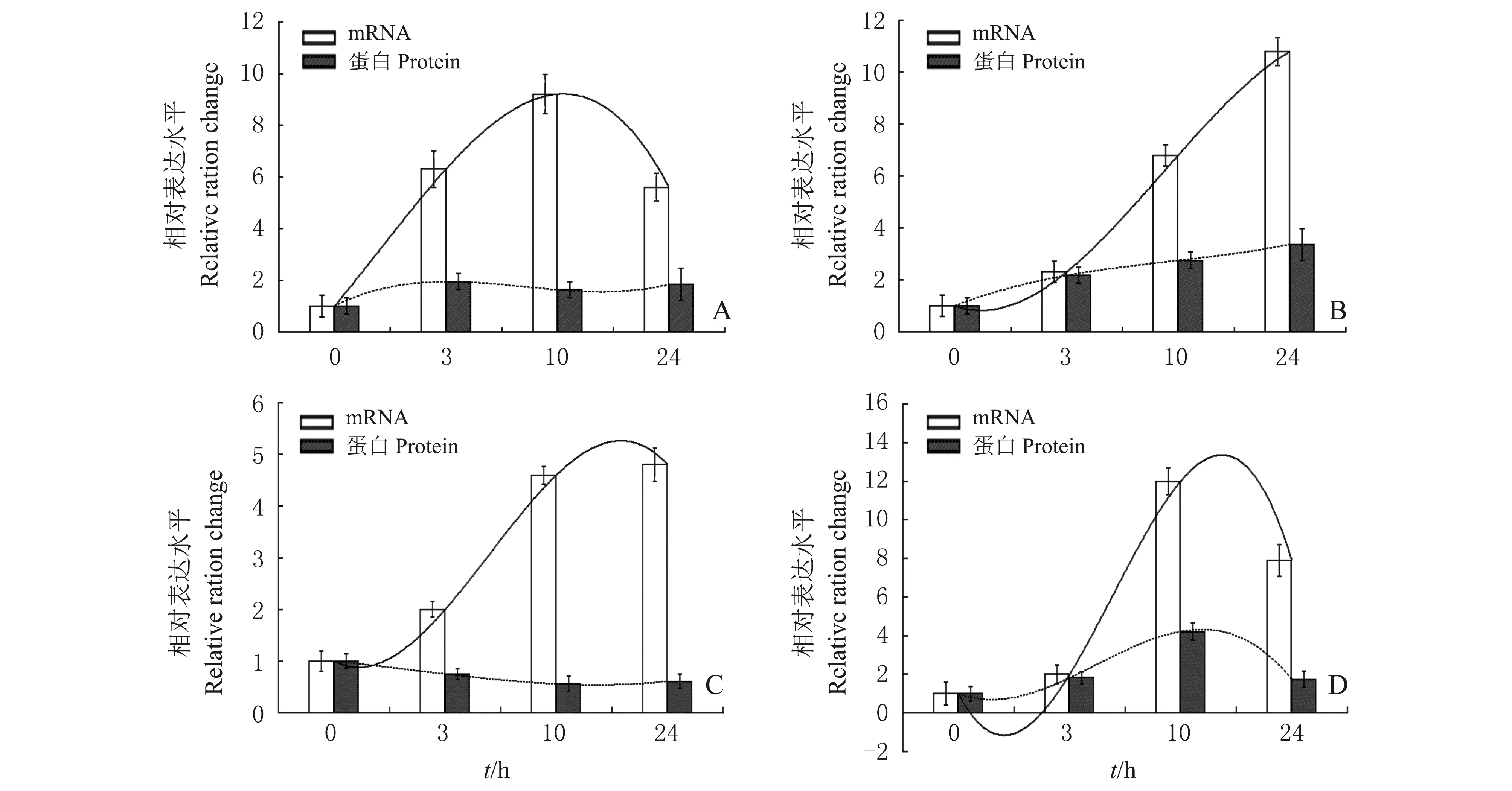
A:丙酮酸羧化酶;B:过氧化氢酶;C:葡萄糖磷酸异构酶;D:尿酸氧化酶.A: Pyruvate carboxylase; B: Catalase; C: Phosphoglucomutase; D: Uricase.图3 4个蛋白质与其对应mRNA的表达变化情况Fig.3 mRNA and protein expression levels of four protein and corresponding genes

图4 三角鲂和团头鲂分别响应嗜水气单胞菌侵染的不同时间点共性应答蛋白质的基因本体分析饼状图Fig.4 Pie charts of common identified responsive proteins of M. terminalis and M. amblycephala infected with A. hydrophila at different time points based on gene ontology
2.3 差异表达蛋白质GO注释功能分析
对三角鲂和团头鲂的差异应答蛋白质进行GO功能注释。在应答蛋白质参与生物学过程中,发现2种鱼类对病菌的响应蛋白质多集中在糖类合成代谢、丙酮酸代谢、碳水化合物合成分解、转录翻译和氧化还原等生物过程中;而高抗品种三角鲂对嗜水气单胞菌的响应中出现了更多地参与氧化还原反应的蛋白质(13%),并且发现了参与低氧反应相关的蛋白质(图4A,B)。在对两者的响应蛋白质进行细胞组分分析时发现,差异蛋白质往往富集在内膜细胞器、核糖体和核蛋白复合体等区域,而团头鲂应答病菌胁迫过程中出现了参与中间纤维组成的响应蛋白质,三角鲂出现的特异应答蛋白质中有15%和3%分别富集在无膜细胞器和珠蛋白复合体中(图4C,D)。在对两者响应蛋白质的分子功能聚类时发现,除了两者应答蛋白质中共同参与的结构分子活性、核糖体结构组成、维生素连接和辅酶连接等分子功能之外,嗜水气单胞菌诱导高抗品种三角鲂中参与血红素连接和氧气转运的相关蛋白质活性发生了变化(图4E,F)。
2.4 差异表达蛋白质表达图谱聚类分析
用MultiExperiment Viewer软件对三角鲂和团头鲂的定量蛋白质组数据进行分析发现:在嗜水气单胞菌的侵染下,团头鲂肝中约40%的蛋白质表达发生上调,包括丙酮酸羧激酶、丙酮酸羧化酶和尿酸氧化酶等;其他蛋白质如葡萄糖基转移酶、丙氨酸-乙醛酸转氨酶和β-球蛋白等表达丰度都发生了下调。而三角鲂肝约达70%的蛋白质表达丰度增强(图5),如有与团头鲂中同样监测到表达丰度上调的丙酮酸羧激酶和丙酮酸羧化酶,以及酰辅酶A脱氢酶和存在于线粒体内的延胡索酸水化酶等,还有部分蛋白质如磷酸葡萄糖变位酶在三角鲂中表达上调,而团头鲂中却呈表达下调趋势;揭示三角鲂在病菌侵染时可能启动了更多的基因参与翻译表达更多的抗性蛋白质,从而抵御嗜水气单胞菌的侵染。
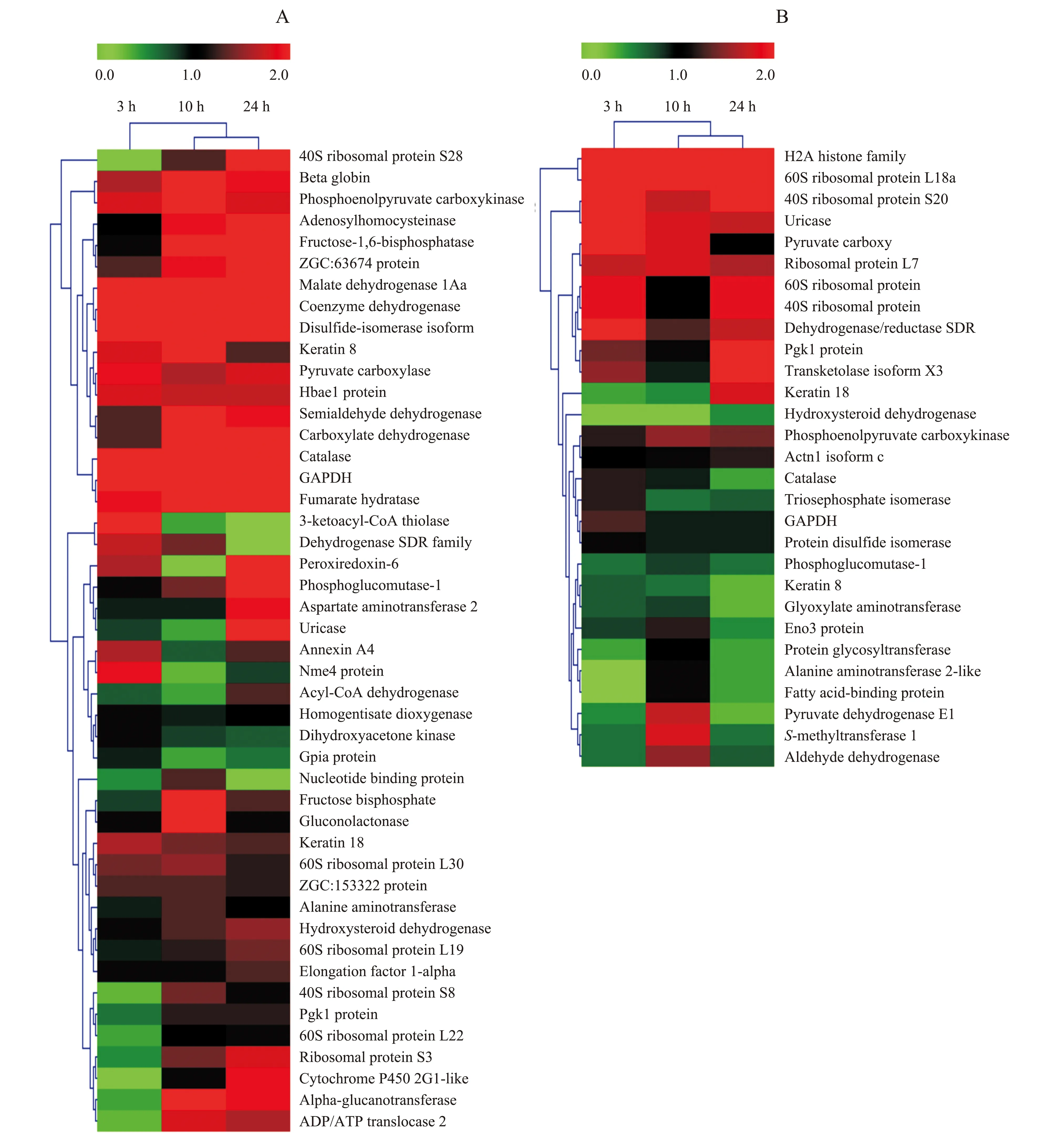
红色表示蛋白质表达上调,绿色表示下调.A:三角鲂在不同时间点46个共性应答蛋白质聚类分析图;B:团头鲂在不同时间点29个共性应答蛋白质聚类分析图。 Red indicates up-regulation, and green indicates down-regulation. A: Clustering chart of 46 proteins in M. terminalis; B: Clustering chart of 29 proteins in M. amblycephala. 图5 嗜水气单胞菌侵染下三角鲂和团头鲂应答蛋白质的聚类表达分析图Fig.5 Clustering charts of common identified responsive proteins of M. terminalis and M. amblycephala infected with A. hydrophila at different time points based on expression level

表示在应答蛋白质中发现参与该代谢通路的蛋白质个数。A:三角鲂在病菌不同时间点共性应答蛋白质团头鲂的响应蛋白质参与的代谢信号路径;B:团头鲂在病菌不同时间点共性应答蛋白质团头鲂的响应蛋白质参与的代谢信号路径。 indicates the number of corresponding proteins found in each pathway. A: Pathway involving in the A. hydrophila-resistence process of M. terminalis; B: Pathway involving in the A. hydrophila-resistence process of M. amblycephala。 图6 嗜水气单胞菌侵染下三角鲂和团头鲂应答蛋白质参与的代谢通路Fig.6 Pathway involving in the A. hydrophila-resistence process of M. terminalis and M. amblycephala
2.5 病菌侵染下不同的代谢信号应答通路
将非标记定量蛋白质组学结果比对KEGG的信号通路发现:在嗜水气单胞菌的侵染下,团头鲂中包括糖酵解与异生、核糖体生成、三羧酸循环和丙酮酸代谢等多条代谢通路都发生了变化(图6)。团头鲂和三角鲂中鉴定到的甘油醛-3-磷酸脱氢酶、葡萄糖磷酸变位酶、磷酸甘油酸激酶、磷酸丙糖异构酶和丙酮酸羧激酶等都参与了糖酵解与糖异生途径,但是大部分在此途径中鉴定到的酶类如葡萄糖磷酸变位酶和磷酸丙糖异构酶在2种鱼类应答病菌侵染过程中表达程度都有所不同。在参与核糖体生成的途径中,团头鲂中鉴定到了核糖体蛋白L7、S14、L18a、S20和S30,三角鲂中发现了核糖体蛋白S3、S19、S23、L18和L19等表达程度都发生了明显变化。在参与三羧酸循环和丙酮酸代谢过程中,2种鱼类都无一例外地发现了丙酮酸羧化酶和羧激酶在病菌侵染后表达程度发生了改变(表2,表3)。更为重要的是,三角鲂中除了上述几条共同的应答途径外,还启动了包括戊糖磷酸途径、脂肪酸代谢和亮氨酸代谢等更多的代谢信号通路,揭示这些信号代谢途径的参与很可能在三角鲂抵御嗜水气单胞菌的侵染过程中发挥的重要作用。
3 讨论
肝是物质代谢、清除毒素和参与各种抗病信号转换的重要器官。肝除了参与各种代谢外,不仅可以促成多种红细胞和血浆蛋白质的生成,起到对外源物质的解毒作用,还可以参与脂肪酸代谢,将脂肪酸运送到其他部位。由于肝良好的代谢能力和解毒作用,本研究利用非标定量蛋白质组学技术探究了不同鲂类抗性品种对嗜水气单胞菌的抗性机制。
研究结果发现嗜水气单胞菌诱使三角鲂调动了更多的基因差异表达,引起了更多的蛋白质丰度上的差异变化,从而在代谢信号通路上采取了更多的病菌防御策略,以下着重对这些病菌侵染下不同响应的代谢通路作一讨论。
3.1 三角鲂和团头鲂在嗜水气单胞菌侵染下共同应答的代谢途径
3.1.1 糖酵解与糖异生途径 糖酵解是指细胞在细胞质中分解葡萄糖生成丙酮酸的过程,而糖异生与糖酵解相反,是由简单的非糖前体转变为糖的系列复杂过程。生物体在病菌侵染过程中,除了核酸、蛋白质等发生快速反应之外,糖类物质也往往参与应答过程中[7-8]。病菌的侵染与宿主对病菌的抗性抵御反应之间所需的能量消耗,必然存在的强烈的竞争关系,碳水化合物代谢在其中会起到重要的生理作用,病原菌的侵入往往使宿主体内的糖含量发生明显改变[9-10]。本研究中发现无论在高抗品种三角鲂还是易感品种团头鲂中,糖代谢是2类鱼采取的最为主要的应答途径之一,揭示糖代谢的变化与2类鱼的抗病反应之间有着密切的关系,也说明糖代谢往往是生物体逆境胁迫过程的重要应答途径之一[11]。
3.1.2 核糖体生成、三羧酸循环和丙酮酸代谢 核糖体是生物体内合成各种蛋白质的重要器官,主要由核糖体RNA和核糖体蛋白组成,核糖体蛋白不仅能参与新蛋白质的生物合成,而且能参与DNA复制、转录和翻译过程中,调控细胞凋亡和转化,积极参与动植物的逆境胁迫过程[12]。本研究过程中发现,2种鱼类肝中有大量的核糖体蛋白(如S20、S30、S23、L18和L19等)表达丰度在嗜水气单胞菌的应答过程中都发生了重要改变,提示核糖体生成很有可能是鱼类参与抗病反应的因素之一。另外,本研究中还发现,三羧酸循环和丙酮酸代谢中有关的酶(丙酮酸羧化酶和羧激酶)活性在病原菌侵染后发生明显改变,很可能意味着这些酶活性的改变,可进一步诱导和激活体内代谢系统,从而增强鱼体的抗病性。
3.2 三角鲂在嗜水气单胞菌侵染下特异应答的代谢途径
3.2.1 戊糖磷酸途径 戊糖磷酸途径是除了糖酵解和三羧酸循环途径以外的另一条非常重要的糖类代谢通路。不同于糖酵解和三羧酸循环,戊糖磷酸途径生成了很多中间产物,如丙糖、丁糖和戊糖等,最后转化为磷酸果糖[13]。在团头鲂和三角鲂的抗病反应中,戊糖磷酸途径开始参与到三角鲂抗病反应中,这一现象的原因很有可能是三角鲂在嗜水气单胞菌胁迫过程中,启动了戊糖磷酸途径在其他糖类代谢途径中的比例,除了供给动物本身抗逆反应所需的能量之外,还生成很多的中间产物,积极紧密地参与到其他代谢过程中起到协同抗性作用,如戊糖磷酸途径中的磷酸核酮糖是合成DNA的原料,磷酸己糖和磷酸丙糖可以重新进入糖酵解途径。
3.2.2 脂肪酸代谢和氨基酸代谢 脂肪酸对于维持细胞膜完整性、调节细胞的免疫功能意义重大。很多研究表明脂肪酸在鱼类的抗病免疫中都发挥着重要作用[14-24]。如脂肪酸值的增大能增加鱼体内的过氧化物酶和超氧化物歧化酶活性[17],往鱼饲料中添加脂肪酸能增加大菱鲆的溶菌酶活性[18],Puangkaew等[21]在虹鳟鱼体内增加脂肪酸的实验中,更是检测到了鱼巨噬细胞中细菌能力的提高和免疫抗体的增加。本研究中发现脂肪酸代谢通路中关键酶乙酰辅酶A脱氢酶在病菌侵染后活性持续增强,而乙醛脱氢酶在经历前期的下调后也开始表达上升,说明在三角鲂肝中脂肪酸代谢通路中相关酶活性的高强度表达,是生成相关脂肪酸产物抵御病菌侵染的积极反应。本研究中发现的参与氨基酸代谢相关的酶类,主要集中在亮氨酸和异亮氨酸的代谢通路上,揭示亮氨酸及其异构体在三角鲂抗病反应中可能发挥一定的作用。
3.3β-球蛋白
目前,对于草鱼、鳜鱼、牙鲆、石斑鱼和斑马鱼等都进行了相应的免疫球蛋白的研究[25-27],免疫球蛋白已经被越来越多的实验证实在鱼类抗病研究中发挥着重要作用[28]。如果能针对免疫球蛋白的抗原表位,制备生产相应的单克隆或多克隆抗体,从而对鱼类免疫器官中产生抗体的细胞或组织进行定位研究,探索免疫器官在疾病防御中的响应机制,对鱼类应用疫苗的研发也具有重要的指导意义。本研究中发现了三角鲂肝内一类重要β-球蛋白在病原菌侵染后各时期分别比对照增强表达了1.64、3.44和1.93倍。β-球蛋白在本研究中高强度表达有着极为重要的科学意义,预示其很有可能是作为嗜水气单胞菌抗病相关的一类免疫球蛋白,对其进行后续深入研究具有一定的价值意义。
4 结论
综上所述,本研究定量分析了不同感抗品种团头鲂和三角鲂感染嗜水气单胞菌前后4个时期肝组织蛋白质组的表达变化,发现了不同抗性鱼类品种之间的差异信号响应通路,预示了不同抗性鱼类品种对嗜水气单胞菌的可能抗性应答机制。本研究结果为进一步深入揭示研究嗜水气单胞菌与鱼类的相互作用机制提供了支撑,为后续鲂鱼类细菌性败血症相关抗体的研制及鱼类抗病品种选育奠定了前期理论研究基础。
[1] Pandey A, Mann M. Proteomics to study genes and genomes.Nature, 2000,405(6788):837-846.
[2] Fang X P, Chen W Y, Xin Y,etal. Proteomic analysis of strawberry leaves infected withColletotrichumfragariae.JournalofProteomics, 2012,75(13):4074-4090.
[3] 陈强,陆新江,黄左安,等.陆封型和洄游型香鱼体肾组织的蛋白质组学分析.生物学杂志,2014,31(2):13-17. Chen Q, Lu X J, Huang Z A,etal. The proteome analysis of the trunk kidney between land-locked type and amphidromous type ayu (Plecoglossusaltivelis).JournalofBiology, 2014,31(2):13-17. (in Chinese with English abstract)
[4] 朱佳杰,沈夏霜,付强,等.吉富罗非鱼肝脏蛋白质组双向电泳技术的建立与优化.西南农业学报,2013,26(5):2122-2126. Zhu J J, Shen X S, Fu Q,etal. Establishment and optimization analysis of two-dimensional electrophoresis system on GIFT tilapia liver.SouthwestChinaJournalofAgriculturalSciences, 2013,26(5):2122-2126. (in Chinese with English abstract)
[5] 朱佳杰,沈夏霜,付强,等.吉富罗非鱼感染无乳链球菌后肝脏组织在不同时期蛋白质组的表达差异.水产学报,2013,37(12):1821-1828. Zhu J J, Shen X S, Fu Q,etal. Proteome analysis of GIFT tilapia (Oreochromisniloticus) liver in different periods afterStreptococcusagalactiaeinfection.JournalofFisheriesofChina, 2013,37(12):1821-1828. (in Chinese with English abstract)
[6] 李明云,冀德伟,吴海庆,等.低温胁迫下大黄鱼肝脏蛋白质组双向电泳分析.农业生物技术学报,2010,18(2):323-328. Li M Y, Ji D W, Wu H Q,etal. 2-DE analysis in liver ofPseudosciaenacroceaduring low temperature stress.JournalofAgriculturalBiotechnology, 2010,18(2):323-328. (in Chinese with English abstract)
[7] Conrath U, Linke C, Jeblick W,etal.Enhanced resistance toPhytophthorainfestansandAltemariasolaniin leaves and tubers of potato plants with decreased activity of the plastidic ATP/ADP transporter.Planta, 2003,217(1):75-83.
[8] Berger S, Papadopoulos M, Schreiber U,etal. Complex regulation of gene expression,photo synthesis and sugar levels by pathogen infect ion in tomato.PhysiologiaPlantarum, 2004,122(4):419-428.
[9] Berger S, Sinha A K, Roitsch T. Plant physiology meets phytopathology: plant primary metabolism and plant-pathogen interact ions.JournalofExperimentalBotany, 2007,58(15/16):4019-4026.
[10] Herbers K, Takahata Y, Melzer M,etal. Regulation of carbohydrate partitioning during the interaction of potato virus Y with tobacco.MolecularPlantPathology,2000,1(1):51-59.
[11] Gupta A K,Kaur N.Sugar signalling and gene expression in relation to carbohydrate metabolism under abiotic stresses in plants.JournalofBioscience, 2005,30(5):761-776.
[12] Warner J R, McIntosh K B. How common are extraribosomal functions of ribosomal proteins?MolecularCell, 2009,34:3-11.
[13] Kruger N J, Schaewen A V. The oxidative pentose phosphate pathway: Structure and organisation.CurrentOpinioninPlantBiology, 2003,6(3):236-246
[14] Blazer V S. Nutrition and disease resistance in fish.AnnalReviewofFishDiseases,1992,2:309-323.
[15] Kiron V, Fukuda H, Takeuchi T,etal. Essential fatty acid nutrition and defense mechanisms in rainbow troutOncorhynchusmykiss.ComparativeBiochemistryandPhysiologyPartA:Physiology, 1995,111(3):361-367.
[16] Chaiyapechara S, Casten M T, Hardy R W,etal. Fish performance, fillet characteristics, and health assessment index of rainbow trout (Oncorhynchusmykiss) fed diets containing in adequate and high concentrations of lipid and vitamin E.Aquaculture, 2003,219:715-738.
[17] Rueda-Jasso R, Conceiçao L E C, Dias J,etal. Effect of dietary non-protein energy levels on condition and oxidative status of Senegalese sole (Soleasenegalensis) juveniles.Aquaculture, 2004,231:417- 433.
[18] 梁萌青,常青,王印庚,等.维生素E及脂肪源对大菱鲆非特异性免疫的影响.海洋水产研究,2005,26(5):15-21. Liang M Q, Chang Q, Wang Y G,etal. Influences of vitamin E and lipid sources on non-specific immunity of turbot (ScophthamusmaximusLinnaeus).MarineFisheriesResearch, 2005,26(5):15-21. (in Chinese with English abstract)
[19] Irshad Ali, Steele J E. Hypertrehalosemic hormones increase the concentration of free fatty acids in trophocytes of the cockroach (Periplanetaamericana) fat body.ComparativeBiochemistryandPhysiologyPartA:Physiology, 1997,118(4):1225-1231.
[20] Pilarczyk A. Changes in specific carp immune reaction caused by addition of fish oil to pellets.Aquaculture, 1995,129: 425-429.
[21] Puangkaew J, Kiron V, Somamoto T,etal. Watanabe Nonspecific immune response of rainbow trout (OncorhynchusmykissWalbaum) in relation to different status of vitamin E and highly unsaturated fatty acids.Fish&ShellfishImmunology, 2004,16:25-39.
[22] Wu F C, Ting Y Y, Chen H Y. Dietary docosahexaenoic acid is more optimal than eicosapentaenoic acid affecting the level of cellular defence responses of the juvenile grouperEpinephelusmalabaricus.Fish&ShellfishImmunology, 2003,14:223-238.
[23] Pisani L F, Lecchi C, Invernizzi G,etal.Invitromodulatory effect ofω-3 polyunsaturated fatty acid (EPA and DHA) on phagocytosis and ROS production of goat neutrophils.VeterinaryImmunologyandImmunopathology, 2009,131(12):79-85.
[24] Lin Y H, Shiau Y S. Dietary lipid requirement of grouper,Epinephelusmalabaricus, and effects on immune response.Aquaculture, 2003,225:243-250.
[25] Zhang Y A, Nie P, Wang Y P,etal. cDNA sequence encoding immunoglobulin M heavy chain of the mandarin fishSinipercachuatsi.Fish&ShellfishImmunology, 2003,14:477-480.
[26] Srisapoome P, Ohira T, Hirono I,etal. Genes of the constant regions of functional immunoglobulin heavy chain of Japanese flounderParalichthysolivaceus.Immunogenetics, 2004,56:292-300.
[27] Cheng C A, John J A C, Wu M S,etal. Characterization of serum immunoglobulin M of grouper and cDNA cloning of its heavy chain.VeterinaryImmunologyandImmunopathology, 2006,109:255-265.
[28] Danilova N, Hohman V S, Kim E H,etal. Immunoglobulin variable-region diversity in the zebrafish.Immunogenetics, 2000,52:81-91.
DifferentialAeromonashydrophilaresistance mechanisms ofMegalobramaterminalisandMegalobramaamblycephalarevealed by quantification proteomics.
Journal of Zhejiang University (Agric. & Life Sci.), 2015,41(5):602-615
Fang Xianping1, Zhu Limin2, Liu Kai2, Ruan Songlin1, Xu Baoqing2, Xie Nan2, Cai Lijuan2, Liu Xinyi2, Dai Yulai2, Feng Xiaoyu2, Li Zhongquan2*
(1.InstituteofBiology,HangzhouAcademyofAgriculturalSciences,Hangzhou310024,China; 2.InstituteofFisheriesResearch,HangzhouAcademyofAgriculturalSciences,Hangzhou310024,China)
Bacterial sepsis is a serious infection for fish. In the past years, the feeding cost ofMegalobramaamblycephalahad been seriously affected by bacterial sepsis. However, bacterial sepsis does not extensively occur during the feeding processes ofMegalobramaterminalis. Therefore,M.terminaliswhich is highly resisted to bacterial sepsis is increasingly favored by farmers.
To study the pathogen resistance mechanism of different varieties ofMegalobramafish in response toAeromonashydrophila, we used label-free based proteomics technology to study the proteome change of the livers ofM.terminalisandM.amblycephalainfected withA.hydrophilaat 0 h, 3 h, 10 h and 24 h.
After identification and relative quantification, 49 and 29 proteins changed at different post-infection time points inM.terminalisandM.amblycephala, respectively. The differentially expressed proteins were deeply analyzed by gene ontology annotation and bioinformatics, and we found that, by comparing withM.amblycephala, the percentage of differentially expressed redox proteins inM.terminalisincreased from 7% to 13%, andβ-globin was up-regulated (1.66, 3.44 and 1.93 times increased at 3 time points). Furthermore, we found thatM.terminalismay specifically induce synergistic pathogen resistance mechanism including the regulation of pentose phosphate pathway, metabolism of fatty acids, leucine metabolism pathway and over-expression ofβ-globin to resist the invasion of pathogens.
In summary, we studied four different stages ofMegalobramaliver proteome expression afterA.hydrophilainfection, and found different pathogen resistance signal response pathway between two fish species, which indicates the resistance mechanism of different fish species afterA.hydrophilainfection. The result is of great benefit to further deeply reveal the molecular mechanisms of fish pathogen interactions and the breeding of pathogen-resistantMegalobramafish varieties.
Megalobramaterminalis;Megalobramaamblycephala;Aeromonashydrophila; quantification proteomics
国家大宗淡水鱼类产业技术体系(CRS20144453)。
联系方式:方献平(http://orcid.org/0000-0001-7461-9170),E-mail:fxpbio@163.com
2015-03-04;接受日期(Accepted):2015-07-23;网络出版日期(Published online):2015-09-18
S 941
A
*通信作者(Corresponding author):李忠全(http://orcid.org/0000-0002-4620-8750),E-mail:hznkylzq@sina.com
URL:http://www.cnki.net/kcms/detail/33.1247.s.20150918.1805.022.html

