离体条件下2种除草剂诱导泸定百合多倍体的比较研究
周玲云,邓 敏,高素萍
(四川农业大学 风景园林学院,成都611130)
植物新品种的选育是一个长期漫长的过程,采取组织培养技术与化学诱变技术相结合的途径能够缩短育种年限。这一技术在天山雪莲[1]、菊花[2]等植物中已获得成功。除了利用传统的秋水仙素作为多倍体诱导剂外[3],除草剂类的诱变剂应用越来越受到重视。除草剂类物质一般通过抑制微管组装从而干扰细胞分裂,因此也可以用作植物多倍体的诱导剂[4]。氟乐灵和二甲戊灵是一种新型除草剂,由于其与植物蛋白亲和力高、动物蛋白亲和力低,从而具有诱导植物多倍体效率高、环境污染小的特点,用此类除草剂已在大蒜[5]、毛新杨[6]、马蹄莲[7]等植物中成功获得多倍体。为保护野生泸定百合种质资源以及培育优良新品种,本试验选用价格低廉的氟乐灵和二甲戊灵作为诱变剂,从细胞学上鉴定其加倍效果,并从形态、气孔特征上比较其诱导效果,为生产上寻求一种经济实用可靠的育种方法。
1 材料和方法
1.1 材 料
试验材料为泸定百合组织培养的无菌生根苗的不定芽。为保证2种试剂处理结果的可比性,材料均选择同一批次,培养基为MS+1.0mg/L 6-BA+0.15mg/L NAA+30g/L 蔗糖+7g/L 琼脂,pH 5.8,温度(25±1)℃,培养条件为光周期12h/d,光照强度为1 500~2 000lx。
1.2 方 法
1.2.1 多倍体诱导方法 根据预备试验,设置氟乐灵(乳油480g/L,镇江建苏农药化工有限公司)和二甲戊灵(乳油330g/L,江苏龙灯化学有限公司)的诱导浓度,采用溶液浸泡法处理材料。浸泡前选取不定芽,剪去叶片,切成大小相同(0.3cm×0.3 cm)的小块。诱变溶液均经过滤灭菌,设置二甲戊灵和氟乐灵(避光)溶液的浓度均为100、200和300 μmol/L,处理时间设置为12、24和36h,用无菌水和质量百分比浓度为0.1%秋水仙素(99%Wolsen秋水仙素粉末)作为对照。每种诱变剂9个处理组合,每种组合处理90个外植体,放置摇床上轻轻摇动,使其与溶液充分接触。处理完毕用无菌水冲洗4~5次,转入培养基(MS+1.0mg/L 6-BA +0.15 mg/L NAA +30g/L蔗糖+7g/L 琼脂,pH 5.8)继续培养,待长势恢复良好,得到完整植株后,用茎尖进行染色体倍性鉴定。
同时,统计形态变异率。与对照相比,以株高、叶片厚度和宽窄、叶色等为指标进行统计。计算公式:
形态变异率=形态变异株数/各处理总数×100%
死亡率(%)=死亡数/接种数×100%
死亡数指接种35d后死亡的总不定芽数,形态变异株数指接种35d后诱变的总不定芽数。
1.2.2 多倍体鉴定 (1)形态特征比较:待各处理植株长出3片新叶(大约45d),选取对照和多倍体植株各20株,用游标卡尺测定其叶长、叶宽(叶片中间最宽部位)、叶厚(叶片中间最厚部位),每指标数据连续测3次,取其平均值作为叶形指数(叶长/叶宽)计算值。
(2)细胞学鉴定:处理后,待植株长出新根,切取对照与形态变异明显植株约2mm 长根尖,采用根尖细胞染色体计数法进行倍性鉴定。具体方法:采用植物染色体常规压片法,上午9:00~10:00选取生长旺盛的1cm 左右长新根,用0.05%秋水仙素室温处理2h后,卡诺固定液(无水乙醇∶冰醋酸=3∶1)在4℃冰箱中固定24h。取出用蒸馏水洗净,放入60 ℃的水浴锅中预热好的1mol/L 盐酸解离液中解离8min后洗净。改良卡宝品红染液染色3 min,压片、显微镜(上海光学XSP-15CA 显微镜,下同)镜检、鉴定、摄像。
(3)叶片气孔特征的观察:诱变处理后第16~24周,撕取加倍苗与对照苗各20株的叶片下表皮制片。具体方法是:上午9:00~10:00,取顶部完全展开的叶子,用镊子撕取下表皮置于载玻片上,加盖玻片,在目镜带测微尺的普通显微镜下取3个视野测气孔长度、气孔宽度、气孔密度、保卫细胞长度和宽度,观察气孔与倍性的关系,明确气孔是否可作为多倍体快速鉴定的一个重要指标。每个样品测定3片叶,每叶重复观测3次,计算平均值,统计并在4倍和10倍显微镜下摄影。
1.3 数据统计
用SPSS 19.0软件进行数据分析,采用单因素方差分析(One-way ANOVA)检验处理的显著性;用LSD 法进行处理间多重比较。用Microsoft Excel 2010制作图表。
2 结果与分析
2.1 2种除草剂诱导下泸定百合的死亡率与形态变异率
与对照(CK)相比,二甲戊灵的不同浓度及浸泡时间均能使泸定百合产生一定程度的变异。以形态变异作为初步统计指标,随二甲戊灵诱变浓度的提高,不定芽死率也明显提高,部分不定芽变黑,生长缓慢或死亡。本试验中考虑到在此浓度时形态变异植株生长良好且变异率较高,可以确定二甲戊灵诱变不定芽的适宜浓度和处理时间为300μmol/L+36h,氟乐灵诱变不定芽的适宜浓度和处理时间为200μmol/L+36h(表1)。
同时试验还表明:氟乐灵诱变后大部分泸定百合不定芽恢复生长与增殖均较困难,继续培养容易出现褐化现象,并最终死亡,而二甲戊灵没有发生此类现象(图版Ⅰ,1A、1B)。与对照相比,秋水仙素的各不同处理也能产生一定程度变异。处理后生长7 d左右一切正常,生长到14d左右就开始出现“烂心现象”,其腐烂部分为褐色(图版Ⅰ,1C)。且随着浓度和时间的增加这种现象就出现的越早、越严重,这可能是秋水仙素对试管苗产生了毒害。在秋水仙素处理浓度和处理时间的最佳组合研究中,以秋水仙素浓度0.1%处理24h诱变率高达34.4%为宜,但死亡率已达40.0%(表1)。
就2 种除草剂与秋水仙素处理的诱变效果比较,形态变异率差异并不显著,但死亡率无论从整体还是个体上,都表现出秋水仙素处理比2种除草剂高,最高浓度处理相同时间秋水仙素死亡率高出除草剂处理17.3%。综合3种诱变剂对泸定百合处理后不定芽死亡率和形态变异率等各项指标的分析结果,初步认为,氟乐灵、二甲戊灵对植物伤害较小,但变异率可达到秋水仙素处理效果。
2.2 多倍体的鉴定
2.2.1 细胞学鉴定 二甲戊灵诱变处理后,产生形态变异的总168株,氟乐灵处理后形态变异177株,秋水仙处理后形态变异194株,抽取各组形态变异数的30%进行染色体制片分析。取变异株与对照株根尖进行染色体制片观察,结果表明:经二甲戊灵、氟乐灵和秋水仙素处理后,植物根尖染色体数目加倍,具有四倍体(2n=4x=48)染色体数特征(图版Ⅰ,2A~2D)。部分变异植株同时存在二倍体和四倍体,或是非整倍体细胞,这是多倍体嵌合现象。
2.2.2 形态特征比较 经细胞学鉴定后,对四倍体植株与无菌水对照植株(非加倍二倍体)的形态学观测发现,四倍体植株的株型矮化,茎粗壮,叶色浓绿,叶片较大、肥厚,叶边呈不规则卷翘、皱缩,生长较为缓慢。图版Ⅰ,3A~3D 和表2是处理后生长45d的二倍体与四倍体植株形态比较。
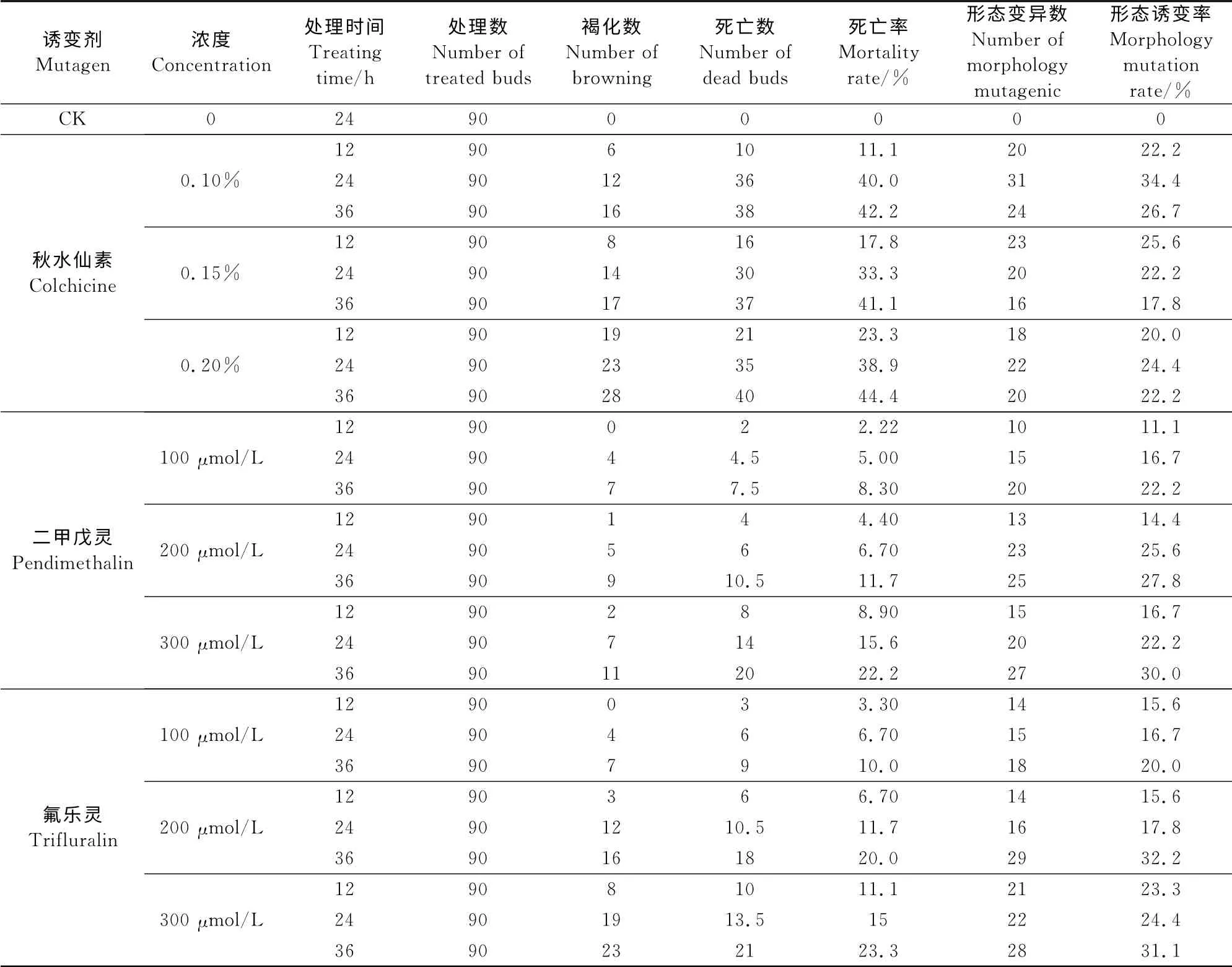
表1 2种除草剂对不定芽死亡率与材料形态变异率的影响Table1 Effects of two herbicides on death rate and variation rate of Lilium sargentiae

表2 泸定百合二倍体与形态变异植株叶片特征比较Table2 Comparison of L.sargentiaeleaf trait between diploid and morphological variation plants
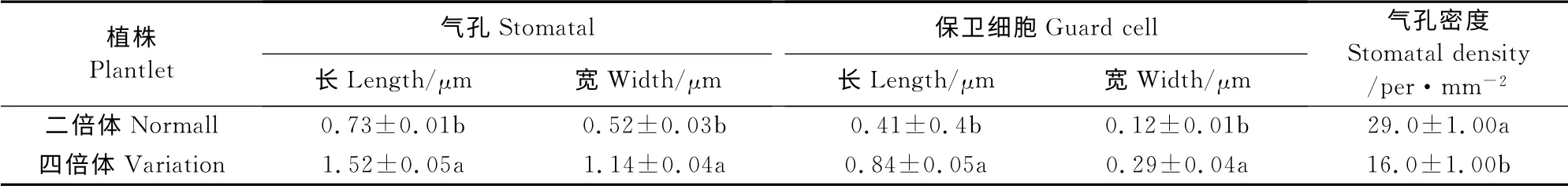
表3 泸定百合二倍体与四倍体植株气孔差异比较Table3 Differences of stomata between diploid and tetraploid L.sargentiae
比较2种诱变剂与秋水仙素处理形态指标的差异,结果显示不显著,但前者处理后约15d就可逐渐恢复生长,而后者需要20d左右,个别还有烂心现象,表明秋水仙素对植物材料的伤害更大。
2.2.3 气孔特征的比较 2种诱变剂处理与秋水仙素处理后气孔特征均表现出相似性,且无显著差异,因此,本特征比较仅选择二甲戊灵处理后叶片的气孔特征为代表(图版Ⅰ,4A~4D、表3)。与二倍体植物气孔特征相比(图版Ⅰ,4A、4B),四倍体植株的气孔(图版Ⅰ,4C、4D)明显增大得多,厚度增加也明显,且有些气孔的外形不规则,四倍体气孔的保卫细胞大小不一(图版Ⅰ,4C),没有二倍体气孔的保卫细胞(图版Ⅰ,4A)那样均匀,同一物镜下数量明显减少,且同一个变异株同一个部位的气孔大小等特征也表现得不尽相同,这种现象一般为嵌合体现象。由此,气孔的变化可以作为多倍体快速鉴定的一个重要指标,其鉴定过程方便又快捷。
3 讨 论
3.1 诱变剂的选择
氟乐灵和二甲戊灵作为诱变剂在大蒜[5]、辣椒[8]、甜瓜[9]、小麦[10]等植物育种中都有应用,而在百合中的应用报道极少,仅有封紫采用氟乐灵诱导百合2n花粉的研究。与秋水仙素相比,硝基苯胺类除草剂除具有低毒价廉的优点,且在本实验中,诱导泸定百合不定芽产生多倍体(四倍体)要优于秋水仙素。此外,2种诱变剂诱导的多倍体无论在细胞学上还是在气孔特征上,均表现出相似性,这与前人的研究大致相似。基于此,全面考虑两种诱变剂在生产中的安全性,成本及效果,可将二甲戊灵、氟乐灵作为秋水仙素的替代品在育种生产中应用。
3.2 倍性的早期鉴定
染色体计数法是鉴定倍性最可靠的方法之一,但难度较大,不易得到典型制片。有学者用扫描细胞光度仪早期检测倍性,但成本昂贵,不易普及[11]。Sari等[12]认为根据保卫细胞的大小、单位面积上的气孔数及保卫细胞中叶绿体数,可以有效区分倍性。本实验中四倍体植株与二倍体相比,单位面积的气孔数量,气孔大小都有显著差异。因此,进一步验证了Sari的方法,将气孔特征作为泸定百合多倍体初步快速鉴定的有效方法。
3.3 处理时间与诱变剂浓度的确定
至于诱变剂处理的适宜时间,以处理材料完全被浸透,并有足够的药量进入生长点细胞为宜。一般来说,处理幼嫩的组织,如萌动的种子及幼苗,处理的浓度要低,处理的时间不少于24h。刘欢等[13]在用二甲戊灵离体诱导虎眼万年青多倍体实验中,二甲戊灵浓度为800μmol/L,处理时间为24h,最高变异率达46.67%;而赵晓潘[14]通过氟乐灵浸泡半枝莲腋芽48h诱导染色体加倍的最适浓度为20 μmol/L,变异率为64.7%。说明二甲戊灵、氟乐灵药液易于进入虎眼万年青、半枝莲、百合等草本植物生长点,从而易获得加倍材料。
确定诱变剂适宜的浓度要综合考虑诱变的效果和对外植体的伤害程度,一般以半致死剂量为参考[15-16]。Bhagwat等[17]则认为通过半致死剂量确定适宜的诱变浓度并不是绝对合适的,还要综合考虑处理后材料的恢复情况、增殖率和再生情况。本试验结果不单一考虑变异率,在同等变异率下,还结合考虑了致死率、恢复时间及其恢复效果。因此,对泸定百合多倍体诱导,诱变剂二甲戊灵300μmol/L与氟乐灵200μmol/L是一个综合各指标后相对适宜的浓度。
3.4 嵌合体问题
试验结果发现,诱变剂处理后直接诱导成功的多倍体大部分均为嵌合体,这与郑思乡等[18]研究结果相同。嵌合体是多倍体育种中一个普遍出现而又难以解决的问题,根据乔永刚等[19]的论述,这可能是因为芽中所有细胞分裂的时间不同步,当幼芽附着有诱变剂溶液时,正在分裂的细胞就发生了加倍,变成四倍体细胞,而此期间该组织中一直处于G0期的细胞没有发生分裂,继续保持着原来的二倍体形式。一旦解除了诱变剂的抑制作用,诱导后的芽中各种倍性的细胞(包括尚未加倍的二倍体细胞)就保持竞争性分裂状态。嵌合体的分离是多倍体育种中的一个关键环节。由于嵌合体中同时存在着二倍体和更高倍性的细胞,倍性高的细胞自身复制和蛋白质合成速度永远不及二倍体细胞快,因此加倍了的细胞分裂速度就放慢,若不及时分离,就会使组织中的多倍体细胞逐渐被二倍体细胞排挤或“淹没”,目前应用最多的方法是通过组织培养技术不断切割继代转接再鉴定来得到纯合多倍体,分离嵌合体。
总之,实验结果表明,2种除草剂在适宜的浓度和时间处理下都能诱导泸定百合试管苗产生多倍体,由原来的二倍体变为四倍体。从形态、结构与染色体三个层次上与传统诱变剂秋水仙素诱变结果无显著差异。因此,综合比较成本、对植物及人的毒性,二甲戊灵和氟乐灵可替代秋水仙素作为诱变剂诱导泸定百合多倍体,是生产中值得推广的诱变剂。

图版Ⅰ 1A.氟乐灵处理后的褐化现象;1B.二甲戊灵处理植株;1C.秋水仙素处理后的“烂心现象”;2A.二倍体(2n=24);2B.二甲戊灵加倍处理(2n=48);2C.秋水仙素加倍处理(2n=48);2D.氟乐灵加倍处理(3n=36);3A.左2株为对照植株,右4株为二甲戊灵处理后变异植株;3B.左为对照叶片,右为氟乐灵处理后变异叶片;3C.左5株为秋水仙素处理后变异植株,右2株为对照植株;4A、4B.二倍体气孔(二甲戊灵处理);4C、4D.四倍体气孔(二甲戊灵处理);每个刻度为1μm。PlatesⅠ Fig.1A.The browning phenomenon by trifluralin;Fig.1B.The pendimethalin treatment plants;Fig.1C.The“rotten heart phenomenon”by colchicine treatment;Fig.2A.Diploid(2n=24);Fig.2B.Chromosome doubled by pendinmethalin(2n=48);Fig.2C.Chromosome doubled by colchicines(2n=48);Fig.2D.Chromosome doubled by trifluralin(3n=36);Fig.3A.Left two of the control plants,right four of the variation pendimethalin treatment plants;Fig.3B.Left two of the control leaf,right two of the trifluralin mutation leaves after treatment;Fig.3C.Left five of the variability colchicine treatment plants,right two of the control plants;Fig.4A,4B.Diploid stomata(conducted by pendinmethalin);Fig.4C,4D.Tetraploid stomata(conducted by pendinmethalin);each scale indicates 1μm.
[1] ZHAO H Y(赵红艳),JIANG L L(江丽丽),MA M(马 淼).Polyploid induction ofSaussureainvolucrataan endangered Chinese Medicinal herb[J].Seed(种子),2012,31(2):21-24,30(in Chinese).
[2] HONG Y H(洪亚辉),ZHU ZH H(朱兆海),HUANG H(黄 璜),etal.On tissue culture and irradiation variation ofChrysanthemum[J].JournalofHunanAgriculturalUnivesity(Nat.Sci.Edi.)(湖南农业大学学报·自然科学版),2003,29(6):457-461(in Chinese).
[3] LIU X L(刘晓露),WANG D X(王冬旭),YANG W R(杨蔚然),etal.Polyploidy induction of aigeiros-luece hybrids ofPopulusby colchicine[J].JournalofAnhuiAgrlculturalSciences(安徽农业科学),2010,38(20):10 532-10 534(in Chinese).
[4] WANG ZH(王 真),CHEN D M(陈道明),LI CH Y(李春燕),etal.Primary studies and identification of polyploid induction inPortulacagrandifloraHook[J].GuangdongAgriculturalSciences(广东农业科学),2010,37(8):74-77(in Chinese).
[5] ZHOU X J(周香君),CHENG ZH H(程智慧),MENG H W(孟焕文).Effects of pendimethalin on garlic chromos-ome doublinginvitro[J].ActaBotanicaBoreali-OccidentaliaSinica(西北植物学报),2009,29(12):2 571-2 575(in Chinese).
[6] HUANG Q J(黄权军),ZHANG ZH Y(张志毅),KANG X Y(康向阳).2npollen ofP.tomentosa×P.bolleanainduced by four antimicrotubule agents[J].JournalofBeijingForestryUnivesity(北京林业大学学报),2002,24(1):12-15(in Chinese).
[7] ZHANG X Q(张锡庆),WU H ZH(吴红芝),ZHOU D(周 涤),etal.Effects of the new herbicide-oryzalin’s concentration and time duration on inducing polyploidy of colouredZantedeschiaaethiopica[J].JournalofYunnanAgriculturalUniversity(云南农业大学学报),2008,23(6):806-810(in Chinese).
[8] HUANG X W(黄新文).Application of trifluralin in chromosome doubling of pepperinvitrotissues[J].JournalofAnhuiAgricultural Sciences(安徽农业科学),2011,39(5):2 706-2 707,2 710(in Chinese).
[9] WEI Y G(魏育国),JIANG J F(蒋菊芳).The preliminary explore on induction of tetraploidin muskmelon with trifluralin[J].ActaAgriculturaeBoreali-Sinica(华北农学报),2006,21(zl):73-76(in Chinese).
[10] ZHANG J Q(张竞秋),LI ZH(李 卓),LI H Y(李海婴).The influence of trifluralin on mitosis of wheat root cells[J].BulletnofBotanicalResearch(植物研究),2008,28(5):552-555(in Chinese).
[11] YAN ZH H(阎志红),LIU W G(刘文革),ZHAO SH J(赵胜杰),etal.Invitroinduction of tetraploid watermelon using dinitroaniline herbicide[J].ActaHorticulturaeSinica(园艺学报),2008,35(11):1 621-1 626(in Chinese).
[12] SARI N,ABAK K,PITRAT M.Comparison of ploidy level screening methods in watermelon:Citrulluslanatus(Thu-nb.)Matsum.and Nakai[J].ScientiaHorticulturae,1999,82:265-277.
[13] LIU H(刘 欢),GAO S P(高素萍),etal.A comparative study of polyploid development induction ofOrnithogalumthyrsoidesby pendimethalin and colchicineinvitro[J].JournalofNuclearAgriculturalSciences(核农 学 报),2014,28(11):1 985-1 992(in Chinese).
[14] 赵晓潘.氟乐灵离体诱导半枝莲多倍体的研究[D].南京:南京师范大学,2013.
[15] HUGDAHL J D,MOREJOHN L C.Rapid and reversible high affinity binding of the dinitroaniline herbicide oryzalin to tubulin fromZeamaysL.[J].PlantPhysiology,1993,10(2):725-740.
[16] ZHANG CH H(张成合),CAO J(曹 军),BAO W K(鲍文奎).Selection and characterization of high pH resistant or salt resistant variants from haploid triticale callus(n=28)[J].ActaBotanicaSinica(植物学报),1986,28(2):137-144(in Chinese).
[17] BHAGWAT B,DUNCAN E J.Mutation breeding of banana cv.Highgate(Musaspp.,AAA Group)for tolerance toFusariumoxysporumf.sp.Cubenseusing chemical mutagens[J].ScientiaHorticulturae,1998,73(1):11-22.
[18] ZHENG S X(郑思乡),ZHANG H L(章海龙),etal.Polyploidy induction andinvitrobulb propagation ofLiliumoriental hybrids[J].JournalofSouthwestAgriculturalUniversity(Nat.Sci.Edi.)(西南农业大学报·自然科学版),2004,26(3):260-263(in Chinese).
[19] QIAO Y G(乔永刚),MA L L(马璐琳),ZHAO X M(赵晓明),etal.Tetraploidy inducement ofCodonopsispilosula(Franch.)Nannf.by colchicine[J].JournalofNuclearAgriculturalSciences(核农学报),2009,23(4):566-571(in Chinese).

