42例舒血宁注射液不良反应/不良事件的文献分析
贺葵邦,卢海儒
(青海省人民医院药学部,西宁 810000)
·药物不良反应与不良事件·
42例舒血宁注射液不良反应/不良事件的文献分析
贺葵邦,卢海儒
(青海省人民医院药学部,西宁 810000)
目的 通过对文献报道的舒血宁注射液致不良反应/不良事件(ADR/ADE)进行分析和归纳,为临床安全合理用药提供参考。方法 检索中国知网(CNKI)中国期刊全文数据库文献,收集2000—2013年舒血宁注射液ADR/ADE的个案报告,并进行统计与分析。结果 共检索到42例舒血宁注射液引起的ADR/ADE报告,男女比例为1:1.47,69.05%ADR/ADE发生在30 min之内。舒血宁注射液引起的ADR/ADE以呼吸系统损伤和皮肤及其附件损伤为主,占全部不良反应例次总数的50.00%以上。结论 舒血宁注射液ADR/ADE比较常见。建议通过生产企业提高药品质量标准,医疗机构加强临床合理用药和提高药物监测水平,药品监管部门应注重ADR/ADE资料收集、报告与评估、警示等措施,确保患者临床用药安全。
舒血宁注射液;药品不良反应;药品不良事件;合理用药
舒血宁注射液是银杏叶提取物制成的中药制剂,主要成分为银杏黄酮苷和银杏内酯,能扩张血管,改善微循环,临床用于缺血性心脑血管疾病,如冠状动脉粥样硬化性心脏病(冠心病)、心绞痛、脑栓塞、脑血管痉挛等。2013年,中国医疗保险研究会发布的一份《2009—2011年全国城镇基本医疗保险参保住院患者中药利用情况分析》报告显示,舒血宁注射液属于内科用药排位第一,使用费用24.93亿元,人均药品费用为1 001元。然而,随着舒血宁注射液临床应用的逐渐广泛,其药品不良反应/不良事件(adverse drug reaction/adverse drug event,ADR/ADE)报道也越来越多[1]。笔者通过对舒血宁注射液所致ADR/ADE病例的相关数据进行归纳分析,探讨ADR/ADE的发生规律和应对措施,以降低ADR/ADE发生率,为临床用药提供参考。
1 资料与方法
1.1 资料来源 在中国知网(CNKI)中国期刊全文数据库以“舒血宁注射液”为主题词进行检索,收集到2000—2013年公开发表的文献中有关舒血宁注射液ADR/ADE的文献共计29篇,包含42例。
1.2 文献纳入及排除标准 文献纳入标准:舒血宁注射液的ADR/ADE个案报道,内容应包括患者基本信息、用药信息和临床表现等。文献排除标准:舒血宁注射液的ADR/ADE汇总分析及文献综述、动物实验研究文献、重复发表的文献。
1.3 方法 采用流行病学和文献计量学方法对文献所载42例患者进行分析,按照世界卫生组织药品不良反应监测中心的规定,统计发生ADR/ADE患者的性别、年龄、用药原因及药物过敏史、用药剂量、给药途径及溶媒、ADR/ADE的临床表现及发生时间、联合用药、预后处理及转归等信息,然后加以汇总分析。
2 结果
2.1 患者性别与年龄 42例ADR/ADE患者中,男17例,女25例,男女患者比例为1:1.47;患者年龄31~85岁,>50岁的患者占69.00%以上。
2.2 用药原因及药物过敏史 42例用药原因分析见表1。多数患者应用舒血宁注射液时遵循药品说明书中规定的适应证,但也有19.05%(“其他”项下8例)的患者存在超适应证用药的情况。42例患者中,有药物过敏史4例,无药物过敏史的18例,其余20例情况不详。
2.3 用药剂量 按照舒血宁注射液说明书规定,舒血宁注射液的用法用量为:肌内注射,一次2~4 mL。静脉滴注,每日20 mL。42例用药情况见表2,用药剂量与说明书完全相符的病例占64.29%。
2.4 给药途径及溶媒 舒血宁注射液说明书规定的给药途径有肌内注射和静脉滴注两种,其中静脉滴注用法为将舒血宁注射液用5%葡萄糖注射液稀释后使用。42例给药途径及给药溶媒情况见表3。
2.5 ADR/ADE的临床表现 42例中,舒血宁注射液引起的不良反应以呼吸系统损伤和皮肤及其附件损伤为主,占全部不良反应例次总数50.00%以上,见表4。
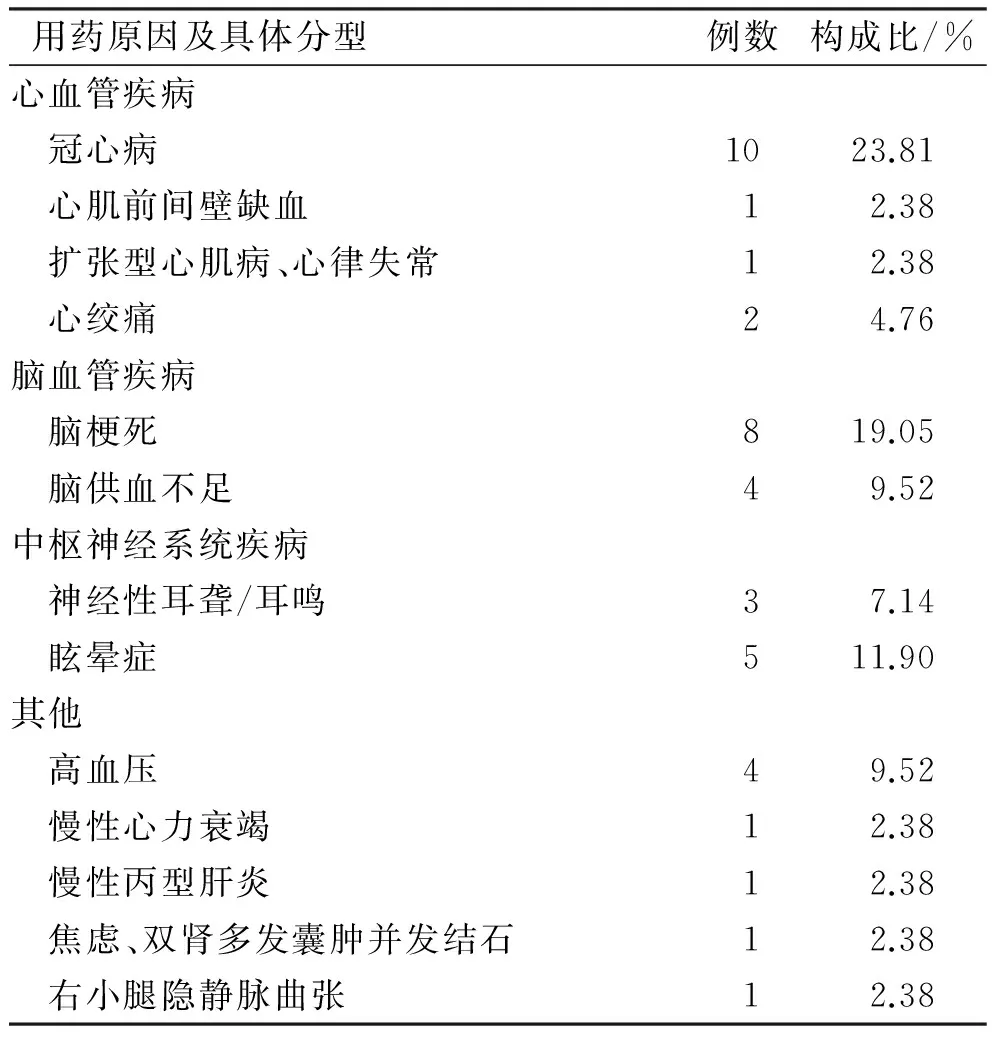
表1 患者用药原因

表2 患者用药剂量情况

表3 给药途径及给药溶媒情况
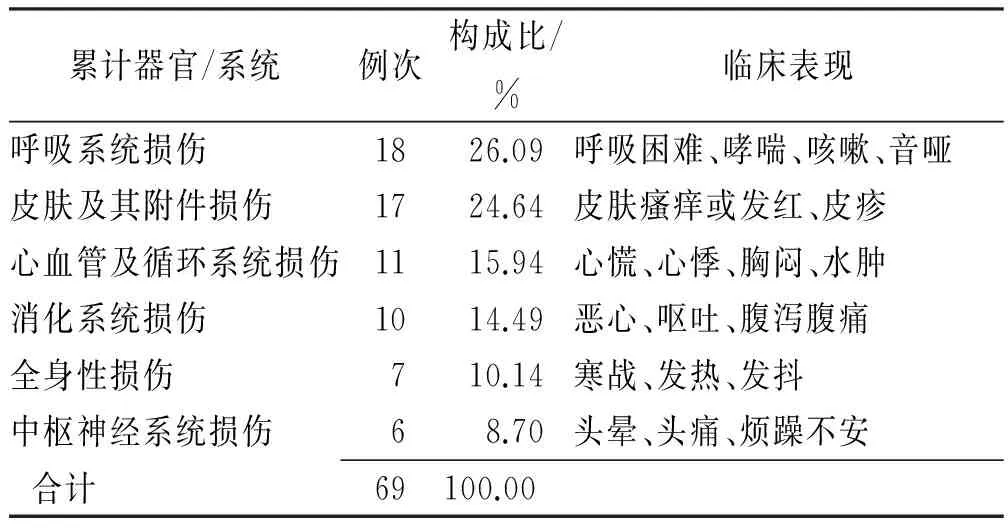
表4 不良反应的主要临床表现
由于有些ADR/ADE累计多个系统/器官,故ADR/ADE例次大于病例数。
2.6 不良反应的发生时间 42例中,不良反应最早出现于输液2 min,最晚出现在连续输液11 d后,既有速发型变态反应,也有迟发型变态反应。ADR/ADE反应发生的具体时间分布见表5,69.05%的ADR/ADE发生时间在30 min之内。

表5 不良反应的发生时间
2.7 联合用药分析 42例中,明确标注联合用药的有6例,明确标注无联合用药的仅2例,其余34例均未标注。6例联合用药的患者在滴注舒血宁注射液期间,均未混合用药;联合用药为缺血性心脑血管疾病的常见药以及抗菌药物。
2.8 处理与转归 42例发生ADR/ADE之后都立即停止输液,严重者进行抗过敏、抗休克等对症治疗,不良反应均得到控制,无死亡病例。
3 讨论
3.1 ADR/ADE发生情况分析
3.1.1 患者年龄 >50岁的患者占69.00%以上,这一方面是因为舒血宁注射液常用于老年患者易发的缺血性心脑血管疾病,如冠心病、脑栓塞等;另一方面是因为老年人肝肾功能减退,对药物的代谢能力减弱,靶器官对某些药物作用的敏感性增高,且老年人存在的原患疾病多、用药复杂和营养欠佳等因素均能诱发ADR/ADE[2]。因此老年人应谨慎使用舒血宁注射液。
3.1.2 用药原因 舒血宁注射液对缺血心肌、受损肝脏再灌注以及缺血区脑组织有保护作用,可改善血管内皮损伤、增加脑血流量、清除自由基、抑制血栓形成、降低血小板黏附率和增强机体细胞免疫活性等[3]。由表1可知,大多数患者的原患疾病均符合舒血宁注射液的用药指征,19.05%患者存在超适应证用药的情况,说明医务人员并未严格遵照说明书要求使用或对患者病情复杂性的重视度不够,应引起临床医务人员的注意。
3.1.3 给药溶媒 中药注射剂的稀释溶媒应严格按照药品说明书选用。本品说明书未提及是否可以选用0.9%氯化钠注射液作为本品的稀释溶媒,但由于部分患者的需要,临床上也将0.9%氯化钠注射液作为本品的稀释溶媒。研究表明[4],舒血宁注射液与0.9%氯化钠注射液、复方氯化钠注射液、葡萄糖氯化钠注射液配伍后,混合液微粒数较高,推测可能是其中盐类的影响所致。因此建议舒血宁注射液在临床使用时最好与5%葡萄糖注射液配伍,且应临用现配,在2 h内使用并且输注时间不宜过长,以保证临床用药安全。也有研究表明采用精密输液器输注中药注射剂可截留大量不溶性微粒,可以减少不溶性微粒进入血液,进而降低静脉炎、变态反应等ADR/ADE的发生,建议静脉滴注时使用精密输液器,可以有效降低其ADR/ADE的发生率[5]。
3.1.4 发生时间 由表5可知,舒血宁注射液引起的不良反应多为速发型,提示用药的初始30 min为重点监测时间,发现异常应立即停药并采取相应措施[6],以最大限度地降低用药风险。
3.1.5 联合用药 《中药注射液临床使用指导原则》中指出:两种以上中药注射剂联合使用,应遵循主治功效互补及增效减毒原则,符合中医传统配伍理论的要求,无配伍禁忌;谨慎联合用药,如确需联合使用时,应谨慎考虑中药注射剂的间隔时间以及药物相互作用等问题;需同时使用两种或两种以上中药注射剂,严禁混合配伍,应分开使用,除有特殊说明,中药注射剂不宜两种或两种以上品种同时共用一条通道。
3.2 ADR/ADE发生机制
3.2.1 药物成分与制剂工艺 银杏叶的化学成分较为复杂,银杏叶提取物中含有160多种成分,主要活性成分为黄酮苷、二萜内酯及有机酸。目前国际上标准银杏叶提取物是按德国Schwabe专利工艺生产的EGb761,其成分包括黄酮(24%)、萜内酯(6%)、原花青素类(7%)、羧酸类成分(13%)等11大类,可控成分比例>37%,特别是规定了有害成分白果酸应控制在0.000 5%以内[7]。我国舒血宁注射液(2 mL)的国家药品标准中规定银杏叶提取物为7.0 mg,其中仅规定含总黄酮醇苷1.68 mg(24%)、银杏内酯0.28 mg(4%),与德国生产的EGb761相比,不仅萜内酯含量较低,而且可控成分比例仅占28%,特别是对有害成分白果酸并未进行限量要求[8]。因此,舒血宁注射液ADR/ADE的发生可能与其可控成分偏少以及对有害成分白果酸未做限量控制等因素有关。
舒血宁注射液制剂工艺较为复杂,在其提取纯化过程中,无法完全除去蛋白质、多肽、挥发油等致敏成分,而灭菌、贮藏过程中的温度、湿度等条件的改变以及制备工艺中稳定剂、增溶剂等辅料的加入也可导致药物成分发生化学反应,产生致敏物质,这些致敏物质可能作为半抗原与血浆蛋白结合诱发过敏[9-10]。因此,中药注射剂制剂工艺中易致敏成分难以彻底去除是导致ADR/ADE发生的一个重要原因。
3.2.2 药理作用 舒血宁注射液通过刺激内皮细胞释放内源性松弛因子,拮抗肾上腺素引起的动脉收缩,能抑制血管紧张肽转换酶的活性而具有扩张血管的作用。因此在用药过程中可能会引起循环系统反应,如静脉炎、心悸等,以及中枢神经系统反应,如头晕、头痛等[11]。
3.2.3 输液操作 舒血宁注射液说明书中明确指出“本品应单独使用,禁忌与其他药品配伍使用”,“静脉滴注时,必须稀释后使用,且应严格控制滴注速度和用药剂量”,“应现配现用,长期静注时应改变注射部位以减少静脉炎发生”。中药注射液临床输液时应严格遵循《中药注射液临床使用指导原则》,注意溶媒的选择、给药剂量和滴注速度的确定,谨慎联合用药,应现配现用,不可与其他药品同瓶输注,两组不同输液之间应“冲管”,从而减少因为输液过程操作不当或应用不合理引起的不良反应。
3.2.4 个体差异 中药注射剂致不良反应与个体差异有一定的关联性。有些患者对舒血宁注射液中某些物质耐受性较差或过于敏感,则容易出现变态反应。中药注射剂的使用同样要遵循辨证施治的原则,根据患者个人体质及差异科学用药,降低不良反应发生率。有药物过敏史的患者,应谨慎使用中药注射剂[12-13]。
3.3 ADR/ADE防范措施
3.3.1 生产企业应严格控制并提高质量标准,积极开展药品上市后安全性再评价研究 舒血宁注射液是治疗心脑血管疾病的有效中药制剂,在国家食品药品监督管理总局网站数据库查询到目前有8个企业生产,规格为2和5 mL。中药注射剂的质量与其安全性有着密切的关系,各生产企业应进一步研究舒血宁注射液的制剂工艺;进一步明确舒血宁注射剂的物质基础,提高质量标准,如控制有害成分白果酸的限量标准等,尽可能提高产品纯度,优化稳定生产工艺,提高产品安全性、稳定性。另外,生产企业还要积极开展舒血宁注射液的上市后安全性再评价研究,揭示临床的安全性风险,进行风险管理,提高风险可控性,切实保证上市药品疗效确切、质量可控。
3.3.2 临床医务工作者应提高合理用药水平 临床医生在应用舒血宁注射剂时首先应询问患者药物过敏史、家族过敏史等,避免ADR/ADE重复发生。其次应遵循药品说明书规定的适应证、用法用量、禁忌、注意事项等,严格掌握用药指征,避免超范围用药引起ADR/ADE发生。第三,中药注射剂宜单独应用,不宜与其他中、西药注射剂配伍使用;另外,已有研究报道舒血宁注射液与呋塞米、阿昔洛韦、注射用奥美拉唑钠、前列地尔注射液、阿莫西林/克拉维酸钾等存在配伍禁忌,特别是与头孢曲松联用可加重其致凝血障碍,临床应用时应注意防范。第四,医护人员要加强用药过程的监护,出现任何不良反应及时停药并采取措施[2]。第五,临床药师应逐渐实施以患者为中心的药学监护模式,深入临床参与查房,向医生和患者提供药学信息或合理用药建议,降低ADR发生率,确保患者治疗安全有效。
3.3.3 注重ADR/ADE相关信息的收集、记录以及资料上报、公布工作 引起药品不良事件的因素较多,有时并不一定是药品的问题,而应该考虑是否规范用药。因此,全面、及时、详细记录ADR/ADE的相关信息,有利于准确评判ADR/ADE,找出主要影响因素。本文收集的42例均存在ADR/ADE信息不完整的情况,很多重要信息的缺失或遗漏使得ADR/ADE分析很难得出规律性的结果。建议医疗机构要严格执行《药品不良反应报告和监测管理办法》的有关规定,临床医护人员在发现ADR/ADE时,应及时和临床药师沟通,及时、准确、详细地记录各项相关信息。各级药品监管部门应该依法对已确认的ADR/ADE采取相关措施,并及时公布ADR/ADE相关信息,指导临床医务工作者合理、安全用药。
[1] 杨德平.154例舒血宁注射液的严重不良反应分析[J].中国药物警戒,2010,7(10):620-622.
[2] 于倩,李忻,金锋.30例舒血宁注射液不良反应文献分析[J].中国药物警戒,2011,8(8):506-508.
[3] 史勇,王雷.舒血宁注射液药理作用研究新进展[J].医学综述,2012,18(10):1555-1557.
[4] 张蓬华,肖淼生,张静,等.舒血宁注射液与五种注射液配伍后的稳定性考察[J].中国药师,2009,12(2):259-260.
[5] 艾青华,魏戌,谢雁鸣,等.舒血宁注射液ADR个案报道文献计量分析[J].中国中药杂志,2013,38(18):3190-3194.
[6] 陈云艳,柯秀芬.舒血宁注射液不良反应287例文献分析[J].环球中医药,2013,6(12):916-918.
[7] 田季雨,刘澎涛,李斌.银杏叶提取物化学成分及药理活性研究进展[J].国外医学(中医中药分册),2004,26(3):142-145.
[8] 朱蓓,张齐,郭桂明.15例舒血宁注射液不良反应/事件分析[J].中国药物警戒,2009,6(6):339-342.
[9] 尚丛笑.24例中药注射剂不良反应报告分析[J].药物流行病学杂志,2010,19(5):267-268.
[10] 王红艳,陈有法.中药制剂致过敏性休克85例分析[J].江西中医药,2006,37(10) :33-34.
[11] 纪立伟,李晓翠,李可欣.26例舒血宁注射液不良反应报告分析[J].中国药物应用与监测,2011,8(4):228-230.
[12] 吕英琦,李彩霞,刁景丽.舒血宁致17例不良反应分析[J].疾病监测与控制杂志,2010,4(6):370-371.
[13] 梁廷燕,刘兰茹,朱虹,等.基于2010~2011年文献中的中药注射剂不良反应/事件分析[J].医药导报,2013,32(6):815-818.
DOI 10.3870/yydb.2015.05.034
2014-03-17
2014-05-18
贺葵邦(1989-),女,青海互助人,药师,硕士,研究方向:医院药学研究,电话:0971-8066280,E-mail:hkb0723@126.com。
卢海儒(1968-),男,青海湟中人,主任药师,研究方向:临床药学与药事管理。电话:0971-8066280,E-mail:315504306@139.com。
R286;R969.3
B
1004-0781(2015)05-0689-04

