贵州产金耳环不同采收期多糖的含量变化及止血作用*
魏学军,夏亚兰,林先燕,李雪营,余跃生
(黔南民族医学高等专科学校药学系,都匀 558003)
贵州产金耳环不同采收期多糖的含量变化及止血作用*
魏学军,夏亚兰,林先燕,李雪营,余跃生
(黔南民族医学高等专科学校药学系,都匀 558003)
目的 观察贵州产金耳环不同采收期多糖含量的变化及止血作用。方法 利用水提醇沉法提取金耳环多糖,经除杂、纯化后,采用紫外分光光度法测定多糖含量;采用剪尾法及玻片法测定小鼠出、凝血时间。结果 不同采收期金耳环中多糖含量具有明显差异,6月采收整体含量较高,为1.78%~1.82%。正常对照组和精制多糖大剂量组小鼠出血时间分别为(6.73±1.21),(4.91±1.58) min(P<0.01);正常对照组和精制多糖中、大剂量组小鼠凝血时间分别为(7.27±2.09),(3.96±1.78),(3.27±1.61) min(P<0.05或P<0.01)。结论 多糖是金耳环止血的活性物质;金耳环用于止血以6月采收为宜。
金耳环,贵州产;采收期;多糖;止血作用
金耳环为马兜铃科植物金耳环(AsaruminsigneD.)的干燥全草,主要分布在我国长江以南各省区,具有温经散寒、祛痰止咳、散瘀消肿、行气镇痛的功能,含黄酮类、氨基酸、糖类和挥发油等成分[1]。在贵州三都水族集聚地,由于疗效显著,采集方便,金耳环被广泛用于风寒感冒、慢性支气管炎、风寒痹痛、跌打损伤、细菌性痢疾等症候的治疗[2-3],《中国水族医药宝典》记载名为骂广瓦[4],民间多用于各种外部损伤引起的出血。研究表明植物多糖可能是止血作用的重要活性成分之一[5-8],因而推测金耳环多糖可能具有一定的止血作用。有关其止血作用的活性成分研究笔者未见文献报道,拟对金耳环多糖的止血作用及不同采收期多糖含量的动态变化进行探讨,初步确定止血作用的物质基础和适宜采收期,为黔产金耳环的开发应用提供理论依据。
1 动物、试药与仪器
1.1 动物 无特定病原体(specefic pathogen free,SPF)级昆明种小鼠,体质量18~22 g,雌雄各半,由贵阳医学院实验动物中心提供,使用许可证号:SCXK(黔)2003-0003,动物合格证号:SCXK(黔)2002-001。饲养在室温 20 ℃、相对湿度 60%的清洁级实验动物房。
1.2 试药 葡萄糖对照品(中国食品药品检定研究院,批号:110833-200904);酚磺乙胺片(张家口云峰制药厂,批号:H13024449,每片0.25 g);其他试剂均为分析纯。金耳环药材于2012年4 ~ 9月采于贵州三都水族自治县境内,经本校药学系朱文仁副教授鉴定为金耳环(AsaruminsigneD.)正品。
1.3 仪器 Cary 100型双光束紫外可见分光光度计(安捷伦科技有限公司);AE 240型十万分之一电子天平(瑞士Mettler公司);DW-60W156型超低温冰箱(青岛海尔集团公司);DHG-9240A型真空干燥箱(上海金山公司);2.0R型大容量低速离心机(德国Heraeus公司)。
2 方法与结果
2.1 金耳环多糖的提取与精制 60 ℃恒温干燥药材,精密称定10 g,石油醚回流脱脂3次。挥去石油醚,在液固比10:1,提取温度80 ℃的条件下加水回流提取2次,每次90 min。合并提取液,滤过,放冷,4 000 r·min-1离心5 min,取上清液,冻融除杂3次,Sevage法除蛋白,活性炭脱色。滤过,滤液用90%乙醇沉淀,静置24 h,除去上清液,沉淀依次用无水乙醇、丙酮、无水乙醚多次洗涤,于60 ℃真空干燥,即得金耳环精制多糖,称质量后计算得率(mg·g-1)[9-10]。
2.2 标准曲线的绘制 葡萄糖对照品105 ℃干燥至恒质量,精密称定10 mg,置100 mL量瓶中,纯化水溶解并定容,配制成100 mg·L-1储备液。精密吸取0.1,0.2,0.4,0.6,0.8,1.0 mL储备液分别加入具塞试管中,加纯化水补至2.0 mL,配制成5,10,20,30,40,50 mg·L-1葡萄糖对照品系列溶液。另取纯化水2.0 mL作为空白对照。向上述葡萄糖系列对照品溶液及纯化水中各加入5%苯酚溶液1.0 mL,混匀,迅速沿管壁加入浓硫酸5.0 mL,摇匀,封口,室温放置30 min。在496 nm波长处测定吸光度,以吸光度(A)为纵坐标,葡萄糖对照品溶液质量浓度(C)为横坐标,绘制标准曲线,得回归方程:A=136.107 2C-0.663 8(r=0.999 6)。实验结果表明,对照品溶液在5~50 mg·L-1范围内与吸光度呈良好的线性关系。
2.3 换算因子的测定 2012年4月15日采收金耳环提取所得的精制多糖于60 ℃干燥至恒质量,精密称取20 mg,置于100 mL量瓶中定容。再吸取上述溶液1.0 mL定容至10 mL,得样品1多糖溶液。吸取上述溶液2.0 mL,按“2.2”项方法显色后,在波长496 nm处测定吸光度,按下式计算换算因子:f=W/(C×D)。式中:W为多糖质量(mg),C为多糖溶液中葡萄糖的浓度(μg·mL-1),D为多糖的稀释倍数。测得换算因子f=1.201 7。
2.4 精密度实验 精密吸取样品1多糖溶液1.0 mL,按测定标准曲线的方法,连续测定6次,其吸光度平均值0.135 3,RSD为0.94%。
2.5 回收率实验 精密吸取样品1多糖溶液1.0 mL共6份,分别置于20 mL试管中,各精密加入10 μg·mL-1葡萄糖标准溶液1.0 mL,按“2.2”项方法操作,计算回收率。结果平均回收率为98.73%,RSD为1.12%。
2.6 同生长期金耳环多糖的含量测定 精密称取不同采收时间金耳环精制多糖各10 mg,定容于50 mL量瓶中,再吸取上述溶液1.0 mL定容至10 mL,摇匀得样品溶液。精密吸取样品溶液1.0 mL,按“2.2”项方法操作,测定多糖质量分数并按下式计算原药材中多糖含量。测定结果见表1。
多糖含量(mg·g-1)=精制多糖得率(mg·g-1)×多糖质量分数(%)。
表1 不同采收期金耳环多糖含量的动态变化

Tab.1 Dynamic changes of polysaccharide content in Asarum insigne from different harvest periodn=3
2.7 金耳环多糖止血作用
2.7.1 供试溶液的制备 酚磺乙胺溶液:取酚磺乙胺粉末2.15 g,加入纯化水100 mL即得。多糖溶液:称取2012年4月15日采收金耳环提取所得的精制多糖适量,使用时加纯化水配成小、中、大3个剂量。
2.7.2 小鼠出血时间的测定 取昆明种小鼠50只,雌雄各半,按数字表法随机分成正常对照组,酚磺乙胺组和多糖小、中、大剂量组,共5组,每组10只,分别灌胃给予0.9%氯化钠溶液,酚磺乙胺和小、中、大剂量(210,420,840 mg·kg-1)金耳环多糖溶液,给药体积为20 mL ·kg-1,每天1次,连续灌胃5 d,末次给药1 h后用解剖剪距小鼠尾尖3 mm处横向剪断,待血液自行溢出计时,每30 s用滤纸吸血1次,直至血液自然停止,所需的时间即为出血时间[11]。
2.7.3 小鼠凝血时间的测定 取昆明种小鼠50只,雌雄各半,动物分组、给药剂量、给药途径均同上。末次给药1 h后用毛细管于小鼠左眼内球后静脉丛取血,滴两滴在玻璃片上并同时计时,每30 s用清洁大头针在玻片上挑血液一次,观察是否有凝血丝,记录从出血至出现凝血丝的时间即为凝血时间[11]。
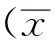
2.7.5 金耳环多糖对小鼠出血、凝血时间的影响 结果见表2。
表2 不同剂量金耳环精制多糖对小鼠出血、凝血时间的影响
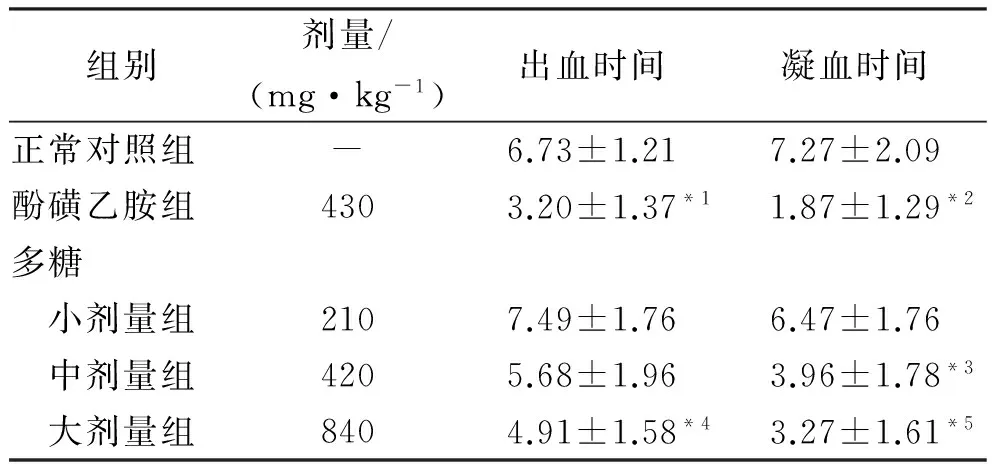
Tab.2 Effect of refined polysaccharide in Asarum insigne at different doses on bleeding and coagulation time of mice min
与正常对照组比较,t=6.11,*1P<0.01,t=6.95,*2P<0.01,t=2.66,*3P<0.05,t=2.89,*4P<0.01,t=4.79,*5P<0.01
Compared with normal control group,t=6.11,*1P<0.01,t=6.95,*2P<0.01,t=2.66,*3P<0.05,t=2.89,*4P<0.01,t=4.79,*5P<0.01
3 讨论
止血作用实验结果表明,与正常对照组比较,酚磺乙胺组和精制多糖大剂量组小鼠出血时间均显著缩短(均P<0.01),精制多糖小剂量组和中剂量组差异无统计学意义(P>0.05);酚磺乙胺组、精制多糖中剂量组及大剂量组小鼠凝血时间均显著缩短(P<0.05或P<0.01),说明金耳环精制多糖具有一定的止血作用,且与剂量相关。考虑到金耳环中尚含有黄酮类、氨基酸和挥发油等化学成分,因而不能确定多糖是其止血作用的唯一活性物质,其止血的作用机制尚不明确,仍需进一步研究。
不同采收期金耳环多糖含量的动态变化实验结果表明,采收时间对多糖含量影响显著。随着植物的生长,多糖含量变化呈先升后降的趋势,以6月下旬采收最高,9月下旬采收最低,6月期间整体含量较高,提示实际应用及药物制剂开发时,如金耳环止血以多糖类成分为主,为使制剂生产获得较多的活性多糖量,建议6月采收为宜。
[1] 中华本草编委会.中华本草(第8 卷)[M].上海:上海科学技术出版社,1999:504-505.
[2] 田庚元,冯宇澄,林颍.植物多糖的研究进展[J].中国中药杂志,1995,20(7):441-444.
[3] 申利红,王建森,李雅,等.植物多糖的研究及应用进展[J].中国农学通报,2011,27(2):349-352.
[4] 司有奇,陆龙辉.中国水族医药宝典[M].贵阳:贵州民族出版社,2007:318.
[5] 王梅,张丽娟,李瑾,等.生地黄汤不同制备方法多糖含量变化及止血作用[J].中国实验方剂学杂志,2010,16(12):115-117.
[6] 武桂娟,刘泓雨,王红,等.白芨多糖对正常小鼠出、凝血时间影响的实验研究[J].黑龙江中医药,2011,(3):49-50.
[7] 杜鹃,许启泰.玉米须多糖的止血作用研究[J].河南医学研究,2011,20(4):398-400.
[8] 王玉挺,宋祖军,王伟,等.多聚糖止血颗粒对兔股动脉出血的止血效果观察[J].现代生物医学进展,2011,10(11):1855-1857.
[9] 魏学军,林先燕,李雪营,等.民族药金耳环总多糖的提取工艺优选[J].中国实验方剂学杂志,2012,18(10):41-44.
[10] 魏学军,林先燕,夏亚兰,等.民族药金耳环多糖的提取和含量测定[J].井冈山大学学报,2012,33(6):86-88.
[11] 李仪奎.中药药理实验方法学[M].上海:上海科学技术出版社,2006:684.
DOI 10.3870/yydb.2015.05.010
Change of Polysaccharide fromAsaruminsigneinGuizhouDuring Different Harvest Period and the Hemostatic Effect of Polysaccharide Study
WEI Xuejun,XIA Yalan,LIN Xianyan,LI Xueying,YU Yuesheng
(DepartmentofPharmacy,QiannanMedicalCollegeforNationalities,Duyun558003,China)
Objective To study the change of polysaccharide fromAsaruminsigneinGuizhouduring different harvest period and its hemostatic effect. MethodsAsaruminsignepolysaccharide was extracted by water isolation and alcohol precipitation.We measured the polysaccharide content by UV spectrophotometry and detected the bleeding and clotting time by tail cutting and slide methods in mice. Results There was significant variation in polysaccharide ofAsaruminsigneat different harvest time, which was at a higher level in June(1.78%-1.82%).The bleeding time in mice of normal control group was (6.73±1.21) min,and that in mice treated with refined polysaccharide at high dose was (4.91±1.58) min,the difference between two groups was statistically significant(P<0.01).The clotting time in mice of normal control group was (7.27±2.09) min,and that in the refined polysaccharide at middle and high dose groups was (3.96±1.78) min and (3.27±1.61) min,respectively(P<0.05 orP<0.01). Conclusion The polysaccharide is an active hemostatic substance inAsaruminsigneand the optimum harvest time of it is in June for the clinical use.
AsaruminsigneinGuizhou;Harvest time;Polysaccharide;Hemostatic effect
2014-03-10
2014-05-12
*贵州省优秀科技教育人才省长专项资金项目[黔省专合字(2010)156号];贵州省黔南州科技局资金项目[黔南科合社字(2010)18号]
魏学军(1972 -),男,四川成都人,副教授,学士,从事中药及民族药开发应用研究。电话:0854-8308038,E-mail:qndywxj@163.com 。
R282.71;R285.5
A
1004-0781(2015)05-0606-03

