预处理制备苯甲酸淀粉酯及性能*
杨小玲,王 珊,张引莉
(咸阳师范学院 化学与化工学院,陕西 咸阳 712000)
淀粉因糊化温度高、易凝沉、稳定性差等缺点限制了其广泛应用,需对其进行改性处理,优化某方面性能甚至形成新的特性,如糊化温度降低,疏水性、凝沉稳定性、热稳定性及冻融稳定性提高等,可广泛应用于纺织、食品、造纸及医药等领域[1-3]。其中酯化是最普遍的改性方法之一,但是物理/化学方法亦有其不足,如取代度不高、且伴有副产物产生、产率低、反应条件苛刻等。
为了获得较高取代度的产物,通常在有机溶剂及酶催化条件下制备淀粉酯,但是亦存在酯化反应时间较长,反应温度较高,造成酶催化易失活,酯化效率不高,在酯化的过程中伴随着淀粉相对分子质量的下降等不利情况[4-6]。其中采用吡啶作为反应介质具有用量少、淀粉降解程度小的优点,同时吡啶还起到了催化反应的作用,合成化合物具有聚合条件温和、高结构选择性、可再生性和无毒环保等优点。
淀粉属于天然的多晶态聚合物,外层主要为结晶区域且非常牢固,对水及化学试剂有较强的抵抗能力,反应往往只在颗粒表面进行,试剂很难进入内部。因此,可以通过酸、碱或酶对淀粉活化预处理来破坏淀粉的颗粒结构,以提高淀粉进一步反应活性和效率[7-9]。
作者结合酯化前酶解预处理及酯化中催化2种方式相结合的协效作用来制备苯甲酸淀粉酯。以可溶性淀粉为原料,选取3种活化方式对淀粉预处理,然后以苯甲酰氯为酯化剂与活化淀粉酯化反应制备苯甲酸淀粉酯。通过IR、SEM及XRD对产物结构和形貌进行表征,并通过测试产物的糊黏度、乳液稳定性,考察淀粉酯化后的物化性能。
1 实验部分
1.1 试剂与仪器
可溶性淀粉:四川省彭州市军乐化工厂;N,N-二甲基甲酰胺:天津登丰化学品有限公司;吡啶:天津风船化学试剂有限公司;苯甲基酰氯:上海同方精细化工有限公司;尿素:西安化学试剂厂;二甲基亚砜:成都金山化学试剂有限公司,以上试剂均为分析纯;胰酶:BR,国药集团化学试剂有限公司。
IRPrestige-21型傅里叶变换红外光谱仪:日本岛津公司;Quanta200型扫描电子显微镜:荷兰Philips-FEI公司;X射线衍射仪:日本理学D/max-ⅢA型。
1.2 淀粉预处理
(1) 碱-尿素活化淀粉:称取30 g可溶性淀粉,溶解于100 mL水中,加入已配置好的pH值在8~9的NaOH/尿素溶液中,30 ℃下搅拌反应1 h,用乙醇洗涤,离心,干燥。
(2) 酸介质活化淀粉:称取30 g可溶性淀粉,分散于100 mL质量分数为1%的盐酸溶液中,50 ℃搅拌反应1 h,用0.1 mol/L NaOH溶液调节至中性,用乙醇洗涤,离心,干燥。
(3) 胰酶活化淀粉:称取30 g可溶性淀粉,溶解于配置好的100 mL pH值为6.8的胰酶溶液中,37 ℃搅拌反应30 min,调节溶液至中性,用乙醇洗涤,离心,干燥。
1.3 苯甲酸淀粉酯的制备
准确称取定量活化淀粉,溶于N,N-二甲基甲酰胺溶液中,加入到带有回流装置的三颈瓶中,40 ℃下搅拌至溶解,加入少量吡啶和定量的苯甲酰氯,一定温度下反应一定时间,用无水乙醇反复洗涤,干燥。
1.4 苯甲酸淀粉酯取代度测定
称取样品2 g,置于250 mL碘量瓶中,加入40 mL水混匀,加3滴酚酞指示剂,然后用0.1 mol/L NaOH溶液滴定至微红,再加25 mL 0.5 mol/L NaOH溶液,盖上瓶塞,振荡30 min进行皂化,再用0.5 mol/L HCL标准溶液滴定至红色退去,记录滴定消耗体积,同时做空白实验对照,记录滴定消耗体积,按如下公式计算酯化淀粉的取代度[10]。
(1)
(2)
式中:A为苯甲酸淀粉的每个葡萄糖单元上含的苯甲酰基的质量分数;V0为滴定原淀粉时所用的盐酸的体积;V1为滴定酯化淀粉时所用盐酸的的体积;c为滴定时盐酸标准溶液的浓度;m为苯甲酸淀粉样品的质量。
1.5 淀粉糊黏度测定
称取0.4 g绝干苯甲酸淀粉酯于烧杯中,加入60 mL二甲基亚砜溶解,转移至100 mL容量瓶中,用二甲基亚砜定容至刻度,摇匀,过滤后放置于25 ℃的恒温槽恒温备用,用乌氏黏度计测定黏度。计算公式如下。
(3)
式中:ηt为相对黏度;t为溶液流出时间;t0为溶剂流出时间。
1.6 乳液稳定性测定
将不同取代度的苯甲酸淀粉酯分别溶于一定量蒸馏水,放入沸水浴中加热并继续搅拌糊化,得到一定质量分数的淀粉酯乳,再加入一定量的油相[V(环己烷)∶V(三氯甲烷)=3∶1]搅拌均匀。将乳状液静置1 h后,以3 000 r/min离心5 min,记录试管中乳化层的高度h1(mm)和乳液总高度h2(mm),乳液稳定性用如下方式表示。
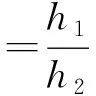
(4)
2 结果与讨论
2.1 淀粉活化方法的选择
对淀粉进行预先活化处理的目的是提高淀粉反应活性,选取3种活化方式:酸解、碱解和酶解(见表1),对3种活化淀粉的产率,及分别与苯甲酰氯的酯化产物的产率及取代度进行对比。

表1 活化方式对苯甲酸淀粉酯产率及取代度的影响
从表1可见,酸解后得到的活化淀粉产率相对较高,但酯化产率却最低;NaOH-尿素水解的活化产率低,酯化产率高;胰酶活化淀粉产率及酯化产率均处于中间,但酯化产物的取代度最高。综合考虑,选取胰酶活化淀粉进行后续酯化反应实验。
对原淀粉、酶解淀粉及酯化淀粉表面形貌进行扫描,结果见图1。
图1从上到下依次为原淀粉、酶解淀粉和苯甲酸淀粉酯的SEM照片。从图1可见,原淀粉颗粒多为形状不规则的多角形,表面光滑;酶解淀粉颗粒形状与原淀粉相似,不同的是表面出现微孔,是由于淀粉在酶介质中发生水解形成的;而酯化淀粉产物苯甲酸淀粉酯颗粒形状更趋于球形,表面粗糙。后两者的分散性更好,与淀粉改性后氢键遭到破坏,溶解度增大,酶解、酯化只在淀粉颗粒表面进行相关。



图1 原淀粉、酶解淀粉及苯甲酸淀粉酯的SEM照片
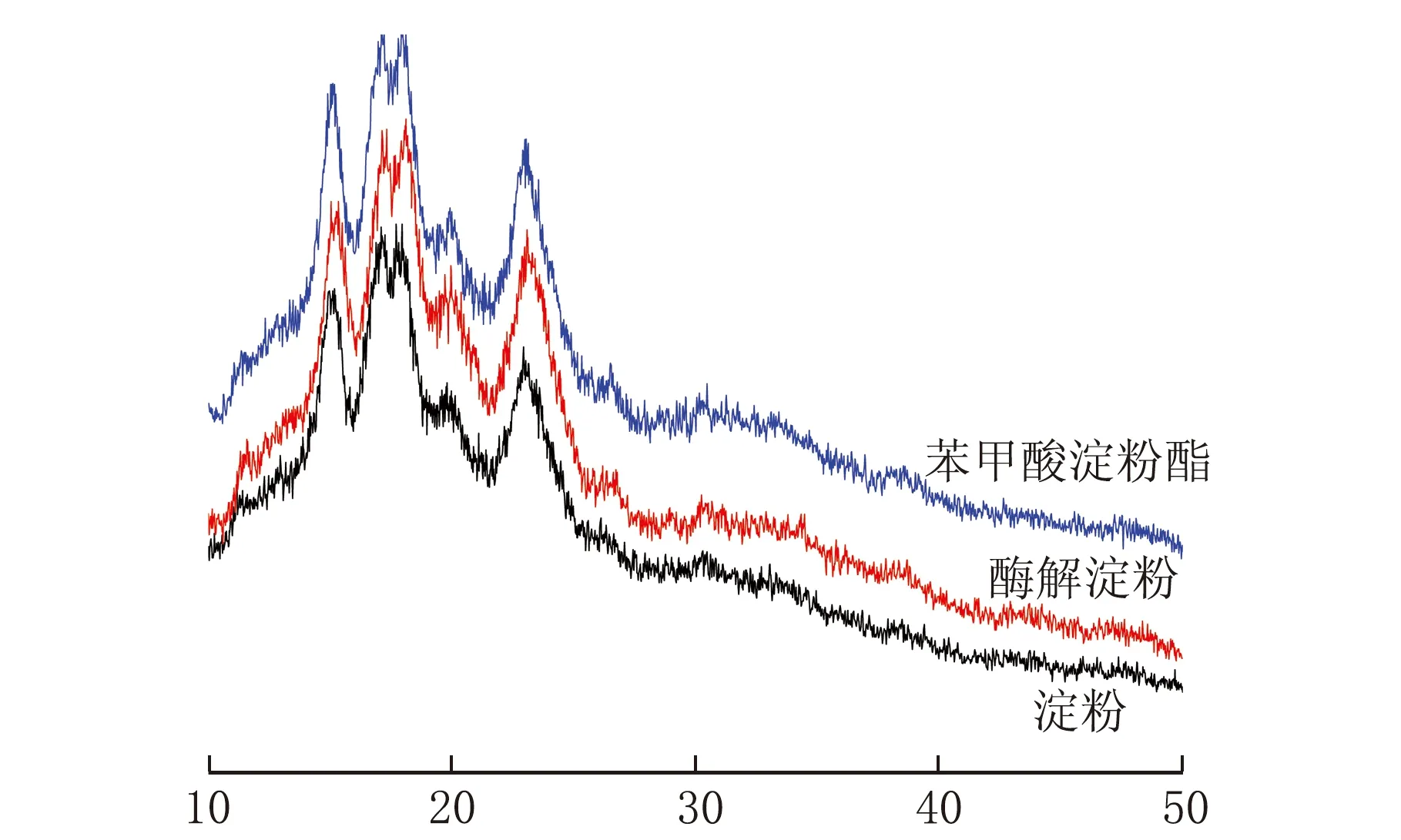
原淀粉、酶解淀粉及苯甲酸淀粉酯的X-射线衍射图谱见图2。
2θ/(°)图2 原淀粉、酶解淀粉及苯甲酸淀粉酯X-射线衍射图谱
图2表明,3条图谱的2θ均在15°、17°、18°、19°和23°附近有强的衍射峰,其中17°和18°附近的衍射峰为相连的双峰,衍射峰峰型和峰位基本上没有发生变化,说明淀粉颗粒的晶型也无明显变化,仍是A型晶体。经酶解和苯甲酰氯酯化后,衍射峰的高度都稍有提高,这说明反应对结晶区产生了不足以破坏淀粉颗粒晶体结构的较小程度的破坏作用,同时说明了酶解和酯化发生在无定型区。
原淀粉、酶解淀粉和苯甲酸淀粉酯红外图谱见图3。
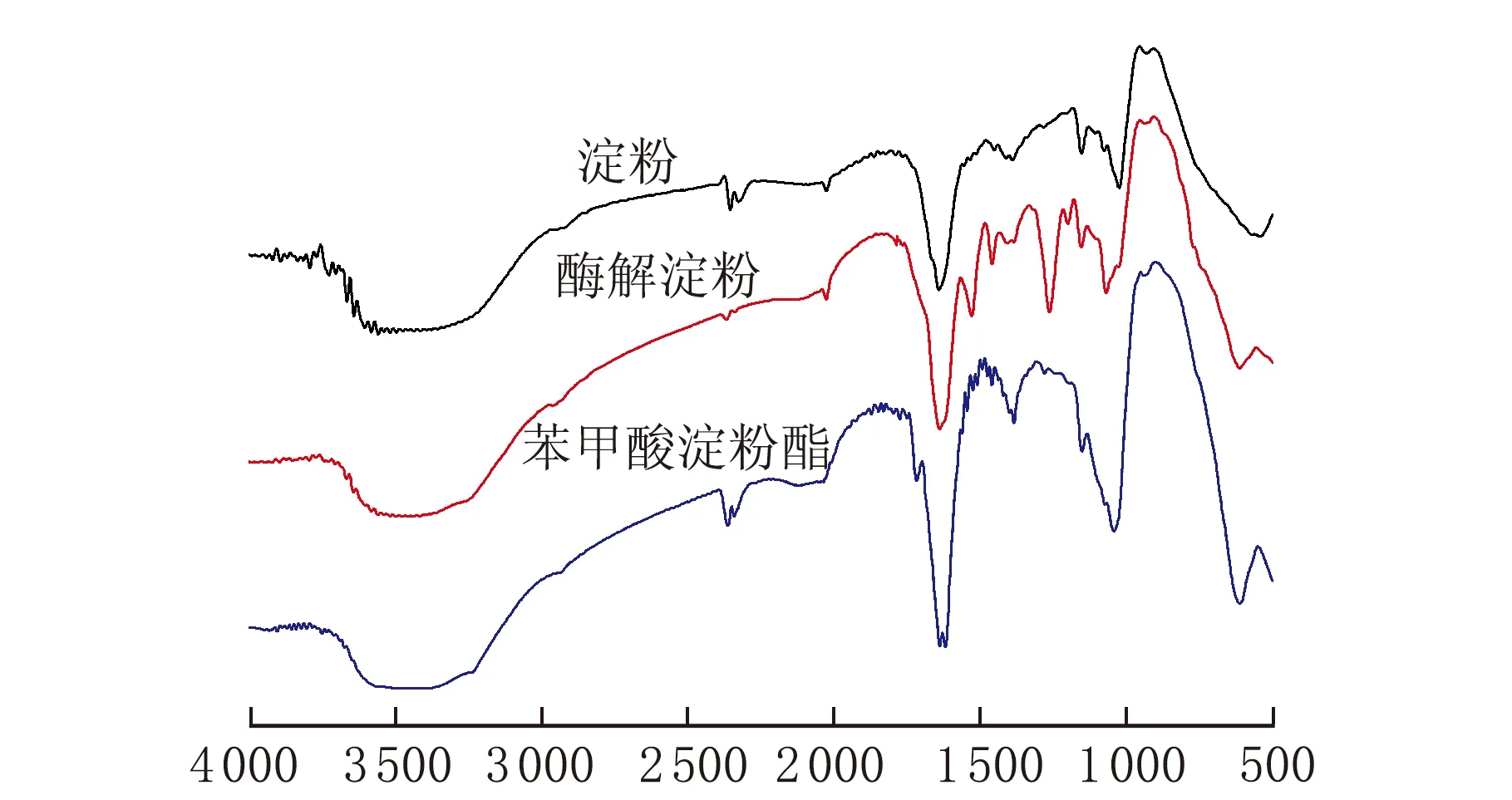
σ/cm-1图3 原淀粉、酶解淀粉及苯甲酸淀粉酯的红外图谱

2.2 取代度对酯化淀粉黏度的影响
淀粉的黏度是指淀粉糊化后的抗流动性。不同取代度的苯甲酸淀粉酯的相对黏度结果见图4。
从图4可见,当苯甲酸酶解淀粉酯取代度DS<0.201 2,苯甲酸酶解淀粉乳黏度较苯甲酸原淀粉乳的低,之后随取代度的升高黏度增大。酶解淀粉酯黏度低于未进行预处理的原淀粉酯是由于酶解预处理导致淀粉相对分子质量降低造成的;之后酶解淀粉乳黏度随取代度的升高而增大原因是:一方面酯化反应引入的苯甲酰基团代替了较小的羟基,减弱了淀粉分子之间的氢键作用力,且大分子取代基团间的排斥力加重了淀粉分子间缔合力的减弱,使淀粉更容易吸水膨胀;另一方面酯化后引入了疏水基团,随着酯化取代度的增加,接到淀粉分子上的疏水基团增多,支链数增加,空间位阻增大,淀粉分子形成更加复杂的网络状结构,因而黏度升高。
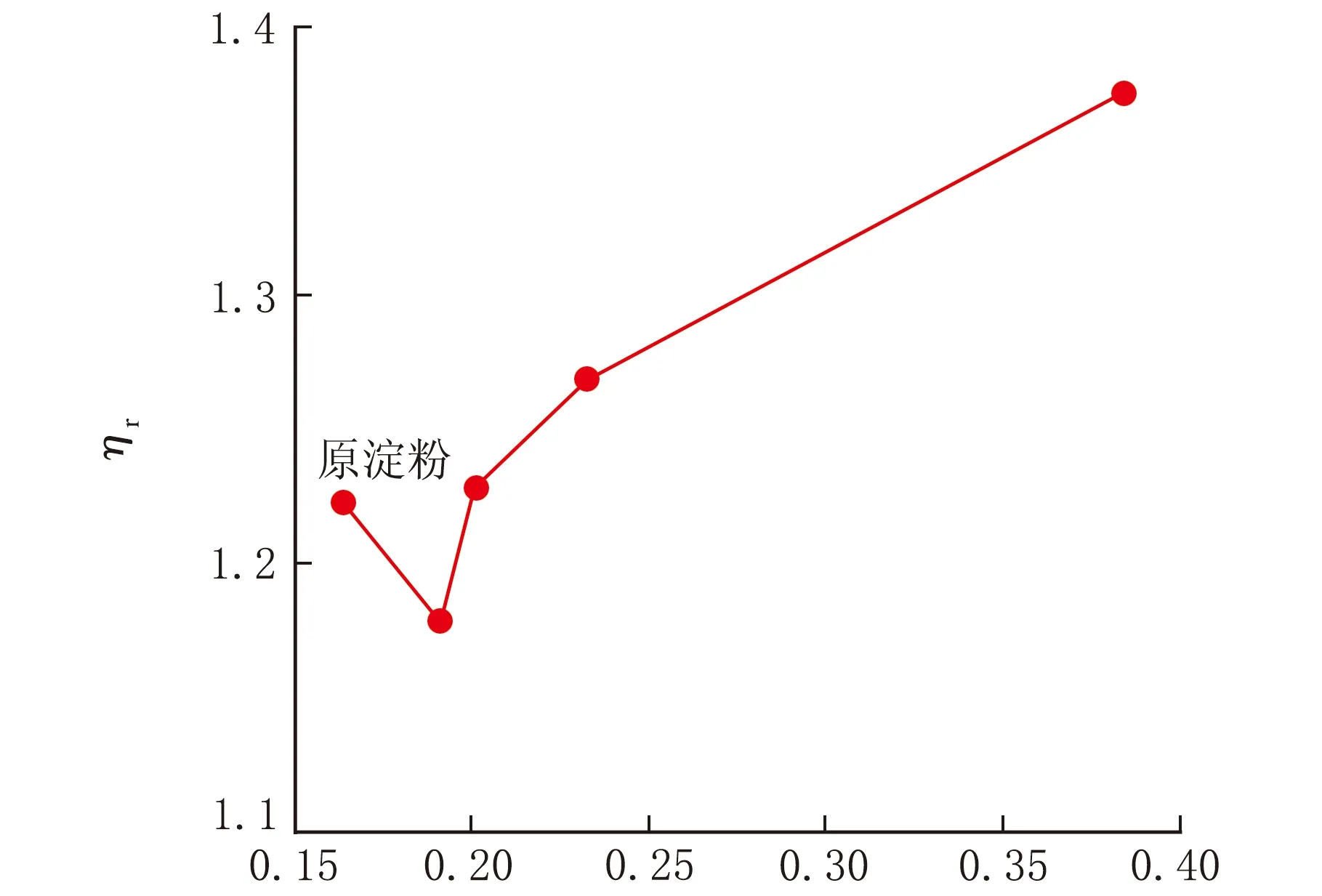
DS图4 淀粉酯取代度与黏度的关系
2.3 苯甲酸淀粉酯乳液稳定性的结果分析
淀粉分子结构具有众多的羟基,亲水性很强,苯甲酰基的引入即在淀粉分子中引入疏水性基团,形成既有亲水基又有疏水基结构,具有一定的表面活性,因此测试其在水油乳液体系的稳定性。
以质量分数为1%的苯甲酸淀粉酯,V(环己烷)∶V(水乳液)=2∶1,比较苯甲酸原淀粉酯(DS=0.164 3)和不同取代度苯甲酸酶解淀粉酯对油水体系的乳化性能,结果见图5。
由图5可见,苯甲酸酶解淀粉酯的乳化稳定性较苯甲酸原淀粉酯(h1∶h2=58.645%)的大,并随着苯甲酸淀粉酯取代度的增加而增强(h1∶h2=76.67%)。乳液稳定性与淀粉酯取代度及相对分子质量均有关,首先是随着取代度增大乳液稳定性上升,其次,可见从苯甲酸原淀粉酯到酶解淀粉酯的乳液稳定性先呈现缓慢上升这是因为酶解淀粉表面出现很多微孔及通道,比表面积增加,溶解性提高,与苯甲酰氯的酯化效率提高,亲水的淀粉分子结构上同时接上了疏水基,且取代度越大,疏水基团的数量越多,从而使油滴之间产生更大的空间位阻,因此乳液稳定性更好。
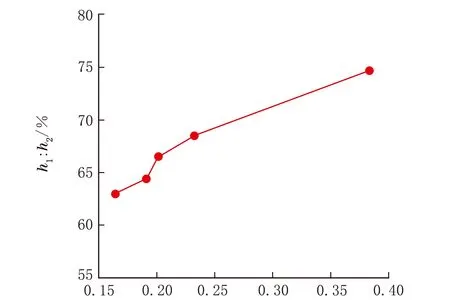
DS图5 淀粉酯取代度和乳液稳定性的关系
3 结 论
3种预处理方法均可提高淀粉的反应活性,其中,酶解淀粉酯取代度最高。苯甲酸酶解淀粉乳黏度大于苯甲酸原淀粉,且随取代度增大上升,以苯甲酸酶解淀粉酯为乳化剂制备的环己烷/水乳液稳定性高于苯甲酸原淀粉,并随取代度增大而升高。
[ 参 考 文 献 ]
[1] X Wang,W Y Gao,L M Zhang,et al.Study on the morphology,crystalline structure and thermal properties of yam starch acetates with different degrees of substitution[J].Science in China Series B:Chemistry,2008,51(9):859-865.
[2] C K Simi,T Emilia Abraham.Hydrophobic grafted and cross-linked starch nanoparticles for drug delivery[J].Bioprocess Biosyst Eng,2007,30:173-180.
[3] S D Zhang,Y R Zhang,H X Huang,et al.Preparation and properties of starch oxalate half-ester with different degrees of substitution[J].J Polym Res,2010,17:43-51.
[4] 林凯,辛嘉英,王艳,等.非水相酶法催化长链脂肪酸淀粉酯反应研究进展[J].食品科学,2014,35(3):276-279.
[5] 汪秀丽 张玉荣 王玉忠.淀粉基高分子材料的研究进展[J].高分子学报,2011,1:24-37.
[6] 张水洞.酯化淀粉的研究进展[J].化学研究与应用,2008,20(10):1254-1259.
[7] Varavinit Saiyavit.Modification and utilizations of sago starch[J].Biotechnol Sustainable Unil Biol Resour Trop,2000,14:36-48.
[8] 黄祖强,陈渊,钱维金,等.机械活化对木薯淀粉醋酸酯化反应的强化作用[J].过程工程学报,2007,7(3):501-505.
[9] 刘粼,王镨.酶法前处理对磷酸酯淀粉制备工艺及产品性能的影响[J].中国食品学报,1998,2(1):5-9.
[10] 唐洪波,马冰洁.低取代度马铃薯醋酸酯淀粉合成工艺及性能研究[J].精细石油化工进展,2004,5(3):44-47.
[11] 郭俊杰,康海岐,孙海波,等.蛋白酶水解马铃薯淀粉对于淀粉化学性质改变的研究[J].食品工业科技,2014,35(23):149-153.
[12] 王德庆,冯吉,付群,等.N-正十八烷基麦芽糖酰胺的合成工艺及其性能研究[J].高校化学工程学报,2009,23(6):1018-1023.
[13] 朱香云.异淀粉酶酶解玉米淀粉的性质及其成膜性研究[D].天津:天津大学,2010:21.
[14] 程宇.利用黄豌豆淀粉酶法制备抗性淀粉的研究[D].哈尔滨:哈尔滨商业大学,2014:53.

