液相丙烯脱CO催化剂的研究
王 育,马天石,刘海江,戴 伟,彭 晖
(中国石化 北京化工研究院,北京 100013)
液相丙烯脱CO催化剂的研究
王 育,马天石,刘海江,戴 伟,彭 晖
(中国石化 北京化工研究院,北京 100013)
采用共沉淀法制备了CuO/ZnO,CuO/ZnO/ZrO2,CuO/ZrO2催化剂,采用XRD,XPS,H2-TPR,HRTEM等方法对催化剂进行了表征,在微反装置上评价了催化剂在气相乙烯脱CO和液相丙烯脱CO反应中的性能。催化剂评价结果和表征结果显示,CuO与ZrO2的协同效应比CuO的晶体尺寸效应对催化剂的活性具有更重要的影响;在两段反应器之间增加脱水干燥器后,催化剂的吸附容量明显提高,可能是因为避免了微量水和CO2对催化剂脱CO的不利影响。在反应压力2.5 MPa、反应温度50 ℃、空速50 h-1的条件下,CuO/ZrO2催化剂可将液相丙烯物料中含量为2.4×10-6(w)的CO深度脱除至30×10-9(w)以下。
氧化铜;氧化锆;脱一氧化碳;液相丙烯;净化催化剂
CO是聚烯烃催化剂的重要毒物,有瞬间阻聚作用,会使催化剂的用量大幅增加,并提高聚烯烃中灰分的含量,从而降低产品的质量。20世纪90年代中国石化北京化工研究院开发的CuO/ZnO催化剂用于脱除气相乙烯中的微量CO,可将入口含量小于等于5×10-6(w)的CO脱除至含量小于等于1×10-7(w)[1]。目前聚合催化剂的活性已大幅提高,从当时的第三代发展到第四代和第五代,对脱CO催化剂也提出了更高的要求:1)提高脱除深度至出口CO含量不大于1×10-9(w);2)降低反应温度,以适应企业为提高经济效益和减少CO2排放对节能降耗的需求,为此需要开发更低温度下脱CO的催化剂;3)目前聚丙烯工艺的反应压力一般不高于3.5 MPa,在此压力下丙烯保持液相的温度一般不高于80 ℃,如果气化会产生相变从而影响系统操作的稳定性,因此需开发脱除液相丙烯中微量CO的催化技术[2-3]。
工业上常用铜氧化物催化剂脱除微量CO,反应机理是物料中的CO与铜氧化物催化剂中的晶格氧发生反应生成CO2。尽管习惯上称铜氧化物为催化剂,实质为吸附剂。该反应为非催化气(液)固相反应,不属于催化反应[3]。因为铜氧化物催化剂参与了反应,其中损失的晶格氧无法在反应过程中得到补充,这一点区别于一般催化反应的redox机理[4]。对于铜氧化物催化剂脱除CO表面反应机理仍存在不同的观点,如CuO-ZnO固溶体、非化学计量比CuOx、CuO晶粒效应以及CuO与ZrO2协同效应[2]等。研究者以Cu-Ag催化剂[5]和Au催化剂[6]等为例,论述了CO2和H2O对CO氧化反应的影响,但对于物料中痕量水蒸气的存在,至今尚未引起研究者的关注。
本工作采用共沉淀法制备了CuO/ZnO,CuO/ ZnO/ZrO2,CuO/ZrO2催化剂,将催化剂用于深度脱除气相乙烯和液相丙烯中的CO;并采用XRD,HRTEM,XPS,H2-TPR等方法对催化剂进行了表征,探讨了CuO/ZrO2催化剂具有优良催化活性的原因。
1 实验部分
1.1 催化剂的制备
采用共沉淀法制备催化剂。首先将硝酸铜、硝酸锌和/或硝酸锆溶解于水中得到混合溶液,将该混合溶液加入到碳酸钠溶液中,经沉淀、老化后得到沉淀物;该沉淀物经抽滤、洗涤至Na2O含量小于0.05%(w),将得到的滤饼在400 ℃下焙烧6 h,压片成型即得CuO/ZnO(标记为CZ)、CuO/ ZnO/ZrO2(标记为CZR)、CuO/ZrO2(标记为CR)催化剂。催化剂经破碎、筛分,取40~60目的试样进行活性评价。
1.2 催化剂的表征
采用美国Quantachrome仪器公司的Nova 3000e型物理吸附仪测定试样的比表面积。采用荷兰Philips公司的X'Pert MPD型X射线衍射仪表征催化剂的物相结构,Cu Kα射线,扫描范围2θ=20º~80º。采用英国Thermo VG公司的Sigma Probe型X射线光电子能谱仪测定试样的结合能,Mg Kα射线,以本体污染碳的C ls结合能(284.16 eV)为标准对试样进行校正。采用美国Micromeritecs公司的Autochem 2900型全自动化学吸附仪对试样进行H2-TPR表征,程序升温范围25~400 ℃,还原气为体积组成10%H2-90%N2的混合气,流量为50 mL/min。采用美国FEI公司的Tecnai 20型高分辨透射电子显微镜测试催化剂的微观形貌。
1.3 催化剂的活性评价
催化剂的微反评价装置如图1所示。微反评价实验在不锈钢反应器内进行,反应器内径8 mm,催化剂堆密度为1.5 g/mL。气相乙烯脱CO反应只采用一段反应器;液相丙烯脱CO反应采用两段反应器,一段和二段反应器的催化剂装填量均为1 mL。反应段设3个测温点,分别测量催化剂床层的上、中、下3点的温度。

图1 微反评价装置的示意图Fig.1 Schematic diagram of experimental setup with a micro-reactor.
反应前后物料的组成用美国瓦里安公司的CP3800型气相色谱仪分析,该色谱仪配有Poraplot填充柱、甲烷化炉、FID和反吹柱系统。色谱柱可分离物流中的CO,CO2,CH4,C2H4,C3H6等,其中,物流中大量的C2H4或C3H6保留时间较长。为了提高分析速度,可在CO,CO2,CH4等组分出峰后通过柱反吹系统将其他组分(如C2H4或C3H6)反吹出来。由于FID无法检测CO和CO2,因此待测物流需先经过甲烷化炉(炉温为380 ℃)将其中的CO和CO2转化为CH4,然后用FID(温度为300 ℃)进行检测。该色谱仪的CO最低检测限为1×10-7(w)。当反应后物料中的CO含量小于1×10-7(w)时,可切换至美国Ametek公司的TR3000A型微量CO分析仪进行分析,该仪器的CO最低检测限为1×10-10(w)。液相丙烯中的微量水采用英国Shaw公司的Super Dew型在线露点仪分析,检测限为1×10-6(w)。聚合级丙烯的组成为:丙烯纯度大于等于99.75%,ρ(H2O)≤2 mg/m3,ρ(O2)≤2 mg/m3,ρ(CO)≤0.03 mg/m3,ρ(总硫)≤1 mg/ m3,ρ(COS)≤0.02 mg/m3,ρ(As)≤0.03 mg/m3,ρ(PH3)≤1 mg/m3,ρ(CO2)≤5 mg/m3,ρ(C2H4)≤ 100 mg/m3。
气相乙烯脱CO反应:气相乙烯与CO混合,经检测反应器入口物流中CO含量稳定在2.4×10-6(w)左右后开始反应,反应压力为常压,反应温度为50 ℃,空速为10 000 h-1。
液相丙烯脱CO反应:1)液相丙烯与CO混合,经检测反应器入口物流中CO含量稳定在2.4×10-6(w)左右后开始反应,反应压力2.5 MPa,反应温度50 ℃,空速50 h-1。2)在一段和二段反应器之间增加一个干燥器,干燥器中装填50 mL的分子筛用于脱水和CO2,保持反应条件不变,进行液相丙烯脱CO反应,其中,一段和二段反应器之间的水含量采用Super Dew型在线露点仪分析,CO2含量采用CP3800型气相色谱仪分析。
催化剂的穿透时间:当物流出口CO含量大于30×10-9(w)时的反应时间;吸附容量:在穿透时间内单位质量的催化剂所转化的CO的质量。
1.4 催化剂的物化参数
催化剂的物化参数见表1。
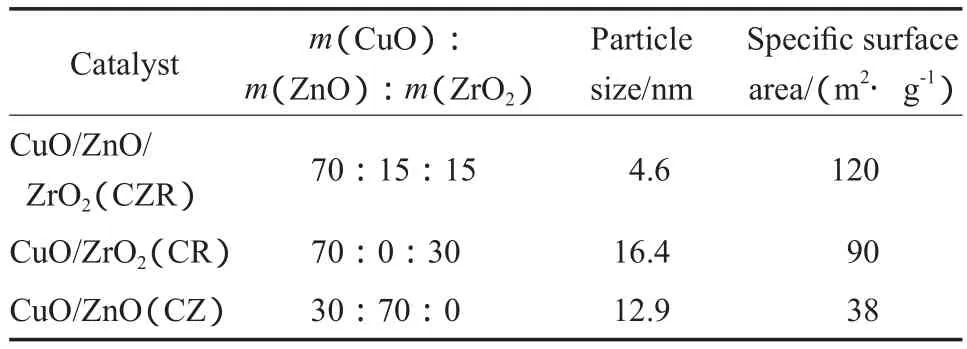
表1 催化剂的物化参数Table 1 Physicochemical parameters of catalysts
2 结果与讨论
2.1 催化剂活性的评价结果
2.1.1 不同催化剂的气相乙烯脱CO性能的对比
通过气相乙烯脱CO反应评价不同催化剂的性能,实验结果见图2。由图2可见,催化剂的活性由高到低的顺序为:CR>CZR>CZ;不同催化剂均能将气相乙烯原料中的CO含量脱除至30×10-9(w)以下,达到聚合级乙烯深度脱除CO的指标。CZ,CZR,CR催化剂的穿透时间分别为96,300,450 h,吸附容量分别为1.98,5.93,8.89 mg/g。

图2 不同催化剂脱气相乙烯中CO的效果对比Fig.2 Comparison of the removal results of CO in gas ethylene on the different catalysts.
2.1.2 液相丙烯脱CO的评价结果
采用CR催化剂,在无干燥器和在一段和二段反应器之间增加一个干燥器的情况下,进行液相丙烯脱CO实验,实验结果分别见图3和图4。由图3可见,在约54 h内CR催化剂可将一段反应器出口CO脱除至含量小于30×10-9(w),而二段反应器出口的CO含量在约94 h内均小于30×10-9(w)。经计算,一段反应器中的CR催化剂(简称一段催化剂)的吸附容量为4.14 mg/g,而两段反应器中CR催化剂的总吸附容量为3.68 mg/g。从吸附容量看,二段反应器中的CR催化剂(简称二段催化剂)远低于一段催化剂;且在一段催化剂完全失活前,二段反应器入口CO含量(即一段反应器出口CO含量)远低于一段反应器入口CO的含量(2.4×10-6(w))。
通过TPD方法,Keskitalo等[7]发现Cu/ZrO2催化剂(其中ZrO2为无定形态)上有3种类型的CO2吸附位,其中,一种为可逆吸附位,另外两种为不可逆吸附位。催化剂吸附的CO2与催化剂表面的羟基形成类碳酸根,从而占据了活性位,抑制了催化剂中晶格氧的流动能力[8-9]。图3中二段催化剂的吸附容量低于一段催化剂的原因可能为:当CO穿透一段催化剂需要二段催化剂发挥作用时,二段催化剂因为过长时间暴露在微量水和CO2下已损失了部分活性。
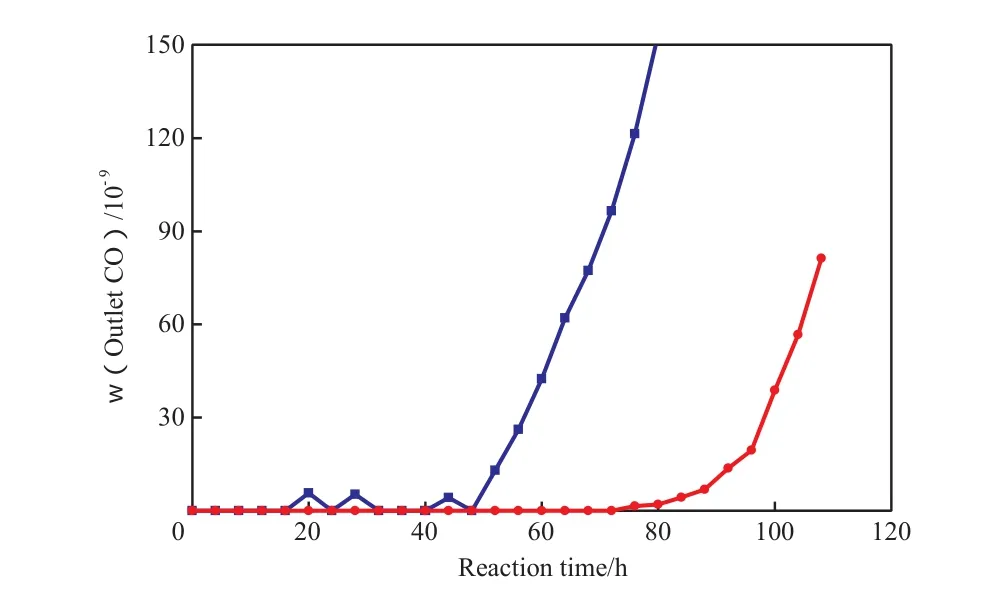
图3 无干燥器时液相丙烯脱CO的反应结果Fig.3 Removal of CO in liquid propylene without water extractor.
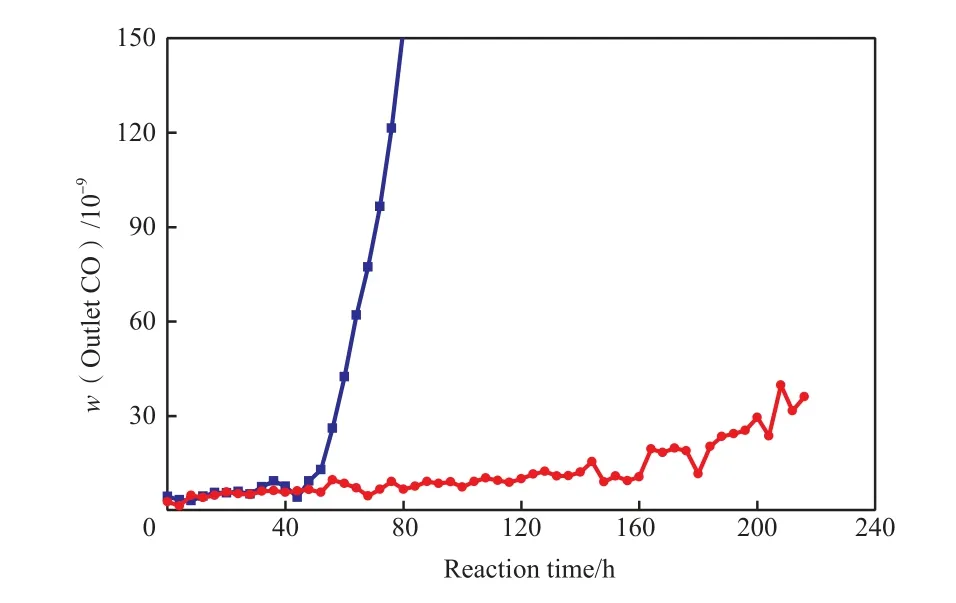
图4 有干燥器时液相丙烯脱CO的反应结果Fig.4 Removal of CO in liquid propylene with water extractor.
从图4可看出,在两段反应器间增加干燥器后,在54 h内一段反应器出口CO含量小于30×10-9(w),在204 h内二段反应器出口CO含量均小于30×10-9(w),穿透时间大幅延长。经计算,一段催化剂的吸附容量为4.14 mg/g,两段催化剂的总吸附容量为7.82 mg/g。
与未增加干燥器的情况相比:1)在实验过程中色谱分析结果表明,一段反应器入口、二段反应器出口CO2含量和水含量分别为~5.0×10-6(w)和小于1×10-6(w)(在仪器检测限以下),这说明干燥前后系统中微量水的含量均极低(低于现有仪器检测限)。2)反应评价结果表明,干燥后催化剂的总吸附容量大幅提高,但仍低于气相乙烯脱CO时CR催化剂的吸附容量,因此可以推测吸附性能的提高归因于增加的干燥器脱除了部分的微量水,但微量水的检测有待于采用更精密的分析仪器进一步确认。
2.2 表征结果
2.2.1 XRD和HRTEM表征结果
催化剂的XRD谱图见图5。由CZ催化剂的XRD谱图可见,催化剂的晶型以CuO和ZnO为主,2θ=35.5º,39.0º处的衍射峰为CuO的特征峰,2θ=31.9º,34.4º,36.2º处的衍射峰为ZnO的特征峰,2θ=35.5º处的CuO衍射峰与2θ= 36.2º处的ZnO衍射峰宽化重叠形成了CuO-ZnO固溶体的衍射峰[10]。在CZR催化剂的XRD谱图中同样出现了CuO-ZnO固溶体的弥合峰。在CZR和CR催化剂的XRD谱图中未发现ZrO2的衍射峰,说明ZrO2是以无定形状态存在的。采用Scherrer公式计算得到CZ,CZR,CR催化剂的CuO晶粒大小分别为12.9,4.6,16.4 nm。结合催化剂的比表面积,由XRD表征结果可推测:1)通过固溶体方式分散CuO的效果优于CuO分散在无定形ZrO2上,CZ和CR催化剂中CuO晶粒大小分别为12.9 nm和16.4 nm,比表面积分别为38 m2/g和90 m2/g;2)在两种分散方式同时存在的条件下(如CZR催化剂),CuO可以得到更好的分散,CuO晶粒最小(为4.6 nm),比表面积最大(为120 m2/g)。HRTEM表征结果(见图6)同样证明了这一点,CZ和CR催化剂的HRTEM图像上出现了明显的晶格条纹,而CZR催化剂的HRTEM图像上未出现明显的晶格条纹,说明ZrO2以无定形状态存在,CuO在ZrO2上分散良好,与XRD表征结果吻合。

图5 催化剂的XRD谱图Fig.5 XRD patterns of the catalyst samples.
2.2.2 XPS表征结果
催化剂的XPS谱图见图7。由图7可见,CR和CZR催化剂的Cu 2p峰的强度明显高于CZ催化剂,这是由于前两者的CuO含量(70%(w))远高于后者的CuO含量(30%(w))。由图7还可见,CR和CZR催化剂的Cu 2p主峰出现在934.2 eV处,CZ催化剂的Cu 2p主峰出现在934.0 eV处,二者的差别可忽略不计。但CZ催化剂与其他两个催化剂的伴峰的形状明显不同,前者呈宽化趋势。Zhou等[11]认为,伴峰的宽化是由于存在CuO微晶。
2.2.3 H2-TPR表征结果
催化剂的H2-TPR曲线见图8。由图8可见,CZR催化剂在164 ℃和181 ℃附近出现了2个还原峰,CZ催化剂在173 ℃和187 ℃附近出现了2个还原峰,CZR催化剂的2个还原峰的温度分别比CZ催化剂降低了9 ℃和6 ℃,这2个还原峰分别为CuO微晶和CuO-ZnO固溶体的还原峰[10-11];CR催化剂在168 ℃附近出现了还原峰,即CuO微晶的还原峰。说明CuO微晶比CuO-ZnO固溶体更易被还原。通过对比CZ和CZR催化剂的XRD和HRTEM表征结果可知,ZrO2的引入促进了小晶粒CuO的形成,从而使得CZR催化剂具有低温高活性。由图8还可看出,与CuO的晶粒效应相比,CuO与ZrO2的协同效应更有助于提高催化剂的脱CO性能。与CZ催化剂相比,尽管CR催化剂的晶粒较大,但由于CuO与ZrO2协同效应的存在,CR催化剂的还原相对容易。
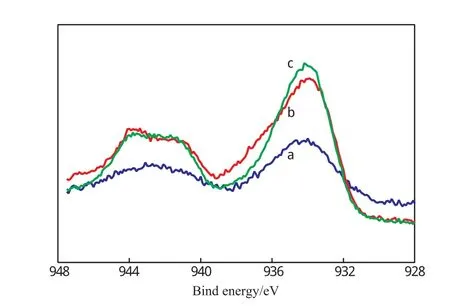
图7 催化剂的XPS谱图Fig.7 XPS spectra of the catalyst samples.

图8 催化剂的H2-TPR曲线Fig.8 H2-TPR curves of the catalyst samples.
值得注意的是,微量CO与常量H2的还原存在较大区别。在微量CO存在下,CZ,CZR,CR催化剂均能在50 ℃下被还原(见图2),而在常量H2下进行H2-TPR测试,3种催化剂在90 ℃或更高温度下才开始被还原(见图8)。其中的原因可能如Nagase等[12]和Kim等[13]所述,在痕量和常量还原气氛(H2或CO)下,CuO纳米颗粒的还原步骤有较大不同。在常量还原气氛下,CuO直接被还原为Cu,还原温度一般在170 ℃左右;而Svintsitskiy等[14]认为在痕量温和的还原气氛下,可能的步骤为(-111)CuO→(202)Cu4O3→(111)Cu2O →Cu,其中,第一步CuO纳米粒子被还原为类Cu4O3中间体是从60℃开始直至135 ℃,第二步Cu4O3→Cu2O的还原在135~164 ℃之间进行,之后进行Cu2O→Cu的还原。若要进一步深入了解CuO催化剂作用下微量CO的脱除过程,尚需有针对10-6数量级的CO存在下纳米CuO的在线表征研究。
3 结论
1)催化剂脱除微量CO的活性取决于两个因素:CuO的晶粒尺寸和CuO与ZrO2的协同效应。催化剂的活性和吸附容量大小的顺序为:CZ<CZR<CR,而 CuO晶粒大小的顺序为:CZR<CZ<CR,这说明CuO与ZrO2的协同效应对催化剂脱CO活性的影响比晶粒尺寸效应更大。
2)微量水和CO2对液相丙烯脱CO的影响较大。在液相丙烯脱CO的一段反应器和二段反应器之间增加干燥器,大幅提高了催化剂的吸附容量,说明反应系统中极其微量的水和CO2会降低催化剂脱CO的性能。
[1] 王桂英,彭晖,顾申,等. 聚合级乙烯净化催化剂的工业应用[J]. 石油化工,2007,36(9):944 - 947.
[2] 王育,戴伟,彭晖,等. 深度脱CO的CuO/ZnO/ZrO2催化剂[J]. 石油化工,2008,37(11):1121 - 1126.
[3] 王志平,陈齐. 乙烯丙烯中微量杂质的脱除方法[J]. 现代化工,1994,14(2):24 - 27.
[4] Xie Xiaowei,Li Yong,Liu Zhiquan,et al. Low-Temperature Oxidation of CO Catalyzed by Co3O4Nanorods[J]. Nature Lett,2009,458(9):746 - 749.
[5] 吴树新,尹燕华,马智,等. 一种新型常温常湿一氧化碳消除催化剂的研制[J]. 现代化工,2006,26(6):33 - 36.
[6] Konova P,Naydenov A,Venkonv Cv,et al. Activity and Deactivation of Au/TiO2Catalyst in CO Oxidation[J]. J Mol Catal A:Chem,2004,213(2):235 - 240.
[7] Keskitalo T J,Niemela M K V,Krause A O I. Modeling of the Adsorption and Desorption of CO2on Cu/ZrO2and ZrO2Catalysts[J]. Langmuir,2007,23(14):7612 - 7619.
[8] Bachiller-Baeza B,Rodriguez-Ramos I,Guerrero-Ruiz A. Interaction of Carbon Dioxide with the Surface of Zirconia Polymorphs[J]. Langmuir,1998,14(13):3556 - 3564.
[9] 叶丽萍,李帅,罗勇,等. CuO-ZnO-ZrO2催化剂低温深度脱除液相丙烯中微量一氧化碳的性能[J]. 精细化工,2013,30(12):1379 - 1393.
[10] 房德仁,刘中民,黎晓琼,等. 沉淀 pH值对CuO/ZnO/Al2O3系催化剂前体性质的影响[J]. 石油化工,2004,33(7):622 - 626.
[11] Zhou Renxian,Jiang Xiaoyuan,Mao Jianxin,et al. Oxidation of Carbon Monoxide Catalyzed by Copper-Zirconium Composite Oxides[J]. Appl Catal,A,1997,162(1/2):213 - 222.
[12] Nagase K,Zheng Y,Kodama Y,et al. Dynamic Study of the Oxidation State of Copper in the Course of Carbon Monoxide Oxidation over Powdered CuO and Cu2O[J]. J Catal,1999,187(1):123 - 130.
[13] Kim J Y,Rodriguez J A,Hanson J C,et al. Reduction of CuO and Cu2O with H2:H Embedding and Kinetic Effects in the Formation of Suboxides[J]. J Am Chem Soc,2003,125(35):10684 - 10692.
[14] Svintsitskiy D A,Kardash T Y,Stonkus O A,et al. In Situ XRD,XPS,TEM,and TPR Study of Highly Active in CO Oxidation CuO Nanopowders[J]. J Phys Chem C,2013,117(28):14588 - 14599.
(编辑 王 萍)
CuO/ZnO/ZrO2Catalyst Used in Deep Removal of Carbon Monoxide in Liquid Propylene
Wang Yu,Ma Tianshi,Liu Haijiang,Dai Wei,Peng Hui
(SINOPEC Beijing Research Institute of Chemical Industry,Beijing 100013,China)
A series of CuO-based catalysts,namely CuO/ZnO,CuO/ZnO/ZrO2and CuO/ZrO2,were prepared by co-precipitation and were characterized by means of XRD,XPS,H2-TPR and HRTEM. The catalysts were used in the removal of trace carbon monoxide(2.4×10-6(w)) in gas ethylene and liquid propylene at low temperature. The synergistic effect between CuO and ZrO2was more important in the reaction activity than the CuO nano-size effect. After a water extractor was installed between the two reactors for removing trace H2O,the adsorption capacity of the CuO/ZrO2catalyst was significantly improved. Under the optimal conditions of 2.5 MPa,50 ℃,50 h-1and CuO/ZrO2as the catalyst,the CO in the liquid propylene was decreased to less than 30×10-9(w).
copper oxide;zirconia;removal of carbon monoxide;liquid propylene;purifying catalyst
1000 - 8144(2015)07 - 0798 - 06
TQ 426.8
A
2015 - 03 - 20;[修改稿日期] 2015 - 04 - 22。
王育(1980—),男,河南省南阳市人,博士,高级工程师,电话 010 - 59202221,电邮 wyu.bjhy@sinopec.com。

