高效液相色谱法测定新保肾片中芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量
乔立业,方 李,曹燕丽,陆 崟,苏 华,王曙东(南京军区南京总医院制剂科,江苏南京210002)
高效液相色谱法测定新保肾片中芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量
乔立业,方 李,曹燕丽,陆 崟,苏 华,王曙东(南京军区南京总医院制剂科,江苏南京210002)
目的建立新保肾片中芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量测定方法,为生产质量提供保障。方法采用高效液相色谱法测定,色谱柱为Lichrospher-C18柱(250 mm×4.6 mm,5μm),流动相为甲醇∶0.1%磷酸溶液(70∶30),流速为1.0 m l/min,柱温为35℃,检测波长为254 nm。结果芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚分别在2.30~18.4μg/m l(r=1.0)、2.930~23.44μg/m l(r=1.0)、5.00~40.0μg/m l(r=1.0)、14.870~118.96μg/m l(r=0.999 8)、7.410~59.28μg/m l(r=0.999 9)范围内有良好的线性关系,平均回收率分别为100.16%、102.91%、99.76%、100.32%、100.44%,RSD分别为1.58%、1.27%、1.67%、1.33%、1.03%(n=9)。结论该方法准确易行,便于质量控制。
芦荟大黄素;大黄酸;大黄素;大黄酚;大黄素甲醚;高效液相色谱法;含量测定
新保肾片是以大黄醇浸膏提取物为有效成分的制剂,能够泻热通肠,逐瘀通经,延缓各类肾小球疾病的进展,尤其适用于硬化性肾小球肾炎,主治各类肾功能衰竭和各期糖尿病性肾病。其原有的质量标准仅采用分光光度法对大黄素进行测定,为了更好地把握产品质量,在查阅相关文献对大黄醇浸膏的质量控制方法后[1],我们采用HPLC法测定该制剂中芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量,为该制剂的质量控制提供一种准确有效的测定方法。
1 仪器与试药
1.1仪器 Agilent 1100型高效液相色谱仪(四元泵、VWD紫外检测器,美国安捷伦有限公司),KQ-250DB型数控超声波清洗器(昆山市超声仪器有限公司),AE240电子分析天平(梅特勒-托利多仪器有限公司,精度为十万分之一),FA1604S电子天平(上海精密科学仪器有限公司,精度为万分之一)。
1.2试药 芦荟大黄素对照品(中国药品生物制品检定所,110795-201007,纯度为98.0%),大黄酸对照品(110757-200206)、大黄素对照品(110756-200110)、大黄酚对照品(110796-201118,纯度为99.5%)、大黄素甲醚对照品(110758-201013,纯度为99.8%)(上述对照品均由中国食品药品检定研究所提供),新保肾片(医院制剂,批号121107、121206、131023),磷酸(南京化学试剂有限公司,批号12041910634),甲醇(色谱纯,美国天地),水为自制超纯水。
2 方法与结果
2.1色谱条件的选择 色谱柱:Lichrospher-C18柱,(250 mm×4.6 mm,5μm);流动相:甲醇∶0.1%磷酸溶液(70∶30);流速:1.0 m l/min;进样量:10μl;检测波长:254 nm;柱温:35℃。芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的保留时间分别约为10、16、30、42、67 min。
2.2溶液的制备①对照品溶液:精密称取芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚对照品2.30、2.93、5.00、14.87、7.41 mg置100 m l量瓶中,加甲醇稀释至刻度,摇匀作为储备液。精密称取4 m l储备液置10 m l量瓶中,加甲醇稀释至刻度,摇匀,作为对照品溶液,浓度分别为9.20、11.72、20.00、59.48、29.64μg/m l。②供试品溶液:取本品20片,除去薄膜衣,精密称定,研细,精密称取0.3 g置平底烧瓶中,加甲醇50 m l,称定重量,加热回流2 h,放冷,用甲醇补足减重,摇匀,微孔滤膜过滤,取续滤液作为供试品溶液。③阴性对照溶液:按处方比例和样品制备工艺不含大黄制成阴性样品,按供试品溶液制备方法制成阴性样品溶液,按上述方法进行测定。阴性样品在芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚吸收峰处均无峰出现,表明其对样品测定无干扰,结果见图1。

图1 HPLC色谱图
2.3线性关系考察 分别精密量取“2.2”项下的混合储备液1.0、2.0、4.0、6.0、8.0 m l置10 m l量瓶中,加甲醇稀释至刻度,摇匀。分别进样,记录色谱图,以峰面积Y对浓度X作线性回归,计算回归方程(见表1),结果表明各成分分别在相应的线性范围内呈良好的线性关系。

表1 5种蒽醌类成分的回归方程及线性范围(n=5)
2.4精密度试验 取“2.2”项下的混合对照品溶液,按上述色谱条件连续进样5次,芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚峰面积的RSD分别为0.68%、0.75%、0.21%、0.16%、1.02%。结果表明该方法的精密度良好。
2.5重复性试验 取同一批号(批号为131023)的样品5份,按“2.2”项下供试品溶液的制备方法进行测定,芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚平均含量分别为0.62、0.67、1.20、4.23、1.19 mg/片,RSD分别0.84%、1.69%、1.60%、1.37%、1.53%。说明方法重复性良好。
2.6稳定性试验 取同一批号(批号为131023)的供试品溶液,在常温下分别于0、1、2、4、8 h进样,记录峰面积,RSD分别为0.42%、0.31%、0.32%、0.21%、0.36%。表明样品溶液在8 h内稳定性良好。
2.7加样回收率试验 精密称取已知含量(批号为131023)的样品0.15 g,共9份,分别置于平底烧瓶中,按80%、100%、120%3个浓度分别精密加入“2.2”项下的混合对照品储备液5、8、10 m l,按“2.2”项下供试品溶液制备方法,即得。精密吸取上述供试液10μl注入色谱仪,测定含量,结果见表2、3、4、5、6。2.8 样品含量测定 取3批新保肾片,按“2.2”项下方法制备对照品溶液和供试品溶液,依法测定,结果见表7。

表2 芦荟大黄素加样回收率测定结果(n=9)

表3 大黄酸加样回收率测定结果(n=9)
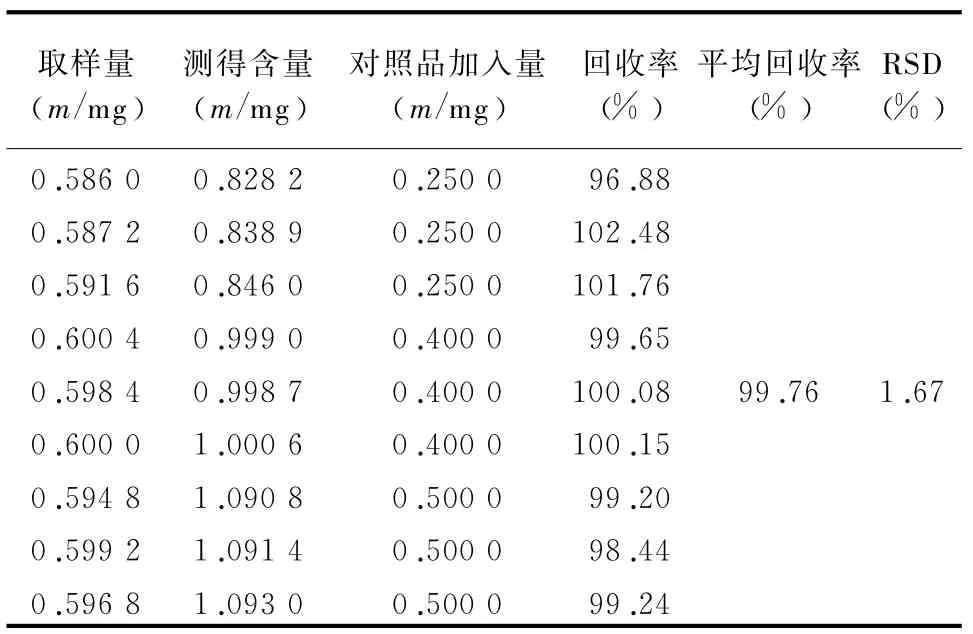
表4 大黄素加样回收率测定结果(n=9)

表5 大黄酚加样回收率测定结果(n=9)
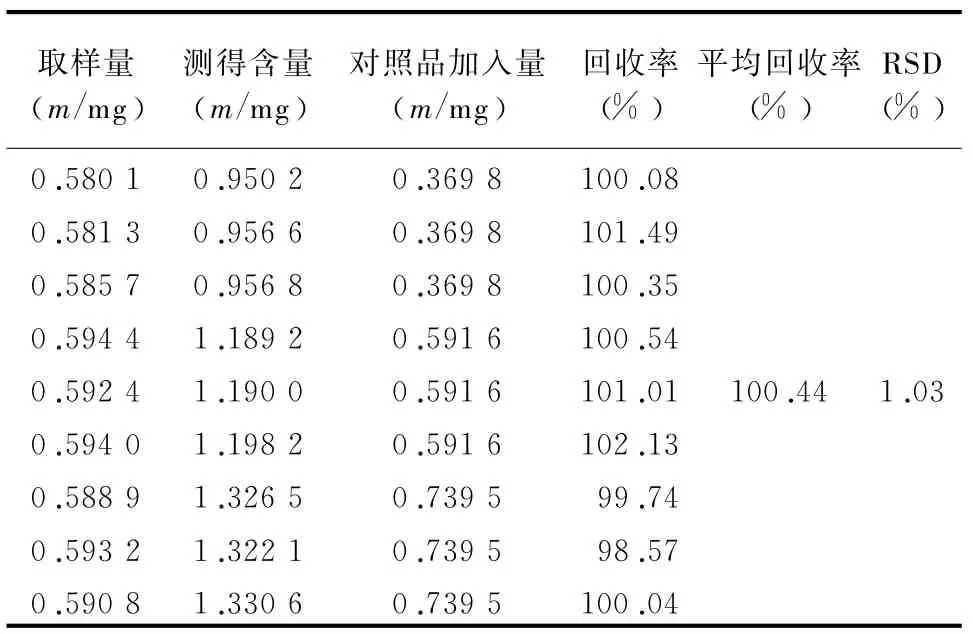
表6 大黄素甲醚加样回收率测定结果(n=9)
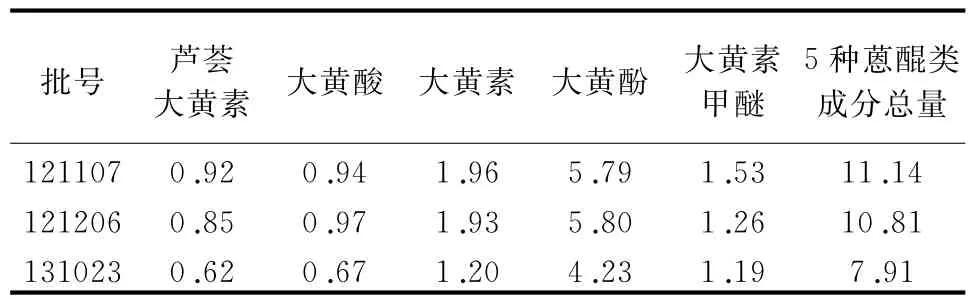
表7 样品含量测定结果(n=3,mg/片)
综合3批样品测定结果,确定本品每片含大黄以芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚总量计不得少于5.0 mg。
3 讨论
大黄的化学成分复杂,所含的有机化合物众多,在采用甲醇-0.1%磷酸溶液(75∶25)、甲醇-1%醋酸溶液(75∶25)和甲醇-0.1%磷酸溶液(78∶22)等流动相后发现磷酸系统比醋酸系统更稳定[2,3],峰形更佳,虽然有机相的减少延长了分析时间,但更利于主成分和杂峰的分离,同时相较于梯度洗脱简便易行,故选择了甲醇-0.1%磷酸溶液(70∶30)作为合适的流动相。
通过与我院同类制剂的含量对比,我们发现新保肾片中大黄素和大黄酚的含量更高,同时有研究表明此类成分对金黄色葡萄球菌和链球菌等均具有较好的抑制作用,且能够通过降低细胞高代谢状态来治疗慢性肾衰竭[4-6],故从一个方面验证了该制剂的有效性。另外,中药的成分复杂,从西药的角度去研究一些指标性成分并不能代表整体的作用,所以我们需要建立一个属于中药的可靠的质量标准体系。
[1] 国家药典委员会.中华人民共和国药典2010年版一部[S].北京:中国医药科技出版社,2010:22.
[2] 李 平,郑艳春,杨冬丽,等.HPLC同时测定新健胃包芯片中5种蒽醌类成分的含量[J].中国现代中药,2013,15(5):406-409.
[3] 徐守竹,谢艳华,张晓卫,等.RP-HPLC同时测定肾康注射液中5种蒽醌类成分[J].中成药,2010,26(21):90-93.
[4] 曾 芳,李 媛.大黄有效化学成分及其药理作用[J].当代医学,2013,19(12):149-150.
[5] 王昕怡,邵加庆.肾功能不全患者的降糖治疗[J].医学研究生学报,2013,26(4):442-446.
[6] 林小凤,李明权,李 琦,等.慢性肾脏病的中西医治疗进展[J].黑龙江医药,2012,1:43-45.
Determ ination of aloe-emodin,rhein,emodin,chrysophanol and physcion in Xinbaoshen tablets by HPLC
QIAO Liye,FANG Li,CAO Yanli,LU Yin,SU Hua,WANG Shudong(Departmentof Preparation,Nanjing General Hospital of Nanjing M ilitary Region,PLA,Nanjing 210002,China)
ObjectiveTo establishmethod of the determination of aloe-emodin,rhein,emodin,chrysophanoland physcion in Xinbaoshen tablet,for the production of quality protection.MethodsHPLC was performed on a Lichrospher-C18column(250mm×4.6mm,5μm)with themobile phase ofmethanol-0.1%H3PO4(70∶30).The flow rate was 1.0 m l/min,the column temperature was at 35℃and the detection wavelength was 254 nm.ResultsThe linear rang of aloe-emodin,rhein,emodin,chrysophanol and physcion were obtained between 2.30-18.4μg/m l(r=1.0),2.930-23.44μg/m l(r=1.0),5.00-40.0μg/m l(r=1.0),14.870-118.96μg/m l(r=0.9998)and 7.410-59.28μg/m l(r=0.999 9),the average recoverieswere 100.16%,102.91%,99.76%,100.32%,100.44%,RSD were 1.58%,1.27%,1.67%,1.33%,1.03%(n=9).ConclusionThe improvedmethod was accurate and feasible which could be used convenient in quality control.
aloe-emodin;rhein;emodin;chrysophanol;physcion;HPLC;content determ ination
R917
A
1006-0111(2015)05-0438-03
10.3969/j.issn.1006-0111.2015.05.015
2014-05-27
2014-07-30
[本文编辑] 顾文华
全军医疗机构制剂标准提高科研专项课题重点项目(13ZJZ13)
乔立业,硕士,药师.E-mail:qlynjutcm@sina.com
王曙东,博士,主任药师.研究方向:中药制剂.Tel:(025)80860166;E-mail:suhuash@sina.com.cn

