持续非卧床腹膜透析低T3综合征患者的内皮功能
郭志玲 梁素忍 胡 昭 (河南科技大学第一附属医院肾内科,河南 洛阳 47000)
甲状腺功能紊乱在长期腹膜透析患者中十分常见,其中有高达20%的患者是低T3综合征〔1〕。慢性病患者伴随甲状腺激素水平的下降是一种机体降低蛋白、能量消耗的保护性因素。甲状腺功能低下患者伴有心、脑血管疾病发病率、死亡率增加〔2,3〕。其具体机制尚未完全清楚。血管内皮功能紊乱被视为心血管系统损伤的一个早期标志〔4〕。血流介导的扩张反应(FMD)为无创评价内皮功能的重要方法,且能够反映一氧化氮(NO)的水平〔4〕。本研究探讨腹膜透析患者中低T3综合征与血管内皮功能之间的关系。
1 对象和方法
1.1 研究对象 2010年10月至2012年10月在河南科技大学第一附属医院肾内科行CAPD治疗的患者135例,男66例,女69例,平均年龄(59±17)岁。纳入标准:①腹透开始即行甲状腺功能检查者;②已行腹膜透析>3个月;③已签署知情同意书者。排除标准:①严重心力衰竭或心律失常者;②低血压者血压<90/60 mmHg;③同时行血液透析的患者;④并发有急性感染并发症者;⑤精神异常或其他原因不能配合本研究者。患者每3个月来门诊复查血生化检查、内皮功能等相关指标。根据患者的甲状腺功能结果分组〔总三碘甲状腺原氨酸(TT3)(0.60~1.81 ng/ml);总四碘甲状腺原氨酸(TT4)(4.50~10.90μg/dl);游离三碘甲状腺原氨酸(FT3)(2.30~4.20 pg/ml);游离四碘甲状腺原氨酸(FT4)(0.89~1.80 ng/ml);促甲状腺素(TSH)(0.35~5.50μIU/ml)〕。若FT3<2.30 pg/ml,T4和TSH在正常范围,诊断为低T3综合征(50例)。5项指标均正常者为正常对照组(85例)。患者原发病有慢性肾小球疾病28例,糖尿病肾病35例,高血压肾病29例,间质性肾病13例,其他30例。
1.2 血压测定 血压的测量由专人负责使用经校正的汞柱式血压计,在一个安静舒适的房间内进行,以保证其真实性和准确性。测量血压前,患者至少休息10 min。最终血压值取两次右侧肱动脉血压值的平均值。
1.3 内皮功能的评估 患者暴露右侧上臂,将血压计袖带绑在肘窝上约5 cm,测量血压,用7 MHz线阵探头纵扫肱动脉,测量肱动脉基础内径,将袖带充气加至收缩压以上约50 mmHg,阻断肱动脉血流5 min,快速放气,约45~60 s后再次测量肱动脉内径。FMD=(充血后管腔内径-充血前管腔基础内径)/充血前管腔基础内径×100%。
1.4 生化指标测量 采取患者早晨空腹外周静脉血,用常规标准测量方法检测甲状腺功能、血白蛋白浓度、血红蛋白、超敏C反应蛋白(hs-CRP)、甘油三酯(TG)、总胆固醇(TC)、血钙、血磷等指标。
1.5 统计学分析 使用SPSS13.0统计软件行t检验及χ2检验。独立危险因素筛选用多元逐步回归分析。
2 结果
2.1 两组患者的基本资料 两组之间的TT3(P<0.01)、FT3(P<0.01)、TSH(P<0.05)之间存在明显差别。舒张压、年龄、女性所占比例、血清TC水平在低T3综合征组明显高于甲状腺功能正常组(P<0.05,P<0.01),FMD在低T3综合征组明显低于甲状腺功能正常组(P<0.01)。其余指标均无明显差异(P>0.05)。见表1。
2.2 FMD与相关指标的相关性 FMD与舒张压(P<0.01)、血尿素氮(P<0.01)、甲状腺功能(1=正常,0=低T3综合征,P<0.01)呈明显正相关,与糖尿病(是 =1,否 =0,P <0.05)、年龄(P<0.01)、透析龄(P<0.05)、残肾功能(KT/V,P<0.05)呈明显负相关。FMD与其他指标均无显著相关性。见表2。
2.3 多元逐步回归分析 为进一步纠正影响FMD的其他影响因素,以FMD为应变量,以与其相关指标糖尿病、年龄、舒张压、尿素氮、甲状腺功能、透析龄、KT/V(残肾)为自变量,其他传统指标血糖、血脂、hs-CRP、血钙、血磷也被选入作为自变量,行多元逐步回归分析。结果显示,年龄、KT/V(残肾)、甲状腺功能是FMD变化的独立危险因素。三者一起决定FMD变化的53.0%。回归方程为:Y=15.034-0.135X1-2.020X2+2.525X3〔X1=年龄;X2=KT/V(残肾);X3=甲状腺功能(1=正常;0=甲低)〕,见表3、表4。
表1 两组基本资料(±s)

表1 两组基本资料(±s)
指标 低T3综合征组(n=50)甲状腺功能正常组(n=85)P值TT3(ng/ml)0.92±0.23 1.17±0.24 <0.01 TT4(μg/dl) 7.82±1.98 8.50±1.60 >0.05 FT3(pg/ml) 2.15±0.35 2.69±0.35 <0.01 FT4(ng/dl) 1.33±1.11 1.24±0.19 >0.05 TSH(μIU/ml) 3.91±3.90 2.61±2.46 <0.05透析时间(个月) 30.07±24.97 22.84±13.90 >0.05残肾(KT/V) 0.51±0.55 0.55±0.62 >0.05收缩压(mmHg) 133.07±24.49 131.89±21.05 >0.05舒张压(mmHg) 73.98±13.15 79.37±13.70 <0.05年龄(岁) 66.00±10.39 55.04±18.38 <0.01性别(男/女,n) 17/33 49/36 <0.01糖尿病(n) 16/50 19/85 >0.05体质指数(BMI,kg/m2) 23.79±3.36 24.58±3.98 >0.05 hs-CRP(mg/L) 0.45±0.54 0.33±0.69 >0.05血尿素氮(mmol/L) 21.60±5.35 22.02±5.41 >0.05血肌酐(μmol/L) 765.87±247.34 883.99±305.83 >0.05血糖(mmol/L) 6.21±2.36 6.15±2.18 >0.05 TC(mmol/L) 5.54±0.96 5.15±1.03 <0.05 TG(mmol/L) 2.71±1.71 2.73±1.80 >0.05血钠(mmol/L) 138.48±3.20 139.10±2.95 >0.05血钾(mmol/L) 4.24±0.67 4.21±0.69 >0.05血钙(mmol/L) 2.33±0.38 2.40±0.31 >0.05血磷(mmol/L) 1.51±0.40 1.52±0.39 >0.05 FMD(%)5.65±3.66 9.05±5.57 <0.01
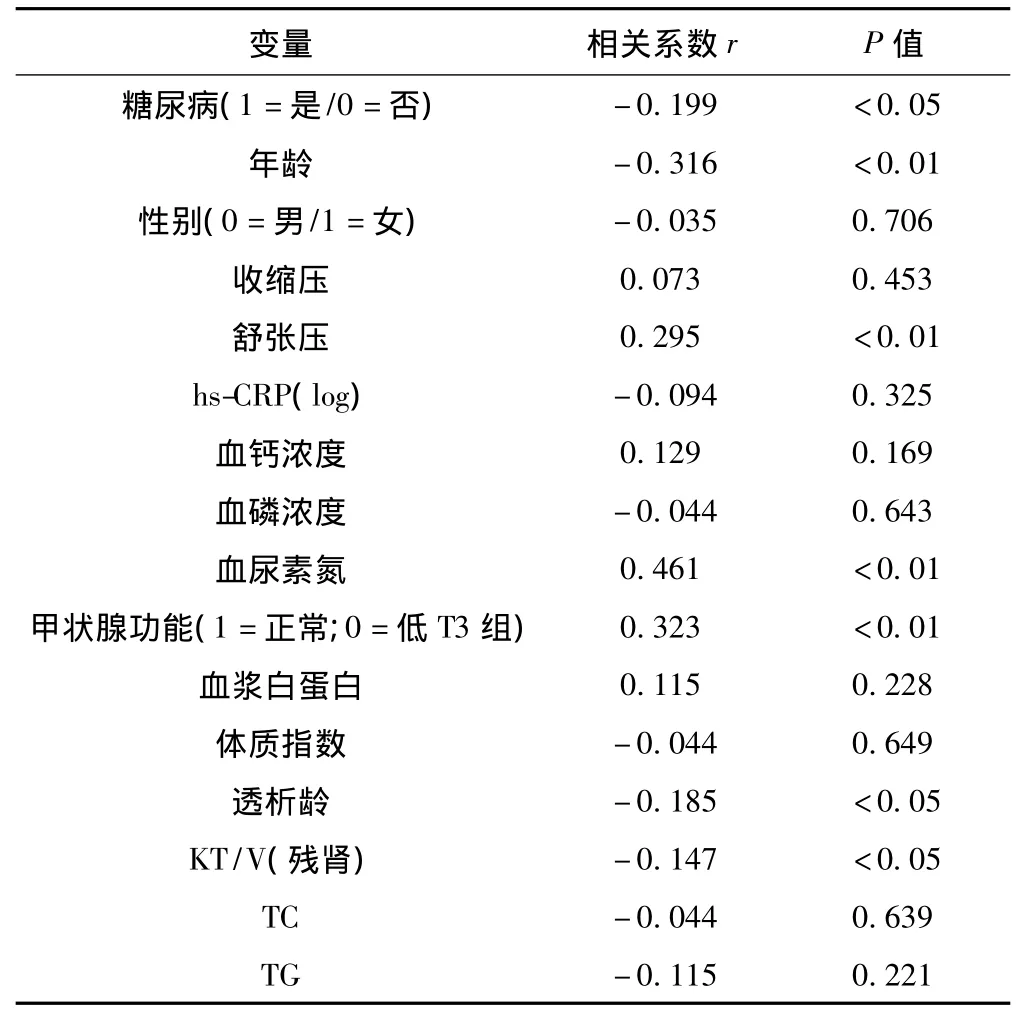
表2 影响因素与FMD的相关性分析
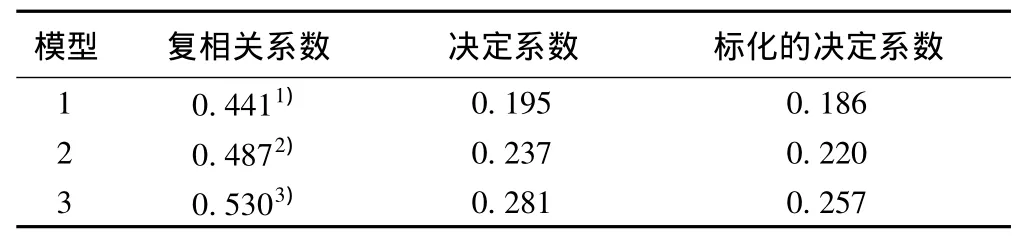
表3 FMD与其影响因子多元线性逐步回归模型
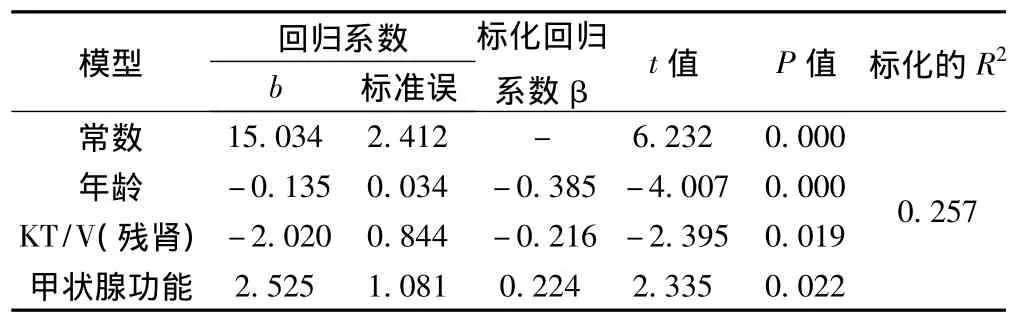
表4 多元回归分析结果
3 讨论
本研究中,腹膜透析患者FMD与“低T3综合征”密切相关,在校正一些混杂因素以后,多元回归分析显示年龄、KT/V(残肾)、甲状腺功能(1=正常,0=低T3综合征)均为血管内皮功能改变的独立危险因素。其中,在腹膜透析人群中,低T3综合征与内皮功能密切相关在国内还是首次报道。
长期腹膜透析可伴发不同程度的甲状腺功能紊乱,包括低T3综合征、亚临床甲状腺功能减退、临床甲状腺功能减退〔5~7〕。这些甲状腺功能异常既不是甲状腺本身的病变所致,也不是“下丘脑-垂体-甲状腺”轴的任何一个环节器质性病变所造成,而是长期慢性肾脏病和腹膜透析过程中多种原因造成的甲状腺功能紊乱,所以患者可能没有明显的临床症状以及电解质、血脂、血压的明显异常。本研究体现了这一点。本研究中,尽管两组患者的FT3、TT3、TSH浓度均存在明显差异,但只有FT3在“低T3综合征”组低于正常范围,而其他甲状腺功能指标在两组中均处于正常范围。可能是因为“低T3综合征”组患者由于自身疾病的严重程度及透析时间的差异,其甲状腺功能紊乱的程度不同。关于这方面也有研究报道“低T3综合征”可以向亚临床甲减和临床甲减转化〔7〕。
本研究发现腹膜透析伴随的低T3综合征存在于年龄较大人群且在女性患者明显高于男性。此外,低T3综合征患者的FMD明显低于甲状腺功能正常组,多元回归分析结果在矫正了影响FMD的其他因素后显示了甲状腺功能是影响FMD的独立危险因素。既往只在亚临床甲减〔8〕或者临床加减〔9〕患者中发现其FMD降低且心、脑血管并发症明显增加。本研究在国内首次报道了腹膜透析低T3综合征患者内皮功能降低。但多元回归分析未发现影响FMD的其他传统因素如血压、年龄等,可能与本研究以大于55岁以上中老年患者这一特殊人群有关,当然也不排除样本量相对较少。既往研究也证实营养良好对FMD是一保护性因素〔10〕,但本研究的两组患者未发现营养状态有明显差异,所以,对于低T3综合征引起的FMD降低的原因之一,并不能完全从低代谢的保护因素考虑。从而可以看出,此类患者伴随的甲状腺功能低下可能作为机体代谢保护因素一面的同时也存在血管内皮功能的受损。
目前低T3综合征患者是否积极替代治疗,仍存在争议。但是,基于本研究的实验结果和结论,对于腹膜透析伴低T3综合征的患者,从保护血管内皮功能并进一步预防心血管疾病的角度来说,应提倡替代治疗,关于这一点,既往研究在其他人群中也有提示〔11~13〕。但是,由于本研究中的腹透患者年龄偏大(平均年龄59岁),故对于年轻的腹透患者是否需要替代治疗还有待进一步研究。其次,至于药物替代治疗的剂量也需要进一步探讨。
1 Ng YY,Wu SC,Lin HD,et al.Prevalence of clinical and subclinical thyroid disease in a peritoneal dialysis population〔J〕.Perit Dial Int,2012;32(1):86-93.
2 Völzke H,Schwahn C,Wallaschofski H,et al.The Association of Thyroid Dysfunction with all-cause and circulatory mortality:is there a causal relationship〔J〕.JClin Endocrinol Metab,2007;92(7):2421-9.
3 Duntas LH,Biondi B.New insights into sunbclinical hypothyroidism and cardiovascular risk〔J〕.Semin Thromb Hemost,2011;37(1):27-34.
4 Rambaran C,Jiang B,Ritter JM,et al.Assesment of endothelial function:comparison of the pulse wave response to beta2-adrenoceptor stimulation with flow mediated dilatation〔J〕.Br J Clin Pharmacol,2008;65(2):238-43.
5 Maues MG,Santos SF,Filho HP,et al.Thyroid hormone losses in CAPD〔J〕.Perit Dial Int,1995;15(6):266-9.
6 Diez JJ,Iglesias P,Selgas R.Pituitary dysfunctions in uremic patients undergoing peritoneal dialysis:a cross sectional descriptive study〔J〕.Adv Perit Dial,1995;11:218-24.
7 Kerr DJ,Singh VK,Tsakiris D,et al.Serum and peritoneal dialysate thyroid hormone levels in patients on continuous ambulatory peritoneal dialysis〔J〕.Nephron,1986;43(3):164-8.
8 Singh S,Duggal J,Molnar J,et al.Impact of subclinical thyroid disorders on cronary heart disease,cardiovscular and all-cause mortality:a meta analysis〔J〕.Int JCardiol,2008;125(1):41-8.
9 Silva-Tinoco R,Castillo-Martinezl,Orea-Tejeda A,et al.Developing thyroid disorders is associated with poor prognosis factors in patients with stable chronic heart failure〔J〕.Int JCardiol,2011;147(2):e24-5.
10 Wen T,Tian X,Lu XH,et al.Factors contributing to formation of edema in volume overloaded continuous ambulatory peritoneal dialysis patients〔J〕.Perit Dial Int,2011;31(2):160-7.
11 Kebapcilar L,Comlekci A,Tuncel P,et al.Effect of levothyroxine replacement therapy on paraoxonase-1 and carotid intima-media thickness in subclinical hypothyroidism〔J〕.Med Sci Monit,2010;16(1):CR41-7.
12 周逸丹.甲状腺激素替代治疗伴有低T3综合征慢性心力衰竭〔J〕.中国基层医药,2011;6(18):1700-1.
13 Razvi S,Ingoe L,Keeka G,et al.The beneficial effect of L-thyroxine on cardiovascular risk factors,endothelial function,and quality of life in subclinical hypothyroidism:randomized,crossover trial〔J〕.JClin Endocrinol Metab,2007;92(5):1715-23.

