多西他赛联合卡培他滨方案在新辅助化疗三阴乳腺癌与非三阴乳腺癌中的近期疗效观察
张 淼,宋 敏,屈淑贤,章国晶,郭 放,韩雅玲,谢晓冬
临床研究
·论著·
多西他赛联合卡培他滨方案在新辅助化疗三阴乳腺癌与非三阴乳腺癌中的近期疗效观察
张 淼,宋 敏*,屈淑贤,章国晶,郭 放,韩雅玲,谢晓冬
目的 探讨三阴乳腺癌(triple-negative breast cancer, TNBC)与非三阴乳腺癌患者应用多西他赛联合卡培他滨(DX)方案行新辅助化疗的临床疗效及不良反应。方法 选择2008年7月—2013年8月收治的102例乳腺癌患者,其中TNBC 27例,非TNBC75例,均应用DX方案新辅助化疗。观察临床疗效和毒副反应发生情况。结果 TNBC患者总有效率与非TNBC患者比较差异无统计学意义(P>0.05)。TNBC患者病理完全缓解率、临床完全缓解率高于非TNBC患者(P<0.01,P<0.05)。毒副反应主要表现为胃肠道反应、骨髓抑制及手足综合征等,TNBC与非TNBC患者毒副反应发生率比较差异无统计学意义(P>0.05)。结论 TNBC患者较非TNBC患者对DX方案新辅助化疗更敏感,且未增加毒副反应发生率。
多西他赛;卡培他滨;三阴乳腺癌;新辅助化疗
无论是在发达国家还是在发展中国家,乳腺癌都已成为女性最常见的恶性肿瘤[1],乳腺癌新发病例估计占所有女性恶性肿瘤新发病例的29%[2],其病死率仅次于肺癌,居第2位[3]。三阴乳腺癌(triple-negative breast cancer, TNBC)是指雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体(Her-2)均无表达的乳腺癌,占乳腺癌的20%~25%,是一类侵袭性强、预后较差的乳腺癌[4-5]。由于其复发、转移率较高,且不能受益于内分泌及分子靶向治疗,因而逐渐引起更多学者的关注。乳腺癌新辅助化疗(new adjuvant chemotherapy, NACT)是指在局部治疗(手术和放疗)前的一种化疗模式,也称术前化疗或早期化疗[6]。本研究对采用多西他塞联合卡培他滨(DX)方案新辅助化疗的27例TNBC和75例非TNBC的临床资料进行回顾性分析,观察临床、病理疗效及其主要毒副反应,现报告如下。
1 资料与方法
1.1 临床资料 选择2008年7月—2013年8月于我院肿瘤科住院治疗的102例局部晚期乳腺癌患者,其中TNBC 27例,非TNBC 75例。均为女性,年龄36~62岁,中位年龄49岁;绝经前43例,绝经后59例;其中Ⅱb期16例,Ⅲa期57例,Ⅲb期29例;可评价的肿瘤直径3.0~7.8 cm,平均5.4 cm;81例可触及患侧腋下增大淋巴结,所有患者就诊前均未接受过化疗、内分泌治疗或局部放射治疗,Karnofsky评分均>70分。化疗前均以粗针穿刺进行组织学检测,病理诊断明确为乳腺浸润性导管癌,同时,检测ER、PR、Her-2及相关基因,化疗前血常规、肝肾功能及心电图均基本正常。
1.2 治疗方法 所有患者采用4个周期DX方案的新辅助化疗。DX方案:多西他赛(山东齐鲁制药有限公司生产,规格:20 mg/支)75 mg/m2,静脉滴注,第l天;卡培他滨(上海罗氏制药有限公司,规格:0.5 g/片)1000 mg/m2,口服,2/d,第1~14天,21 d为1个周期。辅助用药:维生素B、帕洛诺司琼、地塞米松、苯海拉明、泮托拉唑、异甘草酸镁、左卡尼汀和重组人粒细胞集落刺激因子(G-CSF)等。4个周期化疗结束3周后行手术治疗,其中TNBC 行乳腺癌改良根治术21例,非TNBC 38例,TNBC 行乳腺癌保乳根治术1例,非TNBC 22例,治疗无效共20例改用其他化疗方案,其中TNBC 5例,非TNBC 15例,3例疾病进展,TNBC 2例,非TNBC 1例。淋巴结有转移者及保乳者化疗结束后预放射治疗。激素受体阳性者术后化疗结束后行内分泌治疗5年。每3~6个月复查1次。
1.3 疗效及毒性反应评定标准 化疗4个周期后,根据实体瘤疗效评价标准(response evaluation criteria in solid tumors, RECIST)分为:完全缓解(CR):全部病灶消失,至少维持4周;部分缓解(PR):病灶缩小≥30%,至少维持4周;疾病稳定(SD):介于PR和PD之间;疾病进展(PD):病灶增加>20%,或出现新病灶。CR又分为:病理完全缓解(pCR)、临床完全缓解(cCR)。总有效率(OR)包括cCR和PR。pCR定义为原发肿瘤及区域淋巴结均无残留浸润性癌细胞,其中残留原位癌也包括在pCR内。毒性反应按美国国立癌症研究所(national cancer institute, NCI)分级标准分为0~Ⅳ度,主要包括骨髓抑制、胃肠道反应、手足综合征、乏力及肝肾功能损害等。
1.4 毒副反应观察 化疗4个周期后对病灶情况的观察使用触诊及超声等方法检查。此外,在进行新辅助化疗期间,观察患者化疗后症状且每个治疗周期前后均检测白细胞、中性粒细胞、血小板、肝功能、肾功能及心电图,并观察与药物相关的毒副作用。
1.5 统计学方法 采用SPSS 13.0软件对数据进行统计分析,计数资料以率(%)表示,采用χ2检验或Fisher精确概率法,α=0.05为检验水准。
2 结果
2.1 临床特征 TNBC患者中Ki-67表达率较非TNBC患者增高,差异有统计学意义(P<0.05),提示TNBC患者肿瘤分化较差。而年龄、月经状态、临床分期等TNBC与非TNBC比较差异无统计学意义(P>0.05),见表1。
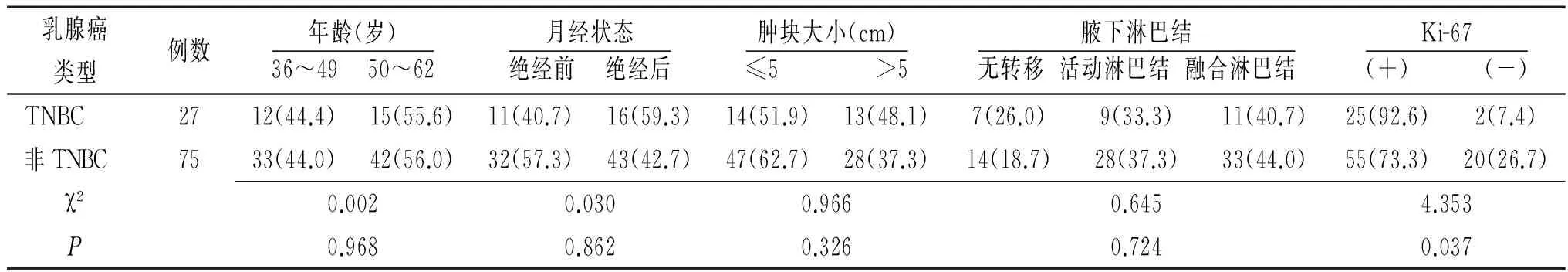
表1 TNBC与非TNBC患者临床特征比较[例(%)]
注:TNBC为三阴乳腺癌
2.2 临床疗效 TNBC与非TNBC患者OR比较差异无统计学意义(P>0.05),TNBC患者pCR、cCR高于非TNBC患者,差异有统计学意义(P<0.01,P<0.05),见表2。
注:TNBC为三阴乳腺癌
2.3 毒副反应 TNBC与非TNBC患者的主要不良反应为胃肠道反应、骨髓抑制、手足综合征等。TNBC与非TNBC患者毒副反应发生率比较差异无统计学意义(P>0.05),见表3。
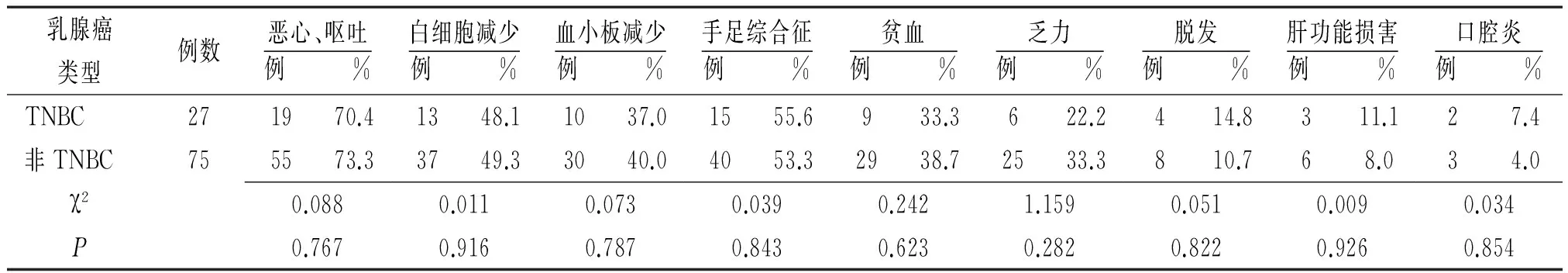
表3 TNBC与非TNBC患者DX新辅助化疗毒副反应发生情况
注:DX为多西他赛+卡培他滨;TNBC为三阴乳腺癌
3 讨论
乳腺癌是一类生物学特性高度异质的恶性肿瘤,由于肿瘤的分子分型不同可导致生物学行为、治疗效果和预后截然不同[7]。新辅助化疗作为局部晚期乳腺癌患者重要的综合治疗方法之一已被广泛接受[8]。新辅助化疗主要是通过杀灭肿瘤细胞,降低患者肿瘤负荷,缩小原发肿瘤的体积,降低分期,增加患者手术切除的机会,而且新辅助化疗可以通过测量肿瘤直径的变化预测个体对化疗方案敏感性[9-10],可用于指导后续治疗。
多西他赛为紫杉醇类抗肿瘤药,促微管蛋白装配成稳定的微管,从而抑制和干扰癌细胞的有丝分裂和分裂间期细胞功能所必需的微管网络,从而发挥抗肿瘤作用[11-15]。卡培他滨作为一种新型口服氟尿嘧啶氨甲酸酯类抗肿瘤药,通过细胞内胸腺嘧啶磷酸化酶(TP酶)的催化作用,在肿瘤细胞内转变为5-氟尿嘧啶,从而发挥抗肿瘤作用。由于乳腺癌细胞内TP酶活性明显高于正常组织,因此卡培他滨具有选择性的局部抗肿瘤作用,且对正常组织毒性较小[16]。有许多研究表明,多西他赛可以增加TP酶的活性,从而通过上调胸腺嘧啶磷酸化酶与卡培他滨起协同抗肿瘤作用[17],最主要是两药联合应用并未增加主要毒性作用[18]。
许多年来,局部晚期乳腺癌有较少的标准新辅助化疗方案,环磷酰胺+丝裂霉素+氟尿嘧啶(CMF)作为基础新辅助化疗方案,疗效不尽人意。近些年来,一些新药的问世,为局部晚期乳腺癌的治疗提供了有效且安全的方案,新辅助化疗的总有效率>80%[19]。多项临床研究结果显示,卡培他滨和多西他赛联合疗法的疗效相当于已被公认的效用较高的蒽环类和紫杉类联合疗法的疗效,由于避免了蒽环类药物的心脏毒性,前者的安全性显著高于后者[20]。本研究结果发现,TNBC组患者OR与非TNBC患者比较差异无统计学意义。而TNBC患者pCR、cCR显著高于非TNBC患者。在应用DX方案新辅助化疗的所有患者中主要毒副反应为骨髓抑制、手足综合征、恶心、呕吐等,且TNBC患者与非TNBC患者比较差异无统计学意义。大多数患者均能耐受,在给予对症治疗后均可缓解,并可继续接受进一步治疗,所有患者术前都能够顺利完成4个周期的新辅助化疗。本研究结果表明,TNBC患者较非TNBC对DX方案新辅助化疗更敏感,更易获得cCR、pCR,可提高乳腺癌根治率及保乳率,延缓局部晚期乳腺癌患者肿瘤的复发、转移,疗效肯定,且不良反应可以耐受,是TNBC新辅助化疗的有效方案。
预后型研究疗效评价的最佳指标是生存期,进一步观察生存期尤为重要,但本研究仅分析了临床有效率及病理有效率,尚存在不足。同时,根据不同的分子分型区分生存预后是目前同类研究的热点。
[1] JemalA,SiegelR,XuJ,etal.Cancerstatistics,2010[J].CACancerJClin,2010,60(5):277-300.
[2] Siegel R, Naishadham D, Jemal A. Cancer statistics,2012[J].CA Cancer J Clin, 2012,62(1):10-29.
[3] Jemal A, Siegel R, Ward E,etal. Cancer statistics,2009[J].CA Cancer J Clin, 2009,59(4):225-249.
[4] Lu H B, Xie X D, Liu Z Z. Research progress in thiple-negative breast cancer[J].Chin Ger J Clin Oncology, 2010,9(4):239-242.
[5] 章国晶,谢晓冬.三阴乳腺癌化疗的研究进展[J].国际肿瘤学杂志,2012,39(1):27-31.
[6] Benson J R, Jatoi I. Sentinel lymph node biopsy and neoadjuvant chemotherapy in breast cancer patients[J].Future Oncol, 2014,10(4):577-586.
[7] Yadav B S, Sharma S C, Chanana P,etal. Systemic treatment strategies for triple-negative breast cancer[J].World J Clin Oncol, 2014,5(2):125-133.
[8] Zaharia M, Gómez H. Neoadjuvant chemotherapy in the treatment of locally advanced breast cancer[J].Rev Peru Med Exp Salud Publica, 2013,30(1):73-78.
[9] 时伟锋,周士福.多西他赛联合卡培他滨在乳腺癌新辅助化疗中的应用[J].中国癌症杂志,2009,19(11):861-863.
[10] 林燕苹,陆劲松,邵志敏,等.乳腺癌新辅助化疗进展[J].中国肿瘤,2009,18(5):391-395.
[11]陆林,徐秀理,卢虎生,等.多西他赛联合卡培他滨治疗耐药性晚期乳腺癌疗效观察[J].中国热带医学,2010,10(7):857-858.
[12]陈金辉,苗玲玲,蒋志斌.多西他赛联合表柔比星新辅助化疗治疗炎性乳腺癌效果观察[J].解放军医药杂志,2014(9):47-50.
[13]陈金辉,吴劲松,蒋志斌.多西他赛联合表柔比星对局部晚期乳腺癌新辅助化疗的效果观察[J].解放军医药杂志,2013,25(10):55-57.
[14]高丽珍,高峨嵋,白云飞,等.顺铂、多西他赛序贯腹腔热灌注联合静脉化疗在中晚期卵巢癌围术期的应用[J].解放军医药杂志,2012,24(8):36-39.
[15]赵增虎,刘俊堂,丁瑞亮,等.吉西他滨联合卡培他滨治疗转移性三阴乳腺癌32例临床观察[J].解放军医药杂志,2013,25(1):36-38.
[16]姜丽娜,于世英,熊慧华,等.胸苷磷酸化酶在瘤组织中表达的研究[J].中华肿瘤杂志,2009,26(5):297-299.
[17]Venturini M, Del M L, Garrone O,etal. Phase I,dosefinding study of capecitabine in combination with docetaxel and epirubicin as first-line chemotherapy for advanced breast cancer[J].Ann Oncol, 2012,13(4):546-552.
[18]Pronk L C, Vasey P, Sparreboom A,etal. A Phase I and pharmacokinetic study of the combination of capecitabine and docetaxel in patients with advanced solid tumurs[J].Br J Cancer, 2000,83(1):22-29.
[19]刘庆仪,黄小云,李少英,等.新辅助化疗治疗局部进展期乳腺癌的临床观察[J].中国癌症防治杂志,2010,2(2):85-88.
[20]Lueck H, Minckwitz G V, Du Bios A,etal. Epirubicin/paclitaxel(EP) vs.capecitabine/paclitaxel(XP) in first-line metastatic breast cancer (MBC):A prospective,randomized multicentre phase Ⅲ study of the AGO breast cancer study group[J].J Clin Oncol, 2006,24(18 Suppl):517.
Short-term Curative Effects of Docetaxel Combined with Capecitabine in Neoadjuvant Chemotherapy of Triple-negative Breast Cancer and Non Triple-negative Brest Cancer
ZHANG Miao1, SONG Min2a, QU Shu-xian2a, ZHANG Guo-jing2a, GUO Fang2a, HAN Ya-ling2b, XIE Xiao-dong2a
(1. Post-graduate School, Dalian Medical University, Dalian, Liaoning,116044,China; a. Department of Oncology, b. Institute of Cardiovascular Diseases of the PLA, 2. General Hospital of Shenyang Military Area Command, Shenyang 110840, China)
Objective To compare the curative effect and adverse reactions of Docetaxel combined with Capecitabine (DX) in neoadjuvant chemotherapy of patients with triple-negative breast cancer (TNBC) or non triple-negative breast cancer. Methods A total of 102 patients with breast cancer during July 2008 and August 2013 underwent DX neoadjuvant chemotherapy, including 27 patients and 75 non-TNBC patients. The curative effect and adverse reactions were observed. Results There was no significant difference in the overall response (OR) between TNBC patients and non- TNBC patients (P>0.05). The pathological complete response and clinical complete remission rates of TNBC patients were significantly higher than those of non-TNBC patients (P<0.01,P<0.05). The main adverse and toxic reactions were gastrointestinal tract indisposition, bone marrow suppression, hand-foot syndrome, etc. There was no significant difference in incidence rates of adverse and toxic reactions between TNBC patients and non- TNBC patients (P>0.05). Conclusion The neoadjuvant chemotherapy using Docetaxel combined with Capecitabine shows a higher sensitivity in TNBC patients, compared with that in non- TNBC patients without an increase of incidence rate of adverse reactions.
Docetaxel; Capecitabine; Triple-negative breast cancer; Neoadjuvant chemotherapy
国家十二五重大新药创制平台子课题(2012ZX09303016-002);2012年辽宁省科技攻关计划课题(2012225019)
116044 辽宁 大连,大连医科大学研究生院(张淼) ;110840 沈阳,沈阳军区总医院肿瘤科(宋敏、屈淑贤、章国晶、郭放、谢晓冬),心血管病研究所(韩雅玲)
谢晓冬,E-mail:510503094@qq.com
R739.9
A
2095-140X(2015)03-0055-03
10.3969/j.issn.2095-140X.2015.03.013
2014-09-20 修回时间:2014-12-25)
*为共同第一作者

