改性笋壳对结晶紫的吸附性能研究
翁 晴
(福建工程学院 生态环境与城市建设学院,福建 福州 350118)
改性笋壳对结晶紫的吸附性能研究
翁 晴*
(福建工程学院 生态环境与城市建设学院,福建 福州 350118)
研究了氯化锌改性笋壳对染料结晶紫的吸附性能与机理,考察了吸附剂投入量、pH值、温度、结晶紫初始质量浓度、吸附时间对改性笋壳吸附结晶紫的影响.实验结果表明,在改性笋壳投入量为0.25 g,pH为8,温度313 K,吸附时间80 min的条件下,对含100 mg/L的结晶紫溶液的吸附量为9.06 mg/g.改性笋壳吸附结晶紫是自发的吸热过程.吸附过程符合Langmuir型等温吸附方程和一级动力学模型,吸附过程的速率控制步骤主要为膜扩散控制.
改性笋壳;吸附;结晶紫
随着经济和社会的发展,废水的排放量越来越大,而染料废水色度深、COD高、难以生物降解.寻找经济有效的方法处理染料废水,一直是研究的热点.国内外已经尝试多种方法和技术,如吸附法、电催化氧化法、声化学法、微波法[1~4]等.而吸附法具有处理效果好、价格低、应用范围广等优点,在染料废水处理中有着广泛的应用.目前比较常见的吸附剂是活性炭,而商品化的活性炭成本高,限制了其使用范围,寻求新的便宜材料做吸附剂成为了新的研究趋势.笋壳在过去一直被当作农作物废弃物被处理掉,不仅资源浪费还会造成环境污染.如果使用笋壳作为吸附剂来吸附处理染料废水,将能变废为宝,开发了笋壳新的价值.
本研究以农作物废弃物笋壳为原料,采用ZnCl2对其进行改性,探究改性后的笋壳吸附结晶紫的最佳吸附条件,探索了吸附剂投入量、pH值、温度、结晶紫的初始质量浓度、吸附时间等因素对吸附性能的影响,分别利用热力学和动力学模型探讨了改性笋壳对结晶紫的吸附热力学、动力学特征及其吸附机理.
1 实验材料和方法
1.1 实验用主要材料和仪器
实验原料:笋壳取自当地市场,清洗干净后,放入烘箱内烘干,粉碎,粉碎后的笋壳经60目分样筛后,置于密封袋中,备用.
化学试剂:结晶紫、氯化锌、盐酸、氢氧化钠均为分析纯,购自中国医药集团上海化学试剂公司.
仪器:SHZ-82恒温振荡器, TU1901紫外分光光度计,BS224S分析天平,80-2台式离心机,PHS-3C酸度计,JW-BK-1112比表面及孔径分析仪.
1.2 实验方法
1.2.1 改性笋壳的制备 称取一定质量的笋壳于锥形瓶中,加入ZnCl2溶液进行改性处理,然后用蒸馏水将其洗涤至无残留,置于烘箱中烘干,制得改性笋壳.
1.2.2 吸附实验 精确称取0.25 g改性笋壳加入到25 mL含一定质量浓度的结晶紫溶液中,置于恒温振荡器中振荡吸附一定时间后,离心分离,取上层清液,用分光光度计在590 nm处测其吸光度,计算出结晶紫的质量浓度.根据公式(1)和公式(2)分别计算改性笋壳对结晶紫的去除率(η)和吸附量(Qe,mg/g).
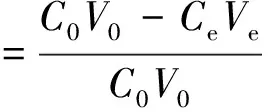
(1)

(2)
式中:C0,Ce分别为吸附前和吸附后结晶紫的质量浓度,mg/L;V0,Ve分别为吸附前和吸附后溶液的体积,L ;m为加入改性笋壳的质量,g.
2 结果与讨论
2.1 笋壳改性前后表面性质对比
在表1中列出了未改性笋壳和改性笋壳的比表面积和孔容量.经过改性处理后笋壳的比表面积和孔容量都明显的增加,其比表面积是未改性笋壳的2.9倍,达到191.7 m2/g.这说明ZnCl2通过对笋壳内部分子结构的电解作用,使笋壳内部形成多孔隙结构,导致了比表面积和孔容量均增大.

表1 改性前后笋壳表面性质变化
2.2 投入量对结晶紫吸附的影响
图1反映了改性笋壳不同投入量在相同条件下(pH=8,温度313 K,结晶紫初始质量浓度100 mg/L,吸附时间80 min)的去除率和吸附量.当吸附剂投入量增大时,吸附剂对结晶紫的去除率随之升高,吸附量则减小.这是由于吸附剂投入量的增加,增加了活性吸附点位,可以吸附更多的染料分子,去除率增加;而活性吸附点位的增加导致了单位质量吸附剂吸附染料分子的能力下降,吸附量减小.当投入量增加到0.25 g时,去除率变化不再明显,可能原因是当吸附剂投入量增大到一定量后,过量的吸附剂将不能被充分利用,产生了空余吸附位,从而吸附剂的吸附量逐渐降低.因此,本实验吸附剂的投入量控制为0.25 g,此时的去除率达到90.6%,吸附量为9.06 mg/g.

2.3 pH值对结晶紫吸附的影响
图2反映了pH值的变化在相同条件下(投入量0.25 g,温度313 K,结晶紫初始质量浓度100 mg/L,吸附时间80 min)改性笋壳对结晶紫的吸附量.随着pH值从4上升到11,吸附量不断增加,从3.9 mg/g增加到9.26 mg/g.在pH值较低时,溶液中存在较多的H+,改性笋壳表面被大量的H+包围,与结晶紫离子产生竞争吸附吸附剂表面的活性吸附点位.pH在8~11时,吸附量增加缓慢,而且pH值越大,需要消耗更多的碱来调节,因此,本实验将pH值控制在8.
2.4 温度对结晶紫吸附的影响及吸附热力学研究
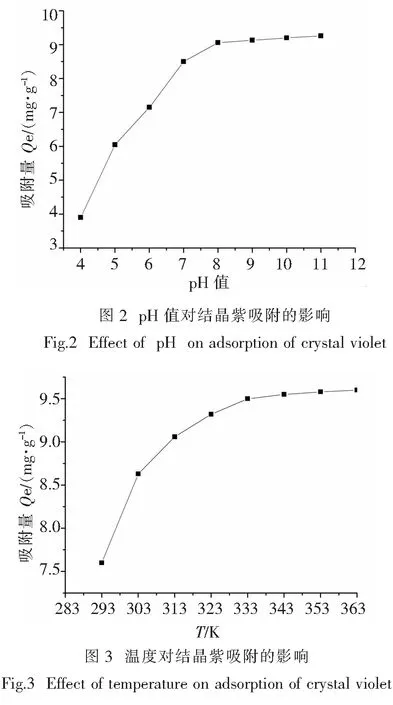
图3反映了不同温度在相同条件下(投入量0.25 g,pH=8,结晶紫初始质量浓度100 mg/L,吸附时间80 min)改性笋壳对结晶紫的吸附量.随着温度的升高,吸附剂对结晶紫的吸附量变大,这是因为温度升高,离子间的碰撞作用随之加强,从而吸附易于进行.温度从293 K上升至363 K,其吸附量从6.6 mg/g增加至9.6 mg/g,表明改性笋壳对结晶紫的吸附过程是吸热过程.温度大于313 K后,吸附量增加趋于缓慢,因此,将实验的温度控制在313 K.
热力学计算方程式为
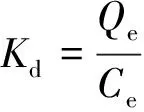
(3)

(4)
△G=△H-T△S,
(5)
式中Ce为吸附后结晶量的质量浓度(mg·L-1),Qe为吸附量(mg·g-1),△H为吸附焓变(kJ·mol-1),△S为吸附熵变(J·mol-1·K-1),△G为吸附吉布斯自由能变(kJ·mol-1),R为理想气体常数(8.314 J·mol-1·K-1),T为绝对温度(K).根据公式(3)和图3的数据计算出不同温度下的Kd,以lnKd与1/T的关系进行线性拟合(R2=0.978 6),由其斜率和截距可推算出△H和△S,再由公式(5)可求得△G,计算结果见表2.
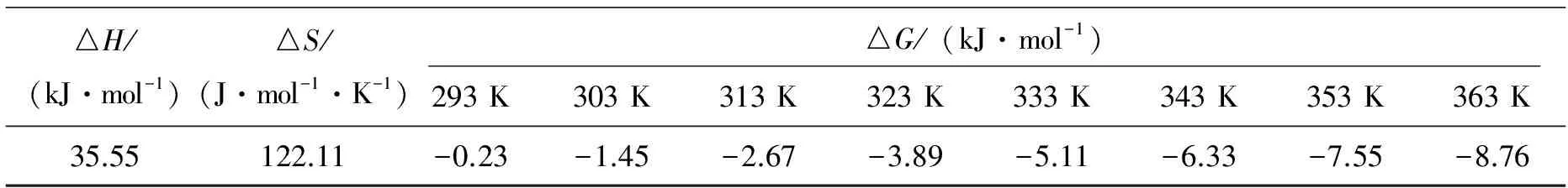
表2 改性笋壳吸附结晶紫的热力学系数
从表2可以看出,吸附过程的焓变△H为正值,吉布斯自由能△G为负值,说明改性笋壳对结晶紫的吸附是自发吸热过程.此外,△H为正值,而△G随温度的升高而降低,表明吸附反应在较高的温度时更容易发生.由于物理吸附的吸附焓变△H的绝对值一般在0~20 kJ·mol-1,化学吸附的焓变绝对值大于20 kJ·mol-1[5],表明改性笋壳对结晶紫的吸附主要是化学吸附.
2.5 初始质量浓度对结晶紫吸附的影响及吸附等温线研究
图4反映了不同初始质量浓度的结晶紫溶液在相同条件下(投入量0.25 g, pH=8,吸附时间80 min,温度313 K)改性笋壳对结晶紫的去除率和吸附量. 随着结晶紫初始质量浓度的增大,改性笋壳对结晶紫的去除率逐渐下降,吸附量增大.在初始质量浓度较低时,改性笋壳对结晶紫的吸附效果比较好,这是因为在初始质量浓度较低时,改性笋壳表面的活性吸附点位大部分是空的,去除率较高,吸附量增幅较大.当初始质量浓度大于100 mg/L时,大部分活性点位已被占据,吸附量增幅减缓.
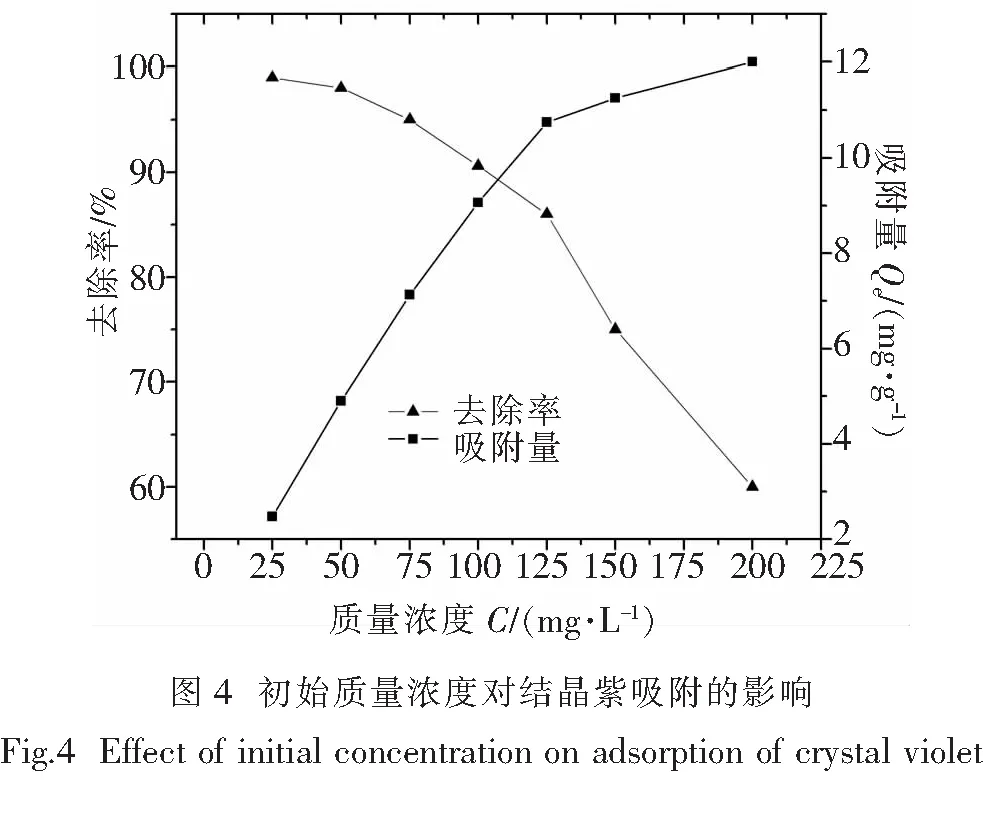
选取常用的Langmuir和Freundlich等温吸附方程[6],将图4的实验数据进行线性拟合分析.Langmuir吸附等温式为:

(6)
Freundlich吸附等温式为:
Qe=KFCe1/n,
(7)
式中Ce和Qe同前,Qm为饱和吸附量,KL为Langmuir参数,KF和n均是Freundlich特征参数.Langmuir型和Freundlich型等温吸附方程参数如表3所示,改性笋壳吸附结晶紫的吸附过程用Langmuir型和Freundlich型等温吸附模型拟合,p值均小于0.01,达到显著水平,拟合效果均较好.对比Langmuir型(R2=0.999 0)和Freundlich型(R2=0.929 3),Langmuir型相关系数R2较大,且p值更小,说明采用Langmuir型拟合效果更佳,表明该吸附主要为单分子层吸附,吸附过程以分配为主.

表3 改性笋壳对结晶紫的等温吸附方程参数
2.6 吸附时间对结晶紫吸附的影响及吸附动力学研究
图5反映了不同吸附时间在相同条件下(投入量0.25 g, pH=8,温度313 K,初始质量浓度100 mg/L)改性笋壳对结晶紫的吸附量.可以看出,在吸附的初期,吸附量随时间的增加而快速增大,80 min后,吸附量增加已不明显,基本到达动态平衡.
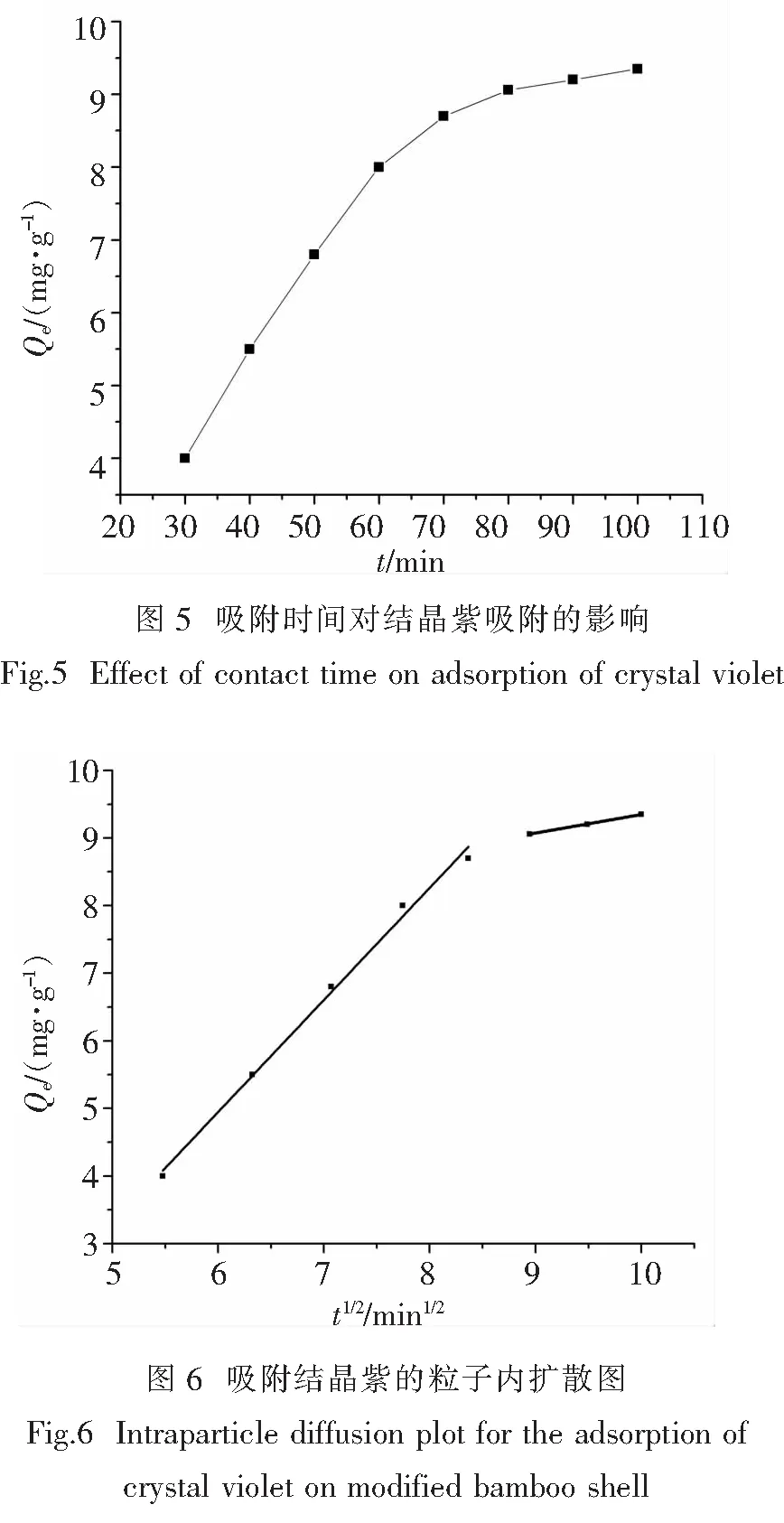
吸附过程的动力学研究[7]可以用来描述吸附剂吸附速率的快慢,一级吸附动力学模型是常用的动力学方程之一,其方程式为

(8)
式中,Qe同前,Qt为吸附过程中任意时间t时的吸附量,k1为一级吸附速率参数,以lg(Qe-Qt)对t作图,如果得到一直线,说明吸附过程符合一级动力学模型.所得动力学参数和相关系数见表4.一级动力学模型的相关系数为0.978 1,拟合效果良好,说明改性笋壳吸附结晶紫的过程符合一级吸附动力学模型,主要是单分子作用的吸附过程.
2.7 吸附机理研究
根据Weber和Morris理论,粒子内扩散模型为
Qt=kidt1/2+C,
(9)
式中,kid是粒子内扩散速率常数,kid值越大,吸附质越容易在吸附剂内部扩散,C是膜扩散程度.以Qt对t1/2作图,如图6所示,可将图中曲线进行分段线性拟合,分为两个线性部分,这表明吸附过程可以分为两个阶段:前半部分是膜扩散,后半部分是粒子内扩散,所得动力学参数和相关系数见表4.前半部分拟合得到的C1值不等于0,说明粒子内扩散并不是速率控制步骤.对比两部分拟合得到的粒子内扩散速率常数kid1和kid2,kid2小于kid1,kid1数值降低,表明随着吸附的进行,吸附质逐渐占领吸附剂的内部活性点位,吸附剂内部的孔径变小,即可扩散的通道变小,导致了吸附速率的降低.

表4 改性笋壳对结晶紫的吸附动力学参数
为了进一步了解吸附过程中速率控制步骤是膜扩散还是粒子内扩散,采用 Boyd动力学方程进行动力学分析,其方程式为

(10)

(11)
式中,Qe,Qt同前,B为时间常数,公式(10)可以转化为
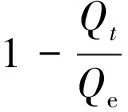
(12)
Bt的数值在不同的吸附时间可以由公式(12)计算得到,以Bt对t作图,B值为斜率.如果该图是线性的,则可以区分出吸附控制步骤是属于膜扩散控制还是粒子内扩散控制.如果直线经过原点,说明吸附的控制步骤是粒子内扩散控制,反之,则为膜扩散控制.从图7中可以看出,该直线并不通过原点,说明吸附速率控制步骤主要为膜扩散控制,粒子内扩散不是速率控制步骤,这与前面的研究结果一致.B值为0.061 65 min-1.
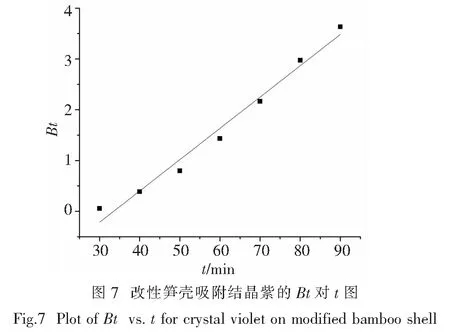
根据公式(13)可以计算得到吸附质在吸附剂中的有效扩散系数Deff

(13)
式中,r为假设吸附剂粒子的半径.实验中所用的改性笋壳为60目,计算得到吸附质在吸附剂中的有效扩散系数Deff为5.627 5×10-6cm2/s,比粒子内扩散为控制步骤的Deff值10-11cm2/s大5个数量级[8],这也表明改性笋壳对结晶紫的吸附控制步骤主要为膜扩散.
3 结 论
(1) 改性笋壳吸附去除结晶紫的最佳吸附条件是:改性笋壳投入量0.25 g,pH为8,温度313 K,吸附时间80 min.在此条件下,对初始质量浓度为100 mg/L的结晶紫的吸附量达到9.06 mg/g.
(2) 改性笋壳吸附结晶紫是一个自发的吸热过程.
(3) 改性笋壳对结晶紫的吸附行为符合Langmuir型等温吸附方程,一级动力学模型,主要是单分子作用的吸附过程.
(4) 改性笋壳吸附结晶紫的吸附控制步骤主要为膜扩散控制.
[1] 王宏杰,董文艺,李伟光,等.活性污泥吸附结晶紫的研究[J].环境科学,2008,29(10):2 856-2 861.
[2] 王苏,颜幼平,邹勇斌,等.电催化氧化法处理阳离子染料废水的试验研究[J].安全与环境工程,2012,19(5):46-50.
[3] 闫烨,杜永峰,姚秉华,等.声化学降解染料结晶紫的研究[J].化学研究,2005,16(4):70-73.
[4] 陈孟林,邹异红,李爱雯,等.微波-活性炭催化法处理结晶紫溶液的研究[J].广西师范大学(自然科学版),2004,22(3):77-80.
[5] 王玲玲,郭佳莉,肖春妹,等.Zn2+改性丝光沸石对甲基橙的吸附性能研究[J].矿物学报,2011,31(2):284-290.
[6] VADIVELAN V, KUMAR K V. Equilibrium, kinetics, mechanism, and process design for the sorption of methylene blue onto rice husk[J].Journal of Colloid and Interface Science,2005,286: 90-100.
[7] SINGH K K ,RASTOGI R,HASAN S H. Removal of Cr(VI) from wastewater using rice bran[J]. Journal of Colloid and Interface Science,2005,290:61-68.
[8] 邹卫华,白红娟,李苛,等. 天然沸石对阳离子染料中性红的吸附及机理研究[J].郑州大学学报(理学版),2011,43(4):71-76.
责任编辑:朱美香
The Mechanism of Crystal Violet Adsorbed by Modified Bamboo Shell
WENGQing*
(College of Ecological Environment and Urban Construction,Fujian University of Technology, Fuzhou 350118 China)
The performance and mechanism about adsorption of crystal violet with ZnCl2modified bamboo shell were studied, and the factors which have influence on the adsorption processing, such as dosage, pH, temperature, the initial concentration of crystal violet, contact time were discussed. The results showed that the crystal violet of adsorption capacity was 9.06 mg/g, while the dosage was 0.25 g, pH at 8, temperature was 313 K, the initial concentration was 100 mg/L and contact time was 80 min. The adsorption of crystal violet on modified bamboo shell was spontaneous and endothermic process. The equilibrium data was well fitted to Langmuir isothermal adsorption equation and the first-order model. The adsorption process was mainly controlled by membrane diffusion.
modified bamboo shell; adsorption; crystal violet
2015-05-11
福建省自然科学基金项目(2013J01215)
翁晴(1981— ),女,福建 永泰县人,实验师.E-mail:wcnjge@163.com
X703
A
1000-5900(2015)03-0068-07

