基于SEM-EDS及GC-MS技术研究有机氯分子结构对零价铜脱氯机制的影响
朱 洪, 刘 静, 焦晗涛, 张 晶, 段江涛, 连兴业, 侯亚楠
(北京农学院生物科学与工程学院, 北京 102206)
基于SEM-EDS及GC-MS技术研究有机氯分子结构对零价铜脱氯机制的影响
朱 洪, 刘 静, 焦晗涛, 张 晶, 段江涛, 连兴业, 侯亚楠
(北京农学院生物科学与工程学院, 北京 102206)
零价铜作为一种廉价金属很少应用于促进氯代有机物脱氯研究,其原因是零价铜的催化还原脱氯活性差,且反应机制复杂。本文采用机械球磨技术制备了Cu-Fe和Cu-Ni合金,研究零价铜在不同微观环境下对对氯苯酚(4-CP)的脱氯行为,旨在考察有机氯分子结构对零价铜脱氯机制的影响。应用扫描电镜-能谱(SEM-EDS)及色相色谱-质谱(GC-MS)分析发现,铜原子的微环境及有机氯分子结构均影响铜的脱氯机制。在Cu-Fe体系中,Cu遵循经典的催化加氢脱氯机制,4-CP的降解产物为苯酚;Cu-Ni体系的还原作用来源于零价铜,其中的镍金属并未起到催化加氢作用,Cu-Ni合金及单独零价铜对4-CP的降解产物是环己酮。零价铜对4-CP的降解率可达70%以上,而Cu-Fe体系的降解率仅为34%,两者对芳香族氯代物的降解效率差距显著。零价铜能够降解化学稳定性高的4-CP和苯酚,但不能降解化学稳定性相对较差的脂肪族氯代有机物(如一氯乙酸和二氯乙酸),因此认为零价铜脱氯机制并非传统的催化加氢机制,而是遵循直接电子传递还原机制,且有机氯分子的苯环结构是零价铜直接电子传递还原的诱因。
氯代有机污染物; 零价铜; 铜系合金; 脱氯机制; 机械球磨; 扫描电镜-能谱(SEM-EDS);气相色谱-质谱法(GC-MS)
金属催化化学还原法处理氯代有机物(CxHyClz)是利用还原剂,针对性地将污染物分子中的氯取代基去除,达到降低氯代有机物的生物毒性、改善其可生化性的方法[1-5]。常用的还原剂主要是一些金属单质,如铁[6-7]、镁[8-9]、铝[10]等,零价金属是一种有效的脱卤还原剂,在氯代有机污染物脱氯降解研究中具有广泛的应用前景。零价铜作为一种环境可容的金属材料,常常被用于催化脱氯领域的研究[11-14],然而其脱氯机制复杂,催化加氢性能远小于Ni、Pd等,关于零价铜的脱氯机制较少有报道。
金属对氯代有机物(CxHyClz)的脱氯过程,相关报道归纳起来可分成2种反应机理[15-16]。机理①:依靠单质金属的还原能力,在水中被氧化,同时给出电子;而氯代有机物则直接接受电子进行还原脱氯,最终生成可生物降解的有机物(CxHy+z)。主要反应过程[17]如下:
CxHyClz+zH++zM0→CxHy+z+zM++zCl-
(1)
机理②:在水环境中,零价金属与H2O或H+发生反应,生成具有还原性的H2,H2与氯代有机物发生反应,使其还原脱氯。主要反应过程[18]如下:
M0+nH2O→Mn++n/2H2+nOH-
(2)
zH2+CxHyClz→CxHy+zCl-+zH+
(3)
以零价金属铁还原脱氯为例,反应符合机理②的可能性较大[19-22]。其中,选择合适的加氢催化剂,使体系中释放出的氢气活化为活性氢是关键,常用的催化剂有Pd、Pt等贵金属。
铜是一种惰性金属,其标准氧化还原电位为+0.36 V,可通过电偶腐蚀加速还原,同时铜也是一种较为温和的加氢催化剂,因此铜通常被认为是机理②的反应[11, 23-24]。相关报道普遍认为零价铜所遵循的也是氢解还原的机制,只是在Yin等[13]的研究中发现了零价铜降解有机氯产生了复杂的降解产物,认为零价铜可能存在直接电子传递机理。
本文首先采用机械球磨技术制备Cu-Fe和Cu-Ni合金,对比氯代有机物对氯苯酚(4-CP)在两种铜系金属体系中的脱氯产物及其脱氯行为,比较芳香族及脂肪族有机氯在铜表面的脱氯差异,研究有机氯分子结构对零价铜脱氯机制的影响,进而试验零价铜对具有苯环结构的苯酚的还原情况,揭示零价铜直接电子传递还原的机理。
1 实验部分
1.1 Cu-Fe和Cu-Ni球磨合金材料制备
Cu-Fe和Cu-Ni球磨合金的制备采用机械球磨技术,因为机械球磨过程中容易造成众多点线缺陷[25-27],还可以引入应变力,能够显著提高催化金属的储氢加氢性能,促进Fe的电催化活性,有利于脱氯的发生[28-30]。实验采用行星式球磨机制备球磨铁镍材料。分别称取一定比例的铜粉-铁粉和铜粉-镍粉置于100 mL不锈钢球磨罐中,罐中的不锈钢磨球总质量为186 g(即球料比为37.5∶1),固定500r/min或800r/min的自转转速球磨相应的时间即得所需的球磨合金材料。
球磨铁镍材料在使用前进行酸洗:称取一定量的球磨材料置于具塞三角瓶中,按100g材料/100mL酸洗液的投加量加入pH=1的酸液中,放入转速为 220r/min的振荡摇床中,在25℃下酸洗15min,取出倒去液体,再用高纯水冲洗3~4次,备用。
1.2 降解实验方法
将一定质量酸洗后的Cu-Fe、Cu-Ni或Cu球磨材料置于50mL具塞三角瓶中,加入30mL有机氯或其他反应物溶液,放入振荡摇床中在一定温度下充分振荡反应。每隔一定时间取样,取样体积为1mL,用高效液相色谱(HPLC)、高效液相色谱(GC-MS)或气相色谱-电子捕获检测器(GC-ECD)分析4-CP及其脱氯产物苯酚、环己酮和脂肪族氯代有机物(一氯乙酸和二氯乙酸);同时测定反应过程中的pH值。实验中三角瓶均用磨口塞密封,反应前的反应液未经N2吹脱除氧,且反应过程中反应液面并未充N2。
1.3 分析仪器和主要试剂
扫描电镜SEM(LEO-1530, 德国LEO公司):表征球磨前后双金属的表面形貌变化,用X射线光谱(EDS)的点扫及微区面扫功能表征双金属中两种元素的含量及分布均匀情况。
4-CP及其降解产物苯酚的浓度采用HPLC检测:色谱柱为ODS-SP柱(5μm,150mm×4.6mmid;GLSciencesInc.,日本),流动相为70%甲醇-30%水,流速1mL/min,柱温40℃。UV/VIS检测波长254nm。
4-CP的另一种降解产物环己酮的浓度采用GC-MS分析:岛津GCMS-QP2010PLUS(配NCI源),进样口温度250℃,不分流进样,进样量1μL;升温程序:初温50℃保持1min,以20℃/min升至300℃保持3min,离子源温度250℃,传输线温度250℃,SIM模式。色谱柱:AgilentDB-5MS(15m×0.25mm×0.1μm)。
脂肪族氯代有机物(一氯乙酸和二氯乙酸)的检测采用GC-ECD分析。先进行酯化处理:取1mL样品置于20mL具塞玻璃比色管中,依次加入0.8mL浓硫酸和1mL甲醇,混合均匀后在65℃恒温水浴40min,加入5mL10%氯化钠及3mL正己烷萃取。再采用7890N气相色谱仪(美国Agilent公司)对一氯乙酸和二氯乙酸进行分析。使用载气为高纯氮(≥99.999%),流量1mL/min。升温程序为:60℃维持2min,以10℃/min升至140℃,维持1min,以20℃/min升至300℃,维持2min。前进样器进样口温度为250℃,后检测器温度为250℃,进样量1μL。一氯乙酸的保留时间为1.13min,二氯乙酸的保留时间为1.53min。
主要试剂包括:铁粉(>99%),铜粉(>99%),苯酚(99%以上),对氯苯酚(4-CP, 99%以上),甲醇(色谱纯)。
2 结果与讨论
2.1 4-CP在Cu-Fe及Cu-Ni球磨合金表面的降解机制
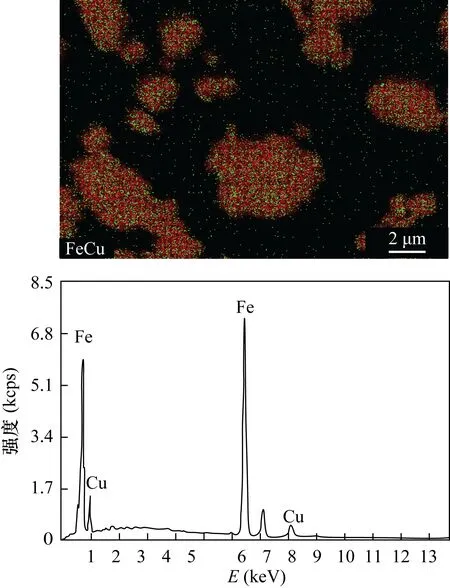
图1 球磨后Cu-Fe混合物的SEM-EDS及元素分布图Fig.1 SEM-EDS images for ball-milled Cu-Fe alloy
首先采用机械球磨技术制备了组分体均匀分散的Cu-Fe双金属复合材料,以pH=2的50μg/L的4-CP溶液的降解率为参照,获得了较佳的球磨制备条件:Cu含量10%,Cu-Fe球磨时间6h,球磨转速 500r/min,球料比37.5∶1。球磨Cu-Fe合金的扫描电镜-能谱(SEM-EDS)如图1所示,球磨后,在微米尺寸的球磨合金中铜铁达到纳米尺寸的混合,Cu与Fe元素分布分别接近混合质量比10%及80%。
球磨混合的Cu-Fe及Cu-Ni合金对4-CP的降解机制不一致,如图2所示。Cu-Fe体系中,在初始pH=2,Cu-Fe双金属比例为1∶9(质量比)时,达到最优的4-CP降解率,为33.97%。Cu-Fe合金遵循催化氢解脱氯机制,Cu与Fe之间以催化金属铜与供氢金属铁协同作用,在一定比例组合时金属的析氢和加氢催化的协同效果最优化。

图2 不同的铜铁比例(a)、铜镍比例(b)球磨合金对初始pH值为2的4-CP降解情况Fig.2 4-CP degradation with different composition ratio of Cu-Fe(a), and Cu-Ni(b) alloy at the initial pH=2
与Cu-Fe体系相反,Cu与Ni金属在Cu-Ni体系并未在合适比例呈现脱氯最优化,Cu-Ni球磨合金对4-CP的降解率仅随着Cu含量的增加而增加,由此推断Ni未起催化作用。改变初始pH值为1~5,Cu-Fe合金对4-CP的降解率在pH=3达到最优化,符合催化金属与供氢金属的需要,因为铜的催化性能与铁的供氢是协同作用机制,过量的析氢容易占据金属表面导致反应活性位点减少,析氢少也不利于加速降解,两者都抑制铜铁双金属不能达到降解所需的氢环境,只能有微弱的降解。与Cu-Fe合金相比,pH对Cu-Ni合金的影响不明显,pH=5的溶液中4-CP的脱氯率比pH=3的脱氯率下降约7%,分析结果表明pH对Cu-Ni体系的影响明显小于Cu-Fe体系,Cu-Ni可能不遵循氢解还原脱氯机制。另外一种金属脱氯机制——直接电子传递还原机制不依赖于还原性氢的出现,因此推断Cu-Ni体系遵循直接电子传递的脱氯机制。
另外,应用HPLC对4-CP降解产物进行分析(图3),在Cu-Fe体系中,4-CP与其降解产物苯酚的总碳基本守恒,表明苯酚是4-CP的主要降解产物,也进一步证实了该降解遵循催化加氢脱氯机制。不同于Cu-Fe体系,在Cu-Ni体系中随着4-CP的降解,所检测到的苯酚含量低,4-CP与苯酚的总碳含量持续下降,下降速率几乎等于其降解速率,表明Cu-Ni体系的最终降解产物并非苯酚,反应产物复杂。
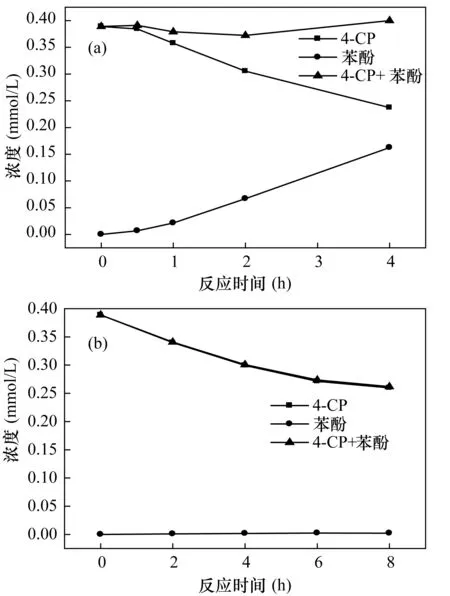
图3 球磨6 h后(a)Cu-Fe合金(1∶9)及(b)Cu-Ni合金降解pH=3的50 mg/L 4-CP溶液降解情况Fig.3 Compound concentrations during the degradation for 50 mg/L 4-CP solution with initial pH=3. The ball-milling time was 6 h for Cu-Fe or Cu-Ni alloy
由此可见,Cu-Ni降解机制异于Cu-Fe降解机制。实验结果表明铜基金属降解有机氯有两种可能路径。由于镍成分越大,降解率越低,推测镍金属并未起到催化加氢的作用,合金的还原作用来源于零价铜。此外,相同条件下对50mg/L的4-CP水溶液降解8h,零价铜获得的降解率达70%以上,而Cu-Fe体系的降解率只有34%,相比之下零价铜的脱氯性能较高,也符合直接电子传递作用比氢解还原活性强的规律。
2.2 4-CP在零价铜表面的降解机制
上述实验并不符合相关文献[11,14]的报道,学者们普遍认为铜是一种惰性金属,它的还原能力差,Cu-Fe、Cu-Al双金属体系普遍只能还原稳定性较差的烷基氯,而对化学稳定性能较好的芳香族有机氯4-CP几乎没有开展研究。
为了求证零价铜高效脱氯的原因,本研究从微观层面考察了4-CP及苯酚在零价铜上降解的路径。由于直接电子传递要求反应物与金属之间间距小,考虑到4-CP的富电子苯环结构可能与零价铜空电子轨道存在共轭作用,实验考察了苯环结构对零价铜表面的还原作用影响。
将零价铜直接处理苯酚溶液,如图4a所示,苯酚的浓度快速下降,降解率上升,表明铜对含有苯环结构的4-CP及苯酚均有高还原活性。还原产物经GC-MS鉴定为苯环加氢产物——环己酮。
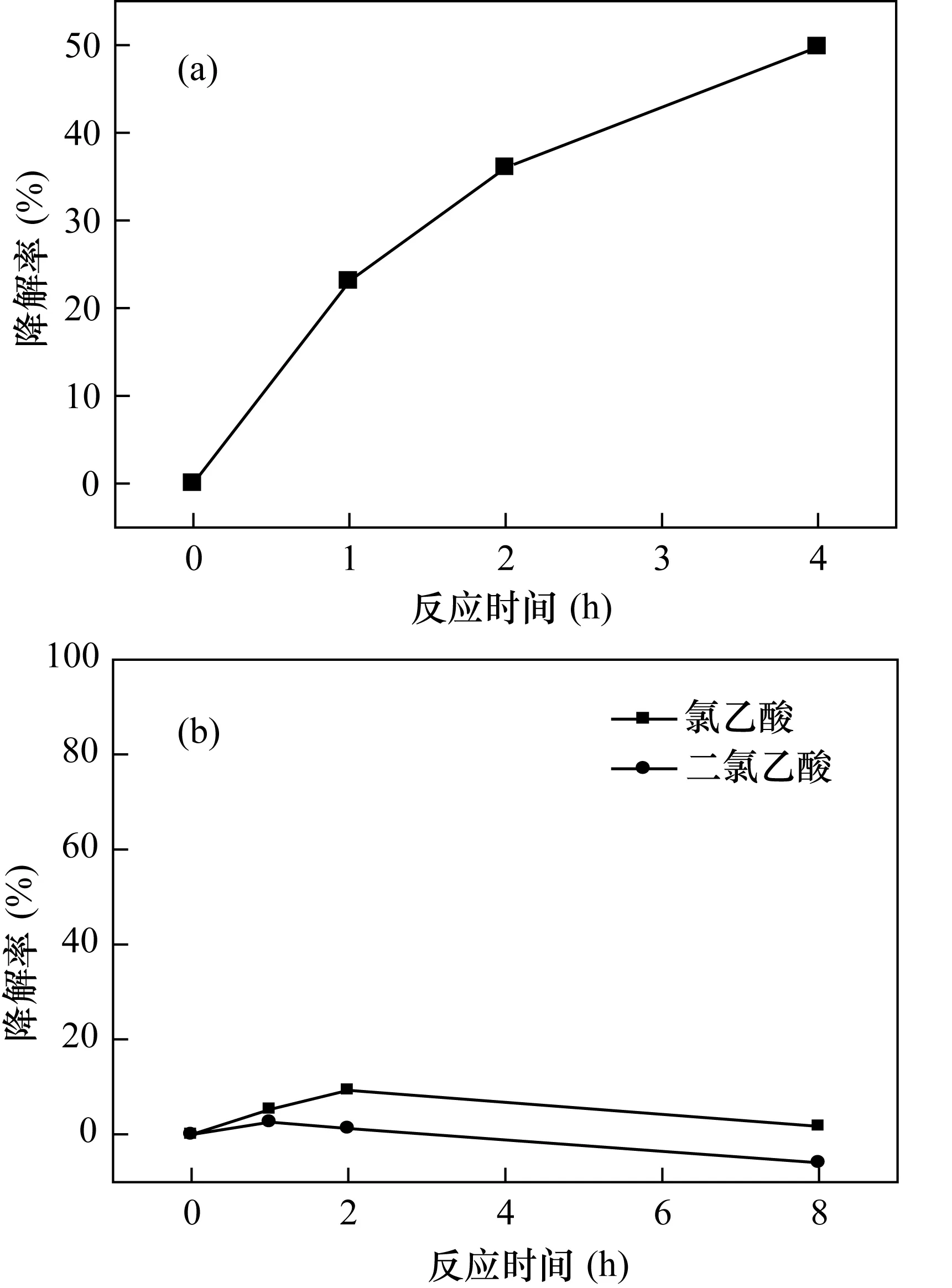
图4 铜粉投加量为100 g/L,对(a)50 mg/L苯酚溶液、(b)500 mg/L一氯乙酸及二氯乙酸的降解情况Fig. 4 Degradation of 100 g/L copper power dosage for (a) 50 mg/L phenol, (b)500 mg/L monochloroacetate and dichloroacetate
苯环是否是零价铜降解有机氯的必要条件?对此,在同样条件下考察了零价铜对脂肪族有机氯(一氯乙酸及二氯乙酸)的降解情况。如图4b所示,零价铜在8h内未能降解一氯乙酸及二氯乙酸。实验结果证实零价铜能够降解化学稳定性比较高的4-CP而未能降解化学稳定性相对较差的一氯乙酸和二氯乙酸,这与催化加氢降解理论相矛盾,进一步证实了零价铜脱氯机制非传统的催化加氢机制,而是直接电子传递还原。苯环分子在零价铜直接电子传递中的重要作用,可能的原因就是零价铜与苯环的pi电子直接的共轭作用,导致有机氯与零价铜的间距减小,实现了电子直接传递。
因共轭作用机理的参与而诱导电子的直接传递机制被不同酸体系下零价铜降解4-CP的结果所证实。以pH=5的盐酸、乙酸、硫酸为溶剂配制相应的50mg/L4-CP溶液,反应的零价铜也以相应的酸进行表面活化,结果如图5a所示。盐酸体系下苯环的降解最快,12h后降解率达92%;乙酸次之,降解率为26%;硫酸几乎不降解。还原反应的速率取决于零价铜表面与有机氯的有效吸附程度,Cl-因强配位作用在零价铜表面的吸附最弱[12,32],大量的表面接触位点被4-CP占据得以被降解。
此外,在盐酸体系中苯酚的浓度呈现先增后减的趋势,4-CP、苯酚及环己酮的总摩尔数稳步下降,如图5b实验结果表明零价铜对4-CP的降解产物——苯酚仍能进一步降解。随着反应进行,环己酮产物增多,同时环己酮的水溶性差且具有挥发性,随着反应进行不断挥发,导致总碳下降,由此可以解释在零价铜直接电子传递还原过程中呈现4-CP与苯酚两物质的质量不断下降。
3 结语
本研究发现零价铜遵循直接电子传递还原脱氯机制。借鉴微观界面分析技术及色谱分离技术,充分表征了界面脱氯机制的选择及复杂产物的转化过程。
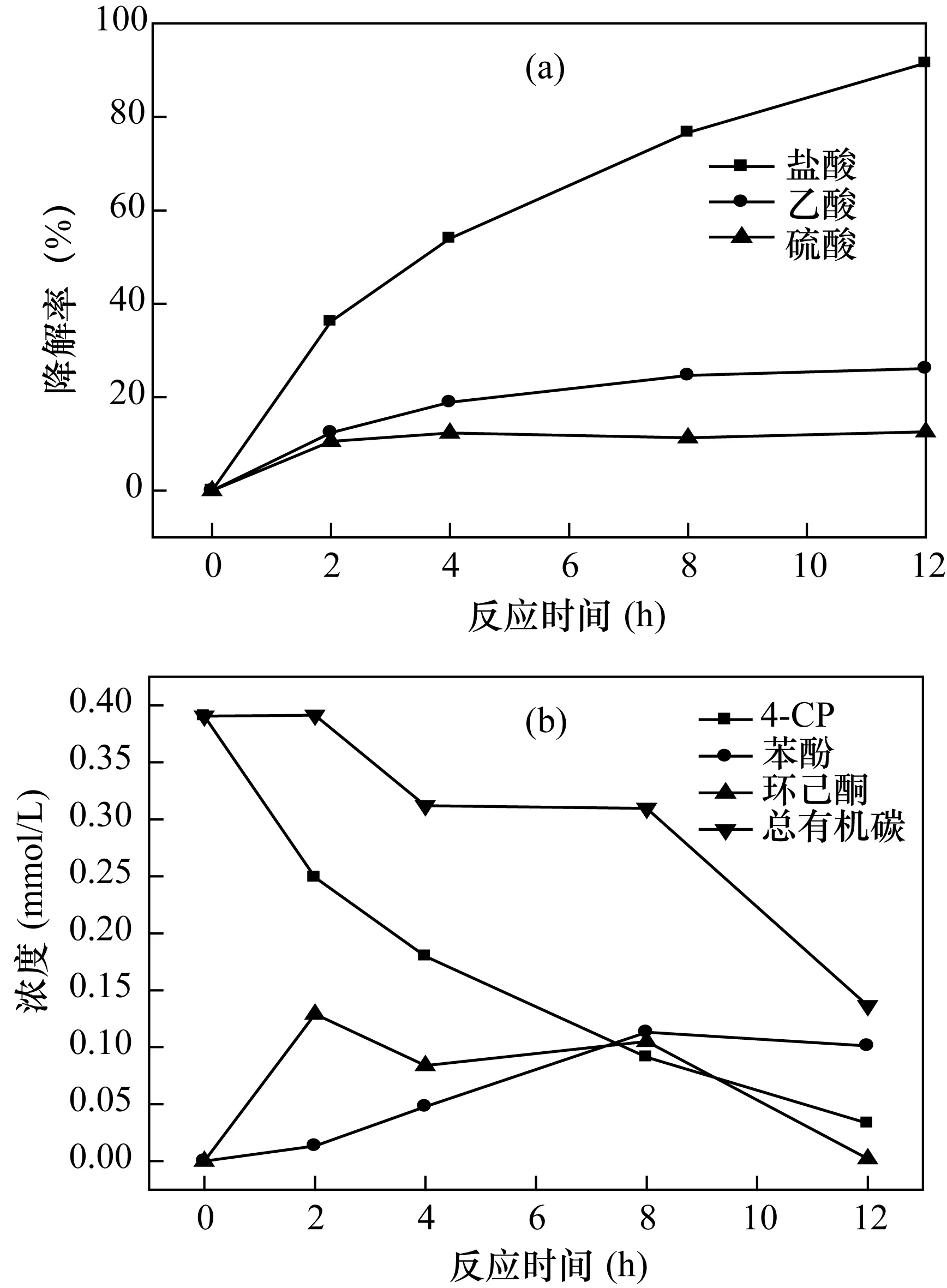
图5 (a) pH=5的不同酸体系下,100 g/L铜粉对50 mg/L的4-CP降解曲线;(b) 盐酸体系中4-CP的降解曲线,苯酚、环己酮生成曲线与总有机碳变化曲线
在Cu-Fe球磨合金的微观环境中与Cu-Ni及单独零价铜的微环境存在下,零价铜对4-CP的还原脱氯机制不一致。在Cu-Fe合金体系中,4-CP的降解产物为苯酚。零价铜对4-CP呈现出强还原活性,最终产物为苯环加氢产物——环己酮。有机氯分子的苯环结构是零价铜直接电子传递还原的诱因,脂肪族与芳香族有机氯在零价铜表面截然不同的降解率表明零价铜的还原活性得益于苯环与零价铜的弱吸附作用。
本研究为零价铜在还原脱氯污染物治理方面的进一步科学研究及实际应用提供了新的理论依据。基于本研究获得的结论,今后有必要更深入地研究铜基材料其他组合方式及相关机理研究,探索零价铜作为环境脱氯材料的工程化应用的可能性。
[1]Escobar-HoyosLF,Hoyos-GiraldoLS,Londoo-VelascoE,etal.GenotoxicandClastogenicEffectstoMonohaloaceticAcidDrinkingWaterDisinfectionBy-productsinPrimaryHumanLymphocytes[J].WaterResearch,2013,47:3282-3290.
[2] 司雄元,司友斌,陈涛,等.纳米Fe、Si体系对3,3’,4,4’-四氯联苯的脱氯降解[J].中国环境科学, 2011,31(5):761-767.
SiXY,SiYB,ChenT,etal.DechlorinativeDegradationof3,3’,4,4’-tetrachlorobiphenylbyNanometer-sizedFeandSi[J].ChinaEnvironmentalScience,2011,31(5):761-767.
[3] 常春,祝凌燕,朱淑贞.纳米零价铁对γ-HCH的降解效果及机理研究[J].中国环境科学,2010,30(2):167-173.
Chang C,Zhu L Y,Zhu S Z.Degradation Efficiency and Mechanisms ofγ-Hexachlorocyclohexane by Nanoscale Zero Valent Iron Particles[J].China Environmental Science,2010,30(2):167-173.
[4] 王姝,杨波,张婷婷,等.钯/泡沫镍对水体中4-氯酚的氢解脱氯研究[J].中国环境科学,2009,29(10):1065-1069.
Wang Z,Yang B,Zhang T T,et al.Catalytic Hydrodechlorination of 4-chlorophenol in Aqueous Solution by a Palladized Foam Nickel Catalyst[J].China Environmental Science,2009,29(10):1065-1069.
[5] 陈卫明,邓天龙,张勤,等.土壤中有机氯农药残留的分析技术研究进展[J].岩矿测试,2009,28(2):151-156.
Chen W M,Deng T L,Zhang Q,et al.Progresses on Organochlorine Pesticide Residue Analysis for Soil Samples[J].Rock and Mineral Analysis,2009,28(2):151-156.
[6] Salter-Blanc A J,Tratnyek P G.Effects of Solution Chemistry on the Dechlorination of 1,2,3-trichloropropane by Zero-valent Zinc[J].Environmental Science & Technology,2011,45:4073-4079.
[7] Xu,F Y,Deng S B,Xu J,et al.Highly Active and Stable Ni-Fe Bimetal Prepared by Ball Milling for Catalytic Hydrodechlorination of 4-chlorophenol[J].Environmental Science & Technology,2012,46:4576-4582.
[8] Agarwal S,Al-Abed S R,Dionysiou D D.Enhanced Corrosion-based Pd/Mg Bimetallic Systems for Dechlorination of PCBs[J].Environmental Science & Technology,2007,41:3722-3727.
[9] Agarwal S,Al-Abed S R,Dionysiou D D,et al.Reactivity of Substituted Chlorines and Ensuing Dechlorination Pathways of Select PCB Congeners with Pd/Mg Bimetallics[J].Environmental Science & Technology,2008,43:915-921.
[10] Yang B,Deng S B,Yu G,et al.Pd/Al Bimetallic Nanoparticles for Complete Hydrodechlorination of 3-chlorophenol in Aqueous Solution[J].Chemical Engineering Journal,2013,219:492-498.
[11] Zhu N,Luan H,Yuan S,et al.Effective Dechlorination of HCB by Nanoscale Cu/Fe Particles[J].Journal of Hazardous Materials,2010,176:1101-1105.
[12] Mahmoud S S.Electrochemical Studies of Pitting Corrosion of Cu-Fe Alloy in Sodium Chloride Solutions[J].Journal of Alloys and Compounds,2008,457:587-592.
[13] Yin L,Dai Y,Niu J,et al.Rapid Dechlorination of Chlorophenols in Aqueous Solution by [Ni|Cu] Microcell[J].Journal of Hazardous Materials,2012,209-210:414-420.
[14] Yuan Y,Li H Q,Lai B,et al.Removal of High-concentration CI Acid Orange 7 from Aqueous Solution by Zerovalent Iron/Copper (Fe/Cu) Bimetallic Particles[J].Industrial & Engineering Chemistry Research,2014,53:2605-2613.
[15] Lei Y Z,Zhao G H,Zhang Y G,et al.Highly Efficient and Mild Electrochemical Incineration: Mechanism and Kinetic Process of Refractory Aromatic Hydrocarbon Pollutants on Superhydrophobic PbO2Anode[J].Environmental Science & Technology,2010,44:7921-7927.
[16] Chu W.Photodechlorination Mechanism of DDT in a UV/Surfactant System[J].Environmental Science & Technology,1998,33:421-425.
[17] Cheng I F,Fernando Q,Korte N.Electrochemical Dechlorination of 4-chlorophenol to Phenol[J].Environmental Science & Technology,1997,31:1074-1078.
[18] Gao X,Yang F,Lan Y,et al.Rapid Degradation of Carbon Tetrachloride by Commercial Micro-scale Zinc Powder Assisted by Citric Acid[J].Environmental Chemistry Letters,2011,9:431-438.
[19] Cheng R,Wang J L,Zhang W X.Reductive Dechlorination of 2,4-dichlorophenol Using Nanoscale Fe0: Influencing Factors and Possible Mechanism[J].Science in China (Series B: Chemistry),2007,4:574-579.
[20] 李智灵,杨琦,尚海涛,等.负载型纳米Pd/Fe对氯代烃脱氯机理研究[J].环境科学,2008,29(4):978-984.
Li Z L,Yang Q,Shang H T,et al.Dechlorination Mechanisms of Chlorinated Hydrocarbons by Supported Nanoscale Pd/Fe[J].Environmental Science,2008,29(4):978-984.
[21] 徐新华,刘永,卫建军,等.纳米级Pd/Fe双金属体系对水中2,4-二氯苯酚脱氯的催化作用[J].催化学报,2004,25(2):138-142.
Xu X H,Liu Y,Wei J J,et al.Catalytic Dechlorination of 2,4-dichlorophenol in Water by Nanoscale Pd/Fe Bimetallic System[J].Chinese Journal of Catalysis,2004,25(2):138-142.
[22] 魏红,李克斌,童少平,等.镍/铁二元金属对莠去津脱氯特性的影响[J].环境科学,2004,25(1):154-157.
Wei H,Li K B,Tong S P,et al.Reductive Dechlorination of Atrazine by Ni/Fe Bimetallic Particles[J].Chinese Journal of Environmental Science,2004,25(1):154-157.
[23] Chang C,Lian F,Zhu L.Simultaneous Adsorption and Degradation ofγ-HCH bynZVI/Cu Bimetallic Nanoparticles with Activated Carbon Support[J].Environmental Pollution,2011,159:2507-2514.
[24] Cao J,Xu R,Tang H,et al.Synthesis of Monodispersed CMC-stabilized Fe-Cu Bimetal Nanoparticles for in situ Reductive Dechlorination of 1,2,4-trichlorobenzene[J].Science of the Total Environment,2011,409:2336-2341.
[25] Zhu L,Huang Q,Zhao H.Effect of Nickel Content and Milling Parameters on Martensitic Transformation of Fe-Ni during Mechanical Alloying[J].Scripta Materialia,2004,51:527-531.
[26] 郭秀芝,刘力,姚斌.机械球磨中Fe与BN反应形成Fe-N合金的结构表征及其磁性[J].吉林大学学报(理学版),2008,46(3):535-538.
Guo X Z,Liu L,Yao B.Structural Characterization and Properties of Fe-N Alloy Prepared by Reaction between Fe and BN during Ball Milling[J].Journal of Jilin University (Science Edition),2008,46(3):535-538.
[27] 罗永春,毛松科,阎汝煦,等.机械球磨固相化学反应制备AlH3及其放氢性能[J].物理化学学报,2009,25(2):237-241.
Luo Y C,Mao S K,Yan R X,et al.Synthesis of A1H3by a Ball-milling Solid-phase Chemical Reaction and Its Hydrogen Desorption Properties[J].Acta Physico-Chimica Sinica,2009,25(2):237-241.
[28] 黄园英,刘菲,汤鸣臬,等.纳米镍/铁和铜/铁双金属对四氯乙烯脱氯研究[J].环境科学学报,2007,27(1):80-85.
Huang Y Y,Liu F,Tang M A,et al.Decldorination of Tetrachloroethene with Nanoscale Ni/Fe and Cu/Fe Bimetallic Particles[J].Acta Scientiae Circumstantiae,2007,27(1):80-85.
[29] 杜永光,张海军,陈吉平,等.氧化铜催化五氯苯生成二噁英的研究[J].环境科学,2010,31(11):2774-2779.
Du Y G,Zhang H J,Chen J P,et al.PCDD/Fs Formation from Pentachlorobenzene under the Catalysis of CuO[J].Environmental Science,2010,31(11):2774-2779.
[30] 王清萍,况烨,金晓英,等.海藻酸钙包覆纳米Ni/Fe颗粒用于同时去除水中铜离子和氯苯[J].环境科学学报,2014,34(5):1228-1235.
Wang Q P,Kuang Y,Jin X Y,et al.Simultaneous Removal of Cu (Ⅱ) and Chlorobenzene from Aqueous Solution by CA-Ni/Fe Nanoparticles[J].Acta Scientiae Circumstantiae,2014,34(5):1228-1235.
[31] Li X C,Ma J,Liu G F,et al.Efficient Reductive Dechlorination of Monochloroacetic Acid by Sulfite/UV Process[J].Environmental Science & Technology,2012,46:7342-7349.
[32] Zhao X,Ding Y,Ma L,et al.Structure,Morphology and Electrocatalytic Characteristics of Nickel Powders Treated by Mechanical Milling[J].International Journal of Hydrogen Energy,2008,33:6351-6356.
Effect of Molecular Structure in Chlorinated Organic Compounds on Zero-valent Copper Degradation Mechanism Based on SEM-EDS and GC-MS Techniques
ZHUHong,LIUJing,JIAOHan-tao,ZHANGJing,DUANJiang-tao,LIANXing-ye,HOUYa-nan
(College of Biological Science and Engineering, Beijing University of Agriculture, Beijing 102206, China)
Zero-valent copper, even cheap, is rarely used in hydrodechlorination (such as chlorinated aromatic hydrocarbons), because Cu has poor catalytical dechlorination activity and complex reaction mechanisms. In this study, Cu-Fe and Cu-Ni alloys were prepared by mechanical ball-milling, and the effect of micro-environment for the chlorophenol (4-CP) dechlorination behavior of Cu was studied in order to investigate the effect of organic chlorine molecular structure on Cu dechlorination. Two reaction mechanisms were examined for low-cost copper during dechlorination. SEM-EDS and GC-MS analyses show that the structure of organic chlorine and Cu metal environment could directly affect the mechanism. In the Cu-Fe system, Cu follows the classic catalytic hydrodechlorination mechanism and the degradation product 4-CP is phenol. But in the Cu-Ni system, nickel metal does not play a catalytic hydrogenation of action, the degraded product for 4-CP by Cu-Ni alloy is cyclohexanone. Copper acts as hydrogen-metal and shows a strong reducing activity by direct electron transfer. 4-CP degradation for Zero-valent copper was up to 70%, while only 34% for Cu-Fe system. These differences concluded that the aromatic ring was a direct electron transfer for Cu. Zero-valent copper can degrade 4-CP and phenol with high chemical stability, but cannot degrade aliphatic chlorinated organics (e.g., monochloroacetic acid and dichloroacetic acid) with relatively poor chemical stability. In conclusion, dechlorination mechanism for zero-valent copper is not traditional catalytic hydrodechlorination, but the direct electron transfer reduction mechanism which is affected by target molecule structure.
chlorinated organic compounds; zero-valent copper; copper alloy; degradation mechanism; mechanical ball milling; Scanning Electron Microscopy-Energy-dispersive Spectrometry (SEM-EDS); Gas Chromatography-Mass Spectrometry (GC-MS)
2014-02-18;
2015-03-19; 接受日期: 2015-03-22
北京农学院促进人才培养综合改革专项计划(BNRC&YX201412);国家自然基金青年基金项目(21207077)
朱洪,博士,讲师,主要从事生物分子检测与有机污染物降解研究。 E-mail: zhuhong80@bua.edu.cn。
0254-5357(2015)02-0169-07
10.15898/j.cnki.11-2131/td.2015.02.003
O657.63
A

