新型石墨烯磁性复合材料的制备及其对水中亚甲基蓝的吸附去除
王赛花,牛红云,蔡亚岐
(中国科学院 生态环境研究中心,北京 100085)
研究报告
新型石墨烯磁性复合材料的制备及其对水中亚甲基蓝的吸附去除
王赛花,牛红云*,蔡亚岐
(中国科学院 生态环境研究中心,北京 100085)
采用绿色、温和的方法合成了一种新型的磁性纳米复合材料(Fe3O4@PDA@RGO),并考察了其对水溶液中亚甲基蓝的吸附去除效果。多巴胺通过自聚合作用可以直接吸附到Fe3O4表面,其既是氧化石墨烯(GO)的还原剂,也是Fe3O4和还原态氧化石墨烯(RGO)组装的偶联剂。反应过程中无需热处理或加入其他有机试剂。利用透射电子显微镜(TEM)、红外光谱(FTIR)、X衍射光谱(XRD)和拉曼光谱等技术对制备的磁性纳米复合材料进行了表征。结果表明,Fe3O4@PDA@RGO具有较强的磁性(37.8 emu·g-1),对亚甲基蓝有较高的吸附去除能力(98 mg·g-1)。Fe3O4@PDA@RGO对亚甲基蓝的吸附能力随着pH值的增大而增强,其吸附过程符合拟二级反应动力学方程和Langmuir吸附模型。Fe3O4@PDA@RGO作为吸附剂,其性质稳定,经磁性分离可重复利用10次以上。
磁性纳米材料;多巴胺;石墨烯;吸附剂
石墨烯(Graphene)是一种由碳原子以sp2杂化方式互相键合形成的蜂窝状结构排布的单原子二维材料,其在光学、电学、热学及力学等方面表现出许多优异的性质,如比表面积大、机械性能独特、导电性高、化学性质稳定等,在电子器件、储氢、纳米材料、传感器、电池和超级电容器等领域有巨大的应用潜力[1-6]。石墨烯是金属或金属氧化物的优良载体,如Xu等[7]以氧化石墨烯(Graphene oxide,GO)为前体,利用水-乙二醇体系中乙二醇的还原作用,将金属纳米粒子(Au,Pt和Pd)负载到氧化石墨烯表面,并生成了石墨烯-金属复合纳米材料;Huang等[8-9]在GO和还原态氧化石墨烯(RGO)表面负载了Au和Ag纳米颗粒。由于负载纳米颗粒的石墨烯不易从溶液中分离出来,不利于其实验操作和材料的回收利用,因此将磁性纳米颗粒和石墨烯相结合,合成的磁性石墨烯复合材料显示了更好的应用前景。
磁性石墨烯复合材料兼具磁性材料和石墨烯的特殊性质,在能量储存、药物传递和污染物去除等领域有广泛的应用[10-12]。在磁性石墨烯复合材料的制备过程中,氧化石墨烯的还原过程往往依赖大量的有机试剂或是高温反应[13-14],危害环境,因此有必要寻找一种绿色、温和的还原剂。多巴胺(Dopamine)是一种重要的神经递质,在神经信号传递和学习记忆活动中发挥着重要作用。在弱碱条件下,多巴胺可在空气中通过氧化-还原反应自聚合形成聚多巴胺(Polydopamine,PDA)并包覆在多种有机和无机材料表面[15]。聚多巴胺也能直接还原金属盐并生成金属纳米颗粒[16-17]。多巴胺特有的吸附性、自聚合性和还原性使其既能作为氧化石墨烯的还原剂,又可作为Fe3O4纳米颗粒和石墨烯的偶联剂。
本研究以多巴胺为媒介,通过绿色、简单的途径成功合成了磁性石墨烯复合材料Fe3O4@PDA@RGO。反应在室温下进行,且反应过程中不涉及有毒有机试剂,降低了能耗,减少了污染。合成的Fe3O4@PDA@RGO可用于水溶液中亚甲基蓝(Methylene blue,MB)的吸附去除。
1 实验部分
1.1 试 剂
六水合三氯化铁(FeCl3·6H2O)、四水合二氯化铁(FeCl2·4H2O)、氢氧化钠(NaOH)、三羟甲基氨基甲烷(Tris)和盐酸(HCl)由北京国药集团提供。多巴胺(98%)购自J&K化学有限公司。氧化石墨烯由先丰纳米材料科技有限公司提供。亚甲基蓝购自Acros Organics。实验用纯水来自于美国Milli-Q纯水系统。所有的化学试剂均为分析纯,且未经过进一步净化。
1.2 Fe3O4@PDA@RGO的制备
磁性纳米颗粒(Fe3O4NPs)通过共沉淀法合成[18]。取400 mg 合成的Fe3O4颗粒,溶于200 mL Dopamine-Tris溶液(2 mg·mL-1,pH 8.5,10 mmol/L Tris-HCl缓冲溶液)中,混合溶液于室温下机械搅拌8 h。产物(Fe3O4@PDA)经磁性分离后,用水清洗3次,然后分散于100 mL水中。50 mg氧化石墨烯超声30 min后溶于100 mL水中,然后与Fe3O4@PDA水溶液混合,继续在室温下搅拌24 h。生成的Fe3O4@PDA@RGO用水和无水乙醇各清洗3次后,于50 ℃烘箱中干燥12 h备用。
1.3 Fe3O4@PDA@RGO的表征
Fe3O4@PDA@RGO的形貌用Hitachi H-7500透射电镜(TEM,Tokyo,日本)进行分析。紫外-可见光谱由Beckman DU 800核酸/蛋白分析仪(Ice.Rosemead,CA)测定。材料的晶体结构由X射线衍射分析仪(XRD,PAN-alytical X’Pert diffractometer,Almelo,荷兰)测定,使用镍过滤Cu Kα射线,扫描速度为4 °·min-1。采用N2吸附BET法(ASAP2000V 3.01 A,Micromeritics,Norcross,GA)测定材料的比表面积。磁性能采用振动磁强计(VSM,LDJ9600)于室温下测得。红外谱图(FTIR)采用KBr压片方式在NEXUS670傅立叶变换红外光谱仪(Nicolet Thermo,USA)上采集。拉曼光谱由拉曼光谱仪(RM2000,Renishaw,UK)获得,其激发波长为514.5 nm,由Ar+激光激发产生。
1.4 批吸附实验
Fe3O4@PDA@RGO对水溶液中亚甲基蓝的吸附实验采用批实验。亚甲基蓝储备液的浓度为200 mg·L-1,使用时再稀释至所需浓度。批吸附实验在聚乙烯小瓶中进行,在恒温振荡器中达到平衡后,进行磁性分离,上清液中剩余亚甲基蓝的浓度通过紫外-可见分光光度计进行分析。单位质量的吸附剂吸附的亚甲基蓝(qe,mg·g-1)由公式(1)计算得出:
qe=(c0-ce)V/m
(1)
式中,c0和ce分别为亚甲基蓝的初始浓度和平衡浓度(mg·L-1),m为吸附剂的质量(g),V为溶液的体积(L)。
吸附剂的浓度为1 g·L-1。用0.1 mol/L的盐酸和氢氧化钠调节溶液pH值,在pH 3.0~10.0的范围内,考察溶液初始pH值对亚甲基蓝吸附去除的影响,亚甲基蓝的浓度为120 mg·L-1,反应时间为6 h。在不同亚甲基蓝浓度(20~200 mg·L-1)下考察温度(298,308,318 K)对其吸附的影响。在反应过程中每隔一定时间对分析溶液(80 mg·L-1)中的亚甲基蓝进行测定,从而得到亚甲基蓝的吸附动力学方程。所有实验重复3次,最后结果取3次实验结果的平均值。
1.5 解吸附实验
将0.01 g Fe3O4@PDA@RGO加入到10 mL亚甲基蓝溶液中(30 mg·L-1),在200 r/min的摇床中平衡6 h,磁性分离后,取上清液分析其中剩余亚甲基蓝的浓度;然后倒掉剩余的上清液,加入20 mL乙醇溶液(pH 3.0),使吸附了亚甲基蓝的吸附剂完全解吸。亚甲基蓝的吸附-解吸过程重复10次。
2 结果与讨论
2.1 Fe3O4@PDA@RGO的表征

图1 Fe3O4@PDA(A)和Fe3O4@PDA@RGO(B)的透射电镜图片
图1是Fe3O4@PDA和Fe3O4@PDA@RGO的透射电镜图片。Fe3O4磁性纳米颗粒粒径均一,平均直径约10 nm。合成的Fe3O4@PDA为明显的核壳结构,聚多巴胺层包覆于Fe3O4表面,为其提供了有效的保护。Fe3O4@PDA颗粒加入到GO水溶液后,在聚多巴胺和GO之间强烈的π-π堆积作用下,沉积在氧化石墨烯表面。同时GO在聚多巴胺的还原作用下转化为RGO,从而形成Fe3O4@PDA@RGO。石墨烯层有明显的单层皱褶结构,显著地增大了纳米颗粒的比表面积。
利用BET法测得Fe3O4,Fe3O4@PDA和Fe3O4@PDA@RGO的比表面积分别为116,63,88 m2·g-1。相较于Fe3O4,Fe3O4@PDA的比表面积有所下降,这是由于包覆多巴胺后,颗粒的粒径变大,同时在反应过程中纳米颗粒出现了部分团聚,导致比表面积减小。加入GO后,由于GO的单层结构和大的比表面积,Fe3O4@PDA@RGO的比表面积又有所增加。
产物的晶体结构由XRD进行表征。如图2A曲线a所示,Fe3O4的晶相符合立方磁铁矿的晶型(JCPDS card no.19-0629)。与Fe3O4相比,包覆无定形的多巴胺后,Fe3O4@PDA的谱图几乎无变化。Fe3O4@PDA@RGO在2θ=21°~27°间有一较宽的小峰,对应RGO层的无序堆积,表明GO被部分还原为RGO[19]。


图2 Fe3O4,Fe3O4@PDA和Fe3O4@PDA@RGO的X射线衍射图(A)和磁滞回线(B)
磁性吸附剂在实际应用中具有超顺磁性和高的饱和磁强度是必要的。如图2B所示,Fe3O4,Fe3O4@PDA和Fe3O4@PDA@RGO均无磁滞现象,矫顽力和剩磁均为0,表现出明显的超顺磁性,其饱和磁强度分别为47.8,42.2,37.8 emu·g-1。尽管非磁性物质的加入使产物的饱和磁强度有所下降,但仍能满足在外加磁场作用下的快速分离。

拉曼光谱用来鉴定反应过程中GO向RGO的结构变化。如图3B所示,GO和Fe3O4@PDA@RGO的拉曼光谱在1 000~1 800 cm-1处均有2个较明显的峰:D峰代表碳原子晶格的缺陷和无序诱导,G峰代表碳原子sp2杂化的面内伸缩振动。GO谱图中,在1 360 cm-1和1 600 cm-1处存在着典型的D峰和G峰。经聚多巴胺还原后,Fe3O4@PDA@RGO的G峰变宽并向左移至1 576 cm-1处,D峰的强度下降。D峰和G峰的强度比(ID/IG)由0.93降至0.80。这一结果表明GO和聚多巴胺间发生了氧化还原作用,GO被还原为RGO,且可以与Fe3O4@PDA稳定结合。


图3 GO,Fe3O4,Fe3O4@PDA和Fe3O4@PDA@RGO的红外光谱(A)及GO和Fe3O4@PDA@RGO的拉曼光谱(B)
2.2 Fe3O4@PDA@RGO对亚甲基蓝的吸附性能
2.2.1 pH值的影响 如图4A所示,Fe3O4@PDA@RGO对亚甲基蓝(120 mg·L-1)的吸附去除能力随着pH值的增大而增强。聚多巴胺和石墨烯均含有大量的苯环结构,可对亚甲基蓝提供π-π堆积作用。由于Fe3O4和多巴胺的pKa分别为6.5和8.87,在酸性溶液中吸附剂表面带正电荷,与带正电的亚甲基蓝存在静电排斥作用,使亚甲基蓝的吸附能力降低。随着溶液pH值增加,Fe3O4和多巴胺所含的正电荷降低,同时石墨烯表面的含氧基团不断电离,使吸附剂表面负电荷增多,与亚甲基蓝之间的静电吸附作用增强,促进了亚甲基蓝的吸附。当pH>8.87时,聚多巴胺的H+全部解离,而吸附剂中的Fe3O4和石墨烯带负电,进一步促进了亚甲基蓝的吸附。因此碱性条件有利于Fe3O4@PDA@RGO对亚甲基蓝的去除。

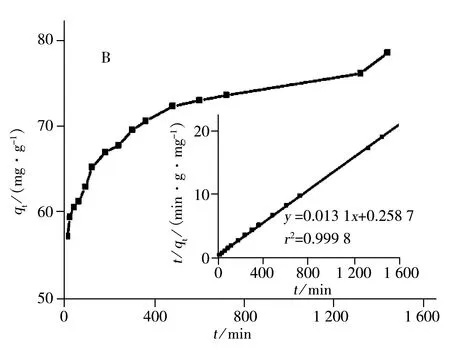
图4 pH值(A)和时间(B)对Fe3O4@PDA@RGO 吸附去除MB的影响

图5 温度对Fe3O4@PDA@RGO吸附 MB的影响(pH 10.0)
2.2.2 吸附动力学 以Fe3O4@PDA@RGO为吸附剂,考察了吸附时间对亚甲基蓝吸附去除能力的影响。如图4B所示,70%的亚甲基蓝在10 min内即可被吸附到材料表面,480 min内吸附率可达90%,24 h内达到吸附平衡。该吸附过程符合拟二级反应动力学方程:
t/qt=1/(k2qe2)+t/qe
(2)
式(2)中k2是拟二级反应动力学的速率常数(g·mg-1·h-1),qe和qt分别表示平衡时或某一时间Fe3O4@PDA@RGO对亚甲基蓝的吸附量(mg·g-1)。以t/qt对t作图(图4B插图),可求出qe和k2。实验测得qe为79 mg·g-1,经计算得出qe为76 mg·g-1,二者非常接近,且直线的相关系数为0.999 8,表明拟二级动力学模型适用于Fe3O4@PDA@RGO对亚甲基蓝的吸附过程。
2.2.3 温度的影响 考察了不同温度对Fe3O4@PDA@RGO吸附亚甲基蓝的影响。如图5所示,Fe3O4@PDA@RGO对亚甲基蓝的吸附容量随着温度的升高而增大。当温度由298 K升至318 K时,亚甲基蓝的吸附容量由98 mg·g-1增至118 mg·g-1。表明Fe3O4@PDA@RGO对亚甲基蓝的吸附为吸热过程。
采用Langmuir和Freundlich吸附模型拟合Fe3O4@PDA@RGO对亚甲基蓝的吸附:
ce/qe=1/(QmKL)+ce/Qm
(3)
lnqe=lnKF+(lnce)/n
(4)
式中,ce(mg·L-1)为亚甲基蓝的平衡浓度,qe(mg·g-1)为单位质量吸附剂吸附的亚甲基蓝的量,Qm(mg·g-1)为最大吸附容量,KL(L·mg-1)为平衡常数,KF(mg·g-1·L1/n·mg-1/n)和n分别为与吸附剂的吸附容量和吸附强度有关的Freundlich系数。如表1所示,Fe3O4@PDA@RGO吸附亚甲基蓝的Langmuir方程的相关系数均大于0.998,表明Fe3O4@PDA@RGO对亚甲基蓝的吸附符合Langmuir方程。Fe3O4@PDA@RGO对亚甲基蓝的吸附容量显著高于亚甲基蓝在GNS/Fe3O4和Magnetic Fe3O4@Graphene上的吸附量,低于文献报道的其他碳材料吸附剂(表2)。但将吸附容量面积归一化后发现,Fe3O4@PDA@RGO对亚甲基蓝的去除能力为1.11 mg·m-2,是其他吸附材料的2~6倍。这一结果表明,Fe3O4@PDA@RGO表面负电荷与亚甲基蓝间的静电吸附作用,以及石墨烯中苯环与亚甲基蓝间的π-π作用显著增强了Fe3O4@PDA@RGO对亚甲基蓝的吸附去除能力。
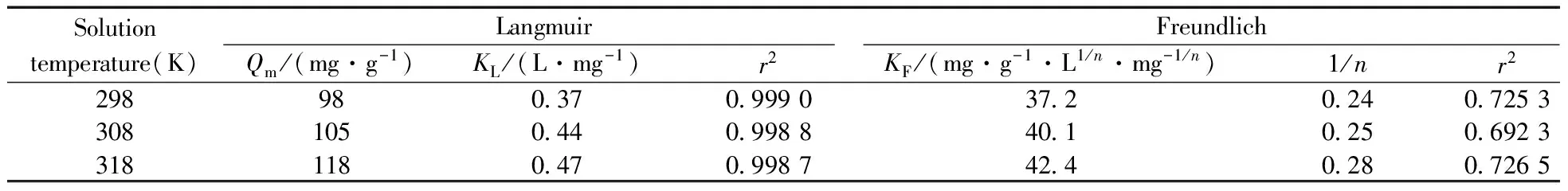
表1 不同温度下Fe3O4@PDA@RGO吸附MB的Langmuir和Freundlich参数

表2 不同吸附剂qe的比较
*the uptake of MB per unit surface area,calculated by theQmobtained from Langmuir model and BET surface area(单位面积吸附剂吸附的亚甲基蓝,由Qm除以BET比表面积获得);-:no data
2.2.4 吸附热力学 吸附过程中的吉布斯自由能可通过亚甲基蓝在固液两相中的分配系数(KD)计算,其公式为:
ΔG°=-RTlnKD
(5)
其吸附过程的熵变(ΔS°)和焓变(ΔH°)可通过公式计算:
lnKD=ΔS°/R-ΔH°/(RT)
(6)
式中,R(8.314 J·mol-1·K-1)为通用气体常数,T(K)为溶液的绝对温度。

表3 Fe3O4@PDA@RGO吸附MB的热力学参数

图6 Fe3O4@PDA@RGO吸附MB的重复利用
Fe3O4@PDA@RGO吸附亚甲基蓝的热力学参数如表3所示,其ΔG°均为负值,表明Fe3O4@PDA@RGO对亚甲基蓝的吸附是自发过程。焓变ΔH°为正值,表明亚甲基蓝的吸附过程为吸热过程,说明升高温度有利于亚甲基蓝在Fe3O4@PDA@RGO上的吸附,这和亚甲基蓝的吸附容量随着温度升高而增大的结果一致。ΔH°大于40 kJ·mol-1,吸附过程是化学吸附;ΔH°小于40 kJ·mol-1,吸附过程是物理吸附[30]。Fe3O4@PDA@RGO吸附亚甲基蓝的ΔH°是17.6 kJ·mol-1,表明其吸附过程是物理吸附。
2.2.5 吸附剂的再生利用 吸附剂的重复利用率是实际应用中需要考察的问题。用外加磁铁将吸附了亚甲基蓝的Fe3O4@PDA@RGO从溶液中分离出来,经酸性乙醇溶液解吸附后,再次吸附亚甲基蓝,这一过程重复10次。如图6所示,Fe3O4@PDA@RGO可以多次吸附亚甲基蓝,去除效率均在98%以上,表明Fe3O4@PDA@RGO的结构稳定,可以重复利用。
3 结 论
本研究通过绿色、温和的方法合成了一种新型的磁性纳米吸附剂(Fe3O4@PDA@RGO)。多巴胺通过自聚合作用可以直接吸附到Fe3O4表面,其既是GO的还原剂,也是RGO组装的偶联剂,且反应过程无需热处理或加入其他有机试剂,简化了实验步骤。合成的Fe3O4@PDA@RGO具有较强的磁性,对亚甲基蓝具有较高的吸附去除能力。Fe3O4@PDA@RGO对亚甲基蓝的吸附随着pH值的增大而增强,其吸附过程符合拟二级反应动力学方程和Langmuir吸附模型,且吸附剂可以再生多次重复利用,有望成为水环境中去除亚甲基蓝的高效、绿色吸附剂。
[1] Sun X,Kang T F.J.Instrum.Anal.(孙雪,康天放.分析测试学报),2013,32(6):693-698.
[2] Yang J,Liu Z M,Zhan H J,Wang Z L.J.Instrum.Anal.(杨君,刘志敏,展海军,王珍玲.分析测试学报),2014,33(4):403-408.
[3] Zhou L Z,Fu S,Yu K P,Gao S Q,He G W.J.Instrum.Anal.(周乐舟,付胜,余克平,高寿泉,贺国文.分析测试学报),2013,32(10):1242-1246.
[4] Im H,Kim J.Carbon,2012,50(15):5429-5440.
[5] Wang S J,Geng Y,Zheng Q,Kim J K.Carbon,2010,48(6):1815-1823.
[6] Balandin A A,Ghosh S,Bao W Z,Calizo I,Teweldebrhan D,Miao F,Lau C N.NanoLett.,2008,8(3):902-907.
[7] Xu C,Wang X,Zhu J.J.Phys.Chem.C,2008,112(50):19841-19845.
[8] Huang X,Zhou X,Wu S,Wei Y,Qi X,Zhang J,Boey F,Zhang H.Small,2010,6(4):513-516.
[9] Zhou X,Huang X,Qi X,Wu S,Xue C,Boey F Y,Yan Q,Chen P,Zhang H.J.Phys.Chem.C,2009,113(25):10842-10846.
[10] Chandra V,Park J,Chun Y,Lee J W,Hwang I C,Kim K S.ACSNano,2010,4(7):3979-3986.
[11] Yang X,Zhang X,Ma Y,Huang Y,Wang Y,Chen Y.J.Mater.Chem.,2009,19(18):2710-2714.
[12] Wang J Z,Zhong C,Wexler D,Idris N H,Wang Z X,Chen L Q,Liu H K.Chem.Eur.J.,2011,17(2):661-667.
[13] Park S,Ruoff R S.Nat.Nanotechnol.,2009,4(4):217-224.
[14] Zhu Y,Murali S,Cai W,Li X,Suk J W,Potts J R,Ruoff R S.Adv.Mater.,2010,22(35):3906-3924.
[15] Lee H,Dellatore S M,Miller W M,Messersmith P B.Science,2007,318(5849):426-430.
[16] Ma Y,Niu H,Cai Y.Chem.Commun.,2011,47(47):12643-12645.
[17] Fu Y,Li P,Xie Q,Xu X,Lei L,Chen C,Zou C,Deng W,Yao S.Adv.Funct.Mater.,2009,19(11):1784-1791.
[18] Zhao X,Shi Y,Wang T,Cai Y,Jiang G.J.Chromatogr.A,2008,1188(2):140-147.
[19] Wu S,He Q,Zhou C,Qi X,Huang X,Yin Z,Yang Y,Zhang H.Nanoscale,2012,4(7):2478-2483.
[20] Xi Z,Xu Y,Zhu L,Wang Y,Zhu B.J.Membra.Sci.,2009,327(1-2):244-253.
[21] Abdelsayed V,Moussa S,Hassan H M,Aluri H S,Collinson M M,El-Shall M S.J.Phys.Chem.Lett.,2010,1(19):2804-2809.
[22] Ai L,Zhang C,Chen Z.J.Hazard.Mater.,2011,192(3):1515-1524.
[23] Yao Y,Miao S,Liu S,Ma L P,Sun H,Wang S.Chem.Eng.J.,2012,184:326-332.
[24] Fan W,Gao W,Zhang C,Tjiu W W,Pan J,Liu T.J.Mater.Chem.,2012,22(48):25108-25115.
[25] Foo K Y,Hameed B H.Chem.Eng.J.,2011,166(2):792-795.
[26] Dural M U,Cavas L,Papageorgiou S K,Katsaros F K.Chem.Eng.J.,2011,168(1):77-85.
[27] Foo K Y,Hameed B H.Chem.Eng.J.,2011,170(1):338-341.
[28] Benadjemia M,Millière L,Reinert L,Benderdouche N,Duclaux L.FuelProces.Technol.,2011,92(6):1203-1212.
[29] Hameed B,Din A M,Ahmad A.J.Hazard.Mater.,2007,141(3):819-825.
[30] Whitehouse B G.Mar.Chem.,1984,14(4):319-332.
Fabrication of a Novel Fe3O4@PDA@RGO Composites and Its Application in Adsorptive Removal of Methylene Blue from Aqueous Solution
WANG Sai-hua, NIU Hong-yun*, CAI Ya-qi
(Research Center for Eco-Environmental Sciences,Chinese Academy of Sciences,Beijing 100085,China)
A facile and low-toxicity approach was proposed to synthesize a new magnetic adsorbent(Fe3O4@PDA@RGO) to remove methylene blue(MB) in water samples.Dopamine could directly adhere to Fe3O4by one-step self-polymerization reaction,which serves as a reducing agent as well as a coupling agent for the assembly of reduced graphene oxide(RGO).The synthetic progress involves no additional chemicals and thermal treatments.Transmission electron microscope(TEM),Fourier transform infrared spectroscopy(FTIR),X-ray diffraction(XRD) and Raman spectroscopy were used to characterize the magnetic composite nanoparticles.The results demonstrated that Fe3O4@PDA@RGO has a strong magnetism(37.8 emu·g-1) and exhibits a high adsorption capacity to MB(98 mg·g-1).The adsorption of MB on Fe3O4@PDA@RGO is pH-dependent and favorable in basic solution.The adsorption behavior of MB on Fe3O4@PDA@RGO could be described by the pseudo-second-order kinetics model and Langmuir isotherm.Furthermore,the as-prepared adsorbent can be easily recovered and reused at least ten times due to its high magnetization and stability.
magnetic nanoparticles;dopamine;graphene;adsorbent
2014-10-14;
2014-11-11
国家973项目(2014CB441102);环保部公益项目(201409037);国家自然科学基金面上项目(21277002)
10.3969/j.issn.1004-4957.2015.02.001
O657.3;F767.4
A
1004-4957(2015)02-0127-07
*通讯作者:牛红云,博士,副研究员,研究方向:纳米材料的制备及其在环境分析化学中的应用,Tel:010-62849182,E-mail:hyniu@rcees.ac.cn

