助剂二氧化硅对CO2加氢制备甲醇CuO-ZnO-Al2O3-ZrO2催化剂性能的影响
贾淼尧,高文桂,王华,王禹皓(昆明理工大学化学工程学院,云南 昆明 650500;昆明理工大学冶金与能源工程学院,云南 昆明 65009;昆明理工大学冶金节能减排教育部工程研究中心,云南 昆明 65009;云南省复杂有色金属资源清洁利用国家重点实验室,云南 昆明 65009)
助剂二氧化硅对CO2加氢制备甲醇CuO-ZnO-Al2O3-ZrO2催化剂性能的影响
贾淼尧1,2,4,高文桂2,3,4,王华2,3,4,王禹皓1,3,4
(1昆明理工大学化学工程学院,云南 昆明 650500;2昆明理工大学冶金与能源工程学院,云南 昆明 650093;3昆明理工大学冶金节能减排教育部工程研究中心,云南 昆明 650093;4云南省复杂有色金属资源清洁利用国家重点实验室,云南 昆明 650093)
第一作者:贾淼尧(1988—),男,硕士。E-mail 475232707@qq.com。
联系人:高文桂,副教授,主要从事能源催化和二氧化碳资源化利用研究。E-mail gao_wengui@126.com。
摘要:采用共沉淀法制备了一系列CuO-ZnO-Al2O3-ZrO2(CZAZ)催化剂,用于二氧化碳加氢合成甲醇。通过加入少量的助剂二氧化硅得到了一系列CZAZ/SiO2改性催化剂。采用XRD、BET、H2-TPR、NH3-TPD以及CO2-TPD等技术进行表征,研究了助剂二氧化硅含量对催化剂的物理化学性质以及组织结构的影响。结果表明,助剂二氧化硅的含量对催化剂的组织结构具有较大的影响。同时评价了该组催化剂参与二氧化碳加氢合成甲醇反应的催化性能。测试结果表明,采用助剂二氧化硅质量分数为4%的改性催化剂,表现出较为优良的催化活性。助剂二氧化硅促进了活性组分氧化铜的分散,并且经过二氧化硅改性的CZAZ催化剂具有更大的比表面积,这些因素都对该催化剂在二氧化碳加氢合成甲醇方面的良好表现起到重要作用。
关键词:二氧化硅;二氧化碳;甲醇;合成;催化剂;共沉淀法
随着近几十年来世界经济的飞速发展,由于全球化石燃料的大量燃烧导致了大气中二氧化碳的浓度不断增加,其引起的“温室效应”严重地威胁到了人类的生存和发展[1-4]。因此,对于二氧化碳的减排以及转化为其他有用的化工原料一直是各国科技工作者研究的课题。二氧化碳加氢转化为甲醇等其他高附加值的化工产品具有资源、环保和经济等方面的重要意义[4]。
综合国内外众多文献可以发现,向铜基催化剂中添加适量助剂可以使Cu的电子状态、Cu的分散度、Cu与载体的相互作用以及载体自身的性质发生变化,从而使催化剂的催化性能发生改变[1]。覃志强等[3]研究发现,稀土助剂Pr改性Cu/Zn/ZrO2催化剂有利于提高其CO2加氢合成甲醇催化性能。王嵩等[5]研究了Cu/ZrO2新型甲醇合成催化剂,发现ZrO2是良好的助剂。徐征等[6]研究了第三组分ZrO2的加入对Cu/ZnO催化剂性能的影响,结果表明适量ZrO2的加入,增加了甲醇的选择性和收率。丛昱等[7]采用了EPR和XPS技术对Cu/Zn/ZrO2催化剂进行研究,发现ZrO2的加入改变了催化剂的表面结构和配位状态,提高了活性组分的分散度和催化剂的稳定性。
张鲁湘等[8]采用TiO2对CO2催化加氢制甲醇催化剂CuO-ZnO-Al2O3进行改性,结果显示,TiO2改性的CuO-ZnO-Al2O3催化剂活性明显提高,而且4%(质量分数)的添加量最佳。另外,他们还发现TiO2的加入可使活性组分CuO分散度提高,使CuO更加容易被还原,并且增加了催化剂对CO2和H2分子的吸附活化,同时降低了催化剂的强酸中心浓度。
1 实验部分
1.1催化剂的制备
本文采用传统的共沉淀法制备CZAZ/SiO2改性催化剂。首先,配置A和B两种溶液。溶液A是将Cu(NO3)2·3H2O、Zn(NO3)2·6H2O、Al(NO3)3·9H2O 及Zr(NO3)4·5H2O共4种硝酸盐按照摩尔比为Cu∶Zn∶Al∶Zr=4.5∶4.5∶0.2∶0.8进行称量混合,加入适量去离子水配置成1.0mol/L的混合溶液。溶液B则包含Na2SiO3和Na2CO3两种易溶钠盐,同样加入适量去离子水以配成1.0mol/L的混合溶液。将两种溶液分别搅拌充分溶解后,缓慢滴入恒温水浴(70℃)内的2000mL大烧杯(提前加入100mL去离子水)中,打开电动搅拌器,匀速搅拌。A和B两种溶液均采用分液漏斗进行并流缓慢滴加,保持速度为1滴/s。在此共沉淀过程中,保持溶液pH值在7左右。滴定完毕,继续在70℃的恒温水浴中搅拌1h。然后将大烧杯取出,放在室温下继续老化2h。随后加入1000mL去离子水进行洗涤、过滤及抽滤,平行操作5次,确保除去滤饼内的钠离子。抽滤完毕后,将滤饼放置于110℃的烘箱内恒温12h。最后将干燥的前体粉末放进马弗炉里,采用程序升温(10 ℃/min)到500℃之后,恒温5h。焙烧结束后,将黑色的催化剂粉末压片,破碎,筛分出20~40目的颗粒备用。
在本文中,为方便书写,将一系列含有助剂SiO2的CuO-ZnO-Al2O3-ZrO2改性催化剂依次缩写成:CZAZ-0.5、CZAZ-1、CZAZ-2、CZAZ-4 和CZAZ-6。例如,CZAZ-2表示其中Cu∶Zn∶Al∶Zr=4.5∶4.5∶0.2∶0.8 (摩尔比),助剂SiO2加入量为2% (质量分数,以氧化物计)。
1.2催化剂的活性测试
将制备得到的CZAZ/SiO2改性催化剂装入固定床微催反应器进行CO2加氢合成甲醇活性评价。准确称取2.0g催化剂(20~40目)装于反应管中部,反应管两端填充石英棉和石英砂(20~40目)。催化剂先通入V(H2)∶V(N2)=1∶10的混合气,调节压力为0.7MPa。然后程序升温至 280℃进行还原,升温速率为1℃/min,持续还原6h。待还原结束后降温至室温,并切换反应气进行活性评价。具体操作条件如下:温度250℃(程序升温,10℃/min),压力为3.0MPa,空速(GHSV)为 3000h−1,反应气组成为V(H2)∶V(CO2)=3∶1。分析系统采用的是Agilent 6890N气相色谱仪及其自带的化学工作站进行在线分析,采用外标法定量分析尾气中各组分的含量。
1.3催化剂的表征
XRD测定在日本理学D/max-2200型X射线衍射仪上进行。具体测定条件为:Cu靶,管电压40kV,管电流40mA,扫描步长为0.01°,扫描速率为2°/min,扫描范围为2θ=10°~90°。催化剂的比表面积在美国Quantanchrome公司的CHEM 化学吸附仪上测定。H2-TPR、NH3-TPD 和 CO2-TPD均采用美国Quantachrome公司生产Chem BET Pulsar TPR/TPD 仪器测量。H2-TPR的测量催化剂用量为50mg,以10℃/min的速率升温至900℃,采用热导池检测器检测信号并采集数据;CO2-TPD 的测量催化剂用量为100 mg,以10℃/min的速率升温至900℃,由热导池检测器检测信号并采集数据。
2 结果与讨论
2.1催化剂的物相分析
图1为添加不同含量助剂SiO2所制备的CZAZ/SiO2催化剂前体的XRD谱图。根据王继元等[9]的研究成果,从图1中可知,CZAZ/SiO2催化剂前体中含有绿铜锌矿物相[Aurichalcite,Zn3Cu2(CO3)2(OH)6]、单斜绿铜锌矿物相[Rosasite,CuZn(CO3)(OH)2]以及它们的混合晶相。经过助剂SiO2改性之后,位于13.2°的绿铜锌矿的衍射峰逐渐宽化减弱,并且随着助剂SiO2的含量逐渐增加,另外几个特征衍射峰也逐渐弥散、宽化。但是由于额外添加少量助剂Al2O3,从而使得CZAZ/SiO2催化剂前体的所有特征衍射峰都变得更加弥散、宽化。
CZAZ/SiO2催化剂前体在500℃焙烧后的XRD谱图如图2所示。根据郭晓明[10]的研究结果,在2θ 为35.6°、38.8°以及48.9°处出现的衍射峰应该归属于CuO;在2θ为34.5°、36.3°等处出现的衍射峰应该归属于ZnO。从衍射峰强度来看,加入助剂SiO2后,特别是对于CZZ-4和CZZ-6,CuO的衍射峰较为弥散、宽化,即为CuO晶粒较小,ZnO 对CuO起到了较好的分散作用。另外,所有500℃焙烧后的样品均在2θ为34°~37°处CuO和ZnO明显包络,而且随着助剂SiO2用量的增加,包络峰的强度逐渐降低,说明了CuO和ZnO很可能是以类似于无定形或者更加无序的形态存在[11-12]。厦门大学杨海贤等[13]研究发现,适量SiO2的加入可以使晶态CuO向着非晶态转变,能有效促进催化剂活性组分之间的分散,增强金属氧化物之间的相互作用,从而阻止铜的深度还原,最终提高催化剂的活性。

图1 CZAZ/SiO2催化剂前体的XRD图谱

图2 CZAZ/SiO2催化剂焙烧后的XRD图谱
从图2中可以发现,对于CZAZ/SiO2两组催化剂,当助剂质量分数达到4%时,CuO的衍射峰较为弥散、宽化,而且ZnO的特征峰逐渐消失,说明此时CuO和ZnO的相互作用很强。以上结果表明,助剂SiO2的加入使焙烧后催化剂的晶形结构发生了改变,促进了催化剂的分散,并延缓了催化剂颗粒的长大。助剂SiO2之所以能延缓了催化剂颗粒的长大,可能是因为CuO、ZnO以及助剂SiO2之间存在某种相互作用[14]。另外由于引入了一定量助剂Al2O3替换助剂ZrO2进行改性,500℃焙烧后的样品均在2θ为34°~37°处CuO和ZnO包络峰的强度更大,说明了助剂Al2O3增强了CuO和ZnO的相互作用。
2.2催化剂的比表面积

表1 CZAZ/SiO2催化剂500℃焙烧后BET值
表1为CZAZ/SiO2催化剂500℃焙烧后BET值。从表1可知,随着助剂SiO2含量的增加,催化剂的比表面积逐渐增加,说明助剂SiO2确实有助于提高催化剂的比表面积且效果显著。
2.3催化剂的还原行为
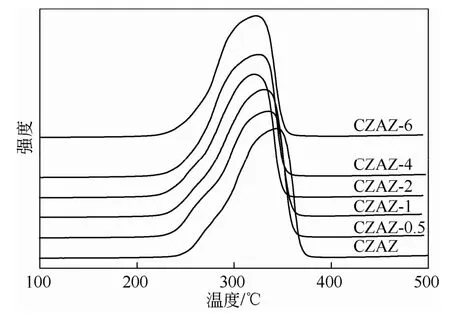
图3 CZAZ/SiO2催化剂的H2-TPR图谱
图3为采用不同含量助剂SiO2改性的CZAZ/ SiO2催化剂的H2-TPR曲线。从图3中可以看出,在230~400℃所有样品均出现一个宽的H2消耗峰。该组催化剂分别出现了主峰和肩峰。杨意泉等[15]在研究Cu-Zn-Al-Zr催化剂时认为主峰对应着Cu+→Cu的还原过程;而该组催化剂的各肩峰温度依次比各主峰的峰顶温度低70~80℃,其对应着Cu2+→Cu+的还原过程。另外一些研究者认为,低温峰归属于高度分散的CuO的还原,这部分CuO 与ZnO和ZrO2之间有较强相互作用,而高温峰则归属于体相CuO的还原[16-17]。而对于CuO的还原温度,很多研究者认为CuO的粒径越小,还原温度则越低[16-18]。
另外可以发现,随着催化剂中助剂SiO2含量的增加,主峰峰顶温度逐渐向着低温方向移动,当添加助剂SiO2质量分数为6%时,达到最低的322.0℃。这充分说明由于助剂SiO2的加入,还原温度降低,晶粒减小,易还原、高度分散的CuO在催化剂总的CuO中所占比例明显提高,即活性组分CuO可以更加均匀地分散在3种助剂上(这与XRD分析结论相一致),使得CuO的还原过程变得更加容易。这预示着催化剂CZAZ-4和CZAZ-6可能具有较好的催化剂活性。而从图3可知,本组CZAZ/SiO2催化剂的主峰峰顶温度比未改性的CZAZ催化剂最多降低了将近40℃。因此可以推测添加助剂SiO2后,催化剂的粒径更小,因而还原温度更低。
2.4催化剂的酸碱性
根据文献[19]可知,催化剂的表面酸碱性可以采用NH3脱附的方式进行检测。在一定的温度范围内,采用程序升温方式考察催化剂表面所吸附的NH3的脱附量和脱附的难易程度,以此来探测催化剂表面的酸中心浓度和酸强度。图4为CZAZ/SiO2催化剂(500℃焙烧后)的NH3-TPD谱图。可以看出,催化剂表面有4个NH3脱附峰,分别以Ⅰ、Ⅱ、Ⅲ及Ⅳ进行标记,分别代表催化剂表面的4种不同的酸性中心。而且,随着NH3的脱附峰温度依次升高,即NH3与酸中心的结合强度逐渐增大,说明这4种酸中心的酸强度依次增强。从图4中可知,低温脱附峰和高温脱附峰的变化趋势全部一致,峰面积均随着助剂SiO2含量的逐渐增加而增加。当助剂质量分数为4%以上时,Ⅲ峰和Ⅳ峰融合成一个更大的高温脱附峰。这个现象说明助剂SiO2可以调变催化剂表面的酸碱性,即由于SiO2是酸性助剂,因此随着助剂SiO2含量的不断增加,催化剂表面的酸性逐渐增加,Ⅲ和Ⅳ两个强酸中心的浓度也不断增加。由于CO2也是弱酸性气体,所以不应该将催化剂表面的酸性增加得过强,因此助剂SiO2含量应该适量,而不能太多。从图4中可知,助剂SiO2加入后,催化剂在低温区Ⅰ峰的峰面积有所增大,而峰温向低温方向移动,这说明助剂SiO2的加入削弱了低温区酸中心的强度,但是增加了酸中心的浓度。如果弱酸浓度大幅度增加,则不太利于CO2的吸附,因此助剂SiO2含量不能太高[20]。
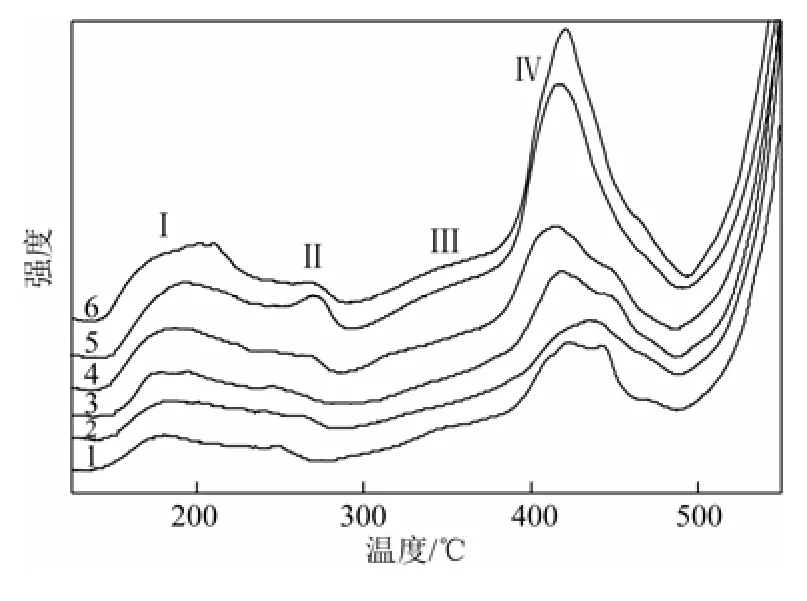
图4 CZAZ/SiO2催化剂的NH3-TPD图谱
图5为CZAZ催化剂的CO2-TPD谱图。从图5中可见,在所研究的温度范围内,二氧化碳在铜基催化剂上有4个脱附峰,其中两个峰温较低,两个峰温较高,分别以α、β、γ及δ进行标记。李基涛等[2]认为CO2在铜基催化剂上有4个CO2-TPD峰,分别代表着催化剂表面上的铜和受到锌作用的铜分别对CO2进行线型吸附和桥式吸附的结果。前者脱附较为容易,后者较难。所以,峰温较低的两个CO2脱附峰可能分别代表催化剂表面两种铜对CO2的线型吸附;而峰温较高的两个CO2脱附峰可能分别代表催化剂表面两种铜对CO2的桥式吸附。
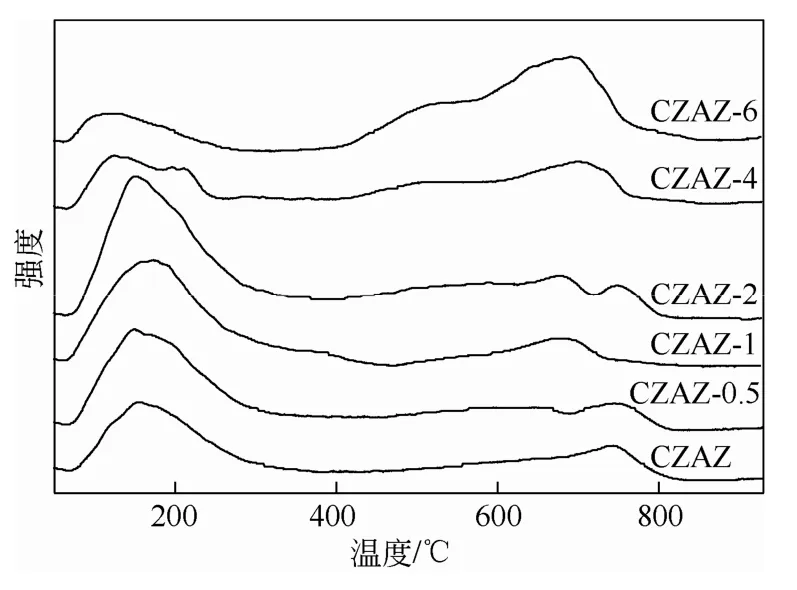
图5 CZAZ/SiO2催化剂的CO2-TPD图谱
由图5可知,加入助剂SiO2之后,CO2低温脱附峰面积先缓慢增大后急剧减小,说明随着助剂SiO2含量的增加,低温范围CO2的吸附量也是先增大后急剧减小。同时低温脱附峰峰顶温度向着高温方向移动,当助剂SiO2添加质量分数为1%时,低温脱附峰峰顶温度达到最高的173.4℃,之后又逐渐降低。当助剂SiO2质量分数为2%时,CO2的线型吸附量达到最大。而随着助剂SiO2含量的增加,CO2高温脱附峰峰顶温度左右偏移,峰面积先减小后急剧增大,刚好与低温脱附峰的变化趋势相反。这个现象说明助剂SiO2的引入对催化剂的低温脱附峰和高温脱附峰均有较为明显的影响,助剂改变了吸附强度和吸附中心的数量。助剂SiO2的加入提高了活性组分分散性,适当地提高了对于CO2的吸附强度,进而促进了反应的进行,提高了CO2的转化率,但是过量的助剂SiO2会覆盖活性位,反而削弱催化剂对于CO2分子的吸附活化。
2.5助剂SiO2含量对CZAZ催化剂性能的影响
表2是CZZ/SiO2催化剂及引入一定量助剂Al2O3替换助剂ZrO2后的催化剂在二氧化碳加氢合成甲醇方面的催化性能数据。随着助剂SiO2含量的增加, CZAZ/SiO2催化剂的CO2转换率不断增加,最高可达23.11%,甲醇选择性最高达到39.81%,CH3OH产率达到9.20%。结合催化剂的XRD表征分析可以看出,此时CuO、ZnO晶粒分散均匀,而且助剂SiO2改性后的催化剂的比表面积较大,所以助剂SiO2改性后的催化剂的二氧化碳加氢合成甲醇效果较好。
从表2可知,CZAZ-2、CZAZ-4和CZAZ-6催化剂的催化活性都较好,在一定质量和时间内生成了更多的产物(主要包括甲醇和水等),而且CO2转化率和甲醇选择性均高于未改性的CZAZ催化剂,因而催化活性相对较好。这个评价结果与本文中的XRD表征、BET表征、H2-TPR表征等得出的结论一致。

表2 SiO2用量对CZAZ/SiO2催化剂性能的影响
3 结 论
通过本文研究发现,助剂SiO2含量对CZAZ/SiO2催化剂的性质影响较为显著。随着助剂SiO2含量的逐渐增加,催化剂活性组分的分散性有所增加,XRD衍射峰显得更加弥散、宽化。另外,比表面积也随之增加,从而促使催化剂的还原温度逐渐降低,进而更有利于二氧化碳加氢合成甲醇反应。因此,助剂SiO2含量对CZAZ/SiO2催化剂在二氧化碳加氢合成甲醇方面影响较为显著,并且当助剂SiO2质量分数为4%时,催化活性较高,CO2转换率达23.11%,甲醇选择性达到39.81%,CH3OH产率达到9.20%。但是,如果添加助剂SiO2的量过多,则可能会覆盖催化剂的活性位,导致催化剂的催化活性降低。
参 考 文 献
[1] 郭晓明,毛东森,卢冠忠,等.CO2加氢合成甲醇催化剂的研究进展[J].化工进展,2012,31(3):477-488.
[2] 李基涛,张伟德,陈明旦,等.铜基催化剂上CO2吸附的TPD和TPSR研究[J].天然气化工,1998,23(5):14-17.
[3] 覃志强,高文桂,王华,等.稀土助剂Pr改性Cu/Zn/ZrO2合成甲醇催化剂的催化性能[J].化工进展,2013,32(4):820-823.
[4] 张鲁湘,张永春,陈绍云.CO2加氢制甲醇、二甲醚的研究进展[J].化工进展,2010,29(6):1041-1046.
[5] 王嵩,毛东森,吴贵升,等.铜/氧化锆催化剂的制备及应用研究进展[J].化工进展,2008,27(6):837-843.
[6] 徐征,千载虎,张强,等.CuO-ZnO基CO2/H2合成甲醇催化剂的反应活性中心[J].催化学报,1994(2):97-102.
[7] 丛昱,包信和,张涛,等.CO2加氢合成甲醇的超细CuZnOZrO2催化剂的表征[J].催化学报,2000,21(4):314-318.
[8] 张鲁湘,张永春,陈绍云.助剂TiO2对CO2催化加氢制甲醇催化剂CuO-ZnO-Al2O3性能的影响[J].燃料化学学报,2011,39(12):912-917.
[9] 王继元,曾崇余,吴昌子.SiO2改性的Cu-ZnO/HZSM-5催化剂及合成二甲醚性能[J].燃料化学学报,2006,34(2):195-199.
[10] 郭晓明.二氧化碳加氢合成甲醇铜基催化剂的研究[D].上海:华东理工大学,2011.
[11] Jun K W,Shen W J,Rama Rao K S,et al.Residual sodium effect on the catalytic activity of Cu/ZnO/Al2O3in methanol synthesis from CO2hydrogenation[J].Applied Catalysis A:General,1998,174:231-238.
[12] Ma Y,Sun Q,Wu D,et al.A gel-oxalate co-precipitation process for preparation of Cu/ZnO/Al2O3ultrafine catalyst for methanol synthesis from CO2+H2:(Ⅱ) Effect of various calcination conditions[J].Applied Catalysis A:General,1999,177(2):177-184.
[13] 杨海贤,贾立山,方维平,等.Cu-Mn/HZSM-5合成二甲醚催化活性的研究[J].天然气化工,2008(1):1-5.
[14] Wu J G,Luo S C,Toyir J.Optimization of preparation conditions and improvement of stability of Cu/ZnO-based multicomponent catalysts for methanol synthesis from CO2and H2[J].Catalysis Today,1998, 45:215-220.
[15] 杨意泉,方雪明,李晨,等.Cu-Zn-Al-Zr甲醇合成催化剂的UVDR、TPD和TPR表征[J].厦门大学学报:自然科学版,2001,40(6):1252-1255.
[16] Avgouropoulos G,Ioannides T,Matralis H.Influence of the preparation method on the performance of CuO–CeO2catalysts for the selective oxidation of CO[J].Applied Catalysis B:Environmental,2005,56:87-93.
[17] Zhang Y P,Fei J H,Yu Y M,et al.Methanol synthesis from CO2hydrogenation over Cu based catalyst supported on zirconia modified gamma-Al2O3[J].Energy Conversion and Management,2006,47:3360-3367.
[18] Avgouropoulos G,Ioannides T.Selective CO oxidation over CuO-CeO2catalysts prepared via the urea-nitrate combustion method [J].Applied Catalysis A:General,2003,244(1):155-167.
[19] Mao D S,Yang W M,Xia J C,et al.The direct synthesis of dimethyl ether from syngas over hybrid catalysts with sulfate-modified gamma-alumina as methanol dehydration components[J].Journal of Molecular Catalysis A:Chemical,2006,250:138-144.
[20] 张鲁湘.CO2催化加氢合成甲醇催化剂CuO-ZnO-Al2O3改性的研究[D].大连:大连理工大学,2012.
Effect of promoter silica on performance of CuO-ZnO-Al2O3-ZrO2catalyst for methanol synthesis from CO2hydrogenation
JIA Miaoyao1,2,4,GAO Wengui2,3,4,WANG Hua2,3,4,WANG Yuhao1,3,4
(1School of Chemical Engineering,Kunming University of Science and Technology,Kunming 650500,Yunnan,China;2School of Metallurgy and Energy Engineering,Kunming University of Science and Technology,Kunming 650093 Yunnan,China;3Engineering Research Center of Metallurgical Energy Conservation and Emission Reduction,Ministry of Education,Kunming University of Science and Technology,Kunming 650093,Yunnan,China;4State Key Laboratory of Complex Nonferrous Metal Resources Cleaning Utilization in Yunnan Province,Kunming University of Science and Technology,Kunming 650093,Yunnan,China)
Abstract:Various CuO-ZnO-Al2O3-ZrO2(CZAZ) catalysts for methanol synthesis from CO2hydrogenation were prepared by the co-precipitation method.A small amount of silica was incorporated into CZZ catalyst to produce these modified ternary CZAZ catalysts.The effects of silica on physicochemical and catalytic properties were studied with XRD,BET,H2-TPR,NH3-TPD and CO2-TPD.The properties of catalysts were strongly influenced by the content of SiO2used as promoter.The catalytic performance for methanol synthesis from CO2hydrogenation was evaluated.CZAZbook=408,ebook=420catalyst modified with 4% SiO2exhibited optimum catalytic activity.Silica improved dispersion of CuO and its modified CZAZ catalysts exhibited higher specific surface area,which were confirmed to be responsible for excellent performance for methanol synthesis from CO2hydrogenation.
Key words:silica dioxide; carbon dioxide; methanol; synthesis; catalyst; co-precipitation
基金项目:国家科技支撑计划(2011 BAC01B03)、国家自然科学基金(51304099)、云南省应用基础研究计划(2013FZ035)及昆明理工大学分析测试基金(20140350)项目。
收稿日期:2014-06-23;
DOI:10.16085/j.issn.1000-6613.2015.02.017
文章编号:1000–6613(2015)02–0407–06
文献标志码:A
中图分类号:O 643
修改稿日期:2014-09-21。

