SI-2树脂对镍离子的静态吸附动力学
金虹,余训民*,关洪亮
武汉工程大学化学与环境工程学院,湖北 武汉 430074
SI-2树脂对镍离子的静态吸附动力学
金虹,余训民*,关洪亮
武汉工程大学化学与环境工程学院,湖北 武汉 430074
为了研究电镀废水中镍的去除方法,采用离子交换树脂法吸附镍离子.首先对SI-2树脂的结构进行能谱分析和红外表征,然后探讨pH、初始浓度、温度和时间对镍离子吸附量的影响,在此基础上研究SI-2树脂对镍离子的等温吸附动力学特性.结果表明,SI-2树脂是无机硅胶型树脂,交联反应发生在树脂中的羟基上;pH=5时吸附最佳,树脂的最大吸附容量为3 000 mg/g;吸附过程中吉布斯自由能为-24.21 kJ/mol,说明吸附过程是自发进行的;SI-2树脂对镍离子的吸附符合Langmuir和Freundlich模型;吸附过程符合拟二级动力学方程,吸附活化能为1.532 kJ/mol.液膜扩散和颗粒内扩散是整个吸附过程的主要速率控制步骤.
离子交换;等温吸附;吸附速率常数;吸附活化能
0 引言
目前,金属镍的需求在全球范围内明显增加[1-2].电镀废水中含有大量重金属离子,如铜、镍、锌、铬、铁等,这些重金属废水的排放,不仅造成环境污染,也造成了贵重金属的流失.在这种情况下,必须对金属离子进行回收.
李玲[3]等人研究了亚氨基二乙酸树脂对镍和镁的吸附性能及吸附模型,发现树脂吸附性能好,对镍的吸附既不符合Langmuir模型也不符合Freundlich模型.肖先念[4]等人用R502螯合树脂对硫酸溶液中高含量Ni2+进行吸附,结果表明,该树脂对Ni2+最高吸附量为26 mg/g.杨金杯[5]等人采用001×14.5离子交换树脂吸附镍(Ⅱ),结果表明,树脂吸附镍(Ⅱ)过程符合Langmuir等温吸附方程,并符合拟二级动力学模型.
本文自配含镍离子溶液,单独研究SI-2树脂对镍离子的吸附,重点考察了树脂对镍离子的吸附动力学特性.
1 实验
1.1 仪器与试剂
火焰原子吸收分光光度计:TAS-990,天津市普瑞斯仪器有限公司;红外光谱仪:WQF-410,上海力晶科学仪器有限公司;X射线光电子能谱仪:ESCALAB 250XiXPS,北极中西远大科技有限公司;恒温水浴振荡器:SHA-C,金坛市科兴仪器厂;真空干燥箱:DZF-6020,巩义市予华仪器有限责任公司;电子天平:BSA-CW,赛多利斯科学仪器有限公司;精密PH计:PHS-3C,上海精密仪器有限公司.
盐酸:AR;氢氧化钠:AR;金属镍粉:纯度≥99.9%,天津市科密欧化学试剂有限公司;SI-2树脂:洛阳鼎力环保科技有限公司.
1.2 试验方法
1.2.1 镍离子浓度的测定镍的测定采用火焰原子吸收分光光度法GB11912-89.
1.2.2 吸附树脂的预处理吸附树脂用去离子水充分浸泡,然后用1 mol/L的盐酸和1 mol/L的氢氧化钠溶液浸洗,再用去离子水洗至中性.树脂外观为黄色不透明球状颗粒.
1.2.3 吸附动力学试验在锥形瓶中放入0.5 g树脂,加40 mL浓度一定的Ni2+溶液,分别在293、303、313 K温度条件下,于一定时间测定溶液吸光度[6].树脂吸附量计算如式(1).
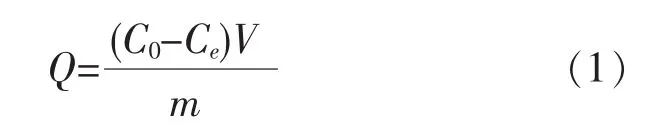
式(1)中C0是初始质量浓度(mg/mL);Ce为平衡质量浓度(mg/mL);V为溶液体积(mL);m为SI-2干树脂质量(g);Q为平衡吸附量(mg/g).
2 结果与讨论
2.1 能谱分析
采用能谱仪(EDS,Energy Dispersive Spectrometer)测定SI-2树脂中元素的种类及含量,结果如图1所示.

图1 树脂的主要化学成分质量分数/%Fig.1 The main chemical ingredient of resin
由检测结果可知,Si的质量分数为21.72%,与公司提供的树脂技术指标一致,是无机硅胶型树脂.
2.2 树脂的红外表征
采用WQF-410红外光谱仪对吸附Ni2+前后的SI-2树脂进行红外光谱分析,结果如图2所示.在3 451 cm-1附近出现OH伸缩振动吸收峰,在1 636 cm-1附近出现C=C伸缩振动吸收峰,在1 098cm-1附近出现OH伸缩振动吸收峰,在464 cm-1附近出现Si-O伸缩振动吸收峰,说明羟基参加了吸附反应.
2.3 pH对吸附效果的影响
在锥形瓶中放入0.5g树脂,加40mL0.5mg/mL的镍溶液,调整溶液pH值分别为0.5、1、1、2、3、4、5、6,在常温20℃下进行吸附,结果如图3所示.
由图3可知,溶液初始pH由0.5增加至1时,树脂的吸附量明显增加,当pH继续增加至5时,树脂的吸附量达到最高值为33.04 mg/g.因此,SI-2树脂对Ni2+的最佳吸附pH为5.
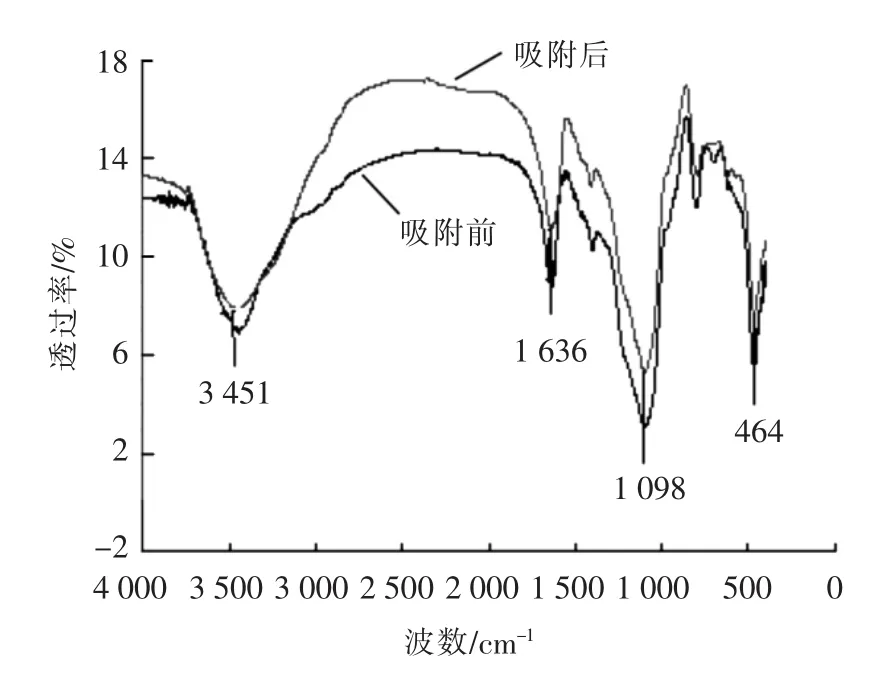
图2 树脂吸附Ni2+前后的红外光谱图Fig.2 IR spectrum of resin fore-and-aft adsorptions

图3 pH对吸附效果的影响Fig.3 Influence of pH on the adsorption effect
2.4 温度对Ni2+吸附率的影响
在溶液pH值为5,不同温度条件下,测得SI-2树脂对Ni2+的吸附率η(表1).考察不同温度下每克干树脂对Ni2+吸附量与Ni2+浓度之比D=Qe/Ce,以lgD对103×1/T作图,如图4所示.
吸附符合温度系数法公式:
lgD=-ΔH/(2.303 RT)+ΔS/(2.303 R)斜率和截距求得ΔH=3.39 kJ/mol,ΔS=73.05 J/(mol·K).再由ΔG=ΔH-TΔS 98 K时ΔG=-24.21 kJ/mol. ΔG<0,说明吸附是正向自发进行的.
2.5 等温吸附特征
在树脂用量为0.5,pH值为5条件下,改变温度,测定溶液中平衡质量浓度与吸附量的关系,并用Langmuir和Freundlich等温吸附模型对数据进行拟合(图5、表2和表3).

表1 温度对Ni2+吸附率η的影响Table1 Influence of different temperatures on adsorption rate of Ni2+

图4 lgD与103×1/T的关系Fig.4 Relationship between lgD and 103×1/T

图5 等温吸附曲线Fig.5 Adsorption isotherms
由图5可知,随着温度的升高,树脂对Ni2+平衡吸附量(Qe)也有所增加.温度从293 K上升到313 K,树脂对Ni2+吸附量由2 796.83 mg/g增至2 978.45 mg/g.说明树脂对Ni2+的吸附是吸热过程.
从表2和表3可以看出,SI-2树脂对Ni2+的吸附符合Langmuir方程和Freundlich方程,Langmuir方程描述更佳.n>1,说明树脂对Ni2+的吸附过程容易进行.

表2 Langmuir等温吸附参数Table 2 Parameters of Langmuir isotherms
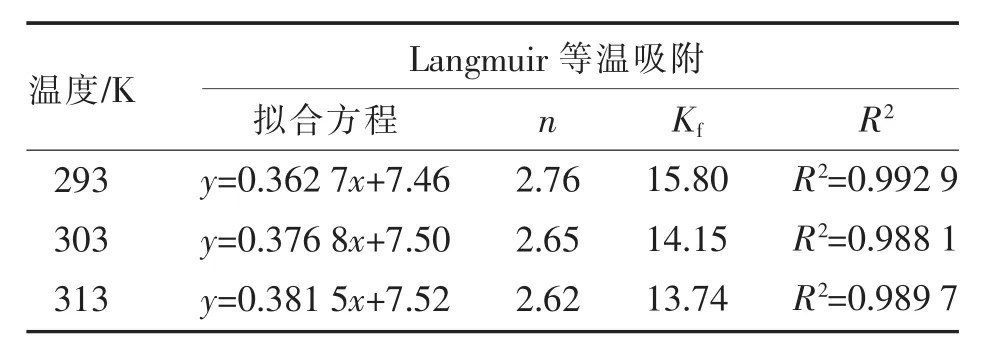
表3 Freundlich等温吸附参数Table3 Parameters of Freundlich isotherms
2.6 吸附动力学
不同时间条件下,树脂对Ni2+的吸附容量的变化数据如图6所示.开始阶段Ni2+吸附量急剧增加,随后吸附速率逐渐减缓,2 h后基本达到平衡.

图6 吸附动力学曲线Fig.6 Curves of adsorption kinetics
2.6.1 速率拟合方程将图6的数据分别使用一级吸附速率方程、二级动力学方程、液膜扩散方程及颗粒内扩散方程[7]进行拟合,结果见图7(a、b、c、d).由此计算出各方程的动力学参数见表4.表中:K1为一级速率常数(min-1);K2为二级速率常数(g/mg·min);K3为液膜扩散速率常数(min-1);Kp内扩散速率常数,C为常数.

表4 不同动力学方程的拟合结果Table 4 Fitting results of different kinetic equations

图7 不同动力学方程的拟合曲线Fig.7 Fitting curves of different kinetic equations
由表4可知,二级吸附动力学方程最适合描述Ni2+在SI-2树脂上的吸附过程,因其拟合线性相关性最高(R2>0.99),计算得到的Ni2+平衡吸附量也与事实更相符.
图7(c)和(d)显示液膜扩散方程和颗粒内扩散方程的拟合曲线均未通过原点,说明整个吸附过程是多步控制,主要受液膜扩散和颗粒内扩散控制[8].
2.6.2 表观吸附活化能根据阿伦尼乌斯公式:

整理表4中二级动力学的数据,以lnk2为Y轴,1/T为X轴作图可得图8.

图8 lnK2与T-1的关系Fig.8 Relationship between lnK2and 1/T
图8中直线的斜率-Ea/R=-184.37,R=8.314 J/(mol·K).由此可求得吸附表观活化能Ea=1.532 kJ/mol,指前因子A为0.003 9.
3 结语
a.Ni2+在SI-2树脂上的最佳吸附pH是5,饱和吸附量为3 000 mg/g.吸附过程的热力学参数ΔH>0和ΔG>0,表明此过程为吸热过程并且自发进行.
b.树脂的吸附过程符合Langmuir和Freundlich等温吸附模型,前者能更好地描述SI-2树脂对Ni2+的吸附效果.
c.SI-2树脂对Ni2+的吸附符合二级动力学方程,主要速率控制步骤是液膜扩散和颗粒内扩散,吸附表观活化能Ea为1.532 kJ/mol,吸附容易进行.
致谢
武汉工程大学测试中心及课题组的老师、同学给予了配合和支持,在此向他们表示最衷心的感谢!
参考文献:
[1]那丹妮,王高尚.我国未来镍需求趋势预测及供应构想[J].中国国土资源经济,2010,23(6):17-19.
NA Dan-ni,WANG Gao-shang.Forecasting the future trends of china's nickel demand and supply concept[J].Natural Resource Economics of China,2010,23(6):17-19.(in Chinese)
[2]江源,侯梦溪.全球镍资源供需研究[J].有色矿冶,2008,24(2):55-57.
JIANG Yuan,HOU Meng-xi.The study of global nickel supply and demand[J].Non-ferrous Mining and Metallurgy,2008,24(2):55-57.(in Chinese)
[3]李玲,黄松涛,温建康,等.亚氨基二乙酸树脂对镍和镁离子的吸附性能研究[J].金属矿山,2008(5):44-48.
LI Ling,HUANG Song-tao,WEN Jian-kang,et al.Study on adsorption of iminodiacetic acid resin for nickel and magnesium ions from solution[J].Metal Mine,2008(5):44-48.(in Chinese)
[4]肖先念,刘杰,黄少斌,等.R502螯合树脂吸附硫酸根溶液中高含量镍离子研究[J].水处理技术,2011,37(4):45-48.
XIAO Xian-nian,LIU Jie,HUANG Shao-bin,et al.Adsorption research of high concentration nickel contained in sulfate solution by using chelating resin R502[J].Technology of Water Treatment,2011,37(4):45-48.(in Chinese)
[5]杨金杯,陈玉成,余美琼,等.001×14.5离子交换树脂对镍(Ⅱ)的吸附[J].环境工程学报,2013,7(8):3019-3023.
YANG Jin-bei,CHEN Yu-cheng,YU Mei-qiong,et al.Adsorption of Ni(Ⅱ)by ion exchange resin(001×14.5)[J].Chinese Journal of Environmental Engineering,2013,7(8):3019-3023.(in Chinese)
[6]党明岩,郭洪敏,谭艳坤,等.复配壳聚糖树脂对Cu2+的等温吸附及吸附动力学研究[J].功能材料,2012,19(43):2616-2618.
DANG Ming-yan,GUO Hong-min,TAN Yan-kun,et al.Adsorption equilibrium and kinetics of Cu2+on complex chitosan resin[J].Functional Materials,2012,19(43):2616-2618.(in Chinese)
[7]北川浩,铃木谦一郎.吸附的基础与设计[M].北京:化学工业出版社,1983:48-50.
BEI Chuan-hao,LIN Mu qian yi-lang.The basis of adsorption and design[M].Bei-jing:Chemical Industry Press,1983:48-50.(in Chinese)
[8]李稳宏,唐璇,李新生,等.黄姜黄色素在大孔树脂上的吸附动力学研究[J].离子交换与吸附,2008,24(6):526-534.
LI Wen-hong,TANG Xuan,LI Xin-sheng,et al.Adsorption kinetics of dioscorea zingiberensis yellow pigment on the macroporous resins[J].Ion Exchange and Adsorption,2008,24(6):526-534.(in Chinese)
Static adsorption kinetics of nickel ions on SI-2 resin
JIN Hong,YU Xun-min,GUAN Hong-liang
School of Chemical and Environmental Engineering,Wuhan Institute of Technology,Wuhan 430074,China
To remove nickel from the electroplating waste water,the adsorption of nickel ions with ion exchange resin was investigated.First,the structure of SI-2 resin was characterized by energy disperse spectroscopy and infrared spectroscopy.Then the effects of pH,initial concentration,temperature and time on the adsorption of nickel ions were discussed and the isothermal adsorption and adsorption kinetics were studied.The results show that SI-2 resin is inorganic silicon and the reaction of crosslinking is on the hydroxyl of the resin;the maximum adsorption capacity of SI-2 resin is 3 000 mg/g when pH is 5;the gibbs free energy in the course of adsorption is-24.21 kJ/mol,which demonstrates that the adsorption of nickel ions is a spontaneous adsorption process;the adsorption isotherm of nickel ions on the resin fits the model of Langmuir and Freundlich;the adsorption kinetics fits the pseudo-second-order equation well,and the activation energy is 1.532 kJ/mol.The adsorption process is controlled by film diffusion and intra particle diffusion.
ion exchange;isothermal adsorption;adsorption rate constant;adsorption activation energy
TQ028.3
A
10.3969/j.issn.1674-2869.2015.05.008
1674-2869(2015)05-0041-05
本文编辑:龚晓宁
2015-03-25
武汉工程大学研究生教育创新基金(CX2013108)
金虹(1988-),女,湖北襄阳人,硕士研究生.研究方向:废物资源化利用.*通信联系人

