基于药物体系质量评价模式的柴胡质量表征关联分析研究
潘 婷 黄亚婷 韩珂卿 孙雅姝 温 静 迟 蕾 陈 唯 杨 元 姜艳艳,3 石任兵,3
(1 北京中医药大学中药学院国家中医药管理局中药经典名方有效物质发现重点实验室,北京,100102;2 首都医科大学中医药学院,北京,100069; 3 北京市教委中药质量控制技术工程中心,北京,100102)
中药研究
基于药物体系质量评价模式的柴胡质量表征关联分析研究
潘 婷1黄亚婷1韩珂卿1孙雅姝1温 静2迟 蕾1陈 唯1杨 元1姜艳艳1,3石任兵1,3
(1 北京中医药大学中药学院国家中医药管理局中药经典名方有效物质发现重点实验室,北京,100102;2 首都医科大学中医药学院,北京,100069; 3 北京市教委中药质量控制技术工程中心,北京,100102)
目的:运用药物体系质量评价模式对柴胡饮片进行质量表征及关联分析,以有效地评价柴胡饮片的质量。方法:采用HPLC法同时测定柴胡饮片中药物体系关联成分芦丁、柴胡皂苷c、柴胡皂苷a、柴胡皂苷d的含量,同时表征主要黄酮类成分含量和及主要皂苷类成分含量和,并采用可见分光光度法测定柴胡饮片中总酚类成分含量。结果:基于药物体系质量评价模式,对柴胡饮片中有效指标性成分含量及其相对比值进行质量表征,同时将不同批次的饮片与经过药效验证的基准饮片进行关联度分析。结果表明,样品7、8、14中有效指标性成分含量总体高于基准批号5,批号6中有效指标性成分含量与基准批次饮片5相近,样品7、8、13、14与基准批次饮片5关联度较高。综合质量表征及关联分析结果,样品7、8、14、5、13的品质居优。结论:基于药物体系质量评价模式对柴胡饮片的质量进行评价,通过有效指标性成分含量及其相对比值的质量表征,以经过药效验证的饮片为基准,结合关联度分析,可综合全面地评价柴胡饮片的质量,为柴胡饮片的资源筛选、药物原料的质量控制和应用提供依据,同时为中药质量评价提供了方法学及其应用借鉴。
柴胡;关联分析;主要黄酮类成分和;总酚类成分含量;柴胡皂苷c、a、d;主要皂苷类成分和
柴胡始载于《神农本草经》,列为上品。其为伞形科植物柴胡(BupleurumChinese,DC)或狭叶柴胡(BupleurumscorzonerifoliumWilld)的干燥根。按性状不同,分别习称“北柴胡”和“南柴胡”。具有疏散退热,疏肝解郁,升阳举陷的作用,用于感冒发热、寒热往来、疟疾、肝郁气滞、胸肋胀痛、脱肛、子宫脱落、月经不调[1-2]。现代药理研究证明柴胡具有解热、镇痛、镇静、抗炎、免疫增强、保肝利胆、抗菌、抗病毒及抗肿瘤等作用[3-4]。在2010版《中华人民共和国药典》中,以柴胡皂苷a和柴胡皂苷d的总量之和表征柴胡饮片的质量[5]。随着对柴胡研究的深入,柴胡中黄酮类成分的研究也受到了人们的关注[6-8]。
在对柴胡饮片的研究中,笔者运用本课题组建立的药代动力学-药效动力学-药物成分相互作用关联分析方法(PK-PD-DI)研究王永炎院士拟定的临床经验方柴金方(柴胡、佩兰、郁金、肉桂、何首乌)以及组方药味的抗抑郁药物体系时,发现柴胡中皂苷类与黄酮类均为其药物体系的组成成分。中药化学成分的有效性与其质量性有关,即与中药化学成分的类型以及存在的量、组成比例等有关[9-11]。
本文报道运用课题组建立的基于药物体系的中药质量评价模式[12-14],对柴胡饮片进行质量评价与控制。以药物体系为导向,对柴胡中的主要黄酮类、主要皂苷类以及总酚类进行质量表征,建立同时测定黄酮类与皂苷类成分含量的HPLC方法。即在基准批次样品饮片中检测到了芦丁的色谱峰,且发现存在3个与芦丁紫外光谱图相似的黄酮类色谱峰,未见文献报道的槲皮素、异鼠李素、山柰素的色谱峰,故测定芦丁的含量,并以其为标尺,以基准饮片样品中标定的4个黄酮类色谱峰为基准,通过主要黄酮类成分峰面积加和表征主要黄酮类成分含量和;同时发现柴胡中皂苷类成分以柴胡皂苷c、柴胡皂苷a、柴胡皂苷d为主,故测定其含量,并以其含量和表征主要皂苷类成分总含量;并首次建立可见分光光度法测定柴胡中总酚类成分含量的方法。关注有效指标性成分的含量及其和,与组成比例,并与有效性确切的基准饮片进行关联度分析比较,对柴胡饮片的质量进行综合考量,以确定其饮片质量优良度,为柴胡饮片的有效应用提供科学依据,亦为有关药物的质量保障提供支撑。
1 仪器与试药
1.1 仪器 Waters X-Bridge C18色谱柱;Waters e2695高效液相色谱仪;Empower Pro软件系统;2998 PDA检测器;METTLER-AE240型电子分析天平(北京赛多利斯仪器有限公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司);TU-1810型紫外-可见分光光度计(北京普析通用仪器有限公司)。
1.2 试药 芦丁,(批号:130507纯度≥98%);柴胡皂苷c(批号:131120,纯度≥98%)购自成都普菲德生物技术有限公司;柴胡皂苷a(批号:MUST-14031014,纯度≥98%)均购自成都曼斯特生物科技有限公司;柴胡皂苷d(批号:130513,纯度≥98%),购自北京方程生物科技有限公司;乙腈(色谱级,Fisher Scientific公司);甲醇(AR,北京化工厂);甲酸(AR,北京化学试剂公司);娃哈哈纯净水(杭州娃哈哈集团有限公司);三氯化铁(分析纯)购自天津市申泰化学试剂有限公司;铁氰化钾(分析纯)购自广东汕头市西陇化工厂;十二烷基硫酸钠(化学纯)购自北京化学试剂公司;浓盐酸(分析纯)购自北京化工厂;其余试剂均为分析纯。15批柴胡饮片:均购自北京市、福建省厦门市、河南省郑州市、湖北省武汉市各药店,经北京中医药大学刘春生教授鉴定,均为正品,饮片标本现存于北京中医药大学中药学院中药化学系。
2 方法与结果
2.1 指标性成分含量测定方法
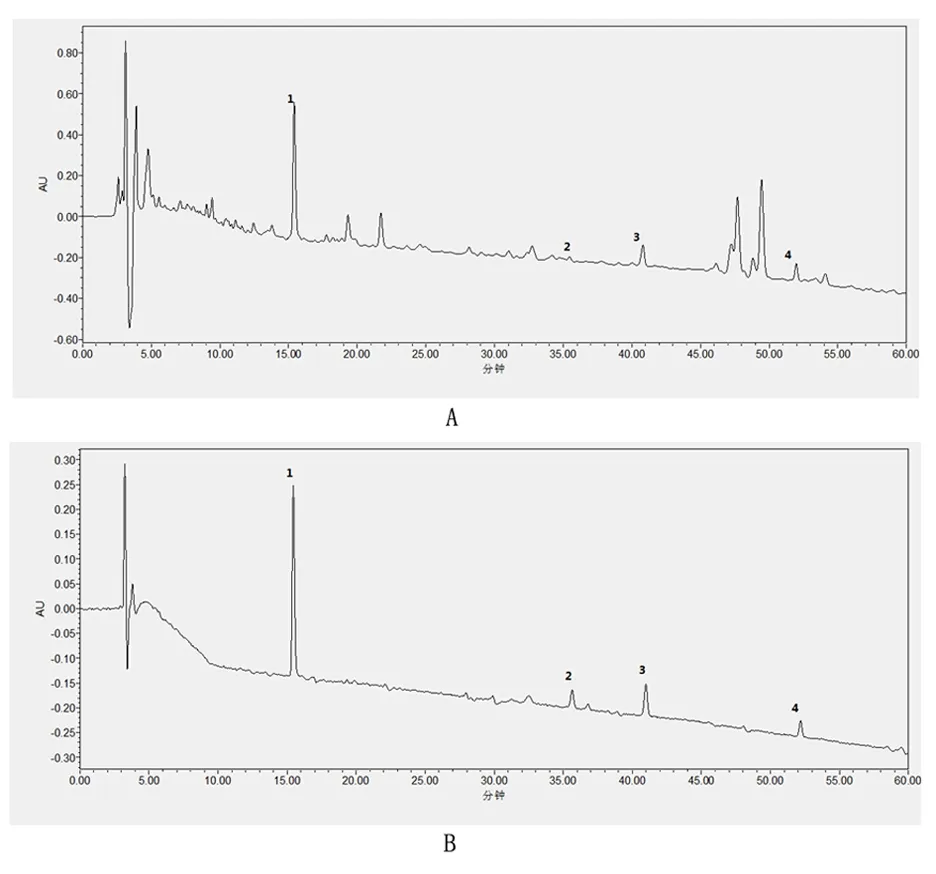
图1 210 nm检测波长下柴胡饮片样品(A)及标准品(B)HPLC色谱图
注:1芦丁;2柴胡皂苷c;3柴胡皂苷a;4柴胡皂苷d
2.1.1 色谱条件 Waters C18色谱柱,流动相乙腈(A)-0.1%甲酸水(B),洗脱梯度(洗脱梯度:0-5 min,10%~25%A;5-40 min,25%~40% A;40-60 min,40%~55% A),流速1.0 mL/min,柱温30 ℃,检测波长分别为360 nm(芦丁),210 nm(柴胡皂苷c、柴胡皂苷a、柴胡皂苷d)。
上述色谱条件下,柴胡对照品及样品的HPLC谱图见图1、图2,4种已知有效指标性成分及3种未知黄酮类成分在各自的检测波长下与其他色谱峰分离度良好。
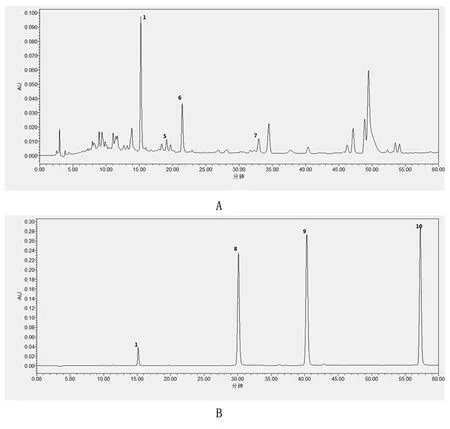
图2 360 nm检测波长下柴胡饮片样品(A)及标准品(B)HPLC色谱图
注:1芦丁;5、6、7为3种黄酮类成分;8槲皮素;9异鼠李素;10山柰素
图1、图2中1~7号峰各峰保留时间及以柴胡皂苷a为参照时的相对保留时间见表1。
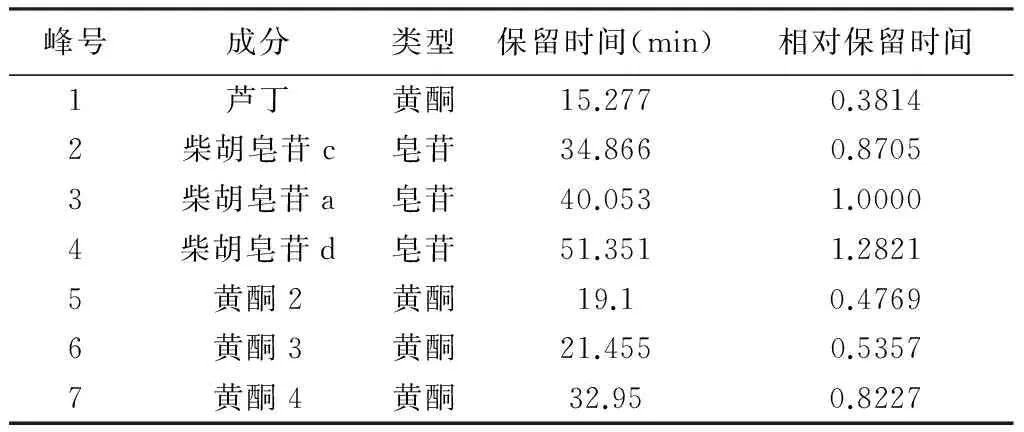
表1 各成分的保留时间及相对保留时间
2.1.2 对照品溶液的制备 分别取上述4种对照品适量,精密称定,加入甲醇制成每1 mL含有芦丁43.6 μg、柴胡皂苷c 273 μg、柴胡皂苷a 450 μg、柴胡皂苷d 324 μg的对照品混合溶液。
2.1.3 供试品溶液的制备 精密称定柴胡饮片粉末(过四号筛)约0.5 g,加甲醇20 mL超声(功率500 W,频率40 kHz)提取30 min,滤过,保留滤液,并用10 mL甲醇洗涤容器及残渣,重复上述操作,提取2次,回收溶剂至干,加甲醇复溶,定容于5 mL容量瓶内,即得供试品溶液。
2.1.4 线性关系考察 将“2.1.2”项下对照品混合溶液进样2 μL、5 μL、10 μL、20 μL、30 μL、40 μL、50 μL,以进样量(mg)为横坐标,峰面积为纵坐标绘制标准曲线,计算回归方程及相关系数,结果见表2。

表2 4种成分的回归方程、相关系数和线性范围(n=7)
2.1.5 精密度实验 取“2.1.3”项下同一柴胡样品溶液,连续进样6次,测得芦丁、柴胡皂苷c、柴胡皂苷a、柴胡皂苷d峰面积的RSD分别为2.58%、1.82%、1.93%、2.24%,精密度良好。
2.1.6 重复性试验 取同一柴胡饮片样品,按“2.1.3”项下方法平行制备供试品溶液6份,测得芦丁、柴胡皂苷c、柴胡皂苷a、柴胡皂苷d的平均含量分别为0.088 7%、0.055 0%、0.263 0%、0.286 3%,RSD分别为1.90%、1.33%、1.97%、1.61%,重复性良好。
2.1.7 稳定性试验 取“2.1.3”项下同一供试品溶液,于室温下放置,分别于0 h、2 h、4 h、8 h、12 h、24 h进样,测得芦丁、柴胡皂苷c、柴胡皂苷a、柴胡皂苷d的峰面积的RSD分别为1.95%、1.21%、2.46%、2.37%,供试品溶液在24 h内稳定。
2.1.8 加样回收率试验 称取同一柴胡样品粉末(过四号筛)约0.25 g,共6份,精密称定,加入对照品适量,按“2.1.3”项下方法制备供试品溶液,进样,测得芦丁、柴胡皂苷c、柴胡皂苷a、柴胡皂苷d的加样回收率分别为98.65%、97.66%、98.46%、99.87%,RSD分别为2.51%、1.54%、1.09%、1.26%,加样回收率合格,说明本方法准确、可靠。
2.2 柴胡总酚类成分含量测定方法
2.2.1 供试品溶液的制备方法 精密称定柴胡饮片粉末(过4号筛)约0.5 g,加甲醇20 mL超声(功率500 W,频率40 kHz)提取30 min,滤过,保留滤液,并用10 mL甲醇洗涤容器及残渣,重复上述操作,提取两次,回收溶剂至干,加甲醇复溶,定容于5 mL容量瓶内,即得供试品溶液。
2.2.2 对照品溶液的制备方法 精密称取一定量的芦丁标准品3.14 mg,置于10 mL容量瓶内,用70%甲醇定容至10 mL,则标准品的浓度为0.314 mg/mL。
2.2.3 显色方法 基于课题组前期考察的全方提取物的总酚类成分的测定方法,采用可见分光光度法测定柴胡饮片中总酚类的含量,方法即以芦丁作为酚类的指标性成分,三氯化铁-铁氰化钾法测定酚类的显色方法,具体是精密吸取一定量的样品溶液于25 mL棕色容量瓶中,加70%甲醇至5 mL,分别加入0.3%十二烷基硫酸钠溶液1.6 mL及0.6%三氯化铁-0.9%铁氰化钾(1:1)混合溶液2.4 mL,暗处放置7 min,用0.1 mol/L盐酸加至25 mL刻度线,摇匀后于暗处静置30 min,于768 nm波长处测定吸光度值[15]。

表3 基于有效指标性成分含量的15个柴胡饮片样品质量表征(%,n=3)
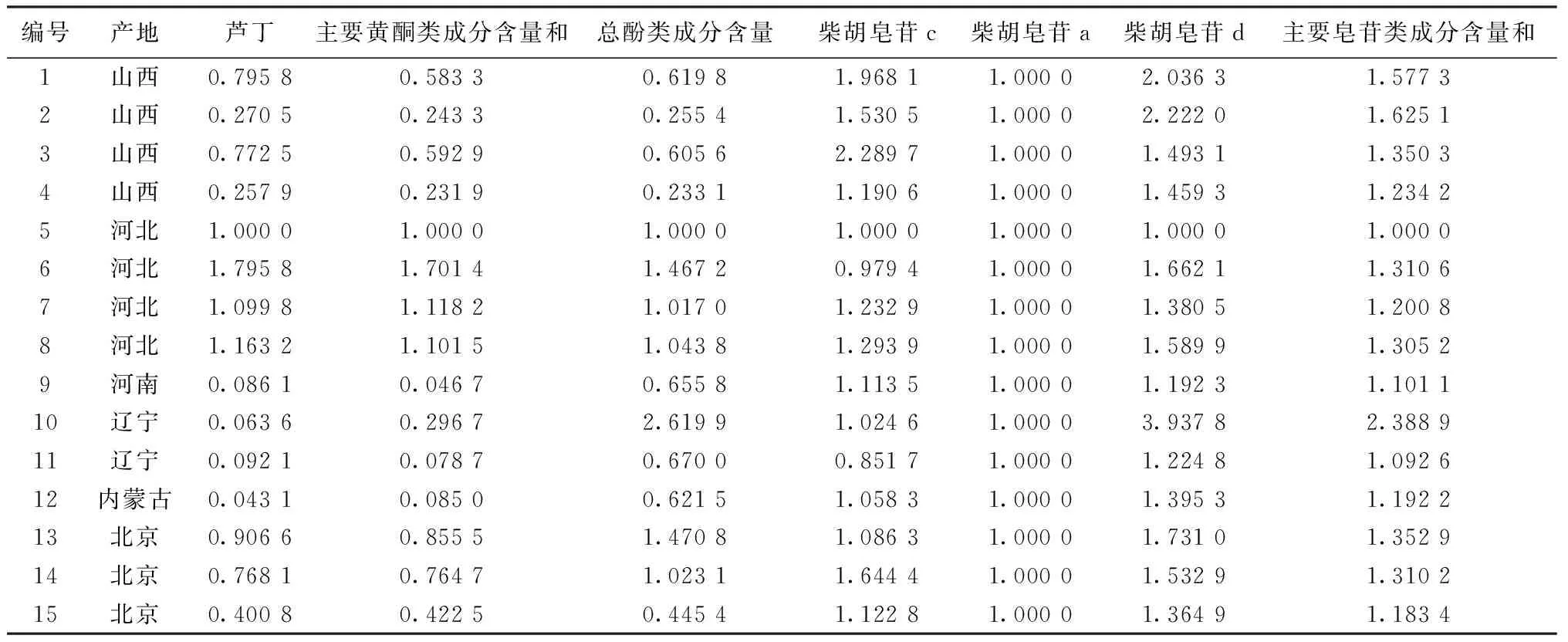
表4 基于有效指标性成分含量相对比值的15个柴胡饮片样品质量表征
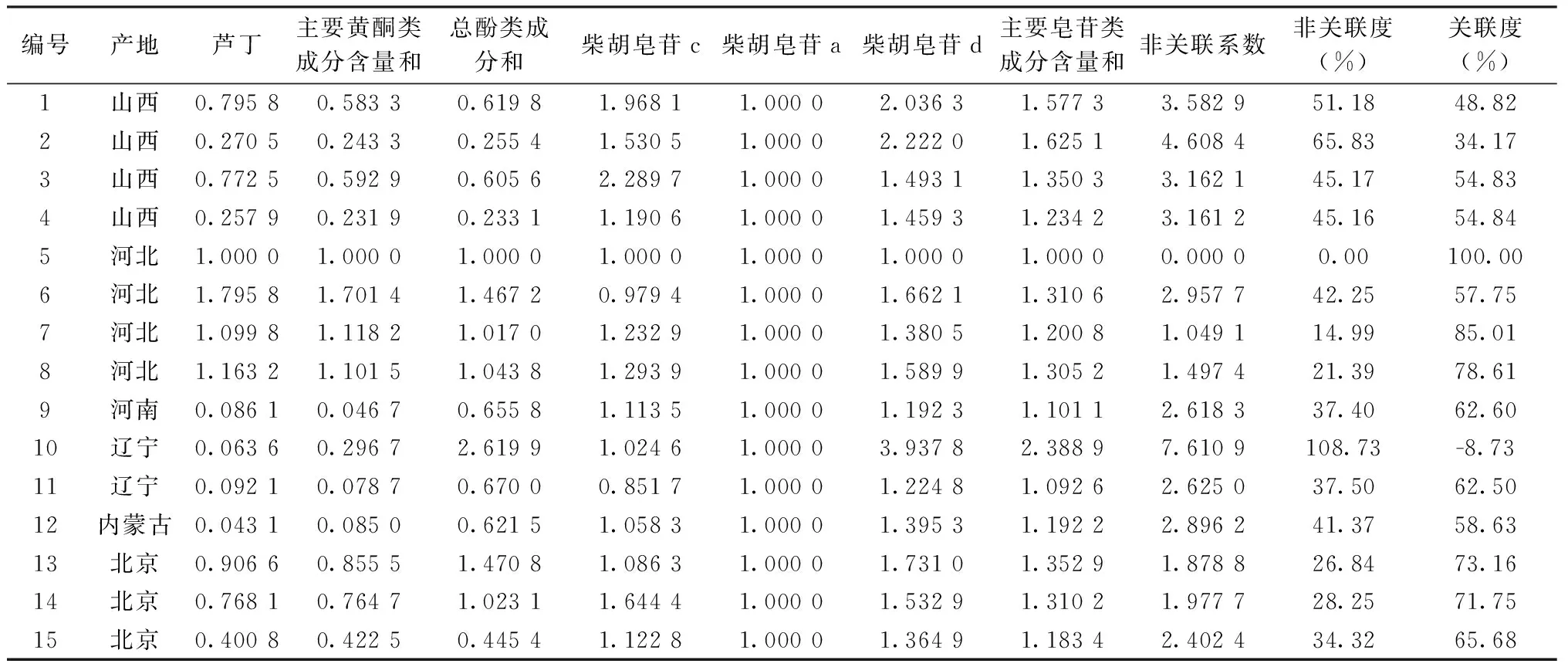
表5 15个柴胡饮片样品关联度表征
2.2.4 线性关系考察 精密吸取2.2.2项下的芦丁对照品0.030 mL、0.05 mL、0.07 mL、0.09 mL、0.11 mL、0.13 mL,按照2.2.3项下的方法进行显色。以对照品浓度为横坐标,吸光度值为纵坐标绘制标准曲线,并进行线性回归分析,计算回归方程为:
Y=498.07X+0.095 7,R2=0.998 6(n=6)
结果表明,芦丁在0.000 376 8 mg/ml~0.001 632 8 mg/mL的浓度范围内与吸光度呈良好的线性关系。
2.2.5 重复性实验 取同一柴胡饮片样品,按“2.2.1”项下方法平行制备供试品溶液6份,测得总酚类成分的平均含量为2.26%,RSD 0.96%,重复性良好。
2.2.6 加样回收实验 称取同一柴胡样品粉末(过四号筛)约0.25 g,共6份,精密称定,加入芦丁对照品适量,按“2.2.1”项下方法制备供试品溶液,测定总酚含量,RSD 2.67%,加样回收率95.55%~101.62%,结果表明该方法加样回收率合格。
2.3柴胡质量表征
2.3.1 基于有效指标性成分含量的质量表征取 15个柴胡饮片样品,按“2.1.3”项下方法制备供试品溶液,每个平行制备3份,按照“2.1.1”项色谱条件进样,测定柴胡饮片中芦丁、柴胡皂苷c、柴胡皂苷a、柴胡皂苷d的含量,并且以芦丁为对照品,通过主要黄酮类成分峰面积和表征主要黄酮类成分含量和;柴胡皂苷c、柴胡皂苷a、柴胡皂苷d的含量加和表征主要皂苷类成分含量和,从而对柴胡饮片中有效指标性成分含量进行全面表征,结果见表3。
2.3.2 基于有效指标性成分含量相对比值的质量表征 以药物体系中有效指标性成分柴胡皂苷a的含量为基准,将15个柴胡饮片样品中各有效指标性成分含量与柴胡皂苷a含量的相对比值予以表征,结果见表4。
2.4 柴胡质量表征关联分析
2.4.1 基于与基准饮片有效指标性成分含量相对比值的质量表征的关联分析
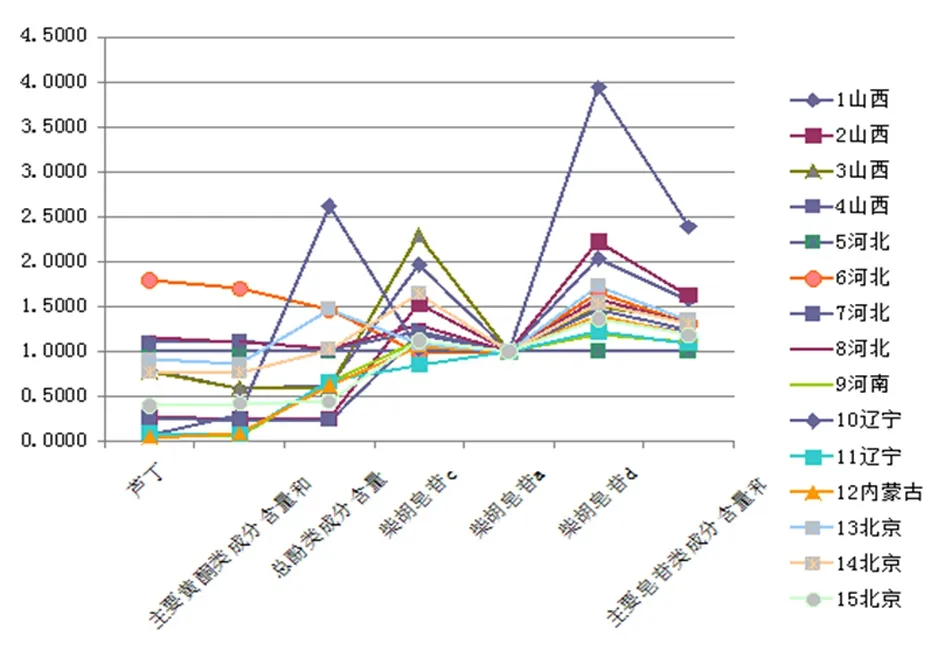
图3 15个柴胡饮片样品中各有效指标性成分含量与基准饮片样品5对应成分含量相对比值
结合表3和图3进行分析,可知在15个不同批次的柴胡饮片中,各指标性成分含量的差异较大,并计算最高比值与最低比值的比,以反映各饮片中有效指标性成分含量的差异。芦丁含量最大比值与最小比值之比为47.95,含量从高到低排序为:14>6>8>5>7>1>3>13>4>2>15>9>11>12>10;主要黄酮类成分含量和最大比值与最小比值之比为15.87,含量从高到低排序为:14>5>6>8>7>1>3>13>4>2>15>9>10>12>11;总酚类成分含量和最大比值与最小比值之比为11.24:10>13>8>14>7>5>11>9>12>1>3>15>6>2>4;柴胡皂苷c含量最大值与最小值之比为6.92,含量从高到低排序为:9>14>2>3>4>1>8>12>7>5>11>15>6>13>10;柴胡皂苷a含量最大值与最小值之比为6.37,含量从高到低排序为:9>14>4>2>12>5>11>8>7>1>3>15>6>13>10;柴胡皂苷d含量最大值与最小值之比为3.5,含量从高到低排序为:9>2>14>4>1>10>12>8>11>7>3>5>6>15>13;皂苷类成分的和含量最大值与最小值之比为4.14,含量从高到低排序为:9>14>2>4>1>12>8>11>7>3>5>10>15>6>13。
分析以上几个指标性成分含量的差异,芦丁(47.95倍)>主要黄酮类成分含量和(15.87倍)>总酚类成分含量和(11.24倍)>柴胡皂苷c(6.92倍)>柴胡皂苷a(6.37倍)>主要皂苷类成分含量和(4.14倍)>柴胡皂苷d(3.50倍)。基于芦丁、主要黄酮类成分含量和、总酚类成分含量、柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、主要皂苷类成分含量和进行综合考量,发现样品7、8、14的指标性成分的含量总体上高于基准饮片样品5,样品6中有效指标性成分含量与基准饮片样品5接近。
2.4.2 基于与基准饮片有效指标性成分含量相对比值的比值质量表征的关联分析
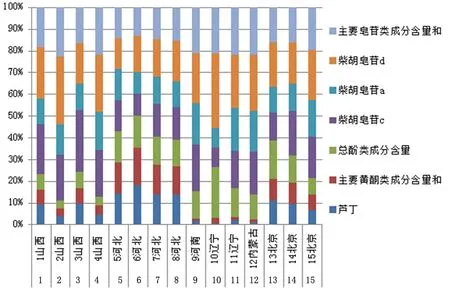
图4 15个柴胡饮片中各有效指标性成分含量相对比值与基准饮片样品5对应成分含量对比值的比值
图4中不同颜色的矩形条代表各饮片中有效指标性成分含量相对比值与基准饮片样品5对应成分含量相对比值的比值,矩形条大小与基准饮片样品5中相同颜色的矩形条大小越相近,代表该饮片有效指标性成分含量比值与基准饮片样品5越接近,即质量表征关联密切。可以看出,样品7、8、13、14与基准饮片样品5质量表征关联密切。以基准饮片样品5为基准,其他样品与其相对比值的比值差值的绝对值之和,即非关联系数;非关联系数与有效指标性成分的数目的比值,即非关联度,进而得到关联度,以反映饮片质量之间的关联性,见表5。
由表5可知,关联度由高到低排序为:5(0/100%)>7(1.0491/85.01%)>8(1.4974/78.61%)>13(1.8788/73.16%)>14(1.9777/71.75%)>15(2.4024/65.68%)>9(2.6183/62.60%)>11(2.6250/62.50%)>12(2.8962/58.63%)>6(2.9577/57.75%)>4(3.1612/54.84%)>3(3.1621/54.83%)>1(3.5829/48.82%)>2(4.6084/34.17%)>10(7.6109/-8.73%),即样品7、8、13、14与基准批次饮片的关联度较高。
3 讨论
本文基于药物体系质量评价模式,对市场上销售的15个不同批次的柴胡饮片进行质量表征及关联分析研究,综合考虑15个不同批次的柴胡饮片与基准饮片样品5的关联度以及指标性成分的含量,样品7、8、14、5、13的品质优良度居前。从以上数据分析看出,柴胡饮片受产地影响比较大,相同产地的饮片各成分在含量上更为接近。
中药饮片质量与其所含有效化学成分类型及其存在的量、组成比例等因素有关。本文在自然药学观相关理论的指导下,基于前期药物体系组成成分的发现,运用相关中药质量评价模式,对15个不同批次的柴胡饮片样品的质量进行表征,并以具有确切药效的样品5为基准,进行质量关联度分析比较,综合精准评价出柴胡饮片质量的优良度。即综合考量了柴胡应用有效性及质量关联性,从而为柴胡资源筛选及其药物的原料质量控制和应用提供了依据,亦为中药药材及其饮片的质量评价提供了研究借鉴。
[1]牛向荣.柴胡药理作用研究概述[J].中国药师,2009,12(9):1310-1312.
[2]田利鲜.柴胡的药理作用和临床运用[J].湖北中医杂志,2008,30(1):59-60.
[3]祖宁,李平.柴胡皂苷的生理作用及临床意义[J].中国中医药信息杂志,2005,12(4):94-96.
[4]李琰.柴胡药理作用的研究进展[J].河北医学,2010,16(5):633-635.
[5]国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2010:357.
[6]韦英杰,王茉,宁青,等.HPLC法同时测定柴胡与春柴胡中皂苷类及黄酮类成分的含量[J].药物分析杂志,2011,31(5):879-883.
[7]梁鸿,赵玉英,崔艳君,等.北柴胡中黄酮类化合物的分离鉴定[J].北京医科大学学报,2000,32(3):223-225.
[8]袁王俊,张维瑞,吴宏欣,等.HPLC法测定柴胡不同部位4种黄酮类成分[J].中成药,2013,35(4):797-800.
[9]石任兵,王永炎,姜艳艳,等.论中药化学发展近况[J].北京中医药大学报,2012,35(3):153-159.
[10]石任兵,王永炎.自然药学观的相关性思考[J].北京中医药大学学报,2012,35(4):221-225.
[11]梅莹莹,许舒娅,左胜,等.基于药物体系的连翘饮药物制备物质量表征分析研究[J].北京中医药大学学报,2014,37(5):338-343.
[12]左胜,孙雅姝,石任兵,等.基于药物体系的藁本质量评价研究[J].北京中医药大学学报,2014,37(7):481-485.
[13]安琪,唐雪阳,石任兵,等.紫苏方药物制备物的质量表征及其关联分析[J].北京中医药大学学报,2014,37(6):414-419.
[14]李焕娟,张璐,石任兵,等.基于药物体系质量评价模式的远志质量表征关联分析研究[J].北京中医药大学学报,2014,37(12):834-840.
[15]韩珂卿.基于药物体系的柴金方药物制备工艺与质量控制技术方法研究[D].北京:北京中医药大学,2014.
(2014-11-25收稿 责任编辑:张文婷)
Quality Representation and Correlation Analysis of Chaihu (Bupleuri Radix) Based on the Quality Evaluation Model of Drug System
Pan Ting1,Huang Yating1,Han Keqing1,Sun Yashu1,Wen Jing1,Chi Lei1,Chen Wei1,Yang Yuan1,Jiang Yanyan1,3,Shi Renbing1,3
(1KeyUnitofExploringEffectiveSubstancesofClassicalandFamousFormulasofStateAdministrationofTraditionalChineseMedicine,SchoolofChinesePharmacy,BeijingUniversityofChineseMedicine,Beijing100102,China; 2CapitalMedicalUniversitySchoolofTraditionalChineseMedicine,Beijing100069,China; 3MunicipalCommissionofEducationQualityControlTechnologyandEngineeringCenterofChineseMedicine,Beijing100102,China)
Objective:To establish quality representation and correlation analysis on Chaihu (Bupleuri Radix) based on the quality evaluation model of drug system.Methods:Use HPLC method to simultaneously determine the 4 effective index components of Chaihu, including rutin, saikosaponin c, a, and d, meanwhile characterize the main contents of flavonoids and saponins. Use visible spectrophotometry to determine the content of total phenolic in Chaihu.Results:Based on the quality evaluation model of drug system to characterize and correlation analysis the effective indicator ingredients and the relative ratio of them. Then evaluate the associate degree of pieces of different batches and the reference piece. The result shows the total content of effective index components in No. 7, No. 8, No. 14 is higher than No. 5 and No. 6 is closer to No. 5. No. 7, No. 8, No. 13 No. 14 have high associate degree with No.5.Comprehensive quality characterization and correlation analysis results, the No.7, No.8, No.14, No.5, No.13 have high quality ranking.Conclusion:Quality representation and correlation analysis of Chaihu are based on a new quality evaluation model of drug system. Considering quality representation based on the content and the content relative ratio of effective index components comprehensively. This paper reports the specific applications of a new way of thinking model for the quality representation and evaluation of Chaihu, providing the foundation of raw material quality control and application screening.
Chaihu (Bupleuri Radix); Correlation analysis; Main flavonoids; Total phenolic ingredients; Saikosaponin c, a, d; Main saponins
十二五国家科技支撑计划项目(编号:2012BAI29B06);北京中医药大学创新团队资助项目(编号:2011-CXTD-12)
潘婷(1989—),女,河南焦作人,在读硕士研究生,E-mail:pantingbest@163.com
石任兵,男,博士,教授,博士生导师,研究方向:中药(复方)有效物质基础研究与药物创新,E-mail:shirb@126.com
R284.1
A
10.3969/j.issn.1673-7202.2015.04.027

