体外膜肺氧合在气管肿瘤切除中的应用
鲁会卿,张强,于艳宏,李宏,李子津,邓乃封
(1 武警后勤学院附属医院麻醉科,天津 300162; 2 河北联合大学基础医学院; 3 天津医科大学第二附属医院麻醉科)
体外膜肺氧合在气管肿瘤切除中的应用
鲁会卿1,张强1,于艳宏1,李宏1,李子津2,邓乃封3
(1 武警后勤学院附属医院麻醉科,天津 300162; 2 河北联合大学基础医学院; 3 天津医科大学第二附属医院麻醉科)
目的 探讨气管肿瘤切除手术中,在常规通气模式难以实现正常气体交换的情况下,体外膜肺氧合(ECMO)辅助下实施外科治疗的可行性及安全性。方法 气道肿瘤病人1例,气道阻塞达95%,局麻下股动脉、股静脉插管,在ECMO辅助下行麻醉及管肿瘤切除气道重建手术。结果 术中氧合满意,尤其在切开气管肿瘤远端、左主支气管插管中,在ECMO辅助下可为机体提供充足的氧合。结论 在气管肿瘤的外科治疗中,对于不适合进行常规气道管理的病人,ECMO可作为一种安全有效的辅助方法。
体外膜肺氧合;气管肿瘤;气道重建术
在气管肿瘤切除及气道重建手术中,气道管理是关键,原因在于麻醉与外科共用气道,既要保证病人术中有足够的氧合,又要为术者提供充分的操作空间。在常规通气管理难以实现有效气体交换满足机体氧供的情况下,就需要采用一些特殊的手段处理。随着体外膜肺氧合(ECMO)技术应用的增加,积累了许多宝贵的经验,为麻醉提供了一种新的选择。本研究对1例气道阻塞95%病人采用ECMO辅助下气管肿瘤切除气道重建手术,效果较好。现将结果报告如下。
1 临床资料
病人,男,31岁,体质量100 kg。因咳嗽、喘息4年余,加重3月入院。电子支气管镜检查可见气管隆突上方3 cm处有一包块,阻塞大气道,左右各叶段支气管管腔通畅(图1)。CT检查见气管占位伴气道狭窄,右肺下叶轻度炎症,双侧胸膜增厚(图2)。病人入手术室后监测右手脉搏氧饱和度(SpO2)为95%,常规面罩吸氧,流量4 L/min,SpO2升至100%,局麻下右手桡动脉穿刺监测有创血压,右颈内静脉置管监测中心静脉压。插管前给予肝素0.5 mg/kg,激活凝血时间(ACT)达246 s,局麻下右侧股动脉插入19Fr肝素化整体股动脉插管作为灌注管,右侧股静脉插入23Fr肝素化整体股静脉插管作为引流管,选用Medt ronic全肝素涂层聚甲基戊烯膜式氧合器以及肝素涂层管道、变温器、离心泵头及血氧饱和度探头。ECMO转流方式为常温转流,转流流量为4.2 L/min,通气量为4 L/min,氧体积分数为0.80。整个转流期间,ACT维持在160~200 s,转流流量维持在3.6~4.2 L/min。麻醉诱导方法:依次经静脉缓慢给予咪达唑仑0.04 mg/kg,舒芬太尼0.7 μg/kg,罗库溴铵0.6 mg/kg,丙泊酚1~2 mg/kg,BIS值降至45~55[1]时停止输注丙泊酚。90 s后于纤维气管镜引导下气管内插入7.0#单腔加强气管导管,导管尖端位于气管肿瘤之上。病人左侧卧位,右侧开胸后切开气管肿瘤远端,由手术医生向左主支气管插入6.5#单腔加强气管导管,保证麻醉和通气,同时主气道气管导管停止通气。在此过程中病人SpO2由100%开始下降,最低达到67%;机械通气参数显示气道压高达42 cm H2O,经由手术医生气管导管内吸引,调整导管位置,气道压力降至2.16 kPa,SpO2迅速回升至95%。切除气管肿瘤及肿瘤底部上、下各一个气管环,共切除气管长度2.0 cm,可吸收线间断缝合气管膜部及软骨部。整个左主支气管通气期间,SpO2始终维持在95%左右。拔除左主支气管气管导管后,将主气道内插管向前推进达气管吻合口以下,充分吸引后进行通气。此后SpO2维持在100%。手术过程中ECMO转流灌注管氧合血氧饱和度为99%,引流管道混合静脉血氧饱和度为80%。手术历时170 min,ECMO辅助时间4 h。术后病人被送往重症监护病房,呼吸机辅助呼吸。24 h支气管镜检查证实无水肿、出血,拔出气管导管,3 d后转入普通病房。术后病理诊断为类癌。
2 讨 论
气道管理是气管肿瘤切除手术麻醉管理的核心,本病例气道严重狭窄,气管管腔堵塞约95%,单纯使用传统的通气管理,可能产生氧合不足甚至致命性的低氧。以往曾有作者将体外心肺转流(CPB)用于气管肿瘤的外科治疗,并取得成功[2-4]。然而,CPB有增加术后出血及潜在的肝、肾功能损害等并发症。而ECMO可以克服CPB的上述缺点。因此,ECMO的应用无疑解决了气道手术中外科医生和麻醉医生最棘手的问题。
ECMO的治疗原理就是通过插管技术,将血液从体内引流到体外,经人工膜肺氧合后,再将氧合血通过离心泵或滚轴泵灌注入体内,以维持机体各器官的供血和供氧。
ECMO在临床上多用于急性呼吸窘迫综合征、心内直视术后低心排综合征和H1N1禽流感呼吸衰竭等病人。近年来,ECMO辅助下气管重建外科手术治疗在西方国家受到越来越多的关注[5]。2010年COLLAR等[6]报道了第1例ECMO转流下成功实施气管隆突肿瘤切除及气道重建手术。然而,国内鲜有该方面应用的报道[7-8]。
在临床上ECMO的治疗模式主要有以下两种,静脉-动脉EMCO(VA-ECMO)和静脉-静脉EMCO(VV-ECMO)。其中VA-ECMO模式在进行呼吸支持的同时能够进行循环支持,适用于严重循环衰竭或者严重循环并发呼吸衰竭病人。
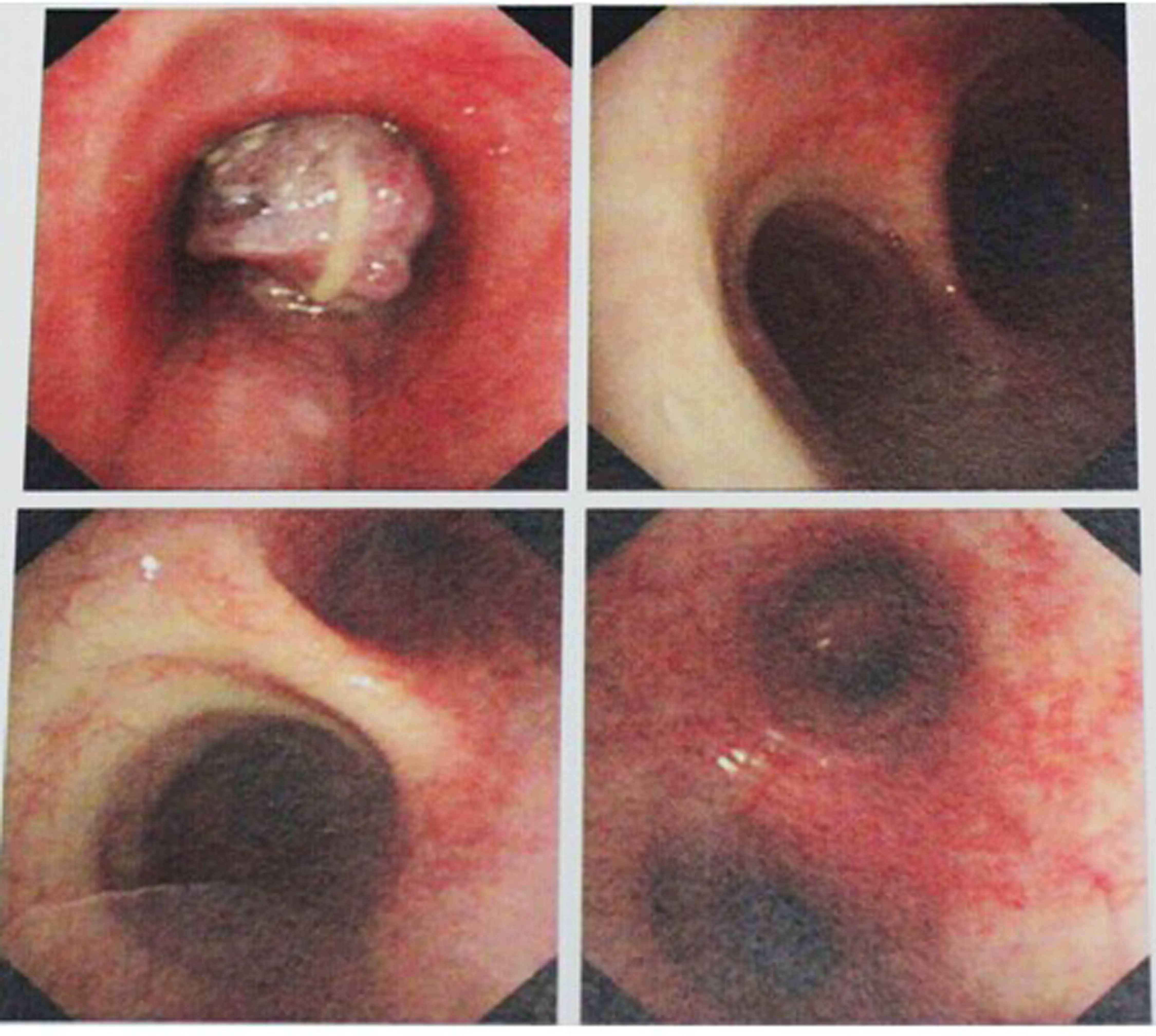
图1 电子支气管镜检查
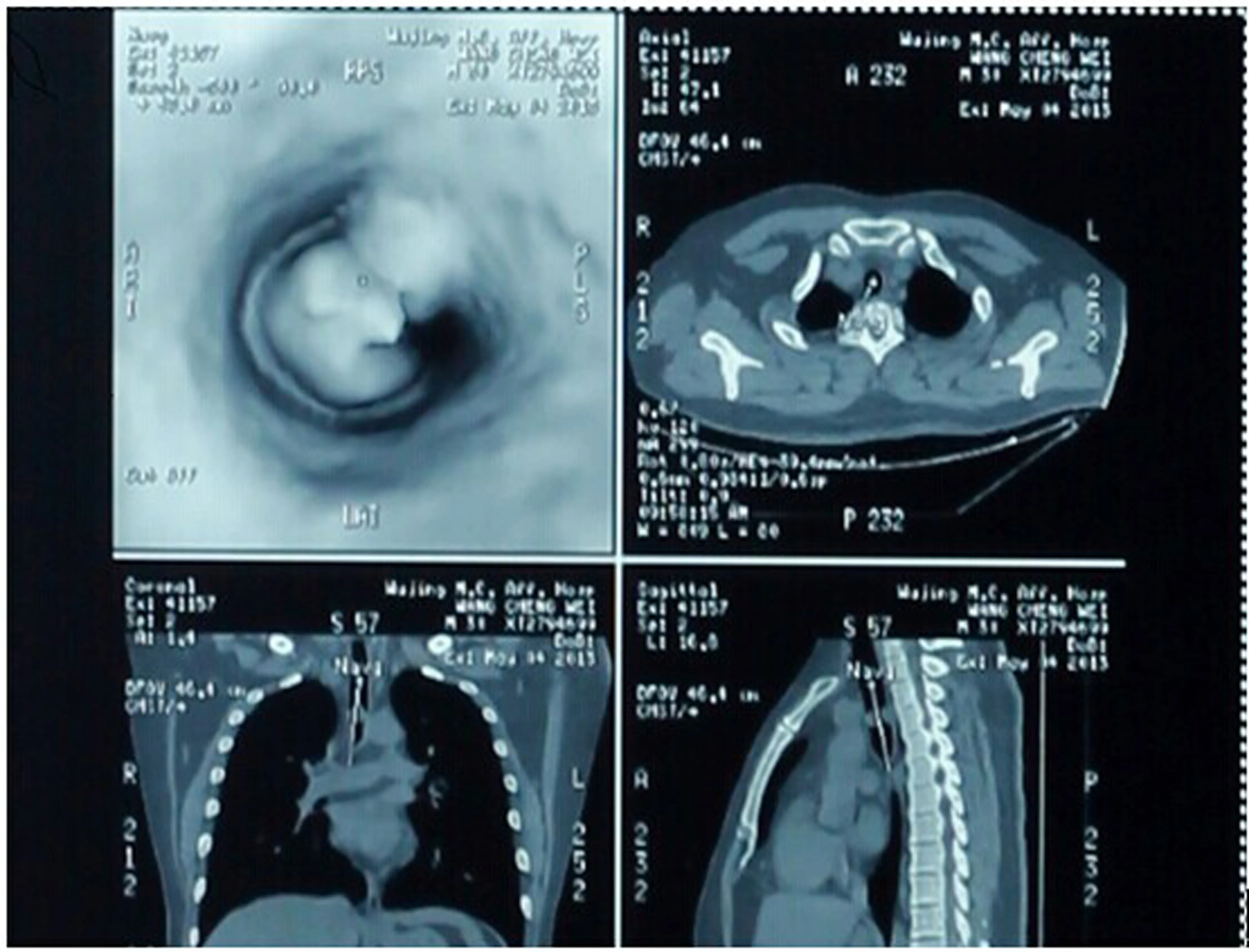
图2 CT检查
VV-ECMO模式只能代替肺脏进行气体交换,不能提供直接循环支持,主要用于严重呼吸衰竭而不需要循环支持的病人。然而在临床实践中观察到,尽管VV-ECMO模式不能提供直接的心脏支持,但通过ECMO的呼吸支持使呼吸系统得到改善和恢复,从而解决了与呼吸衰竭相关的血流动力学功能紊乱[9]。
本例病人在左主支气管通气的过程中,SpO2维持在95%,这提示右上半身氧供不足。同时ECMO转流监测指标显示,灌注管氧合血氧饱和度为99%,引流管混合静脉血氧饱和度为80%,提示下半身氧合良好。究其原因为: 股动脉灌注管射出的氧合血与主动脉射出的血相互抵抗,使得氧合血难于达到身体的上部,越接近主动脉近段阻力越大,尤其是身体的右上部很难得到氧合血的灌注[8]。这提示VA-ECMO并不是ECMO辅助下气道重建手术的最佳选择。相比之下,VV-ECMO避免了VA-ECMO两个重要的弊端:①不需要动脉插管;②保证了身体上部的氧合。因而,VV-ECMO是气道重建外科治疗中更为合理的模式。
ECMO辅助期间氧供不足还可能与以下因素有关:①病人CO增加或氧代谢增加,相比之下,ECMO可以提供的转流量有限;②存在“再循环”,即ECMO灌注的氧合血未通过肺循环进入体循环增加机体供氧,直接经ECMO引流管引流回氧合器,该部分对机体氧供无贡献的循环部分称之为“再循环”;③肺换气功能严重障碍;④氧合器失效,如氧合器内形成血栓;⑤转流量过大(>6 L/min),超过氧合器气体交换能力。
对于该例病人,我们选择23Fr股静脉插管,ECMO转流量最高只能达到4.2 L/min,按体表面积计算则仅为1.91 L/(min·m2),仅能达到该病人正常心指数的60%。从理论上来讲,在肺组织不参与气体交换的情况下,ECMO转流量至少应达心输出量的70%,SpO2才能达到预期的目标值。因此,本病例仅靠ECMO不能维持满意的氧合,术中需持续机械通气来维持上半身氧供。SIDEBOTHAM等[9]认为,在必须的情况下,可以通过增加一个引流管来增加ECMO转流量,从而达到满意的氧合。
综上所述,严重气道阻塞病人行外科治疗,在清醒状态下建立ECMO,保证充足氧供是可行、有效的。即使将传统的通气方式作为首选方案,ECMO也应备好处于待命状态,一旦出现紧急事件,立即投入使用。
[1] 王培,冀翔宇,王世端,等. 七氟醚与异丙酚麻醉BIS为50时血流动力学参数变化[J]. 齐鲁医学杂志, 2010,25(5):424-426.
[2] TYAGI I, GOYAL A, SYAL R, et al. Emergency cardiopulmonary bypass for impassable airway[J]. J Laryngol Otol, 2006,120(8):687-690.
[3] NAKAMURA H, TANIGUCHI Y, MIWA K, et al. Primary adenocarcinoma of the trachea resected using percutaneous cardiopulmonary support (PCPS)[J]. Ann Thorac Cardiovasc Surg, 2007,13(5):338-340.
[4] GAO H, ZHU B, YI J, et al. Urgent tracheal resection and Reconstruction assisted by temporary cardiopulmonary bypass: a case report[J]. Chin Med J, 2013,28(1):55-57.
[5] SMITH I J, SIDEBOTHAM D, MCGEORGE A D, et al. The use of ECMO during of tracheal papillomatosis[J]. Anesthe-siology, 2009,110:427-429.
[6] COLLAR R M, TAYLOR J C, HOGIKYAN N D, et al. Awake extracorporeal membrane oxygenation for management of critical distal tracheal obstruction[J]. Otolaryngol Head Neck Surg, 2010,142(4):618-620.
[7] 王宏伟,费悦,祝继洪,等. 体外膜肺氧合用于重度气管狭窄病人气道重建术的效果[J]. 中华麻醉学杂志, 2012,32(6):765-766.
[8] 田丰,王小平,李小飞,等. 体外膜肺氧合在气管肿瘤外科治疗中的辅助应用[J]. 现代肿瘤医学, 2009,17(10):111-113.
[9] SIDEBOTHAM D, ALLEN S J, MCGEORGE A A, et al. Venovenous extracorporeal membrane oxygenation in adults: practical aspects of circuits, cannulae, and procedures[J]. J Cardiothorac Vasc Anesth, 2012,26(5):893-909.
(本文编辑 厉建强)
2014-01-16;
2014-07-24
鲁会卿(1976-),女,硕士研究生,主治医师。
李宏(1968-),男,博士,主任医师,硕士生导师。
R614.2
B
1008-0341(2015)01-0112-02

