测定不同浓度舒芬太尼硬膜外分娩镇痛后残存的临床意义
时 捷,董 丽,毛 鹏,赵瑞卿,尚莉莉,胡海珍,路秀莲
(1.新乡市妇幼保健院麻醉科,河南新乡453000;2.新乡医学院基础学院化学教研室,河南新乡453003)
高效液相色谱(HPLC)法具有检测限低,线性好,灵敏度和精确度高等特点,本研究用于检测硬膜外分娩镇痛后舒芬太尼在母体、新生儿及产妇初乳内的残存,指导临床安全应用最低有效的舒芬太尼剂量。
1 资料与方法
1.1 一般资料 选择新乡市妇幼保健院2011年10月至2013年10月,300例,单胎,足月,初产,头位,美国麻醉医师协会(ASA)Ⅰ级,宫口开大到3cm,自愿接受分娩镇痛的产妇。
1.2 方法
1.2.1 仪器 SHIMADZU LC-6AD 型高效液相色谱仪,SPD-20A紫外检测器。TG16-W 高速离心机,PHS-3TC数显酸度计。
1.2.2 试剂 枸橼酸舒芬太尼(171259-200601,中国药品生物制品检定所),枸橼酸芬太尼(171204-200704,中国药品生物制品检定所);色谱纯乙腈(20111021,国药集团化学试剂有限公司);色谱纯正己烷(12010242,国药集团化学试剂有限公司)。
1.2.3 色谱条件 Hypersil BDS C18柱(4.6mm×200mm,5 μm);流动相:0.02mol/L KH2PO4(pH 3.0,内含0.5%三乙胺)∶乙腈=69∶31;检测波长:230nm;柱温:35℃;流速:1.2 mL/min。进样量:20μL。
1.2.4 硬膜外用药 甲磺酸罗哌卡因(浙江仙琚制药股份公司批准文号H20051520),枸橼酸舒芬太尼(湖北宜昌人福药业有限责任公司,批号2100006)。
1.2.5 用药方法与剂量 当宫口开大到3cm时,开始硬膜外分娩镇痛。根据首次不同浓度舒芬太尼负荷量,把产妇随机分成 A、B、C 3组:A组0.089%甲磺酸罗哌卡因1.5mL+舒芬太尼7.5μg;B组0.089%甲磺酸罗哌卡因1.5mL+舒芬太尼5μg;C组0.089%甲磺酸罗哌卡因1.5mL+舒芬太尼3μg。硬膜外注射完毕后接镇痛泵,根据配制镇痛泵内舒芬太尼浓度不同又分别分3个亚组:A 组(A1、A2、A3)、B组(B1、B2、B3)、C组(C1、C2、C3)。A1、B1、C1组舒芬太尼浓度为0.5μg/mL;A2、B2、C2组舒芬太尼浓度为0.4μg/mL;A3、B3、C3舒芬太尼浓度为0.3μg/mL。镇痛泵设置背景剂量8mL/h,自控镇痛每次2mL,锁定时间15min。
1.2.6 样本采集 宫口开全后,关闭镇痛泵,抽取产妇静脉血,胎儿娩出后结扎脐带前抽取脐静脉血,血样本即刻离心留取血浆为检测样本。产妇初乳2mL为检测样本。
1.2.7 样本处理 在洁净的15mL塑料离心管中,各加100 μL内标液(2.08μg/mL枸橼酸芬太尼),1mL血浆,50μL 2 mol/L NaOH。涡旋混合10s。各加5mL正己烷-无水乙醇溶液。手持震荡10min,4 000r/min离心10min。分离出各离心管中的正己烷层于洁净的玻璃离心管中,在50℃水浴中用空气流将吹干。残渣各加流动相100μL,涡旋3min。将溶液转移至1mL离心管中,12 000r/min离心4min。进样20μL。
1.3 统计学处理 采用SPSS17.0软件进行统计学分析,计量资料采用±s表示,组间比较采用独立样本t检验,计数资料用率表示,采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 标准曲线Y(A枸橼酸舒芬太尼/A内标)=0.086 04+959.156 00×C(C枸橼酸舒芬太尼/C内标),r=0.998 00。
2.2 不同浓度舒芬太尼在母血、脐血、初乳中的检测率比较B组、C组与A组比较差异有统计学意义(P<0.05);C组与B组比较差异有统计学意义(P<0.05);A组内A3组与A1、A2组比较差异无统计学意义(P>0.05);B组内B3组与B1、B2组比较差异无统计学意义(P>0.05),C组内C3组与C1、C2组比较差异无统计学意义(P>0.05);乳汁组在首量大于5μg时与母血、脐血组比较差异有统计学意义(P<0.05),见表1。
2.3 舒芬太尼总用量与检出率 一般镇痛时间大于或等于6h,总剂量大于或等于25μg;镇痛时间小于或等于1h,总剂量小于或等于8.5μg。每组母血、脐血和乳汁3种样本相加,即每组样本增加2倍。总剂量大于或等于25μg:A1、A2、A3、B1、B2、B3与C1、C2、C3比较差异有统计学意义(P<0.05),A1组与A2、A3、B1、B2、B3组比较差异有统计学意义(P<0.05),A1、A2、A3组与B1、B2、B3组比较差异有统计学意义(P<0.05);总剂量小于或等于8.5μg:A1、A2、A3、B1、B2、B3与C1、C2、C3比较差异有统计学意义(P<0.05)。A1、A2、A3组与B1、B2、B3组比较差异有统计学意义(P<0.05);当总量8.5~25μg时:C1、C2、C3组与A1、A2、A3、B1、B2、B3组比较差异有统计学意义(P<0.05)。在 A组内,≥25μg组、≤8.5μg组与8.5~25μg组比较差异有统计学意义(P<0.05),见表2。
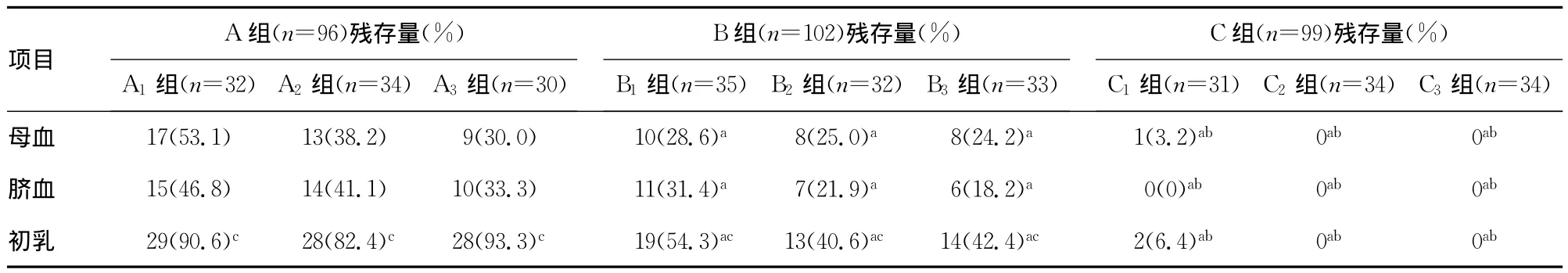
表1 不同浓度舒芬太尼在母血、脐血、初乳中的检测率比较

表2 舒芬太尼总用量与检出率[n(%)]
3 讨 论
舒芬太尼是一种新合成的强效拟吗啡类镇痛药,为芬太尼N-4位取代的衍生物,是μ阿片类受体高选择性激动药;其脂溶性强与阿片类受体亲和力强,镇痛效价是芬太尼的5~10倍。是临床上手术、镇痛首选药物之一,使用广泛、安全、剂量小,血浆浓度也少,尤其硬膜外用药后,血浆含量更少,一般仪器不能测定其含量。HPLC是目前化学分析最强大的工具之一,能分离定性、定量任何可以溶解在液体中的化合物。测试中能定性定量,但是低于3.0nmol/L浓度测定量不准确。
硬膜外分娩镇痛要求产妇用药后不影响下床活动,不影响产程进展,对胎儿安全无影响。低浓度罗哌卡因表现出感觉与运动分离的特性[1]。大于0.2%浓度下肢运动受影响病例增加,还增加了器械助产率。过低浓度又镇痛效果不佳,辅以小剂量舒芬太尼可以减少25%的局麻药用量[2]。且起效快,作用更强[3],其镇痛效果不单是两药的简单相加,而有协同增强作用[4]。
本研究显示舒芬太尼首次负荷量越大加上镇痛泵内浓度越高,检测出残存的例数越多。其中首量7.5μg舒芬太尼(A组)较5μg(B组)、3μg(C组)检出率明显升高。首量3μg舒芬太尼,即使镇痛泵内最高的浓度,检出率也不高。A1组首量最大量7.5μg时,总剂量大于或等于25.0μg时较小于25.0 μg检出率高。还显示总产程小于1h即总量小于或等于8.5 μg较8.5~25.0μg检出率高,差异有统计学意义。因此考虑:(1)首量大,产程越长,总累计药物剂量越大,检出率也越高;(2)首量药量大,产程小于1h,首量代谢不完全,相对检出率高;(3)首量3μg(C组),无论产程长短,检出率均不高,所以首量很关键。
以往认为硬膜外使用阿片类药物镇痛主要是通过脊髓上的β受体介导而起作用,而越来越多证据表明在这个过程中,阿片类药物的全身吸收和神经根被脂溶性高的阿片类药物所激活也起着重要作用[5]。由于舒芬太尼脂溶性高,组织吸收与分布广泛,在延长药物排出方面起了重要作用。徐凯智等[6]研究进出周边室的速率常数为7.6(K13/K31),消除速率常数K10比K31大6.9倍,在理论上说明周边室起到药物储存库作用,延缓了药物返回中央室进行代谢,从而延缓了药物的作用时间。肺脏对外源性物质有选择摄取和释放作用,注射舒芬太尼后,肺摄取总量的(48.9±18.6)%,随后缓慢释放[7]。肌肉也可以摄取大量的舒芬太尼,随后再释放到血液中引起一小的峰值[8]。同样母体乳腺细胞也会大量摄取舒芬太尼,并进入到初乳中,本研究显示硬膜外分娩镇痛首量中舒芬太尼应用大于5μg时,初乳中检测残存量大于40.6%,定量也比脐血、母血含量高。舒芬太尼主要在肝和小肠代谢,24h后80%排泄,本研究采集的初乳,常常在48~72h,或大于72h,在乳腺组织中的代谢是否延长,有待进一步大样本证实。初乳是产妇产后5d内的乳汁,量少,含蛋白、脂肪、无机盐及各种抗体,是新生儿宝贵的营养,新生儿进食含有舒芬太尼残存的乳汁有否不良影响,目前长期大量的跟踪数据不完善。
婴儿在母体内时,此时是舒芬太尼进入脐带血后可产生累积效应,加上胎儿代谢慢等原因[9]。因此出生后脐带血有极少数量的药物浓度;虽然王宗杰等[10]的研究显示胎儿出生后临床观察评分和血液肝功能、肾功能、血常规等检查结果无异常,但是即使少量的药物残存对新生儿长期或未经发现的可能影响还不明确,减少或不使新生儿体内、母体初乳中有药物残存是最好的药物剂量。
注射舒芬太尼后血药浓度下降很快,在血浆和组织之间快速到达平衡。在给药后1h血药浓度仅为0.52ng/mL,有96.8%的舒芬太尼离开血浆[11-12],孕妇首次鞘内注入舒芬太尼后1h血药浓度最高,而注药后5h血药浓度降至最低值[13]。
硬膜外分娩镇痛后多在1~4h分娩,在本研究中首量3 μg舒芬太尼的3个泵浓度无明显差异,检测药物残存基本无,对新生儿安全性高,适于临床应用。
采用HPLC测定硬膜外分娩镇中舒芬太尼血浆浓度可行,可以指导临床安全用药剂量,减少药物残存可能带来的,或可能未知的不良后果,具有很好的临床应用价值。
[1]Gautier P,De Kock M,Van Steenberge,et al.A dubleblind comparison of 0.125%ropivacaine with sufentanil for epidural analgesia[J].Anesthesiology,1999,90:772-778.
[2]Knudsen K,Beckman Suurküla M,Blomberg S,et al.Central nervous and cardiovascular effects of i.v.infusions of ropivacaine,bupivacaine and placebo in volunteers[J].Br J Anaesth,1997,78(5):507-514.
[3]徐建国,沈晓凤,唐跃,等.不同浓度舒芬太尼或芬太尼对硬膜外罗哌卡因分娩镇痛效应的影响[J].中华麻醉学杂志,2007,27(7):599-602.
[4]刘继云,李荣胜,吴为玲,等.舒芬太尼用于分娩镇痛的临床研究[J].中华妇产科杂志,2004,39(10):56-57.
[5]Menigaux C,Guignard B,Fletcher D,et al.More epidural than intravenous sufentanil is required to provide comparable postoperative pain relief[J].Anesth Analg,2001,93(2):472-476.
[6]徐凯智,李宇虹,岳静玲,等.国产芬太尼在骨科手术患者的药代动力学研究[J].华北煤炭医学院学报,2005,11(6):698-700.
[7]Boer F,Olofsen E,Bovill JG,et al.Pulmonary uptake of sufentanil during and after constant rate infusion[J].Br J Anaesth,1996,76(2):203-208.
[8]Boer F,Engbers FH,Bovill JG,et al.First-pass pulmonary retention of sufentanil at three different background blood concentrations of the opioid[J].Br J Anaesth,1995,74(1):50-55.
[9]Rassi S,Kyck JB,Yaksh IL.simultatumas acham of sufentail andmidawlamfrom human plam[J].Clin Chim,1996,244(1):103-105.
[10]王宗杰,黄卫彤,廖旺.酶联免疫吸附法检测血清舒芬太尼血药浓度的应用价值[J].检验医学与临床,2013,10(16):2100-2101.
[11]Bovil JG,Sebel PS,Blackburn CL,et al.The pharmaco-kinetics of sufentanil in surgical patients[J].Anesthesology,1984,61(5):502-506.
[12]徐凯智,靳彦涛,李宇虹,等.国产舒芬太尼在心内直视手术患者的药代动力学研究[J].中国循环杂志,2010,5(5):375-378.
[13]劳诚毅,黎君君,周朝明,等.分娩镇痛鞘内注射舒芬太尼最佳剂量的临床研究[J].广西医学,2012,9(9):1126-1129.

