人胎胃成纤维细胞hTERT和端粒酶的表达*
程永波,郭丽萍,王 磊,房殿春△
(1.新疆医科大学第一附属医院消化内科,乌鲁木齐830054;2.第三军医大学西南医院消化内科,重庆400038)
一般认为,人端粒酶逆转录酶(human telomerase reverse transcriptase,hTERT)和端粒酶多表达于绝大部分癌细胞和少数正常高增殖细胞如造血干细胞、基底表皮细胞等,正常成熟细胞尤其是成纤维细胞检测不到hTERT和端粒酶活性[1-3]。但近年来一些研究证实hTERT和端粒酶在成人成纤维细胞中有表达[2-4],以往的研究也证实了hTERT和端粒酶可以在成人胃成纤维细胞中表达[5]。在本项实验中,作者初步检测了hTERT和端粒酶在人胎胃成纤维细胞的表达,以期弥补有关研究的不足。
1 材料与方法
1.1 材料 胶原酶Ⅱ(Sigma),分散酶(Roche);Ham F12培养液和胎牛血清(GIBCO),培养皿(Corning);端粒酶检测试剂盒(北京鼎国),hTERT兔抗人一抗、TRITC标记羊抗兔二抗
(中杉金桥),CK-18小鼠抗体和FITC标记羊抗小鼠IgG(武汉博士德生物工程有限公司);DAPI(Vector Laboratories)。
1.2 细胞培养 经过学校、医院伦理委员会和人流者同意,由引产死胎取胎胃,3个月胎龄。采用磁性搅拌酶分离法分离细胞[6],接种于塑料培养皿中,常规培养。CK-18免疫细胞化学染色排除上皮细胞。
1.3 hTERT免疫细胞化学观察 细胞固定、透膜处理后一抗4℃孵育13h,FITC标记二抗常温避光孵育40min,DAPI核染色后封片,Leica TCS SP5激光扫描共聚焦显微镜观察。以PBS代替一抗作为阴性对照。
1.4 端粒酶活性检测 采用端粒重复序列扩增法(TRAP)。上游引物:5′-ATT CCG TCG AGC AGA GTT-3′,下游引物:5′-CCC TTA CCC TTA CCC TAA-3′(FITC标记)。步骤:细胞消化后离心,提取蛋白;取蛋白上清、上游引物与PCR反应液20℃温育40min,90℃3min灭活端粒酶。加入下游引物和Taq酶进行PCR扩增,PCR反应条件为94℃2min;94℃30s,55℃30s,72℃1min,35个循环;72℃5min。聚丙烯酰胺凝胶电泳3h。以热处理后的蛋白上清作为阴性对照,已证明有端粒酶活性的成人胃成纤维细胞(实验室有冻存)作阳性对照,同时对二者的端粒酶活性作比较。ABIPrism 377测序仪分析胶图。
2 结 果
2.1 细胞培养 细胞分离后,培养到第9天可见成片成纤维细胞,CK-18免疫染色阴性,见图1。
2.2 hTERT表达 原位监测胎胃成纤维细胞hTERT表达呈阳性,胞质和胞核中均可见细颗粒状FITC红色荧光,阴性对照胞质和胞核中都未见荧光,见图2。
2.3 端粒酶活性 胎胃成纤维细胞可观察到端粒酶延伸的端粒片断,长度约为170bp,略高于与阳性对照组成人胃成纤维细胞(160bp),阴性对照未见延伸的端粒片断,见图3。

图1 人胎胃成纤维细胞形态和CK-18免疫染色(×100)
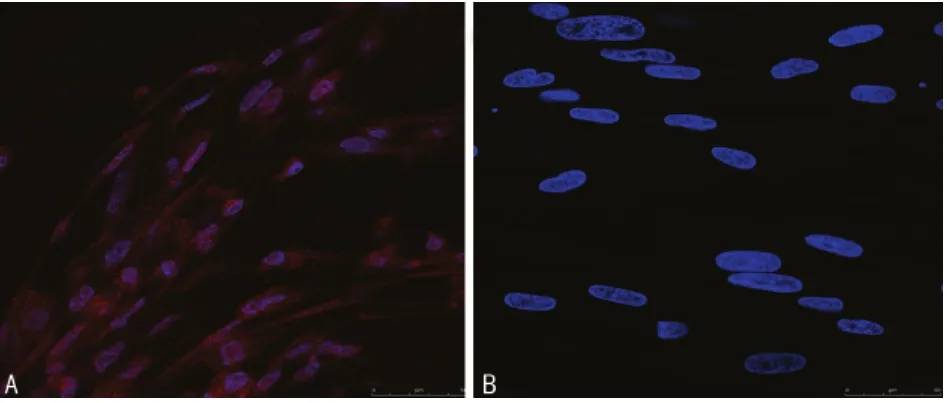
图2 人胎胃成纤维细胞hTERT表达

图3 人胎胃成纤维细胞端粒酶活性
3 讨 论
端粒酶可以通过延伸端粒长度使细胞避免老化和死亡,因此其多与细胞增殖有关。95%以上的癌细胞不同程度地表达端粒酶[7],正常体细胞中少数增生能力强的如滋养层细胞、造血干细胞、子宫内膜细胞等也可检测到端粒酶活性。端粒酶的组分之一hTERT表达是端粒酶活性的限速步骤,其表达水平和端粒酶的活性高低基本平行[8-10]。成纤维细胞是一种多形性细胞,是机体组织的主要修复细胞。在静息状态下其增生较弱或不增生,被称为纤维细胞,但在组织损伤修复过程中则表现出多种功能活性,增殖便是其中之一[11]。在这一阶段,检测到hTERT和端粒酶表达是和上述理论相符合的。成纤维细胞的离体培养,实际上也是一个不断分裂增殖的过程,理论上也应该有hTERT和端粒酶表达,不管是成人还是胎儿的,都应如此,这在既往[5]和现在的研究中也得到了证实。在实际操作中,从光镜下形态学和hTERT细胞免疫结果看胎胃和成人胃成纤维细胞分裂增殖能力无明显差别,但从端粒酶的延伸片断长度看,前者要略长于后者,说明前者的增生能力要强于后者,这也符合常理。
成纤维细胞在组织创伤、炎症后的修复过程中发挥重要作用,但在修复过程中,若成纤维细胞过度增殖则会引起一些病理性变化如皮肤瘢痕、类风湿性关节炎特征性血管翳等;其他如肺纤维化、肝硬化、心瓣膜病等都与成纤维细胞增殖有关[11]。以往和现在的研究采用成人和胎胃成纤维细胞为工具,证实它们都表达hTERT和端粒酶,这为成纤维细胞合理修复的进一步研究打下基础;另外,也为除细胞因子外,从hTERT和端粒酶为切入点预防成纤维细胞修复过程中的弊端提供了一种新的思路。
[1] Masutomi K,Yu EY,Khurts S,et al.Telomerase maintains telomere structure in normal human cells[J].Cell,2003,114(3):241-253.
[2] Ge Z,Liu C,Bjrkholm M,et al.Mitogen-activated protein kinase cascade-mediated histone H3phosphorylation is critical for telomerase reverse transcriptase expression/telomerase activation induced by proliferation[J].Mol Cell Biol,2006,26(3):230-237.
[3] Nakayama J,Tahara H,Tahara E,et al.Telomerase activation by hTRT in human normal fibroblasts and hepatocellular carcinomas[J].Nat Genet,1998,18(370):65-68.
[4] Philippi C,Loretz B,Schaefer UF,et al.Telomerase as an emerging target to fight cancer--opportunities and challenges for nanomedicine[J].J Control Release,2010,146(3):228-240.
[5] Cheng YB,Guo LP,Yao P,et al.Telomerase and hTERT:Can they serve as markers for gastric cancer diagnosis[J]World J Gastroenterol,2014,20(40):6615-6619.
[6] 程永波,房殿春,郭立萍,等.一种简便的人正常胃黏膜上皮细胞原代培养方法[J].胃肠病学,2007,12(1):31-35.
[7] Sabah M,Path M,Cummins R,et al.Immunohistochemical detection of hTERT protein in soft tissue sarcomas correlation with tumor grade[J].Appl Immun,2006,14(2):198-202.
[8] Horilawal I,Barrett JC.Transcriptional regulation of the telomerase hTERT gene as a target for cellular and Viral oncogenic mechanisms[J].Carcinogenesis,2003,24(20):1167-1176.
[9] Guilleret I,Benhattar J.Demethylation of the human telomerase catalytic subunit(hTERT)gene proII]Ioter reduced hTERT expression and telomerase actiVity and shortened telomeres[J].Exp Cell Res,2003,289(4):326-334.
[10]Braunstein I,Cohen-Barak O,Shachaf C,et al.Human telomerase reVerse transcriptase pronloter regulation in nomal and malignant human ovarian epithelial ceUs[J].Cancer Res,2001,61(60):5529-5536.
[11]李忠廉,崔乃强.成纤维细胞的双重特性[J].中国中西医结合外科杂志,2008,14(2):176-179.

