感悟“定性到定量”的立体探究式复习
任婷婷
(连云港市新海实验中学教育集团凤凰校区 江苏 连云港 222000)
《义务教育化学课程标准》指出:义务教育阶段的科学探究,是学生积极主动地获取化学知识、认识和解决化学问题的重要实践活动。它既是一种重要的学习方式,也是义务教育阶段化学课程的目标和重要内容,对发展学生的科学素养具有不可替代的作用。
一、“定性到定量”立体探究式复习的提出
在实际教学中,科学探究主要运用在新授课和习题中,在复习课中还没有被广泛地采用。运用探究式的复习模式,需要集中教师的智慧,进行精心的教学设计和准备,需要的精力和时间比较长,这也是探究式复习没有被广泛运用的原因之一。但是如果能结合具体教学认真思考,探究式复习往往在化学复习课中起到事半功倍的效果。从人教版九年级化学第三单元学习“构成物质的奥秘”开始,就在化学学习中融入了定量计算, 所以化学中的探究往往和计算密不可分,通过计算,可以加深对知识的理解。下面我以“探秘暖宝宝”为例,谈谈对“定性到定量”的立体探究式复习的认识。
二、同一探究主题在不同复习课中的运用
1.探究复习在章节复习中的运用
“探秘暖宝宝”这一个题目,变换探究方式,可以运用到不同的复习课中。在复习第八单元“金属和金属材料”第3 节的时候,我首先运用了这个探究主题。
第八单元第3 节是“金属资源的利用和保护”。这节常规的复习方法是按顺序做习题再归纳知识点,但我在运用探究式复习后变换了下复习的顺序,设计如下:
【查阅资料】每到冬天,市面上便有“暖宝宝”出售,它是一个装有化学药品的小袋。使用时,撕去它的保护膜贴在身体上,不久便会产生热量。已知小袋中装有铁粉、碳粉和少量氯化钠。
思考:1.暖宝宝的发热原理2.氯化钠的作用3.如何保存暖宝宝。
通过这一个小小的问题,让学生回顾铁生锈的条件和如何防止铁生锈的方法,再让学生完成“探究铜生成铜绿的条件”的习题,对金属生锈和防护的知识点加以巩固,共用10-15 分钟时间完成第3 节重点内容的复习。
接着给出信息:暖宝宝发热后生成Fe2O3,某化学兴趣小组对一包使用过的暖宝宝粉末进行探究,其中氯化钠和碳粉已除去。
【提出问题】 使用过的暖宝宝粉末组成情况有几种?
【实验探究】(1)由于无法分辨粉末颜色,如何判断使用过的暖宝宝组成情况? 写出两种判断的方法。
此问关键是铁有没有被完全氧化,也就是还有没有铁剩余。学生很快知道实际就是验证是否存在铁,可以利用铁的物理和化学性质进行判断。这样又通过问题对铁的部分性质进行了复习。
(2)为进一步探究暖宝宝的组成情况,小组成员称取21.6g 该粉末装入硬质玻璃管中, 按右图在通风橱中进行实验。开始时缓缓通入CO 气体,待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:


反应前 反应后Ⅰ组 玻璃管和红色粉末的总质量为66.9g玻璃管和固体物质的总质量为62.1g
从提问(2)开始,已经慢慢把复习从定性转变为定量。
【交流讨论】
1.在装置A 中先通CO 气体的作用,停止加热后继续通CO 气体的作用。
2.写出A 装置中发生反应的化学方程式,实验过程中观察到B 装置中的现象。
3.请根据表中数据计算出粉末组成和各成分的质量。
通过以上3 个问题, 首先复习实验室CO 还原Fe2O3的相关知识点,然后根据表格所给数据,从定量的角度进一步分析该粉末的组成。为了考虑课堂容量和学生的实际水平, 我对此处探究的内容进行了删减, 原来的探究比现在的探究要更延伸:1.在表格中给出两组数据,还有一组是“反应前洗气瓶和石灰水的总质量和反应后洗气瓶和石灰水的总质量”, 通过比较两组数据得出用哪种数据计算粉末成分更为准确并分析原因。2.还有一处改动在第(3)小题,我去掉了“计算铁的氧化程度”这个问题,让计算难度减小,也更符合学生的真实水平。
【反思评价】丁同学指出,从环保角度,上图装置有严重不足之处,你认为该如何改进?
通过反思评价,让学生复习了该实验中重要的尾气处理。
过渡信息:暖宝宝中的铁粉来源工业,主要是炼钢后所得,炼钢的主要原料是生铁。
思考:
1.请写出生铁炼钢关键一步的化学方程式。
如图是炼铁高炉及炉内化学变化示意图,请回答下列问题。
(1)高炉炼铁原料有哪些?
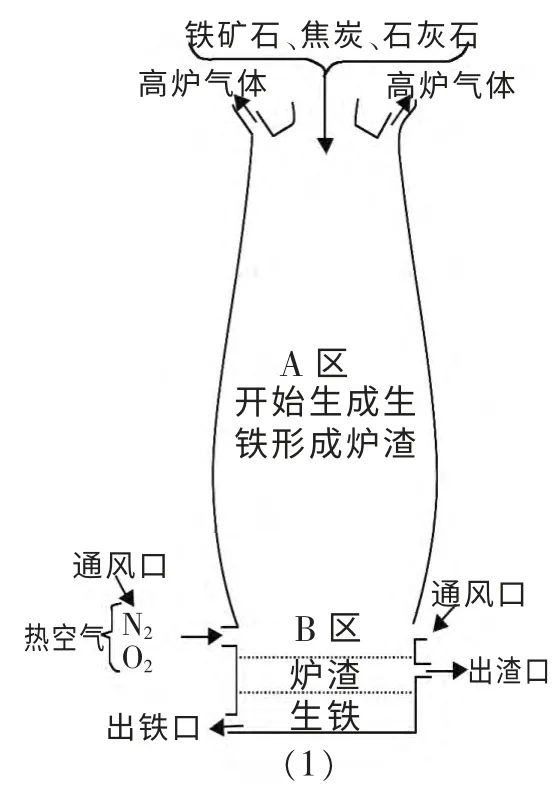
(2) 下列铁矿石主要成份表达错误的是
A.磁铁矿(Fe3O4)
B.赤铁矿(Fe2O3)
C.黄铁矿(FeS)
D.菱铁矿(FeCO3)
(3)请写出产生CO的化学方程式。
(4) 要炼出含杂质2%的生铁3200 吨,需要含氧化铁质量分数为80%的赤铁矿石多少吨?
通过这样一个过渡,巧妙的进行工业炼铁的相关复习,通过整个这样一个探究,就把第3 节“金属资源的利用和保护”复习完了,共用25-30 分钟。由于在复习过程中穿插了大量习题,可以将剩余习题在课后完成。
2.探究复习在总复习中的运用
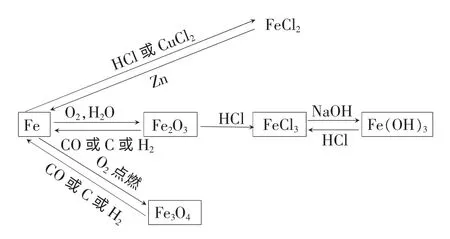
“探秘暖宝宝” 这一探究主题还可以用在中考总复习中。告诉学生暖宝宝由铁粉、活性炭和氯化钠组成,打开后发现灰黑色的固体中还夹杂着少量的红棕色粉末,提出问题:这些固体的成分可能是什么? 怎样验证这些固体成分? 通过这两个问题,引出探究一:怎么证明暖宝宝中还有铁粉? 归纳Fe 和Fe2O3的性质,得出铁及其化合物间的转化。
探究二:暖宝宝的工作原理
思考:1.暖宝宝的发热原理2.氯化钠的作用3.活性炭的作用4.如何保存暖宝宝。
通过探究二,复习了铁的生锈和铁的防护。
探究三:暖宝宝中各成分含量的测定,从而把探究从定性转向定量。让学生思考,如何利用现有的仪器和试剂,设计实验方案,测定暖宝宝中各成分质量分数(提醒:灰黑色固体中还夹杂少量红棕色粉末)。现有仪器:电子天平、烧杯、小试管、洗气瓶、锥形瓶、分液漏斗、量筒、玻璃棒、漏斗、铁架台、药匙、试管架、废液缸,现有药品:滤渣、蒸馏水、盐酸、暖宝宝。
学生思考出可能成分为:铁粉、活性炭、氯化钠、氧化铁, 进一步提出成分测定顺序: 氯化钠→活性炭→铁→氧化铁。教师进一步给出实验步骤。
实验步骤1:称取10.00g 样品于一烧杯中,加足量水充分搅拌溶解后, 过滤,将滤渣洗涤、干燥、称得其质量为7.28g。步骤2:如右图,将得到的7.28g 固体与足量稀盐酸反应,用电子秤称得反应前后总质量差为0.15g。

步骤3:将锥形瓶中反应后的液体过滤,并将滤渣洗涤、干燥后,称得其质量为1.20g。
质疑与反思:(1) 按照步骤2 测得氢气质量往往会有偏差,为什么? (2)实验装置和药品可怎样改进?得出改进后步骤2 中称得质量差为0.14g, 从而计算各成分含量。
通过这种实验探究,让学生复习了相关的实验操作,同时运用所学知识定量解决实际问题,让学生在探究中获得知识的复习, 比单一的讲解更为生动形象。
以上只是“从定性到定量”立体探究式复习的一个案例, 更多的方案需要我们不断地积累并付诸实践。这种探究式复习可以让知识结构更系统化、网络化,所以可以推广和使用。只是在使用过程中,我们需要把握住主线和核心,不能滥用散用,这样不但让课堂显得冗繁,也让探究式复习失去了本有的效果。
[1]中华人民共和国教育部.义务教育化学课程标准(2011版)[S].北京:北京师范大学出版社,2012

