大剂量应用维生素C治疗相关疾病安全性的系统评价
许 婧,刘京铭,付 雷,王 彬,赵伟杰,王慧琳,高孟秋(北京市结核病胸部肿瘤研究所/首都医科大学附属北京胸科医院,北京 101149)
维生素C是人类常见的必需营养素之一,又名抗坏血酸(Ascorbic acid,AA)。临床中维生素C不仅用于预防或治疗坏血病,同时在补充与替代医疗领域(CAM)也有广泛应用,如肿瘤、感染性疾病、免疫性疾病及一些病因不明的疾病[1-3]。美国医学研究院公布数据表明,维生素C无可见的有害作用水平(No-observed-adverse-effect level,NOAEL)为每日摄入不超过2 g,出现副作用的最小剂量(Lowest-observed-adverse-effect level,LOAEL)为每日3 g,而过量使用维生素C可发生恶心、腹泻、高尿酸血症、尿道结石、溶血、皮疹、过敏等不良反应[4-6]。然而,由于实际临床治疗的需要,大剂量(>2 g/d)维生素C在临床治疗中已经应用于多种疾病,而目前这种治疗的安全性尚缺乏循证医学的论证。因此,本研究系统评价了应用大剂量维生素C治疗相关疾病的安全性,以为临床应用提供循证参考。
1 资料与方法
1.1 检索策略
计算机检索Medline、EMBase、Cochrane图书馆、中文科技期刊数据库、中国期刊全文数据库(CNKI)和万方数据库。英文检索式:(“Ascorbic acid”or“Vitamin C”)and(“Safety”or“Adverse effect”);中文检索式:(“维生素C”or“抗坏血酸”)and(“安全性”or“不良反应”)。检索时限为各数据库建库起至2014年8月26日。
1.2 纳入与排除标准
1.2.1 研究类型 检索国内外公开发表的应用大剂量维生素C治疗相关疾病的随机对照试验(RCT)、前瞻性研究、回顾性研究等。语种限定为中文和英文。
1.2.2 研究对象 纳入研究中包含的全部患者,年龄、性别不限,基础疾病不限。
1.2.3 干预措施 有对照组的研究中,对照组患者给予对症常规治疗,试验组患者在此基础上加用维生素C;无对照组的研究中,试验组治疗方案中均含有维生素C,给药方式为静脉注射或口服,用药剂量>2 g/d[4]。
1.2.4 结局指标 ①总体不良反应发生率;②腹痛发生率;③口干发生率;④头痛发生率;⑤恶心发生率;⑥腹泻发生率;⑦其他不良反应发生率。
1.2.5 排除标准 排除体外实验、动物实验、个案报道、信件、综述、观点性研究;未明确描述安全性或不良反应的研究;受其他药物影响或疾病影响无法判断安全性或不良反应归属的研究。
1.3 资料提取
由两位研究者独立检索各数据库,筛选文献,若发生分歧则讨论解决或交第三方协助解决。按事先设计的信息提取表提取以下信息:研究类型、样本量、适应证、组别、不良反应症状与例数、药物剂量疗程等。
1.4 纳入研究质量评价
1.4.1 RCT评价标准 按照Cochrane系统评价员手册5.0.1版对文献质量进行评分:①随机方法是否正确;②是否实施分配隐藏;③是否采用盲法;④有无失访或退出(如有失访或退出,是否采用意向性分析);⑤基线是否一致。评分结果分为A、B、C级。A级为所有质量标准均满足者,为高质量研究;B级为任意一条质量评价标准仅部分满足或不清楚者,为中等质量研究;C级为任意一条未满足者,为低质量研究[6]。
1.4.2 非RCT评价标准 采用MINORS条目对文献质量进行评价,包括:A.是否明确给出研究目的;B.纳入患者的连贯性;C.预期数据的收集;D.终点指标能否恰当反映研究目的;E.终点指标评价的客观性;F.随访时间是否充足;G.失访率低于5%;H.是否估算了样本量;I.对照组的选择是否恰当;J.对照组是否同步;K.组间基线是否可比;L.统计分析是否恰当。每个分项为0~2分,0分表示未报道;1分表示报道了但信息不充分;2分表示报道了而且信息充分[7]。A~H项针对无对照组的研究,总分最高16分;A~L项针对有对照组的研究,总分最高24分。
1.5 统计学方法
使用R语言3.1.1版的Meta软件包对提取数据进行合并分析。根据P值和I2评价纳入研究有无异质性。当各研究间存在异质性时(P<0.1,I2>50%),采用随机效应模型分析;反之,则采用固定效应模型分析。计数资料采用相对危险度(RR)及95%可信区间(CI)为分析统计量。P<0.05为差异有统计学意义。
2 结果
2.1 资料筛选结果
最初检索到1 557篇文献,排除重复文献155篇,阅读标题、摘要排除文献1 254篇,剩余148篇文献。根据文献纳入与排除标准进行筛选,最终纳入23篇(项)研究,合计2 069例患者。
2.2 纳入研究基本信息与质量评价结果
23项研究中包含9项RCT、14项非RCT[8-30]。纳入研究基本信息与质量评价结果详见表1。
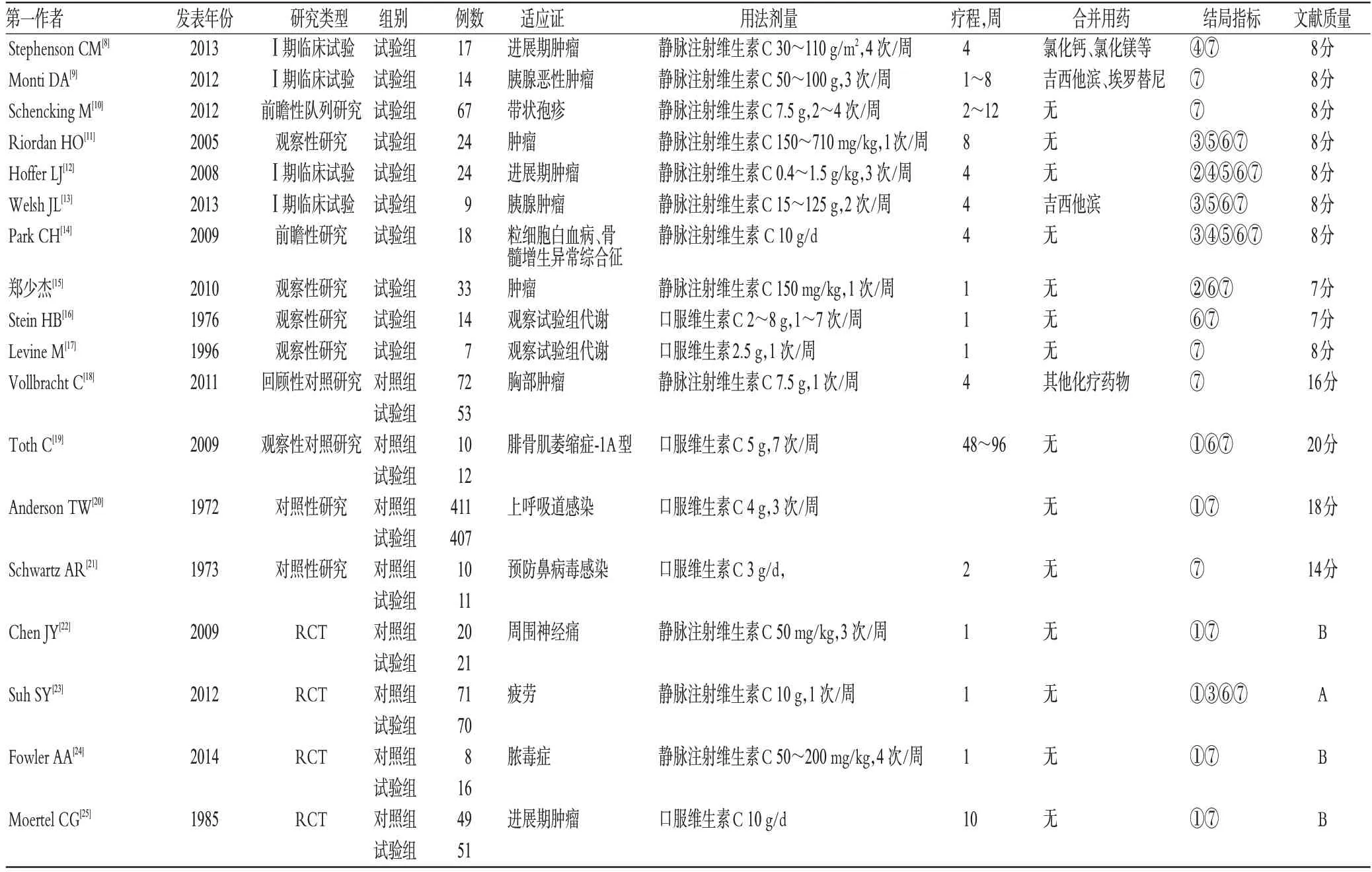
表1 纳入研究基本信息与质量评价结果Tab 1 Basic information of included studies and results of quality evaluation

续表1Continued tab 1
2.3 不良反应发生情况
本研究共纳入受试者2 069例,发生不良反应540例。其中躯体感觉症状274例,包括恶心(60例)、胃灼热(43例)、口干(28例)、注射部位感觉异常(11例)、疲倦(9例)等;临床发病例数225例,包括腹泻(61例)、水肿(45例)、呕吐(31例)、睡眠障碍(9例)、皮疹(3例)等;实验室诊断例数20例,包括低钾血症(6例)、高钠血症(3例)、贫血(2例)等。纳入研究均未发现严重不良反应。本文对发生率较高的5种不良反应(腹痛、口干、头痛、恶心、腹泻)进行Meta分析。
2.4 Meta分析结果
2.4.1 总体不良反应发生率 8项研究报道了总体不良反应发生率[19-20,22-25,28-29],各研究间有异质性(P=0.010,I2=61.9%),采用随机效应模型分析,Meta分析结果见图1。由图1可见,试验组患者总体不良反应发生率与对照组比较,差异无统计学意义[RR=1.42,95%CI(0.92,2.20),P=0.382]。
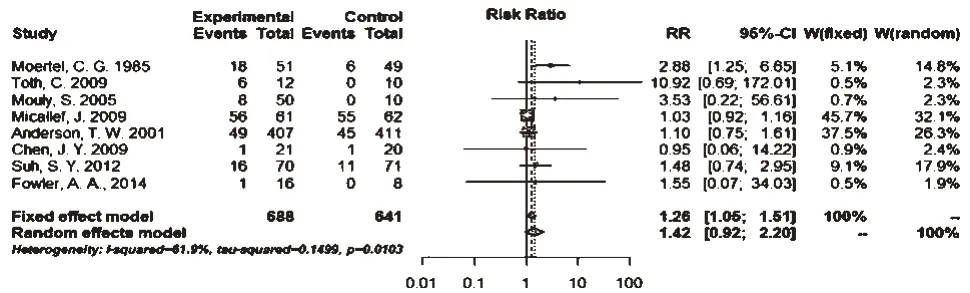
图1 两组患者总体不良反应发生率的Meta分析森林图Fig 1 Forest plots of Meta-analysis of incidence of adverse reactions in 2 groups
2.4.2 各项不良反应发生率 本研究对腹痛、口干、头痛、恶心、腹泻的发生情况进行了Meta分析,结果见表2。
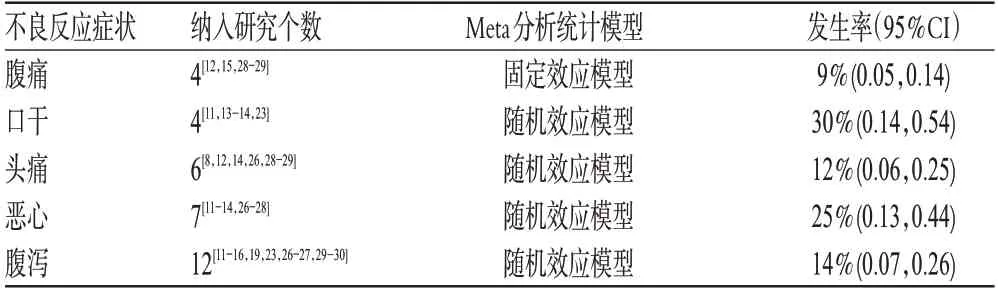
表2 各项不良反应发生率的Meta分析结果Tab 2 Results of Meta-analysis of ADR rate
2.5 发表偏倚分析
通过Egger检验进行发表偏倚分析,结果总体不良反应发生率、头痛发生率、腹痛发生率存在发表偏倚(P<0.1);恶心发生率、腹泻发生率、口干发生率不存在发表偏倚(P>0.1)。
2.6 敏感性分析
剔除漏斗图中一个异常点改变效应模型来评价结果的稳定性。结果发现,腹痛、恶心、腹泻的结论较为稳定,其他几项指标的结论稳定性有待加强,详见表3。
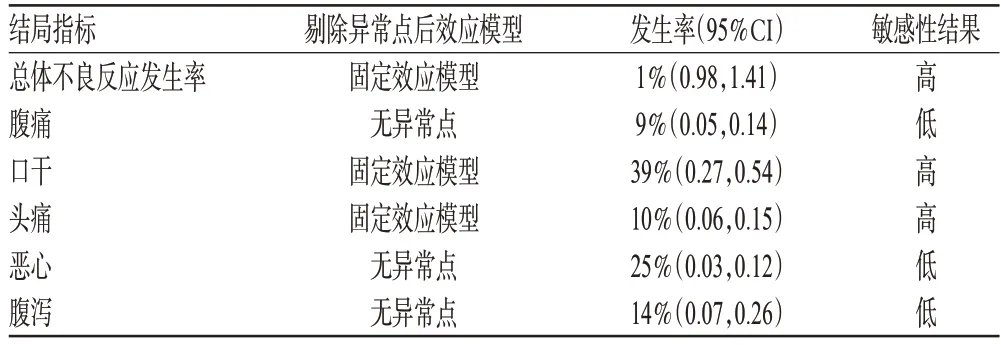
表3 敏感性分析结果Tab 3 Sensitivity analysis of outcomes
3 讨论
曾有葡萄糖-6-磷酸脱氢酶(Glucose-6-phosphate dehydrogenase,G6PD)缺乏患者大剂量应用维生素C后发生急性溶血[31-35],肾功能异常患者大剂量应用维生素C后出现草酸盐肾病(高草酸尿症导致的泌尿系草酸盐结石、肾脏钙化、肾功能衰竭等的代谢性肾病)的报道[34-36]。但本次系统评价纳入研究中,仅1例患者出现肾结石,其他患者并未出现急性溶血、草酸盐肾病等严重不良反应。
目前,全球范围内尤其在CAM领域(如晚期恶性肿瘤、危重症治疗等),大剂量应用维生素C已非常广泛。在对患者潜在危险因素(如G6PD酶缺乏、肾功能异常、存在泌尿系统疾病病史等)进行筛查并排除后,大剂量应用维生素C产生的不良反应发生率较低,且多为轻度,但应注意其与其他药物联合应用的不良反应。另外,在非常规药物(中药、保健品)治疗被广泛应用的大背景下,维生素C与非常规药物联合应用后的不良反应亦值得关注。曾有个案报道,同时口服大剂量维生素C与苦杏仁苷的患者发生了严重的氰化物中毒反应[37]。因此,在今后的临床应用中,研究者除重视受试者的临床常规用药外,更应关注潜在的药物相互作用。
本次Meta分析结果显示,试验组患者总体不良反应发生率与对照组比较,差异无统计学意义。说明大剂量应用维生素C不会增加不良反应风险。笔者对其中发生人数、研究分布相对较多的5种不良反应进行合并分析,统计了各类不良反应的发生概率。结果发现,发生率最高的不良反应为口干,这可能与高浓度维生素C的高渗状态相关;分布最广泛的症状为腹泻,其发生率为14%。结果提示,大剂量应用维生素C于人类疾病治疗是相对安全的。
本研究的局限性包括:纳入研究适应证广泛,较难进行各亚组的Meta分析;个别研究可能存在规避不良反应发生的报道,故可能存在一定程度的发表偏倚;此外,本研究仅检索中文、英文研究,无其他语种,可能造成语言或分布偏倚。
综上所述,大剂量应用维生素C治疗相关疾病的安全性较好。但由于缺乏大样本RCT资料,且随访时间较短,故对其综合评价仍受到限制,需要开展更多的RCT予以确证。
[1]Gonzalez MJ,Miranda-Massari JR,Mora EM,et al.Orthomolecular oncology review:ascorbic acid and cancer 25 years later[J].Integr Cancer Ther,2005,4(1):32.
[2]Riordan N,Riordan H,Casciari JJ.Clinical and experimental experiences with intravenous vitamin C[J].J Orthomolecular Med,2000,15(201):3.
[3]Heimer KA,Hart AM,Martin LG,et al.Examining the evidence for the use of vitamin C in the prophylaxis and treatment of the common cold[J].J Am Acad Nurse Pra-ct,2009,21(5):295.
[4]Norman I.Dietary reference intakes for vitamin C,vitam-in E,selenium,and carotenoids[M].Washington DC:National Academies Press,2000:162.
[5]Verhamme C,de Haan RJ,Vermeulen M,et al.Oral hig-h dose ascorbic acid treatment for one year in young CMT1A patients:a randomised,double-blind,placebo-controlled phase Ⅱtrial[J].BMC Med,2009,doi:10.1186/1741-7015-7-70.
[6]Julian H,Sally G,Acquadro C,et al.Cochrane handbo-ok for systematic reviews of interventions version 5.1.0.[EB/OL].(2011-03)[2014-07].http://www.cochrane-h-andbook.org.
[7]Slim K,Nini E,Forestier D,et al.Methodological index for non-randomized studies(minors):development and validation of a new instrument[J].ANZ J Surg,2003,73(9):712.
[8]Stephenson CM,Levin RD,Spector T,et al.PhaseⅠcl-inical trial to evaluate the safety,tolerability,and pharmacokinetics of high-dose intravenous ascorbic acid in patients with advanced cancer[J].Cancer Chemother Pharmacol,2013,72(1):139.
[9]Monti DA,Mitchell E,Bazzan AJ,et al.PhaseⅠevaluation of intravenous ascorbic acid in combination with gemcitabine and erlotinib in patients with metastatic pancreatic cancer[J].PLoS One,2012,7(1):e29794.
[10]Schencking M,Vollbracht C,Weiss G,et al.Intravenous vitamin C in the treatment of shingles:results of a multicenter prospective cohort study[J].Med Sci Monit,2012,18(4):Cr215.
[11]Riordan HD,Casciari JJ,Gonzalez MJ,et al.A pilot clinical study of continuous intravenous ascorbate in terminal cancer patients[J].P R Health Sci J,2005,24(4):269.
[12]Hoffer LJ,Levine M,Assouline S,et al.PhaseⅠclinical trial of i.v.ascorbic acid in advanced malignancy[J].Ann Oncol,2008,19(11):1 969.
[13]Welsh JL,Wagner BA,van’t Erve TJ,et al.Pharmacological ascorbate with gemcitabine for the control of metastatic and node-positive pancreatic cancer(PACMAN):results from a phaseⅠclinical trial[J].Cancer Chemother Pharmacol,2013,71(3):765.
[14]Park CH,Kimler BF,Yi SY,et al.Depletion of L-ascorbic acid alternating with its supplementation in the treatment of patients with acute myeloid leukemia or myelodysplastic syndromes[J].Eur J Haematol,2009,83(2):108.
[15]郑少杰.33例大剂量维生素C静滴治疗晚期肿瘤的不良反应分析[J].河北医学,2010,16(8):984.
[16]Stein HB,Hasan A,Fox IH.Ascorbic acid-induced uricosuria.A consequency of megavitamin therapy[J].Ann Intern Med,1976,84(4):385.
[17]Levine M,Conry-Cantilena C,Wang Y,et al.Vitamin C pharmacokinetics in healthy volunteers:evidence for a recommended dietary allowance[J].Proc Natl Acad Sci U S A,1996,93(8):3 704.
[18]Vollbracht C,Schneider B,Leendert V,et al.Intravenous vitamin C administration improves quality of life in breast cancer patients during chemo-/radiotherapy and aftercare:results of a retrospective,multicentre,epidemiological cohort study in Germany[J].In Vivo,2011,25(6):983.
[19]Toth C.Poor tolerability of high dose ascorbic acid in a population of genetically confirmed adult Charcot-Marie-Tooth 1A patients[J].Acta Neurol Scand,2009,120(2):134.
[20]Anderson TW,Reid DB,Beaton GH.Vitamin C and the common cold:a double-blind trial[J].Can Med Assoc J,1972,107(6):503.
[21]Schwartz AR,Togo Y,Hornick RB,et al.Evaluation of the efficacy of ascorbic acid in prophylaxis of induced rhinovirus 44 infection in man[J].J Infect Dis,1973,128(4):500.
[22]Chen JY,Chang CY,Feng PH,et al.Plasma vitamin C is lower in postherpetic neuralgia patients and administration of vitamin C reduces spontaneous pain but not brush-evoked pain[J].Clin J Pain,2009,25(7):562.
[23]Suh SY,Bae WK,Ahn HY,et al.Intravenous vitamin C administration reduces fatigue in office workers:a double-blind randomized controlled trial[J].Nutr J,2012,doi:10.1186/1475-2891-11-7.
[24]Fowler AA,Syed AA,Knowlson S,et al.PhaseⅠsafety trial of intravenous ascorbic acid in patients with severe sepsis[J].J Transl Med,2014,doi:10.1186/1479-5876-12-32.
[25]Moertel CG,Fleming TR,Creagan ET,et al.High-dose vitamin C versus placebo in the treatment of patients with advanced cancer who have had no prior chemotherapy:a randomized double-blind comparison[J].N Engl J Med,1985,312(3):137.
[26]Lewis RA,McDermott MP,Herrmann DN,et al.Highdosage ascorbic acid treatment in Charcot-Marie-Tooth disease type:results of a randomized,double-mas-ked,controlled trial[J].JAMA Neurol,2013,70(8):981.
[27]Creagan ET,Moertel CG,O’Fallon JR,et al.Failure of high-dose vitamin C(ascorbic acid)therapy to benefit patients with advanced cancer:a controlled trial[J].N Engl J Med,1979,301(13):687.
[28]Mouly S,Mahe I,Knellwolf AL,et al.Effects of the addition of high-dose vitamin C to polyethylene glycol solution for colonic cleansing:a pilot study in healthy volunteers[J].Curr Ther Res Clin Exp,2005,66(6):486.
[29]Micallef J,Attarian S,Dubourg O,et al.Effect of ascorbic acid in patients with Charcot-Marie-Tooth disease type1A:a multicentre,randomised,double-blind,placebo-controlled trial[J].Lancet Neurol,2009,8(12):1 103.
[30]Brody S,Preut R,Schommer K,et al.A randomized controlled trial of high dose ascorbic acid for reduction of blood pressure,cortisol,and subjective responses to psychological stress[J].Psychopharmacology,2002,159(3):319.
[31]Campbell GD,Steinberg MH,Bower JD.Letter:ascorbic acid-induced hemolysis in G-6-PD deficiency[J].Ann Intern Med,1975,82(6):810.
[32]Rees DC,Kelsey H,Richards JD.Acute haemolysis induced by high dose ascorbic acid in glucose-6-phosphate dehydrogenase deficiency[J].BMJ,1993,306(6 881):841.
[33]Mehta JB,Singhal SB,Mehta BC.Ascorbic-acid-induced haemolysis in G-6-PD deficiency[J].Lancet,1990,336(8 720):944.
[34]Lawton JM,Conway LT,Crosson JT,et al.Acute oxalate nephropathy after massive ascorbic acid administration[J].Arch Intern Med,1985,145(5):950.
[35]Wong K,Thomson C,Bailey RR,et al.Acute oxalate nephropathy after a massive intravenous dose of vitamin C[J].Aust N Z J Med,1994,24(4):410.
[36]McAllister CJ,Scowden EB,Dewberry FL,et al.Renal failure secondary to massive infusion of vitamin C[J].Jama,1984,252(13):1 684.
[37]Bromley J,Hughes BG,Leong DC,et al.Life-threatening interaction between complementary medicines:cyanide toxicity following ingestion of amygdalin and vitamin C[J].Ann Pharmacother,2005,39(9):1 566.

