雷公藤甲素脂肪乳的制备及其体外性质研究
李 雪,毛玉玲,李 凯,程 丹,王淑君*
(1. 沈阳药科大学 中药学院,辽宁 沈阳 110016;2. 沈阳药科大学 药学院,辽宁 沈阳 110016)
雷公藤甲素脂肪乳的制备及其体外性质研究
李 雪1,毛玉玲1,李 凯2,程 丹2,王淑君2*
(1. 沈阳药科大学 中药学院,辽宁 沈阳 110016;2. 沈阳药科大学 药学院,辽宁 沈阳 110016)
目的确定雷公藤甲素脂肪乳的处方及制备工艺,并对其体外性质进行考察。方法采用高压匀质法制备雷公藤甲素脂肪乳,单因素和正交设计法考察制备工艺及处方;采用激光粒度测定仪测定其粒径及电位;采用超滤离心法测定包封率;采用可见分光光度法对其进行体外溶血性评价。结果制备的雷公藤甲素脂肪乳剂外观呈白色乳状,粒径为(154.6±8.3) nm;平均电位为(-0.903±0.024) mV;包封率可达到85%以上;溶血率均小于5%。结论高压匀质法可用于雷公藤甲素脂肪乳的制备,并且所获得的脂肪乳剂性质良好。
药剂学;脂肪乳;高压匀质法;雷公藤甲素;包封率;溶血试验
雷公藤甲素(triptolide,TP)是从卫矛科植物雷公藤(Tripterygium wilfordii Hook. F. )中分离出的活性最高的环氧二萜内酯化合物,是雷公藤的主要有效成分之一,具有免疫抑制、抗炎、抗生育及抗肿瘤等多种药理活性[1]。在临床上广泛应用于治疗风湿类疾病、器官移植、肾病、哮喘和肿瘤。近年来,广泛的抗肿瘤作用使雷公藤甲素受到极大关注,其不仅可以抑制体外多种癌细胞的增殖,还能够抑制体内实体瘤的生长和转移[2-3]。但是由于雷公藤甲素的低水溶性及其对胃肠道、肾脏、造血系统及生殖系统的毒性及不良反应使其临床应用受到限制[4-5]。
脂肪乳作为一种新型的载药体系,是脂溶性药物的良好载体,具有增溶和降低药物不良反应等特点。同时,药物被包裹于油相或油水界面层中,避免与体液直接接触,降低刺激性。脂肪乳中油的种类、乳滴粒径及表面电荷电性等因素直接影响静脉乳剂的体内分布,并且具有一定的靶向性,能够使其更好地发挥疗效,降低药物的毒性及不良反应[6]。由此可见,脂肪乳剂是雷公藤甲素静脉给药的良好载体。
1 仪器与材料
高效液相色谱仪(紫外SPD-10A 检测器, LC-15C液相泵,日本Shimadzu 公司),pH计(上海宇隆仪器有限公司),TGL-18C-C快速离心机(上海安亭科学仪器厂),SCQ2201超声波清洗器(上海声彦超声波仪器有限公司),分析天平(TG328A,上海精密科学仪器有限公司),DF-101S集热式恒温磁力搅拌器(巩义市英峪予华仪器厂),AH100D高压匀质机(加拿大 ATS公司),Mastersizer-2000-激光粒度电位测定仪(英国Malvern仪器公司),UV-2000紫外可见分光光度计(尤尼柯(上海)仪器有限公司)。
雷公藤甲素(triptolide,TP,南京泽朗医药科技有限公司),大豆磷脂(磷脂酰胆碱含量质量分数≥98%,上海太伟医药科技有限公司),油酸、注射用大豆油(LCT)、中链油(MCT)(中航铁岭药业),F68(德国BASF公司),无水乙醇(分析纯,天津富宇精细化工有限公司),甲醇、乙腈(色谱纯,天津康科德科技有限公司),其他试剂(分析纯,市售)。
2 方法与结果
2.1 雷公藤甲素脂肪乳的制备
将处方量雷公藤甲素和磷脂分散于注射用油、油酸中,于 80 ℃加热磁力搅拌下溶解均匀,得澄清得含药油相;将处方量甘油、F68、EDTA分散于适量注射用水中,于80 ℃加热磁力搅拌使分散均匀得水相。在高速组织捣碎机搅拌下(1×104r·min-1)迅速将水相加入到油相中,高速剪切10 min,制得均匀初乳。初乳冷却至室温,以0.1 mol·L-1氢氧化钠或盐酸调节溶液pH值,注射用水稀释至全量,转移至高压匀质机中,800 bar匀质8次。装瓶,充氮,密封,121 ℃热压蒸汽灭菌10 min,取出后于冷水浴中迅速冷却。
2.2 雷公藤甲素脂肪乳制备工艺的考察
2.2.1 初乳制备温度的选择
磷脂存在相转化温度,在其相转化温度为70~80 ℃内制备的乳剂粒径较小,也比较稳定[7];而在高温时油相的黏度较低,外部施加的剪切力所作的功较小,利于乳化。因此采用 80 ℃为水相、油相的制备温度。
2.2.2 药物加入方法的考察
不同药物制备载药型脂肪乳的方法和技术各不相同,一般情况下制备载药型脂肪乳的方法是将脂溶性药物与乳化剂直接溶解于油相中,利用两步乳化法进行制备。但是,在本实验中,若将药物与磷脂直接加入到油相中,80 ℃加热搅拌1 h后仍不能溶解完全,说明药物与磷脂未完全溶解于油相中,且高温长时间的溶解对药物的化学稳定性也很不利。因此,本研究中将药物与磷脂先溶解于适量无水乙醇中,然后挥干乙醇加入油相,药物与磷脂溶解迅速而完全,能够得到澄清的载药油相,避免磷脂和药物长时间加热而引起的降解。
2.2.3 高压匀质压力和次数的考察
脂肪乳的粒径大小及分布是影响制剂物理稳定性的重要因素,而高压匀质过程对粒径大小和粒径分布影响很大,因此,本实验对高压匀质操作参数进行了优化。匀质压力的考察范围为 600~1 000 bar,每个样品匀质8次,结果见图1A。在确定最佳匀质压力后,根据所确定的匀质压力匀质4~12次,进行匀质次数的考察,结果见图1B。
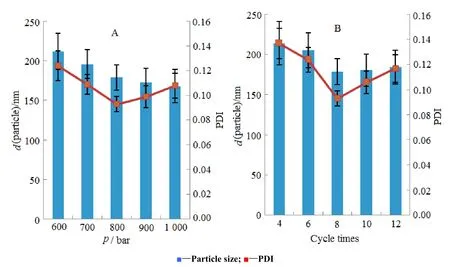
Fig. 1 Influence of different homogenization pressures on particle size of TP-LE(A) and different cycle times on particle size of TP-LE (B)±s, n=3)图1 不同匀质压力对雷公藤甲素脂肪乳粒径的影响(A)和不同匀质次数对雷公藤甲素脂肪乳粒径的影响(B)

由图1A可见,随着匀质压力的不断增加,TP-LE的粒径逐渐减小,当压力达到800 bar时,进一步增加压力,粒径基本不再降低,而代表粒径分布的PDI值却有增大趋势。考虑到较高的匀质压力需要更多的能量消耗,同时在较大的匀质压力下进行高压匀质易出现制剂过热而影响制剂的稳定性,因此,将制备TP-LE的高压匀质压力确定为800 bar。由图1B可见,在高压匀质压力为800 bar时,随着匀质次数的增加,TP-LE的平均粒径都逐渐减小,当匀质次数达到8次以后,继续增加匀质次数,粒径不再减小,而代表粒径分布的PDI值却有增大趋势,因此,将制备TP-LE的高压匀质次数确定为8次。
2.2.4 pH值的考察
pH值是影响制剂物理稳定性的重要因素之一,临床常用的脂肪乳注射液pH值多在5~8内,而雷公藤甲素在酸性条件下较稳定,碱性条件下降解明显,在pH值为6时降解最慢。本实验分别考察了pH值为5.0、5.5、6.0、6.5、7.0时TP-LE的物理和化学稳定性。实验发现,pH值在5.0~7.0内乳剂灭菌前后的物理稳定性均较好,进一步对制剂的化学稳定性进行了考察,不同 pH值的脂肪乳剂灭菌后的药物含量变化见图2。结果表明,pH值为6时药物含量最高,化学稳定性最好。考虑到TP-LE的灭菌稳定性及人体的耐受性,最终确定灭菌前以0.1 mol·L-1氢氧化钠将TP-LE的pH值调为5.5~6.0。
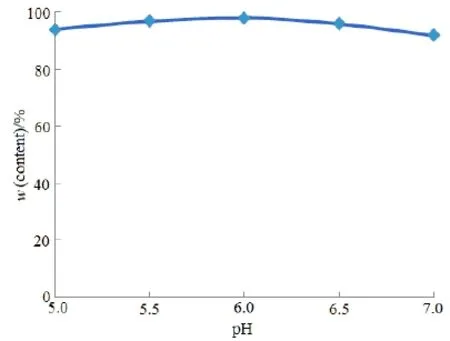
Fig. 2 Influence of pH value on the content of TP-LE图2 pH值对雷公藤甲素脂肪乳含量的影响
2.3 正交试验设计处方优化
油相和乳化剂是脂肪乳处方中重要的组成部分,油相的组成和比例直接影响脂肪乳的溶解性能、外观和粒径分布,乳化剂直接影响脂肪乳乳化过程,进而影响制剂的物理化学稳定性。本实验对脂肪乳处方组成中油相比例、磷脂、F68及油酸的用量进行了正交设计优化,各因素安排见表1。

Table 1 Factors and levels of the orthogonal design表1 正交设计试验表
采用L9(34)正交设计进行处方筛选,按表2所示制备雷公藤甲素脂肪乳后,以外观和粒度测定结果为指标进行处方筛选,以粒径均匀且较小为好。

Table 2 Investigation on the optimum conditions for preparing TP-LE by orthogonal design表2 雷公藤甲素脂肪乳处方正交设计优化

Continued table 2
根据表2中极差值(R)可知,各因素对粒径影响的主次顺序是B>C>A>D,说明磷脂和F68的用量对TP-LE影响最为显著,其次是油相比例和油酸用量。由此得出各因素最佳组合为A3B3C2D2。通过分析正交设计表及综合因素筛选得最优处方为(质量分数):LCT为2.5%、MCT为7.5%、磷脂为2.4%、F68为0.2%和油酸为0.05%。
2.4 雷公藤甲素脂肪乳稳定性研究
以雷公藤甲素脂肪乳粒径、含量、包封率、pH值为指标,对雷公藤甲素脂肪乳进行稳定性考察。
2.4.1 灭菌稳定性考察
制备3批雷公藤甲素脂肪乳样品分别装瓶、充氮、密封,121 ℃热压蒸汽灭菌10 min,取出后于冷水浴中迅速冷却,灭菌后进行各项理化性质检查和测定,与灭菌前相比较,结果见表 3。结果表明,雷公藤甲素脂肪乳灭菌稳定性良好。
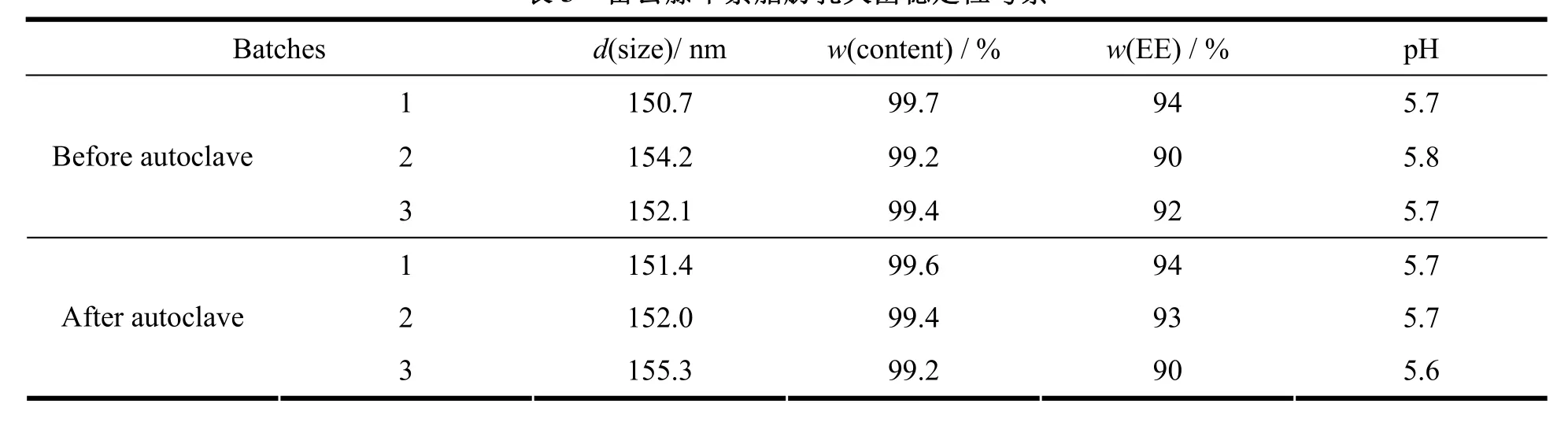
Table 3 Results of TP-LE autoclave test表3 雷公藤甲素脂肪乳灭菌稳定性考察
2.4.2 冻融稳定性考察
将灭菌后的3批雷公藤甲素脂肪乳样品于-20 ℃条件下冻融3次循环,冻融后的脂肪乳样品进行理化性质检查和测定,与冻融前相比较,结果见表 4。结果表明,雷公藤甲素脂肪乳冻融稳定性良好。
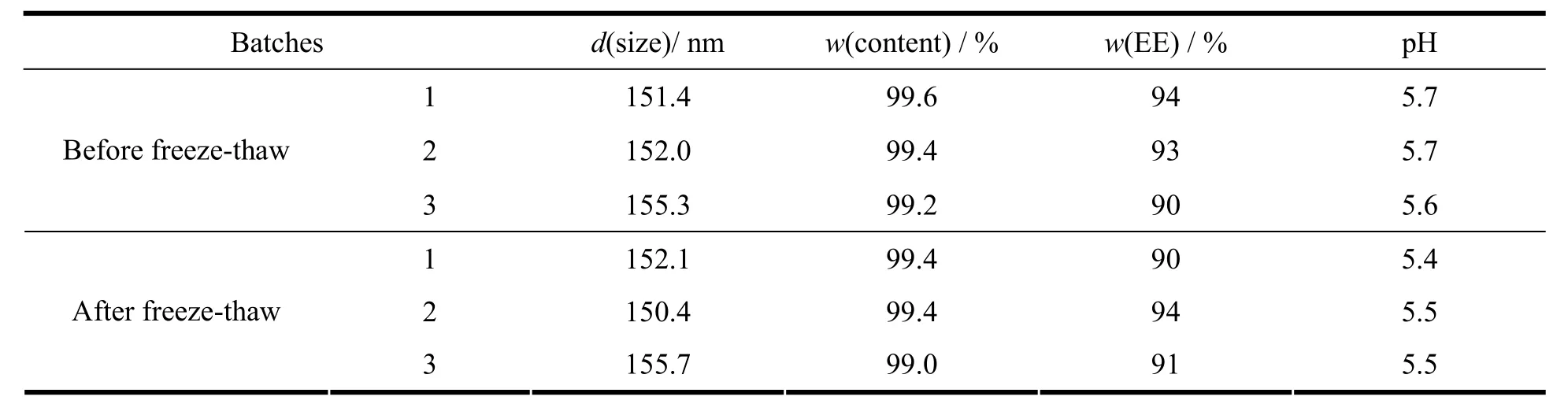
Table 4 Results of freeze-thaw stability表4 雷公藤甲素脂肪乳冻融稳定性考察
2.4.3 加速稳定性考察
将灭菌后的3批雷公藤甲素脂肪乳样品于 (40±2) ℃加速试验3个月,进行理化性质检查和测定,与加速试验前相比较,结果见表5。结果表明,雷公藤甲素脂肪乳稳定性良好。

Table 5 Results of accelerated stability表5 雷公藤甲素脂肪乳加速稳定性考察
2.5 雷公藤甲素脂肪乳处方工艺的确定
雷公藤甲素脂肪乳的处方为:雷公藤甲素12.5 mg、油相(LCT-MCT质量分数比为2.5∶7.5)10 g、磷脂2.4 g、油酸50 mg、F68 0.2 g、甘油2.5 g和EDTA50 mg,制成100 mL。
雷公藤甲素脂肪乳的制备工艺:称取处方量注射用油(LCT-MCT质量分数比2.5∶7.5)、油酸于80 ℃下搅拌分散均匀得油相,称取处方量雷公藤甲素、磷脂于适量无水乙醇中,80 ℃下搅拌至完全溶解,挥尽乙醇,加入油相,80 ℃下继续搅拌,得澄清含药油相;称取处方量甘油、F68、EDTA加至适量注射用水中,80 ℃下磁力搅拌使溶解,分散均匀得水相;在高速组织捣碎机搅拌下(1×104r·min-1)迅速将水相加入到油相中,高速剪切10 min,制得均匀初乳;将初乳冷却至室温,以0.1 mol·L-1氢氧化钠调节溶液pH值至5.5~6.0,注射用水稀释至全量,转移至高压匀质机中,800 bar匀质8次,制得终乳;将所得终乳装瓶、充氮、密封,于121 ℃热压蒸汽灭菌10 min,取出后于冷水浴中迅速冷却即得雷公藤甲素脂肪乳。
2.6 雷公藤甲素脂肪乳粒径及zeta电位的测定
将按“2.5”条方法制备的雷公藤甲素脂肪乳过0.22 μm微孔滤膜,注射用水稀释500倍,采用Mastersizer-2000-激光粒度分析仪测定其粒径大小及分布。制备的雷公藤甲素脂肪乳剂为均一稳定而带有淡蓝色乳光的均匀分散体系,其粒径分布在(154.6±8.3) nm,PDI值为(9.3±0.8)×10-2;以Mastersizer-2000-激光粒度分析仪测定其电位,平均电位为(-0.903±2.4×10-2) mV。
2.7 雷公藤甲素脂肪乳的含量及包封率考察
2.7.1 含量测定
以雷公藤甲素为指标,采用HPLC法测定雷公藤甲素脂肪乳中雷公藤甲素的含量。
色谱条件:色谱柱为Kromasil C18柱 (4.6 mm×250 mm,5 μm),流动相为乙腈-水(体积比40∶60),流速为1 mL·min-1,检测波长为220 nm,进样量为20 μL,柱温为室温。
取0.1 mL雷公藤甲素脂肪乳剂置于10 mL量瓶中,用甲醇破乳稀释并定容至刻度。用0.22 μm微孔滤膜过滤,取续滤液20 μL注入高效液相色谱仪,以外标一点法测定雷公藤甲素脂肪乳中雷公藤甲素含量。HPLC法测定3批雷公藤甲素脂肪乳中雷公藤甲素含量质量分数均在98%以上。
2.7.2 包封率考察
采用超滤离心法测定雷公藤甲素脂肪乳包封率,分别测定脂肪乳剂中药物总量及水相中药物含量,由以下公式计算包封率(EE%):w(EE) =(ρtotalVtotal-ρwaterVwater)/ρtotalVtotal×100%。
式中ρtotal为脂肪乳中药物总质量浓度(g·L-1);Vtotal为脂肪乳总体积(L);ρwater为水相中药物质量浓度(g·L-1);Vwater为水相体积(L)。
药物总量的测定:按“2.7.1”条色谱条件测定脂肪乳剂中药物总量。
水相中药物含量测定:精密吸取雷公藤甲素脂肪乳液2 mL置于截留分子质量为1×104u的超滤离心管中,4 000 r·min-1离心15 min,重复3次,取滤液20 μL注入高效液相色谱仪,测定水相中药物含量。
包封率计算:按上式计算3批雷公藤甲素脂肪乳包封率,结果表明雷公藤甲素脂肪乳包封率质量分数均大于85%。
2.8 雷公藤甲素脂肪乳体外溶血试验
红细胞悬液的配制:取新鲜家兔耳缘静脉血5 mL,置烧杯中,玻璃棒搅拌除去纤维蛋白原,1 000 r·min-1离心10 min,除去上清液,沉淀的红细胞用生理盐水轻轻摇匀,洗涤数次,直至上清液不显红色为止,弃去上清液,用生理盐水配制体积分数为2%的红细胞悬液。
溶血试验:取洁净试管7支,1~5号管为供试品,按表6依次加入体积分数2%红细胞悬液、生理盐水、雷公藤甲素脂肪乳注射夜;6号管为阴性对照;7号管为阳性对照。混匀1~7号管,置(37±0.5)℃恒温水浴中温浴。3 h后取样,1 000 r·min-1离心10 min,取上清液适当稀释后,以蒸馏水为对照,于波长545 nm处测定吸光度,按下式计算溶血率:HD=(As-An-ATP-LE)/(A0-An)×100%。
式中:As为供试品吸光度、An为阴性对照品吸光度、Ao为阳性对照品吸光度、ATP-LE为雷公藤甲素脂肪乳样品吸光度。表6结果表明各管雷公藤甲素脂肪乳的溶血率均小于5%。
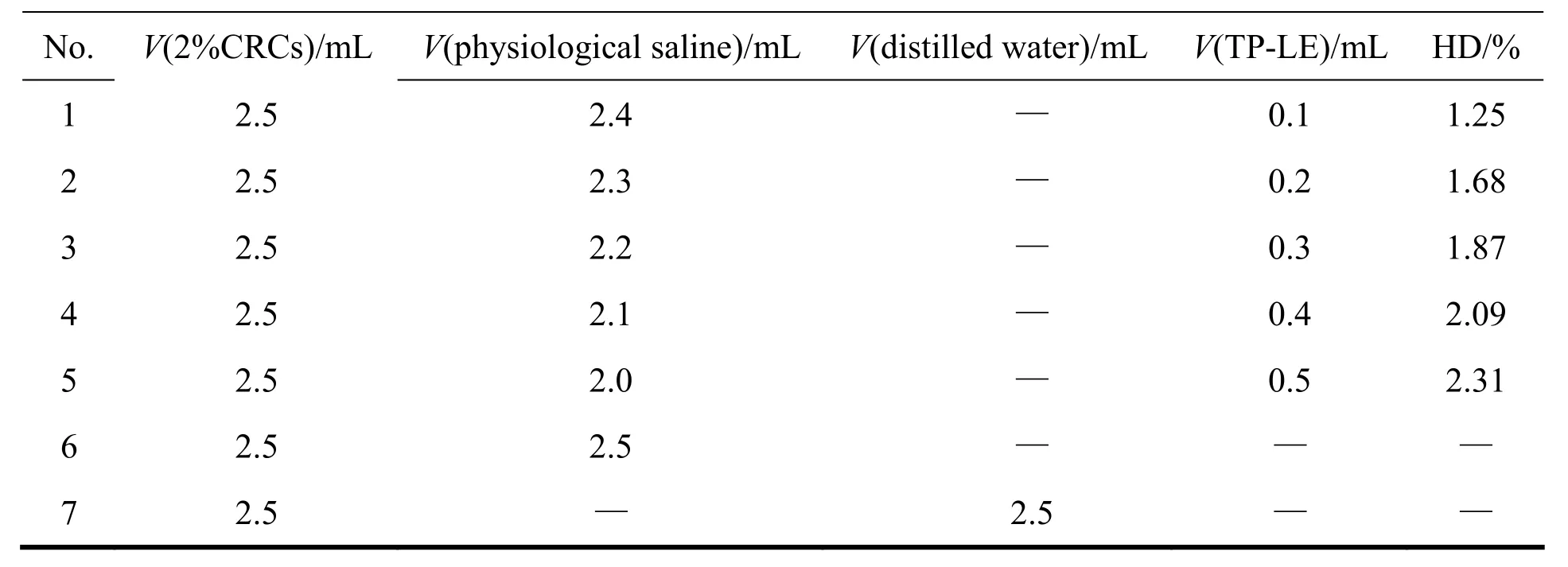
Table 6 Design and results of hemolysis test of TP-LE表6 雷公藤甲素脂肪乳溶血试验设计及结果
3 讨论
a. 脂肪乳的制备受到许多因素的影响,其中工艺参数包括药物加入方法、pH值的调节、高压匀质压力和次数;处方因素包括油相的组成和比例、乳化剂的选择及用量等。脂肪乳注射液油相最初主要是选择植物来源的长链甘油三酯(LCT),如大豆油、玉米油等。虽然 LCT脂肪乳能够为患者提供必需的脂肪酸和能量,但LCT进入线粒体代谢需依赖于肉毒碱转运,氧化代谢速度慢,长期使用可能对机体免疫功能有抑制作用。中链甘油三酯(MCT)分子质量较小,有较大的水溶性及较低的 pKa值,不需依赖肉毒碱即可进入线粒体进行快速氧化,在血液循环中的清除速度较快,不易在肝脏中蓄积。但不足之处是不能提供必需的脂肪酸,应用纯MCT可引起代谢性酸中毒和神经系统不良反应。所以根据正交试验设计结果将LCT与MCT按照质量分数2.5∶7.5比例进行物理混合后所制备的脂肪乳能够达到扬长避短的效果[8-9]。磷脂是最常用的天然乳化剂,具有良好的乳化性能,无毒且生物相容性好。但对于载药型脂肪乳来说,单一的乳化剂并不足以维持脂肪乳的稳定,通常将磷脂与F68合用,制备载药脂肪乳注射液以增加制剂的稳定性[10]。油酸能够促进磷脂、F68分子间的相互作用,形成复合膜[11];同时能够增加分子间作用力及乳滴表面静电电荷,进而增大界面膜的稳定性。作者通过正交设计考察最终确定油相组成为LCT与MCT的质量分数比为2.5∶7.5,磷脂用量的质量分数为2.4%,F68用量的质量分数为0.2%,油酸用量的质量分数为0.05%。
b. 超滤离心法是常见的药物测定包封率的方法,本文作者利用该法成功分离出脂肪乳中水相,由于药物主要包裹于油相和油水界面层中,处方组成中其水相的体积占总体积的90%,通过测定水相中药物含量和脂肪乳中药物总量,计算脂肪乳包封率。该法操作简单、快速、重现性好。
c. 注射药物的安全性评价是药物安全性试验的一个重要组成部分,溶血试验结果表明不同浓度的雷公藤甲素脂肪乳并未产生溶血现象,不会导致红细胞发生溶血和凝聚反应,为临床安全用药提供重要依据。
参考文献:
[1] LIU Qiu-yan. Triptolide and its expanding multiple pharmacological functions [J]. International Immunopharmacology, 2011, 11 (3): 377-83.
[2] YANG Shan-min, CHEN Jing-uo, GUO Zhen, et al. Triptolide inhibits the growth and metastasis of solid tumors [J]. Mol Cancer Ther, 2003, 2: 65-72.
[3] CHUGH R, SANGWAN V, PATIL S P, et al. A preclinical evaluation of minnelide as a therapeutic agent against pancreatic cancer [J]. Sci Transl Med, 2012, 4: 139-156.
[4] SHAMON L A, PEZZUTO J M, GRAVES J M, et al. Evaluation of the mutagenic, cytotoxic, and antitumor potential of triptolide, a highly oxygenated diterpene isolated from Tripterygium wilfordii [J]. Cancer Lett, 1997, 112: 113-117.
[5] SUN Xin, ZHANG Su-min, TIAN Chun-hua, et al. Safety of Tripterygium wilfordii[J]. Chin J New Drugs, 2001, 10: 539-543.
[6] 陆斌. 药物新剂型与新技术[M]. 北京: 人民卫生出版社, 2002: 53-54.
[7] YU Ye-ling, LU Yan, TANG Xing, et al. Formulation preparation and evaluation of an intravenous emulsion containing brucea javanica oil and coix seed oil for anti-tumor application [J]. Biol Pharm Bull, 2008, 31: 673-680.
[8] SMYRNIOTIS V E, KOSTOPANAGIOTOU G G, ARKADOPOULOS N F, et al. Long-chain versus medium-chain lipids in acute pancreatitis complicated by acute respiratory distress syndrome: effects on pulmonary hemodynamics and gad exchange [J]. Clin Nutr, 2001, 20: 139-143.
[9] 曹新伟. 脂肪乳剂的特点和应用[J]. 腹部外科, 2000, 13(4):206-208.
[10] GROVES M J, WINEBERG M, BRAIN A P R. The presence of liposomal material in phosphatide stabilized emulsions [J]. J Dispersion Sci Technol, 1985, 6: 237-243.
[11] LEVY M, SEHUTZE W, FUHRER C, et al. Characterization of diazepam submicron emulsion interface: role of oleic acid [J]. J Microencapsulation, 1994, 11: 79-92.
Preparation and characterization of triptolide-loaded lipid emulsion
LI Xue1, MAO Yu-ling1, LI Kai2, CHENG Dan2, WANG Shu-jun2*
(1. School of Traditional Chinese Materia Medica, Shenyang Pharmaceutical University, Shenyang 110016, China; 2. School of Pharmacy, Shenyang Pharmaceutical University, Shenyang 110016, China)
ObjectiveTo optimize the formulation and preparation of triptolide-loaded lipid emulsion (TP-LE) and investigate its characterization in vitro.MethodsTP-LE was prepared by a high-pressure homogenization method. The preparation technology and formulation were investigated by single factor exploration and orthogonal design. The particle size and zeta potential were determined by a laser scattered particle analyzer. The ultrafiltration centrifugation method was used to determine drug entrapmentefficiency (EE%) of triptolide in TP-LE. UV-VIS spectrophotometry was used for in vitro hemolytic evaluation.ResultsThe prepared TP-LE was milky white in appearance, with particle size of (154.6±8.3) nm; zeta potential of (-0.903±0.024) mV; EE% of >85%; hemolysis ratio of <5%.ConclusionsHigh-pressure homogenization method can be used to prepare triptolide-loaded lipid emulsion for i.v. administration, and the character of TP-LE was pretty good.
Pharmaceutics; Lipid emulsion; High-pressure homogenization method; Triptolide; Entrapment efficiency; Hemolysis test
R94
:A
(本篇责任编辑:赵桂芝)
(2015)04-0134-10
10.14146/j.cnki.cjp.2015.04.003
2015-02-12
李雪(1990-), 女(汉族), 辽宁沈阳人, 硕士研究生,,E-mail lixuelixue75@163.com; *
: 王淑君(1972-), 女(汉族), 辽宁沈阳人, 教授, 博士, 博士生导师, 主要从事药物制剂研究, Tel. 024-23986360, E-mail 1252116911@qq.com。

