翻转课堂下的课堂观察——以“化学平衡常数”教学为例
安双马 卢 伟
(浙江师范大学 教师教育学院 浙江 金华 321004)
受建构主义教育理论的影响,教育界普遍认为学生学习是一个有意义的建构过程,学生理解知识是基于自身的经验背景来建构,这往往取决于特定情境。受此影响教学通常包括知识传授和知识内化两个阶段。传统的课堂教学一般是课堂上知识传授,课后进行知识内化。然而作为新型的教学模式,翻转课堂不同于传统课堂的教学模式,知识传授通过信息技术的辅助在课前完成,知识内化则在课堂中经过同学的帮助与教师的协助来完成[1]。
翻转课堂的发展往往需要教师自身反思,而课堂观察是反思的基础;教师专业成长的主阵地在课堂。因此通过课堂观察,对改进翻转课堂教学,提高教学效率和质量,提升教师专业发展水平有很大帮助[2][3]。
基于翻转课堂的特殊性,笔者将本次翻转课堂分为课前观察、课中观察和课后反思三个部分。
一、课前观察
在上课之前,化学教师提前准备好教学资源上传到学生的公共学习平台,一般包含了给学生提供的参考书籍、电子课件、教案、微视频教程以及有关于化学平衡常数这一专题学习拓展素材的资料。教学视频的制作作为化学课程资源准备中的核心内容,在本次课堂观察过程中,化学教师根据化学平衡常数的课堂教学目标运用视频软件对本次课程视频进行录制和后期制作。教师还为学生准备了教学课件,以及一些有关本次课的练习题。制作完成后,将这教学视频和其他电子资源上传到本班的公共学习平台上,方便学生下载观看。
二、课中观察
笔者提前5分钟进入教室,观察到学生已经在上课之前提前将座位按照四人一小组的方式排列好并安静地坐在座位上,做好上课准备。由于教室所限,为了最大限度减少课中观察对学生学习的影响,笔者选择坐在教室的最后一排,因此无法详尽的记录前排学生的交流讨论情况,主要记录离我比较近的学生的讨论情况[3]。
在课堂观察过程中将本次翻转课堂分为四个部分:
1.合作探究(0-13min)
[教师]同学们,我依据大家昨天在公共学习平台上反馈的问题作了一定的归纳总结,大家对本次化学平衡常数的一些问题分歧比较大,我们加强小组之间的团队互助意识,相互讨论,如果大家在相互交流之后还是不懂,那我就和同学们一起相互交流探究!
[投影](1)化学平衡常数为何与反应物和生成物的浓度无关?
(2)如何运用化学平衡常数来判断可逆反应进行的方向?
(3)化学平衡常数和化学平衡转化率在现实生活中有何应用?

[学生乙]我知道化学平衡常数能反映一个可逆反应的限度,但如何运用我确实不会。
[学生甲]我看了教学视频、教材和课外参考资料,我认为化学平衡常数反映了一个可逆化学反应进行的程度。例如对于同一个可逆反应,如果一个化学平衡常数较大说明他的反应进行程度较大。
[学生丙]我从化学平衡常数的公式中推出,如果对于一个可逆反应,如果一个平衡常数越大,则其中生成物的比例也就越大。
此时教师走过来,站在旁边仔细倾听,未参与讨论。
[学生乙]我看到课外参考书上写化学平衡常数可以用来判断一个反应的热效应,例如:如果一个反应升高温度,它的化学平衡常数增大,那说明可逆反应的正反应是一个吸热反应,加热更有利于正反应进行。相反,如果这可逆反应升高温度,他的化学平衡常数减小,那就说明这个可逆反应的正反应是一个放热反应,降低温度反而更利于反应朝正反应方向进行。
[学生丙]我想对乙同学提出的观点进行补充,我们可以运用化学平衡常数来提高可逆反应中反应物的转化率。例如,在工业合成氨中不同温度下化学平衡常数是不同的,具体的数据可以看教材第45页表2-8,从这些数据中我们可以看出在373K时化学平衡常数最大,说明从理论上来说这时的温度是合成氨转化率最好的,因此可以说明理论基础对于促进工业生产是很有价值的,可以减少原料的浪费,使工厂达到最佳的经济效益。
2.释疑解惑(13-20min)
[教师]刚才的几分钟,大家讨论十分激烈,我站在旁边听到也看到大家结合自己昨天自学的知识为小组同学解释并且相互交流。那我想请几位小组代表来为我们全班同学答疑解惑。
全班积极性高涨,教师选择了A同学代表他们小组来回答。
[学生A]通过教材中第44页中的表2-6中计算以及推理可以得出化学平衡常数K是一个不变的定值。因此可以得出化学平衡常数与温度有关与反应物和生成物的浓度无关。
[教师]除了这些,大家还有别的想要补充?
等待10s。
[教师]那第二题我想请B同学为我们大家解释一下。
[学生B]结合之前我们小组讨论的结果,引入一个浓度商Qc,Qc是可逆反应中生成物的浓度幂之积与反应物浓度幂之积的比值,和平衡常数相似,只是它是代表在一定温度下任何时刻,反应物与生成物的关系。当Qc>K时,此时反应过程中生成物浓度相较于化学平衡时的生成物浓度大,此时代表反应正朝向逆方向进行即 v(逆)>v(正);当 Qc=K 时,此时反应过程中反应物浓度与此反应平衡时的反应物浓度相同,说明此反应已经达到平衡即 v(逆)=v(正);当 Qc<K 时,此时反应过程中反应物浓度大于此反应平衡时的反应物浓度,说明反应还在朝正反应方向进行即v(正)>v(逆)。
[教师]回答得很好,能够挖掘出教材中未知的知识点,课前看课外资源很仔细!值得大家学习。第三小题我们就请C同学来帮我们解决一下。
[学生C]化学平衡常数和化学平衡转化率应用非常广泛。例如在工业生产中我们往往要考虑反应达到平衡时,反应物的转化率,为了提高转化率,我们一般会采取各种措施,降低生产成本,提高经济效益。同时化学平衡常数还能判断可逆反应的程度,化学平衡常数越大说明在反应体系中生成物所占的比例越大,化学反应进行程度也就越大。
[教师]本节课中的化学平衡常数是具体的数值,当化学平衡常数达到多少时可判断这个可逆反应基本完全了?
[学生C]一般来说,化学反应平衡常数的K>105时可以判断该反应已经进行完全了。同理如果化学平衡常数K<10-5时,可以判断该反应的正反应很难进行,或者说该反应的逆反应已经完全了。
[教师]C同学讲解的非常好。大家对之前的3个问题进行了很好的解决,还有别的疑问?
全班很安静,无人回答。
3.达标测试(21-35min)
[教师]看到大家对于化学平衡常数的知识点掌握得相当不错,我来检测一下大家对本节课内容的掌握程度。
[投影]已知反应 C(s) +2H2O(g)⇌CO2(s) +2H2(g)的平衡常数K为A,用A表示下列各反应的平衡常数K:

1分钟后教师见学生都做得差不多了,请学生D回答。
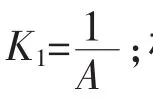
[教师]大家对同一个可逆反应之间的化学平衡常数的相互转换的方法已经掌握了,下面我将要稍加难度。
[投影]合成氨的反应 N2(g) + 3H2(g)⇌2NH3(g)在某温度下各物质的平衡浓度是 c(N2)=3mol·L-1,c(H2)=9mol·L-1,c(NH3)=4mol·L-1,求:
①该反应的化学平衡常数。
②N2、H2的初始浓度。
2分钟后教师请学生E上讲台,在黑板上将整个过程进行演示。
学生E在黑板上的演示:
[教师]关于化学平衡常数的计算,我们一般采用起始、变化、平衡这三段式,这样可以明确各物质之间的对应关系。既然大家对化学平衡常数的计算已经掌握,那我们来一起做一题关于化学平衡的转化率的题目。
[投影]在一个密闭容器中,CO与H2O混合加热到773K达到下列平衡:此时平衡常数K=9,若反应开始时 c(H2)=c(CO)=0.020mol·L-1,求达到平衡时 CO的转化率。
2分钟之后教师请学生F上讲台,在黑板上将整个过程进行演示。
[学生F]设达到平衡时CO的转化率为x,

[教师]F同学和E同学的方法差不多,可见掌握一种好的解题方法往往是成功的一半。
4.小结提升(35-40min)
[教师]同学们讨论很激烈也很投入,解题正确率也很高。我相信大家都有一定的收获和心得,那我想请一位同学上台来讲一讲你在本节课中学到了什么,还有什么不懂,需要大家来帮助你。下面我请同学G上台讲一下。
[学生G]在本节课中我学习了化学反应平衡常数的表达式,跟同学一起讨论和老师的讲解之后,我知道了化学平衡常数的影响因素只与温度有关,与各物质的浓度、分压无关。
G同学站在讲台上,暂时停顿。
[教师]那你谈谈化学平衡常数在衡量化学反应限度方面有什么作用?
[学生G]化学平衡常数可以判断化学反应的进行程度,以及可以判断可逆反应的反应方向,还可以求出在反应的某一个时刻或者反应平衡时的转化率和各个物质的平衡浓度。
[教师]经过大家的共同合作、努力之下我们学习了化学平衡常数,化学平衡常数为我们今后学习化学平衡的移动、离子反应的电离平衡打下坚实的基础。
三、课后反思
反思翻转课堂观察可以为一线教师研究翻转课堂提供一个观察翻转课堂、思考翻转课堂、研究翻转课堂的支架,为每一位教师提供交流的平台。在反思翻转课堂观察过程中,观察者能通过一种全新的视角了解翻转课堂教学,获得深入的反思性认识。
特别是在此次翻转课堂的观察中,笔者发现将这节课的课堂完全交给学生,学生课前自学,课堂上讨论,自己总结,教师只是点评,辅助学生,课堂氛围更好,学生学习积极性更高,观察到有一些平时不怎么说话的学生也乐于参与同学之间的交流。翻转课堂教学过程改变了传统教学过程,加强了学生课前与课堂教学过程中的自学能力、思维能力以及合作学习时的交流讨论能力,使学生能够主动探求化学知识、应用化学知识。
通过此次对翻转课堂的观察、反思、分析,笔者认为翻转课堂对学生充分利用课外时间,提高自觉性和获取多样的课外学习资源提出了更高的要求。对教师而言为学生提前筛选学生学习所需的教学资源,并提前做好充足的课堂教学准备,高效利用课堂教学时间。同时教师之间相互观察、探讨翻转课堂,加强交流、合作与探究,共同促进。只有这样翻转课堂才能真正改善学生学习,促进教师专业化发展[4]。
[1] 王春.基于“翻转课堂”教学模式下的同课异构—以“化学平衡常数的应用”为例[J].化学教学,2014,(9):47
[2] 王文.课堂观察一教师专业成长的必由之路[D].福州:福建师范大学,2008,1
[3] 夏雪梅.以学习为中心的课堂观察[M].北京:教育科学出版社,2012 :136-147
[4] 陈瑶.课堂观察指导[M].北京:教育科学出版社,2012:148

